連続処理(24時間)および短時間処理(6時間)における 50 %細胞増殖抑制濃度は,連続処理では0.03 mg/mL, 短時間処理におけるS9 mix存在下およびS9 mix非存在下では0.06 mg/mLであった.各系列での処理濃度は,50 %細胞増殖抑制濃度の2倍濃度を最高処理濃度とし,それぞれ公比2で5濃度設定した.連続処理では,24時間および48時間処理後,短時間処理ではS9 mix存在下および非存在下で6時間処理し,新鮮培地で更に18時間培養後,標本を作製し,検鏡することにより染色体異常誘発性を検討した.染色体分析が可能な最高濃度は,24時間および48時間連続処理では0.015 mg/mL,短時間処理のS9 mix存在下では0.12 mg/mLであったことから,これらの濃度を高濃度群として3濃度群を観察対象とした.短時間処理のS9 mix非存在下では,細胞毒性により3濃度の観察対象が得られなかったため,公比2で8濃度設定し再試験を実施したところ,染色体分析が可能な最高濃度は0.0075 mg/mLであったことから,この濃度を高濃度群として3濃度群を観察対象とした.
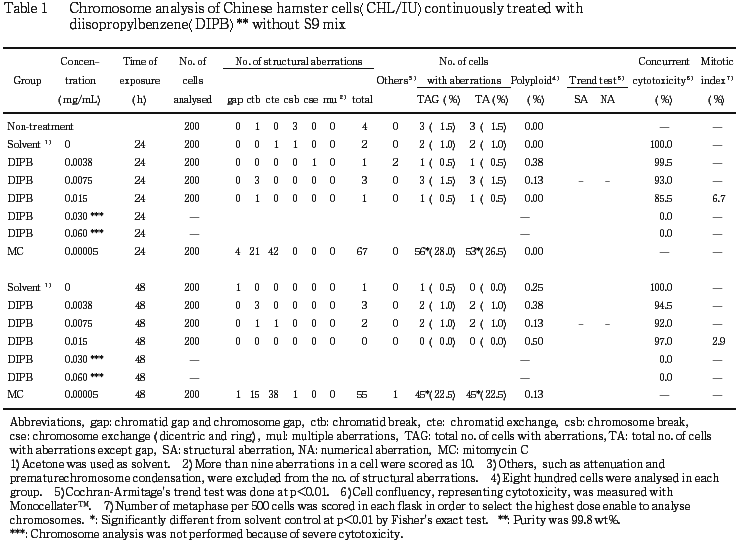
CHL/IU細胞を24時間および48時間連続処理したいずれの処理群においても,染色体の構造異常や倍数性細胞の誘発作用は認められなかった.短時間処理では,S9 mix 存在下および非存在下で6時間処理したいずれの処理群においても,染色体の構造異常や倍数性細胞の誘発作用は認められなかった.
以上の結果より,ジイソプロピルベンゼンは,上記の試験条件下で染色体異常を誘発しないと結論した.
 )培養液を用いた.
)培養液を用いた.
 パナファーム・ラボラトリーズ)は,無色透明液体で,水に対しては100 mmol/L未満,DMSOでは50 mg/mL以上,1 mol/L未満で溶解,アセトンでは2 mol/L以上で溶解し油溶性で,分子量162.28,沸点203-210℃,純度99.8 wt%(不純物は不明)の物質である.被験物質原体は,熱,光,衝撃,摩擦に対して安定である.
パナファーム・ラボラトリーズ)は,無色透明液体で,水に対しては100 mmol/L未満,DMSOでは50 mg/mL以上,1 mol/L未満で溶解,アセトンでは2 mol/L以上で溶解し油溶性で,分子量162.28,沸点203-210℃,純度99.8 wt%(不純物は不明)の物質である.被験物質原体は,熱,光,衝撃,摩擦に対して安定である.
 )を用いた.原体を溶媒に溶解して原液を調製し,ついで原液を溶媒で順次希釈して所定の濃度の被験物質調製液を作製した.被験物質調製液は,すべての試験において培養液の 0.5 vol%(v/v)になるように加えた.
)を用いた.原体を溶媒に溶解して原液を調製し,ついで原液を溶媒で順次希釈して所定の濃度の被験物質調製液を作製した.被験物質調製液は,すべての試験において培養液の 0.5 vol%(v/v)になるように加えた.
 )を用いて各群の増殖度を計測し,被験物質処理群の溶媒対照群に対する細胞増殖の比をもって指標とした.
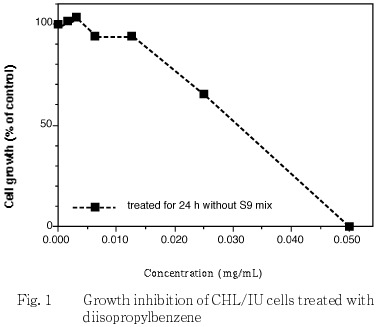
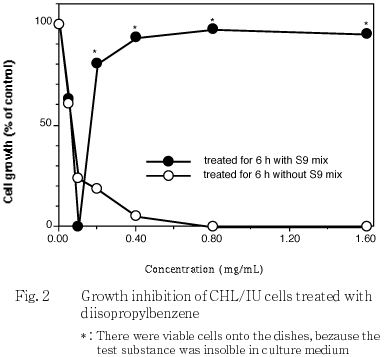
)を用いて各群の増殖度を計測し,被験物質処理群の溶媒対照群に対する細胞増殖の比をもって指標とした.その結果,連続処理における50 %細胞増殖抑制濃度は0.03 mg/mLであった(Fig. 1).また,短時間処理におけるS9 mix存在下および非存在下では,ともに0.06 mg/mLであった(Fig. 2).

 )およびシクロホスファミド(CPA,Sigma Chemical Co.)は,注射用蒸留水(
)およびシクロホスファミド(CPA,Sigma Chemical Co.)は,注射用蒸留水( 大塚製薬工場)に溶解して調製した.それぞれ染色体異常を誘発することが知られている濃度を適用した.
大塚製薬工場)に溶解して調製した.それぞれ染色体異常を誘発することが知られている濃度を適用した.染色体異常試験においては1濃度あたり4枚のディッシュを用い,そのうちの2枚は染色体標本を作製し,別の2枚については単層培養細胞密度計により細胞増殖率を測定した.
作製したスライド標本のうち,1つのディッシュから得られた異なるスライドを,4名の観察者がそれぞれ処理条件が分からないようにコード化した状態で分析した.染色体の分析は,日本環境変異原学会・哺乳動物試験研究会(MMS)1)による分類法に基づいて行い,染色体型あるいは染色分体型のギャップ,切断,交換などの構造異常の有無と倍数性細胞(polyploid)の有無について観察した.また,構造異常については1群200個,倍数性細胞については1群800個の分裂中期細胞を分析した.
染色体異常を有する細胞の出現頻度について,溶媒対照群と被験物質処理群および陽性対照群間でフィッシャーの直接確率法2)により,有意差検定を実施した(p<0.01).また,用量依存性に関してコクラン・アーミテッジの傾向性検定3)(p<0.01)を行った.最終的な判定は,統計学的および生物学的な評価に基づいて行った.
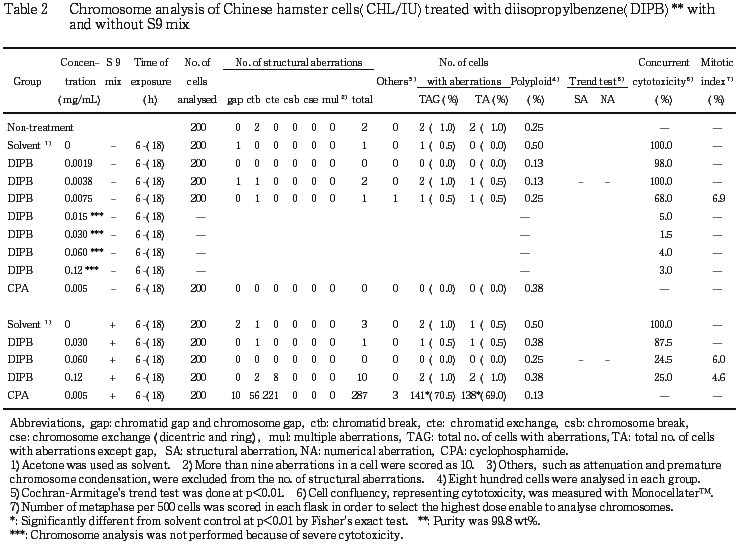
短時間処理による染色体分析の結果をTable 2に示した.ジイソプロピルベンゼンを加えてS9 mix存在下および非存在下で6時間処理したいずれの処理群においても,染色体の構造異常および倍数性細胞の誘発作用は認められなかった.
従って,ジイソプロピルベンゼンは,上記の試験条件下で,試験管内のCHL/IU細胞に染色体異常を誘発しないと結論した.
| 1) | 日本環境変異原学会・哺乳動物試験分科会編,"化学物質による染色体異常アトラス," 朝倉書店,東京,1988. |
| 2) | 吉村 功編,"毒性・薬効データの統計解析,事例研究によるアプローチ," サイエンティスト社,東京,1987. |
| 3) | 吉村 功,大橋靖夫編,"毒性試験講座14,毒性試験データの統計解析," 地人書館,東京,1992,pp. 218-223. |
| 連絡先 | |||
| 試験責任者: | 佐々木澄志 | ||
| 試験担当者: | 日下部博一,佐々木澄志,若栗 忍,中川ゆづき,大嶋節子,橋本恵子 | ||
| (財)食品薬品安全センター 秦野研究所 | |||
| 〒257-8523 神奈川県秦野市落合729-5 | |||
| Tel 0463-82-4751 | Fax 0463-82-9627 | ||
| Correspondence | ||||
| Authors: | Kiyoshi Sasaki(Study director) Hirokazu Kusakabe, Kiyoshi Sasaki, Shinobu Wakuri, Yuzuki Nakagawa, Setsuko Ohshima, Keiko Hashimoto | |||
| Hatano Research Institute, Food and Drug Safety Center | ||||
| 729-5 Ochiai, Hadano, Kanagawa, 257-8523, Japan | ||||
| Tel +81-463-82-4751 | Fax +81-463-82-9627 | |||