2,2,6,6-テトラメチル-4-ヒドロキシピペリジンの
ラットを用いる反復経口投与毒性・生殖発生毒性併合試験
Combined Repeat Dose and Reproductive/Developmental Toxicity Screening Test of
2,2,6,6-Tetramethyl-4-hydroxypiperidine by Oral Administration in Rats
要約
2,2,6,6-テトラメチル-4-ヒドロキシピペリジンの60,200および600 mg/kgをSD系(Crj:CD)のラットの交配前2週間および交配期間の2週間を通じて経口投与し,さらに雄では交配期間終了後20日間,雌では妊娠期間を通じて分娩後の哺育3日まで連続投与し,親動物の反復投与毒性および生殖能ならびに児動物の発生・発育に及ぼす影響について検討した.
1. 反復投与毒性
被験物質投与に起因すると考えられる死亡が,雌の60 mg/kg群および雌雄の600 mg/kg群で観察された.一般状態の観察で被験物質投与後に眼瞼下垂および散瞳が雌雄の60 mg/kg以上の投与群で,自発運動低下が雌雄の600 mg/kg群で認められた.また,雌雄の200 mg/kg以上の投与群で体重増加抑制が認められ,摂餌量の高値が雌雄の600 mg/kg群で認められた.雄の血液学検査,血液凝固能検査および血液生化学検査には被験物質投与の明らかな影響は認められなかった.器官重量では雌雄の600 mg/kg群で副腎重量が高値を示し,雌の600 mg/kg群で肝臓重量が高値を示した.
病理学検査の結果,生存例には被験物質投与の影響が示唆される病変は観察されなかった.600 mg/kg群の死亡例では被験物質投与の直接的な刺激に起因すると考えられる消化管の赤色斑点や腺胃の潰瘍に伴う所見が認められた.また,死亡動物に共通して腎臓の皮質や皮髄境界部に尿細管上皮の空胞変性が観察され,被験物質投与の影響が示唆された.しかし,生存例では腎臓の異常は認められなかった.
2. 生殖発生毒性
600 mg/kg群で連続した発情休止期像が観察される性周期の停止が3例認められ,平均性周期が延長した.交尾能および受胎能に被験物質投与の影響は認められなかった.分娩時観察では妊娠動物の全例が正常に分娩し,妊娠期間にも被験物質投与の影響は認められなかった.妊娠黄体数,着床痕数,出産児数,出産生児数,着床率および分娩率に明らかな被験物質投与の影響は認められなかった.600 mg/kg群で雌雄の新生児の生後0日体重および4日の生存率が低値を示した.新生児の外表に異常は認められず,死亡児および哺育4日の剖検でも被験物質投与による影響は認められなかった.
以上の結果から,本試験条件下における 2,2,6,6-テトラメチル-4-ヒドロキシピペリジンの反復投与毒性に関する無影響量(NOEL)は雌雄とも60 mg/kg/day未満と判断された.雄の生殖に及ぼす影響は600 mg/kg/day投与でも認められず,無影響量は600 mg/kg/dayと判断された.雌の生殖に及ぼす影響は600 mg/kg/day投与で平均性周期が延長したことから,無影響量は200 mg/kg/dayと判断された.児動物の発生・発育に及ぼす影響は600 mg/kg/day投与で発育抑制が認められ,生後4日生存率が低値傾向を示し,無影響量は200 mg/kg/dayと判断された.
方法
1. 被験物質
2,2,6,6-テトラメチル-4-ヒドロキシピペリジン〔別名TAAM,三井石油化学工業 製造,Lot No. 650905,純度99.8 wt%,分子量157.26,融点129℃〕は,白色の顆粒であり,使用時まで室温で遮光下密栓保管した.本ロットは,投与期間中安定であったことを確認した.
製造,Lot No. 650905,純度99.8 wt%,分子量157.26,融点129℃〕は,白色の顆粒であり,使用時まで室温で遮光下密栓保管した.本ロットは,投与期間中安定であったことを確認した.
被験物質は,注射用蒸留水( 大塚製薬工場製)に溶解し,6,20および60 mg/mLの濃度になるよう各群の投与液を調製した.調製後は,使用時まで冷暗条件下で密閉保管した.調製液中の被験物質は,6 mg/mL溶液の場合冷暗条件下で少なくとも7日間安定であることを確認した.
大塚製薬工場製)に溶解し,6,20および60 mg/mLの濃度になるよう各群の投与液を調製した.調製後は,使用時まで冷暗条件下で密閉保管した.調製液中の被験物質は,6 mg/mL溶液の場合冷暗条件下で少なくとも7日間安定であることを確認した.
投与液の濃度および均一性の分析は,調製開始時に調製した各群のバッチから無作為にサンプルを抽出し実施した.その結果,誤差範囲が設定濃度の-2.70〜0.68 %であり,基準範囲内(±10 %以内)であった.したがって,投与液にはほぼ所定量の2,2,6,6-テトラメチル-4-ヒドロキシピペリジンが含有されており,適切に混合されていたことを確認した.
2. 使用動物および飼育条件
試験には,日本チャールス・リバー から購入した生後8週齢のSprague-Dawley(Crj:CD(SD), SPF)系雌雄ラットを使用した.購入した動物は7日間検疫・馴化飼育した後,一般状態に異常が認められなかったものを10週齢で群分けして試験に用いた.群分け時の体重は,雄で359〜400 g,雌で 227〜282 gの範囲であった.
から購入した生後8週齢のSprague-Dawley(Crj:CD(SD), SPF)系雌雄ラットを使用した.購入した動物は7日間検疫・馴化飼育した後,一般状態に異常が認められなかったものを10週齢で群分けして試験に用いた.群分け時の体重は,雄で359〜400 g,雌で 227〜282 gの範囲であった.
動物は,温度24±2℃,湿度55±10 %,換気回数15回/時間,照度150〜300 lux,照明時間12時間(午前7時点灯,午後7時消灯)に設定されたバリアシステムの飼育室でアルミ製前面・床ステンレス網目飼育ケージに1匹ずつ収容し飼育した.妊娠18日以降の母動物は哺育4日までアルミ製前面・床ステンレス網目飼育ケージに哺育トレーおよび巣作り材料(CareFRESH TM)を入れて飼育した.
飼料は,オリエンタル酵母工業 製造のNMF固型飼料(放射線滅菌飼料)を使用し,飼育期間中自由に摂取させた.飲水は,水道水を自由に摂取させた.
製造のNMF固型飼料(放射線滅菌飼料)を使用し,飼育期間中自由に摂取させた.飲水は,水道水を自由に摂取させた.
3. 群分け
動物は投与開始日の体重をもとに層別化し,無作為抽出法により1群当たり12匹を振り分けた.
4. 投与量,群構成,投与期間および投与方法
本試験の用量は先に実施した予備試験「2,2,6,6-テトラメチル-4-ヒドロキシピペリジンのラットを用いる反復投与毒性・生殖発生毒性併合試験-2週間毒性試験(試験番号 3184)」の結果を参考にして決定した.すなわち,0,20,60,200および600 mg/kgを雄および雌に14日間連続経口投与した結果,雄の600 mg/kg群で投与11日に1例死亡した.一般状態の変化として,投与後に眼瞼下垂および自発運動低下が200および600 mg/kg群で雌雄ともに全例に観察され,散瞳および流涎が200 mg/kg群で少数例に,600 mg/kg群でほぼ全例に観察された.その他,縮瞳が200および600 mg/kg群で少数例に観察された.また,600 mg/kg群の雄に体重増加抑制が認められ,同群の雌雄で投与1から3日の平均1日摂餌量が低値を示した.雄の血液学検査では600 mg/kg群で好中球比率が高値を示し,リンパ球比率が低値を示した.血液生化学検査では60 mg/kg以上の投与群で総コレステロールが高値を示したが,対照群の値が背景値に比べ低かったため被験物質投与の影響かどうかは明らかではなかった.剖検では,雌雄のいずれの投与群にも被験物質投与の影響と考えられる所見は認められなかった.剖検時の器官重量では,雄の600 mg/kg群で肝臓の絶対重量が低値を示した.以上の結果から,本試験の最高用量を明らかな毒性兆候が現れることが予想される600 mg/kgに設定し,以下公比3で除し,200および60 mg/kgを設定した.
投与容量は,体重100 g当り1 mLとし,交配前および交配期間中の雌雄では,個体別に測定した最新体重に基づいて算出を行った.また,妊娠期間および哺育期間中の雌は,妊娠0,7,14,21および哺育0日に測定した個体別体重に基づいて算出を行った.胃ゾンデを用いて毎日1回(7日/週)強制経口投与した.対照群には注射用蒸留水のみを同様に投与した.
雄の投与期間は,交配前14日間と交配期間14日間および交配期間終了後20日間の連続48日間とした.雌の投与期間は,交配前14日間と交配期間中(最長14日間)ならびに交尾雌の妊娠期間を通じて分娩後の哺育3日まで(41〜52日間)とした.なお,交尾しなかった雌は交配期間終了後20日間の連続48日間とした.
1)一般状態
雌雄とも,全例について試験期間中毎日観察した.
2) 体重
雄では,投与1(投与開始日),8,15,22,29,36,43および49日(剖検日)に測定し,投与1から43日までの体重増加量を算出した.雌では,投与1(投与開始日),8および15日に測定し,投与1から15日までの体重増加量を算出した.交尾成立後の雌は,妊娠0,7,14および21日に,分娩した雌は哺育0および4日に測定し,それぞれ妊娠0から21日および哺育0から4日までの体重増加量を算出した.
3) 摂餌量
雄では,投与1(投与開始日),8,15,22,29,36,43および48日(剖検前日)に餌重量を測定し,測定日から次の測定日までの間の摂餌量を求め平均1日摂餌量を算出するとともに投与1から15日および投与22から48日までの累積摂餌量を算出した.雌では,投与1(投与開始日),8および15日に餌重量を測定し,測定日から次の測定日までの摂餌量を求め平均1日摂餌量を算出するとともに投与1から15日までの累積摂餌量を算出した.また,交尾成立の雌は妊娠0,7,14および21日に,分娩した雌は哺育0および4日に餌重量を測定し,測定日から次の測定日までの間の摂餌量を求め平均1日摂餌量を算出するとともにそれぞれ妊娠0から21日および哺育0から4日までの累積摂餌量を算出した.なお,交配期間中の摂餌量は測定しなかった.
4) 交配
交配前14日間の性周期観察を行った雌を同群内の雄のケージに入れ1対1で最長14日間毎晩同居させた.翌朝,腟垢中の精子確認をもって交尾が成立したとし,その日を妊娠0日とした.性周期観察は交尾成立日まで行い,発情期から次の発情期までの間の日数を性周期日数として平均性周期を算出した.交配結果から,各群について交尾率[(交尾動物数/同居動物数)×100]を算出した.
5) 自然分娩時および新生児の観察
妊娠動物は全例を自然分娩させた.分娩の確認は午前9〜10時に行い,この時間帯に分娩が完了していることを確認した個体についてその日を哺育0日とした.午前10時を過ぎて分娩が完了した個体については,翌日を哺育0日とした.分娩を確認した全例について妊娠期間(哺育0日の年月日から妊娠0日の年月日を減じた日数),受胎率[(受胎動物数/交尾動物数)×100)],出産率[(生児出産雌数/妊娠雌数)×100〕,着床率[(着床痕数/妊娠黄体数)×100)〕,分娩率[(総出産児数/着床痕数)×100〕,出生率[(出産生児数/総出産児数)×100)〕を算出した.妊娠25日の午前9時までに分娩のみられない動物は病理解剖した.母動物は哺育4日に病理解剖した.
新生児は哺育0日に出産児数(生存児+死亡児)を調べ,性別を判定するとともに外表異常の有無を調べた.また,哺育0および4日に雌雄個体別の重量を測定し,1腹の雌雄別平均体重を算出した.
哺育4日に出生児の重量を測定後,全例をエーテル麻酔により安楽死させ,主要器官の肉眼観察を行った.なお,哺育期間中の死亡児についても同様に主要器官の肉眼観察を行った.また,出生児の4日生存率[(哺育4日生児数/出産生児数)×100〕を求めた.
6) 臨床検査
各群の雄全例について剖検時に実施した.動物を最終投与日(投与期間:48日間)の夕方から翌朝まで約16時間絶食させた後,エーテル麻酔下で開腹し,腹部大動脈から採血した.
a) 血液学検査
検査はEDTA-3Kを添加した初血について,THMS H・1E(米国マイルス社)を用いて白血球数(WBC:暗視野板法),赤血球数(RBC:暗視野板法),ヘマトクリット値(HCT:全赤血球の容積により補正),ヘモグロビン量(HGB:シアンメトヘモグロビン法),平均赤血球容積(MCV:暗視野板法),平均赤血球血色素量(MCH:HGB,RBCより算出),平均赤血球血色素濃度(MCHC:HGB,HCTより算出),血小板数(PLT:暗視野板法)および白血球百分率(フローサイトケミストリー法)を測定した.白血球百分率は前述の機器で測定したが,別途血液塗抹標本を作製し,メイ・グリュンワルド・ギムザ染色して保管した.網赤血球(RC)比率の算定については,EDTA-3K添加血液をニューメチレンブルーで染色後,血液塗沫標本を作製した.各群とも貧血傾向が認められなかったため,標本の観察は行わなかった.
b) 血液凝固能検査
検査にはクエン酸ソーダ添加血液を3000 r.p.m.,13分間遠心分離して得た血漿について,血液凝固測定装置 KC-40(独国アメルング社)を用いてプロトロンビン時間(PT:Quick 1段法),活性化部分トロンボプラスチン時間(APTT:クロット法)およびフィブリノーゲン量(Fibrinogen:トロンビン時間法)を測定した.
c) 血液生化学検査
検査はクリーンシール( ヤトロン)に血液を採取し,30分間静置後3000 r.p.m. 7分間遠心分離して得た血清について,多項目生化学自動分析装置CentrifiChem ENCORE
ヤトロン)に血液を採取し,30分間静置後3000 r.p.m. 7分間遠心分離して得た血清について,多項目生化学自動分析装置CentrifiChem ENCORE (米国ベーカー社)およびEKTACHEM 700N(米国コダック社)を用いて総蛋白(ビューレット法),アルブミン(B.C.G.法),A/G(計算値),血糖(グルコースオキシダーゼ法),中性脂肪(酵素色素法),総コレステロール(コレステロールオキシダーゼ法),尿素窒素(ウレアーゼアンモニウム指示薬法),クレアチニン(Jaff
(米国ベーカー社)およびEKTACHEM 700N(米国コダック社)を用いて総蛋白(ビューレット法),アルブミン(B.C.G.法),A/G(計算値),血糖(グルコースオキシダーゼ法),中性脂肪(酵素色素法),総コレステロール(コレステロールオキシダーゼ法),尿素窒素(ウレアーゼアンモニウム指示薬法),クレアチニン(Jaff 法),総ビリルビン(ジアゾ法),グルタミン酸オキザロ酢酸トランスアミナーゼ(IFCC法),グルタミン酸ピルビン酸トランスアミナーゼ(IFCC法),γ -グルタミルトランスペプチダーゼ(Orl謡ski法),ナトリウム(電極法),カリウム(電極法),塩素(電極法),カルシウム(アルセナゾ
法),総ビリルビン(ジアゾ法),グルタミン酸オキザロ酢酸トランスアミナーゼ(IFCC法),グルタミン酸ピルビン酸トランスアミナーゼ(IFCC法),γ -グルタミルトランスペプチダーゼ(Orl謡ski法),ナトリウム(電極法),カリウム(電極法),塩素(電極法),カルシウム(アルセナゾ 法)および無機リン(モリブデン酸青法)を測定した.
法)および無機リン(モリブデン酸青法)を測定した.
7) 病理学検査
a) 剖検および器官重量
 死亡動物
死亡動物
剖検では主要器官の肉眼的観察を行い,皮膚,乳腺,リンパ節,唾液腺,胸骨,大腿骨(骨髄を含む),胸腺,気管,肺および気管支,心臓,甲状腺および上皮小体,舌,食道,胃,十二指腸,小腸,大腸,肝臓,膵臓,脾臓,腎臓,副腎,膀胱,精嚢,前立腺,眼球,ハーダー腺,脳,下垂体および脊髄を10 %中性緩衝ホルマリン液で固定した.精巣および精巣上体はブアン氏液に固定した.
 雄動物
雄動物
48日間投与した日の夕方から,約16時間絶食をさせた後エーテル麻酔下で採血し安楽死させた.主要器官の肉眼的観察を行った後,脳,胸腺,肝臓,腎臓,脾臓,副腎,精巣および精巣上体重量を測定し器官重量・体重比(相対重量)を算出した.また,全動物の重量測定器官に加えて心臓,精嚢,前立腺および下垂体を10 %中性緩衝ホルマリン液で固定した.なお,精巣および精巣上体はブアン氏液で固定した.
 自然分娩した雌
自然分娩した雌
哺育4日にエーテル麻酔下で放血安楽死させた.主要器官の肉眼的観察を行った後,脳,胸腺,肝臓,腎臓,脾臓,副腎および卵巣重量を測定し器官重量・体重比(相対重量)を算出した.また,全動物の重量測定器官に加えて心臓,下垂体および肉眼所見として変化が認められた器官・組織として皮膚を10 %中性緩衝ホルマリン液で固定した.また,剖検時に黄体数および着床痕数を調べた.
 交尾の成立しなかった雌
交尾の成立しなかった雌
48日間投与した翌日,エーテル麻酔下で放血安楽死させ,器官・組織の肉眼的観察を行った後,皮膚,乳腺,リンパ節,唾液腺,胸骨,大腿骨(骨髄を含む),胸腺,気管,肺および気管支,心臓,甲状腺および上皮小体,舌,食道,胃,十二指腸,小腸,大腸,肝臓,膵臓,脾臓,腎臓,副腎,膀胱,卵巣,子宮,腟,眼球,ハーダー腺,脳,下垂体および脊髄を10 %中性緩衝ホルマリン液で固定した.
 哺育期間中に全児が死亡した母動物(全児死亡動物)
哺育期間中に全児が死亡した母動物(全児死亡動物)
生存児すべての死亡または喰殺が確認された翌日にエーテル麻酔下で放血安楽死させ,器官・組織の肉眼的観察を行った後,皮膚,乳腺,リンパ節,唾液腺,胸骨,大腿骨(骨髄を含む),胸腺,気管,肺および気管支,心臓,甲状腺および上皮小体,舌,食道,胃,十二指腸,小腸,大腸,肝臓,膵臓,脾臓,腎臓,副腎,膀胱,卵巣,子宮,腟,眼球,ハーダー腺,脳,下垂体および脊髄を10 %中性緩衝ホルマリン液で固定した.なお,剖検時に黄体数および着床痕数を調べた.
b) 病理組織学検査
 死亡動物および全児死亡動物
死亡動物および全児死亡動物
死亡動物(雄の600 mg/kg群の3例,雌の60および600 mg/kg群の各1例)および全児死亡動物(雌の600 mg/kg群の1例)の皮膚,乳腺,リンパ節,唾液腺,胸骨,大腿骨(骨髄を含む),胸腺,気管,肺および気管支,心臓,甲状腺および上皮小体,舌,食道,胃,十二指腸,小腸,大腸,肝臓,膵臓,脾臓,腎臓,副腎,膀胱,精嚢,前立腺,精巣,精巣上体,卵巣,子宮,腟,眼球,ハーダー腺,脳,下垂体および脊髄について実施した.
 妊娠を成立させた雄
妊娠を成立させた雄
対照群と高用量群では脳,胸腺,心臓,肝臓,腎臓,脾臓,副腎および精巣について実施し,低および中用量群では腎臓について実施した.
 自然分娩した雌
自然分娩した雌
対照群と高用量群では脳,胸腺,心臓,肝臓,腎臓,脾臓,副腎および卵巣について実施し,加えて高用量群の1例の皮膚について実施した.また,低および中用量群では腎臓について実施した.
 交尾の成立しなかった雄雌
交尾の成立しなかった雄雌
600 mg/kg群の雌雄各1例の脳,胸腺,心臓,肝臓,腎臓,脾臓,副腎,腟,子宮,卵巣,精巣,精巣上体,精嚢,前立腺,下垂体について実施した.脳,胸腺,心臓,肺,胃,肝臓,腎臓,脾臓,副腎,腟,子宮,卵巣,精巣,精巣上体,精嚢,前立腺,下垂体および腹腔の塊について実施した.
5. 統計解析
体重,摂餌量,黄体数,着床痕数,出産児数,死産児数,性比,平均性周期,妊娠期間,着床率,分娩率,出生率,外表異常発現率,新生児の4日の生存率,器官重量,器官重量・体重比(相対重量),血液学的および血液生化学検査値については多重比較検定1-3)を行った.
出産率,交尾率および受胎率についてはc 2検定4,5)を用いた.病理学検査の所見の発生率については,Fisherの直接確率検定法5)を用いて検定し,グレードのある所見は,−を「1」,+1を「2」,+2を「3」および+3を「4」に割り当てた後,順位和検定であるMann-WhitneyのU検定5)を用いて検定した.なお,哺育期間中の新生児に関する成績は1母体当りの平均を1標本とした.有意水準は *:P<0.05および**:P<0.01の2段階とした.
結果
1. 反復投与毒性
1) 死亡および一般状態
死亡例が雄では,600 mg/kg群で投与6および9日に1および2例観察された.雌では,60 mg/kg群で投与16日に1例,600 mg/kg群で投与3日に1例観察された.
雄の一般状態の変化では,投与後の症状として,すべての被験物質投与群で散瞳および眼瞼下垂が認められた.散瞳は60 mg/kg群の1例でごくまれに,200 mg/kg群のほぼ全例で散発的に,600 mg/kg群の全例で毎日観察され,発現の強さは60 mg/kg群で軽度,200および600 mg/kg群で軽度から重度であった.眼瞼下垂は60 mg/kg群のほぼ全例で散発的に,200および600 mg/kg群の全例で毎日観察され,発現の強さは60 mg/kg群で軽度,200 mg/kg群で軽度から中等度,600 mg/kg群で軽度から重度であった.また,これらの症状の発現はいずれの群も投与後30分から認められ,60 mg/kg群では投与後2時間,200 mg/kg群では投与後4時間以内にほぼ消失したが,600 mg/kg群では投与後2時間でもっとも強く発現し,投与後6時間でもほぼ全例が軽度または中等度の症状を呈していた.また,自発運動低下が600 mg/kg群で交配前・交配期間中ほぼ全例で低頻度に認められた.その他,脱毛が60 mg/kg群で交配前・交配期間中に1例(両前肢),600 mg/kg群の死亡例に被毛の汚れ,体温低下,眼分泌物,鼻分泌物,流涎,腹臥位,よろめき歩行および振戦が1から3例に認められた.
雌の一般状態の変化では,投与後の症状として,すべての被験物質投与群で散瞳および眼瞼下垂が認められた.散瞳は,60 mg/kg群の1例で投与期間中ごくまれに,200 mg/kg群の少数例で妊娠期間までは散発的,哺育期間では毎日,600 mg/kg群のほぼ全例で投与期間中毎日観察された.眼瞼下垂は60 mg/kg群では交配前・交配期間中はほぼ全例に毎日,妊娠期間はほぼ全例で散発的に,哺育期間は少数例で散発的に,200および600 mg/kg群では全例に投与期間中ほぼ毎日観察された.その他交配前・交配期間では,体温低下および自発運動低下が600 mg/kg群で少数例に,同群の交尾不成立の雌で削痩,軟便および流涎が認められた.妊娠期間では,脱毛(胸部,両前肢)が600 mg/kg群で1例,自発運動低下が200 mg/kg群で1例,600 mg/kg群で4例,血尿が60 mg/kg群で1例,流涎が600 mg/kg群で1例認められた.哺育期間では,全児死亡が600 mg/kg群で哺育2日に1例,自発運動低下が600 mg/kg群で哺育0日に1例認めらた.
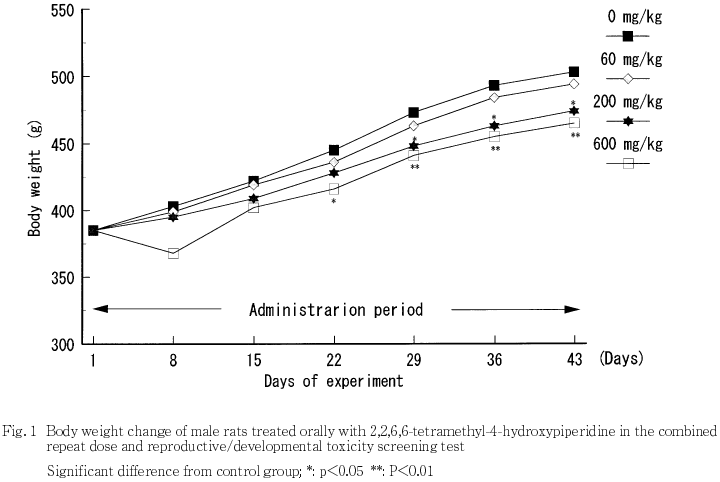
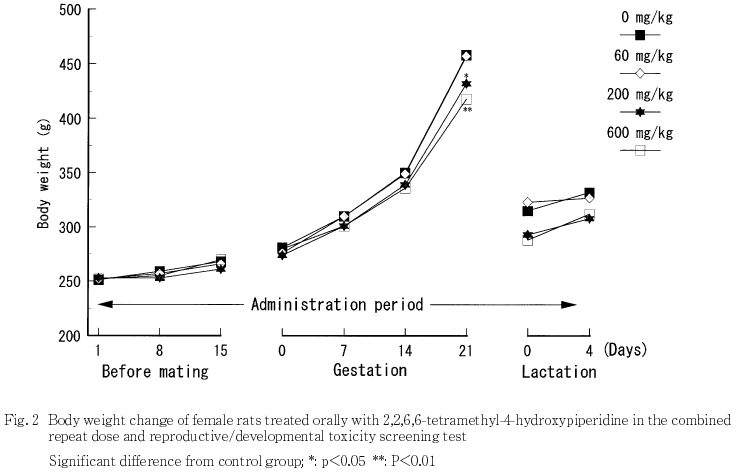
2) 体重(Fig.1,2)
雄では,対照群に比べて200 mg/kg群で投与29日以降,600 mg/kg群では投与22日以降に低値を示し,両群ともに投与1〜43日の体重増加量も低値を示した.雌の交配前投与期間では対照群と被験物質投与群との間に差は認められなかった.妊娠期間では,対照群に比べて200および600 mg/kg群で妊娠21日に低値を示し,両群ともに妊娠0〜21日の体重増加量も低値を示した.哺育期間では,対照群と被験物質投与群との間に差は認められなかった.
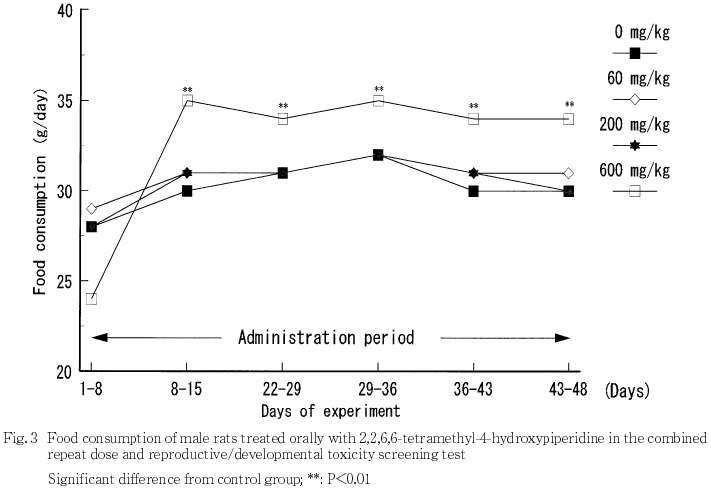
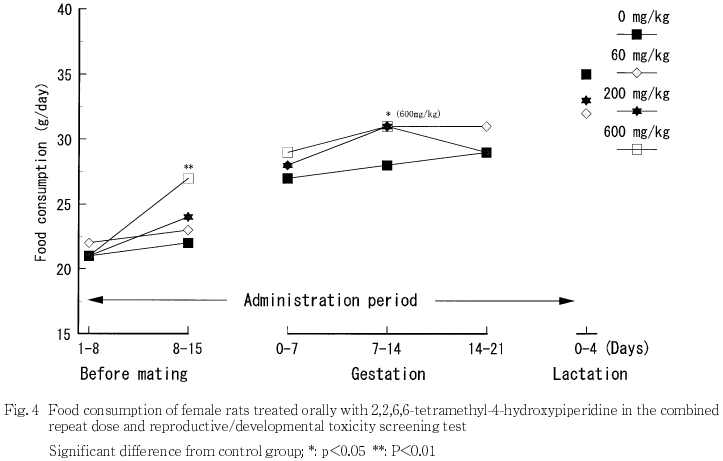
3) 摂餌量(Fig.3,4)
雄では,対照群に比べて600 mg/kg群で投与8日以降高値を示し,投与22〜48日の累積摂餌量も高値を示した.
雌の交配前期間では,対照群に比べ600 mg/kg群で投与8から15日の平均1日摂餌量が高値を示し,投与1〜15日の累積摂餌量も高値を示した.妊娠期間では,同群で妊娠7から14日の平均1日摂餌量が高値を示した.哺育期間では,対照群と被験物質投与群との間に差は認められなかった.
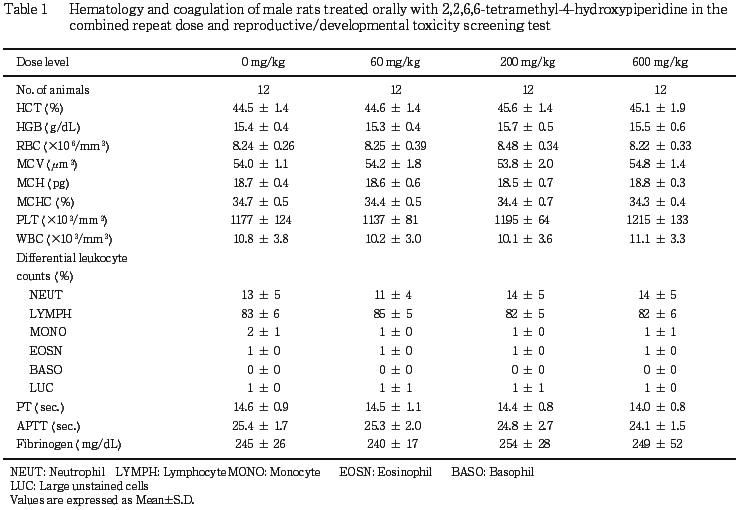
4) 雄の血液学検査(Table 1)
血液学検査および血液凝固能検査では,いずれの検査項目についても対照群と被験物質投与群との間に差は認められなかった.
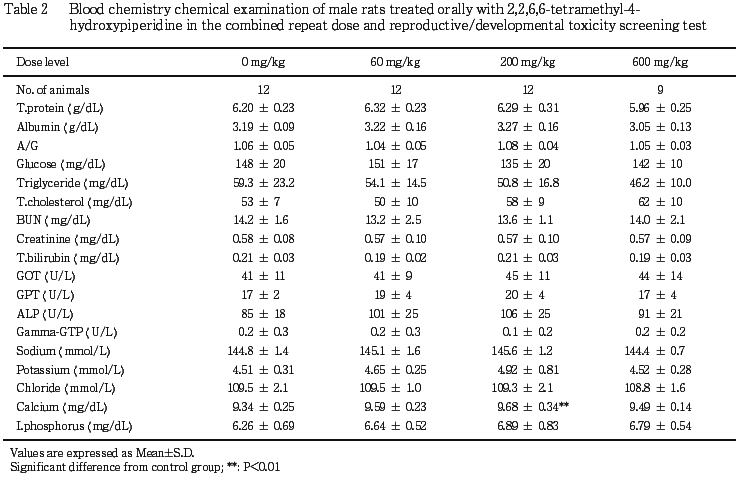
5) 雄の血液生化学検査(Table 2)
200 mg/kg群で対照群に比べカルシウムが高値を示したが,用量に関連した変化ではなかった.他の検査項目では対照群と被験物質投与群との間に差は認められなかった.
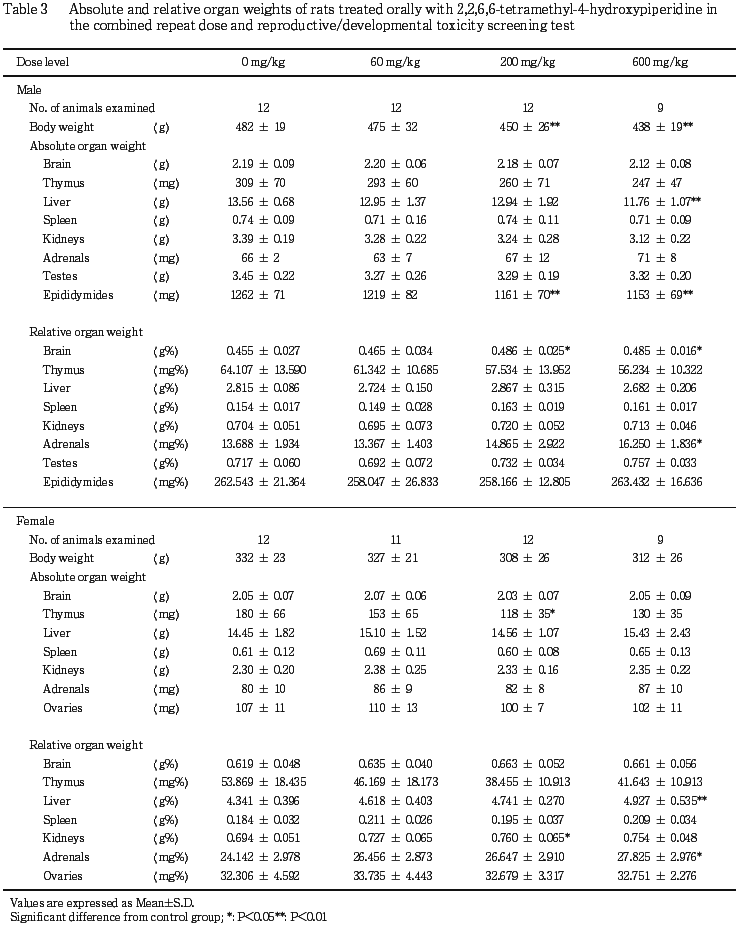
6) 器官重量(Table 3)
雌雄ともに対照群に比べ600 mg/kg群で副腎の相対重量が高値を示し,絶対重量も高値傾向を示した.さらに雌では600 mg/kg群で肝臓の相対重量が高値を示し,絶対重量も高値傾向を示した.その他,体重の低値に起因すると考えられる変化として雄では200および600 mg/kg群で脳の相対重量が高値を,精巣上体の絶対重量が低値を示し,さらに600 mg/kg群で肝臓の絶対重量が低値を示した.雌では,対照群に比べ200 mg/kg群で胸腺の絶対重量が低値を示し,腎臓の相対重量が高値を示した.
7) 剖検所見
死亡例は,雄の600 mg/kg群で3例,雌の60および600 mg/kg群で各1例であった.雄の死亡例の剖検では1例に胃の穿孔性潰瘍,内腔拡大および肝臓との癒着,小腸の内腔拡大および赤色斑点,大腸の内腔拡大および内容物の赤色化,腹水貯留,胸腺の萎縮および全身性の削痩が観察された.その他2例の雄では,胸腺の赤色斑点,肺の赤色化,胃の内容物の赤色化,小腸ならびに大腸の内腔拡大および内容物の赤色化,大腸の赤色斑点,胸水貯留,全身性の削痩がいずれかの1例,膀胱の内腔拡大が2例に観察された.雌の死亡例の剖検では,60 mg/kg群の1例に胸腺および肺の赤色斑点,胃の内腔拡大および内容物の赤色化および小腸の内容物の赤色化が,600 mg/kg群の1例に胸腺および肺の赤色斑点,胃および小腸の赤色化,肝臓の黒色斑点が観察された.
雄では,200 mg/kg群で肺の褐色斑点および横隔膜との癒着が各1例,腎臓の瘢痕および嚢胞が1例,600 mg/kg群で精巣上体の黄色結節が1例に観察された.
雌では,対照群で腎臓の瘢痕および肺の赤色斑点が同一個体の1例に,胸腺の赤色斑点および肺の褐色斑点が各1例,60 mg/kg群で卵巣の嚢胞が2例,600 mg/kg群で胸腺の赤色斑点および卵巣の嚢胞が同一個体の1例に,脱毛が1例に観察された.
交尾の成立しなかった動物は600 mg/kg群で雌雄各1例であった.剖検で異常は認められなかった.
全児死亡動物は600 mg/kg群で1例認められ,胸腺の萎縮が観察された.
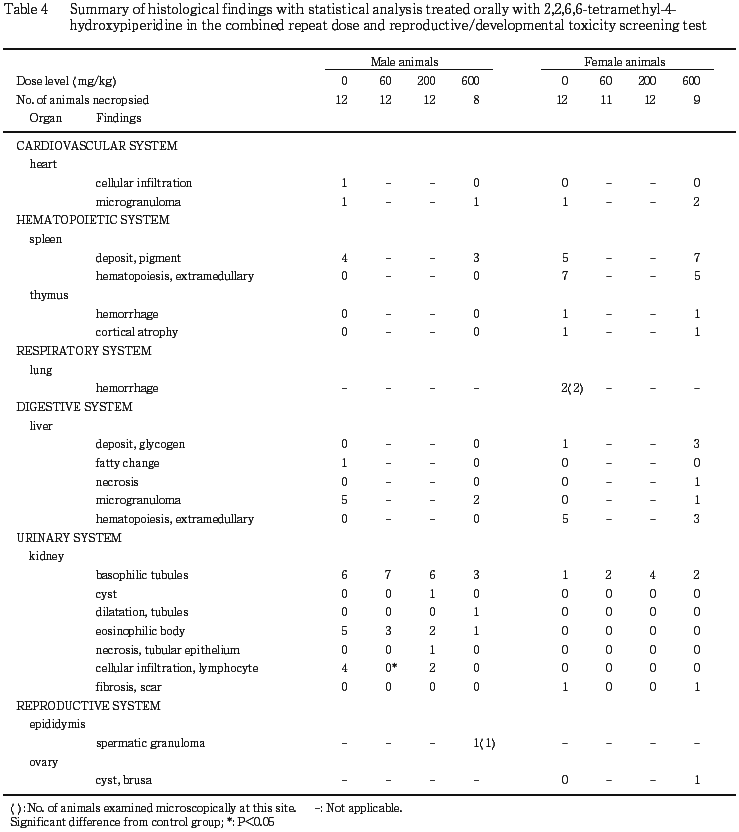
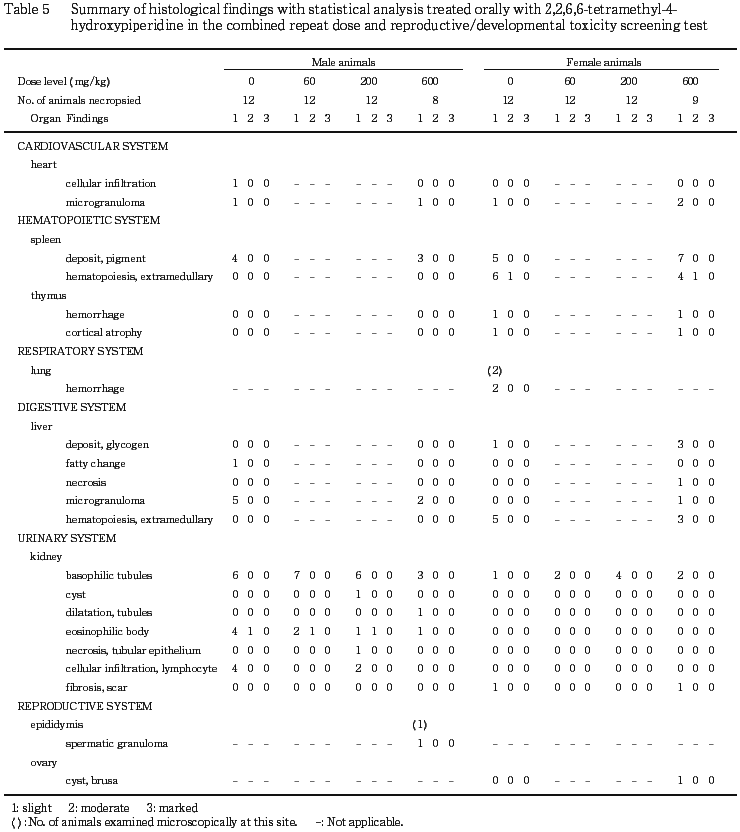
8) 病理組織学検査(Table 4,5)
600 mg/kg群の死亡動物で雌雄に共通して腎臓の皮質ないし皮髄境界部における尿細管上皮の空胞変性が認められ,被験物質投与の影響が示唆された.その他これら死亡動物の腎臓には,皮髄境界部の尿細管上皮の壊死および尿細管上皮の好塩基化が雌雄に,硝子円柱が雄に観察された.また,600 mg/kg群の死亡動物では空胞変性が腎臓以外の臓器にも認められ,全例の脾臓および唾液腺,雌雄各1例の膵臓の外分泌腺および肺,雌1例および雄2例の毛嚢,雄1例の舌,前胃,肝臓,胸腺および上皮小体にそれぞれ空胞変性が観察された.これら600 mg/kg群の死亡例に観察された空胞は中性脂肪とは異なり,大小の球状空胞形成が数個から多数認められ,内部に弱好酸性の無構造もしくは網状構造物が認められるものも存在しており,リン脂質様であった.さらに,これらの動物には腺胃の潰瘍および胸腺の萎縮が雄の全例に,骨髄の造血低下ならびに脾臓の萎縮が雌雄とも全例に,胸腺の核崩壊ならびに肝臓の壊死が雌雄各1例に観察された.
60 mg/kg群の死亡動物の雌1例では600 mg/kg群の死亡動物と同様な腎臓の皮髄境界部と膵臓の外分泌腺の空胞変性が観察された他,胸腺の出血も観察された.その他観察された所見は単発性の発生であった.600 mg/kg群の全児死亡動物では,腺胃の浮腫,細胞浸潤,糜爛ならびに上皮の再生,肺では巣状の浮腫,気管支上皮の糜爛や扁平上皮化生ならびに線維化,胸腺の萎縮が観察された.
雄では,腎臓の尿細管の好塩基化が対照群,60,200および600 mg/kg群でそれぞれ6,7,6および3例,好酸性小体がそれぞれ5,3,2および1例,リンパ球浸潤がそれぞれ4,0,2および0例,巣状の尿細管上皮の壊死が200 mg/kg群で1例に観察され,リンパ球浸潤の60 mg/kg群の発現率が対照群に比べ低値を示した.さらに肝臓の小肉芽腫が対照群および600 mg/kg群でそれぞれ5および2例,脾臓の色素沈着が4および3例,精巣上体の精子肉芽腫が600 mg/kg群で1例に観察された.その他観察された所見は単発性の所見であった.なお,死亡動物の腎臓で認められた空胞変性は生存例の雄では観察されなかった.
雌では,腎臓の尿細管の好塩基化が対照群,60,200および600 mg/kg群でそれぞれ1,2,4および2例,脾臓の色素沈着が対照群および600 mg/kg群でそれぞれ5および7例,脾臓の髄外造血が7および5例,肝臓の糖質沈着が1および3例,肝臓の髄外造血が5および3例,心臓の小肉芽腫が1および2例に観察された.生存例の雌にも死亡動物の腎臓で認められた空胞変性は観察されなかった.
交尾の成立しなかった雌雄動物では,脾臓の色素沈着が雌雄に,腎臓の尿細管の好塩基化および好酸性小体の出現が雄,肝臓の小肉芽腫が雌で観察された.死亡した10 mg/kg群の雄の1例には肺の鬱血,細胞浸潤および肝臓の鬱血が,100 mg/kg群の雄の1例には肺の鬱血および前胃の角化亢進がそれぞれ認められたが,死因については不明であった.
2. 生殖発生毒性
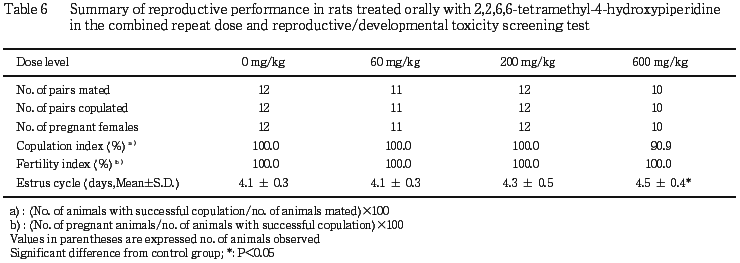
1) 交尾および受胎能(Table 6)
交尾は 600 mg/kg群を除き対照群を含むすべての群で全例成立した.600 mg/kg群では1組が交尾不成立であり,交尾率は90.9 %であった.受胎は全ての群の交尾成立雌で成立した.
性周期観察では,600 mg/kg群で連続した発情休止期像が観察される性周期の停止が3例に認められ,対照群に比べ平均性周期の延長が認められた.
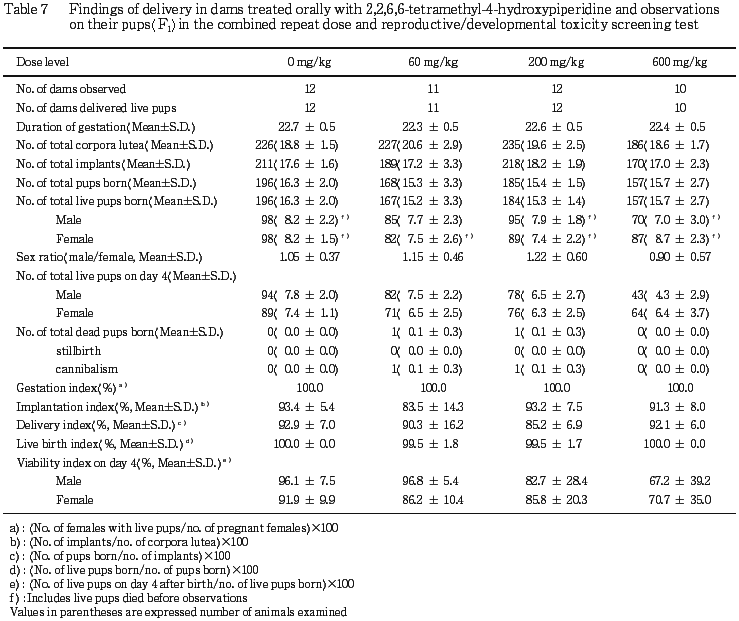
2) 分娩および哺育(Table 7)
600 mg/kg群で対照群に比べ雌雄の哺育4日生児数が低値傾向を示し,4日生存率も低値傾向を示した.その他,妊娠期間,妊娠黄体数,着床痕数,出産児数,出産生児数,性比,死産児数,着床率,分娩率および出生率に群間差は認められなかった.
3) 新生児の形態,体重および剖検所見
新生児の外表検査では,600 mg/kg群で皮下出血が1例認められたのみであった.哺育期間中の体重では,生後0日に対照群に比べ600 mg/kg群で雌雄とも低値を,生後4日に雌雄とも低値傾向を示した.死亡児の剖検では,200 mg/kg群の雄の1例に腎盂拡大が観察された.哺育4日の剖検で,雄では対照群で胸腺頸部残留が5例および肝臓の結節が1例,60 mg/kg群で腎臓の腎盂拡大が2例に観察された.雌では対照群で腎臓の腎盂拡大が2例,600 mg/kg群で胸腺の頸部残留が1例に観察された.
考察
1. 反復投与毒性
死亡例が,雄では600 mg/kg群の3例,雌では60および600 mg/kg群で各1例に認められた.これら死亡例の病理学検査の結果,600 mg/kg群の剖検所見では胃の穿孔性潰瘍,内容物の赤色化,小腸および大腸の内腔拡大,赤色斑点および内容物の赤色化等が認められ,組織所見では腺胃の潰瘍に伴う所見が認められた.600 mg/kg群の全児死亡動物の腺胃に糜爛が認められた.同一被験物質のラットを用いる急性経口毒性試験では,1690 mg/kg以上の用量群の死亡動物における剖検で,腺胃のび慢性出血や十二指腸の赤色斑点,組織学的検査で腺胃の出血,壊死および空胞変性,十二指腸の浮腫,出血および壊死が観察され,強アルカリ性物質である本被験物質の直接的な影響による消化管出血を死因としている.本試験で600 mg/kg群の死亡例の消化管に認められた上記の所見も被験物質投与による直接的な刺激に起因した変化と考えられた.また,死亡例には共通して腎臓で皮質や皮髄境界部に尿細管上皮の空胞変性が観察され,被験物質投与の影響が示唆された.600 mg/kg群の中には肝臓,脾臓,胸腺,肺,舌,前胃,膵臓,唾液腺および毛嚢にまで空胞変性が観察される例もあった.
一般状態の観察では,投与期間を通じ散瞳および眼瞼下垂が,雌雄ともにすべての被験物質投与群で認められた.これらの症状は用量に関連した発現頻度および持続時間の増強が認められ,被験物質投与による影響と考えられた.また,600 mg/kg群で観察された自発運動低下は低頻度ながら雌雄ともに認められ被験物質投与によるものと考えられた.主に600 mg/kg群の死亡例で認められた流涎,体温低下および削痩は被験物質の影響が強く現れたことによる全身状態の悪化に伴った変化と考えられた.その他,認められた所見はしばしば対照群でも認められるものであり,被験物質投与の影響とは考えなかった.
体重について,雄では200および600 mg/kg群で投与期間の半ばから明らかな低値を示し,被験物質投与による体重増加抑制と考えられた.雌では200および600 mg/kg群で妊娠21日に低値を示し被験物質投与の影響が示唆された.摂餌量について,雄では600 mg/kg群で投与開始以降高値を示した.雌では600 mg/kg群で交配前から妊娠期間にかけて高値を示す期間が認められた.いずれも機序は不明であるが被験物質投与の影響が示唆された.
雄の血液学検査,血液凝固能検査および血液生化学検査では,被験物質投与の影響は認められなかった.
器官重量について,雌雄ともに対照群に比べ600 mg/kg群で副腎重量が高値を示し,さらに雌では600 mg/kg群で肝臓重量が高値を示し被験物質投与に起因した変化と考えられた.その他の器官で認められた変化は体重の低値に起因する二次的な変化と考えられた.
病理学検査の結果,妊娠を成立させた雄および自然分娩した雌の剖検所見は,いずれも単発性あるいは少数例の発生であり被験物質投与の影響が示唆される病変は観察されなかった.また,組織所見では腎臓のリンパ球浸潤の発現率が60 mg/kg群で低値を示したが,用量に関連した変化ではないことから被験物質投与の影響とは考えなかった.その他認められた組織所見は群間の発現率に差はなかった.死亡動物の組織所見から被験物質の腎臓への影響が示唆されたが,生存例では腎臓に対する影響は認められなかった.
以上のことから,2,2,6,6-テトラメチル-4-ヒドロキシピペリジンの反復投与により雌の60 mg/kg群および雌雄の600 mg/kg群で死亡例が認められ,投与後の一般状態の変化では 60 mg/kg以上の投与群で眼瞼下垂および散瞳が,600 mg/kg群で自発運動低下が観察された.死亡例には腺胃の潰瘍に伴う所見および腎臓で皮質や皮髄境界部に尿細管上皮の空胞変性が観察された.また,雌雄とも200 mg/kg以上の投与群で体重の増加抑制が,600 mg/kg群で摂餌量の高値が認められた.したがって,雌雄とも無影響量は60 mg/kg/day未満と判断された.
2. 生殖発生毒性
600 mg/kg群で連続した発情休止期像が観察される性周期の停止が3例認められ,平均性周期も延長を示し,被験物質投与の影響が疑われた.交尾率および受胎率に被験物質投与の影響は認められなかった.交尾の成立しなかった動物の病理学検査では特に生殖器系に変化は認められなかった.600 mg/kg群で雌雄の新生児の生後0日体重が低値を示し,4日の生存率が低値傾向を示したことから,被験物質投与による新生児の発育抑制または周産期の母動物の哺育行動に対する影響が疑われた.
その他,出産率,出生率に被験物質投与の影響は認められず,新生児の外表にも被験物質投与の影響は認められなかった.また,死亡児および哺育4日の剖検でも被験物質投与による影響は認められなかった.
以上のことから,2,2,6,6-テトラメチル-4-ヒドロキシピペリジンの雄の生殖に及ぼす影響は600 mg/kg投与でも認められず,無影響量は600 mg/kg/dayと判断された.雌の生殖に及ぼす影響は600 mg/kg投与で平均性周期が延長したことから,無影響量は200 mg/kg/dayと判断された.新生児の発生・発育に及ぼす影響は600 mg/kg投与で発育抑制が認められ,新生児の4日の生存率が低値傾向を示したことから無影響量は200 mg/kg/dayと判断された.
文献
| 1) | C.G. Shayne, S.W. Carrol, "Statics and Experimental Design For Toxicologists," Telford Press, 1986. |
| 2) | 佐野正樹,岡山佳弘,医薬安全性研究会会報,32, 21, (1990). |
| 3) | M. Yoshida, J. J. Soc. Comp. Stat., 1, 111(1988). |
| 4) | 佐久間昭,"薬効評価 −計画と解析−,"東京大学出版会,東京,1977. −計画と解析−,"東京大学出版会,東京,1977. |
| 5) | 石居 進,"生物統計学入門,"培風館,東京,1975. |
| 連絡先 |
| 試験責任者: | 田中亮太 |
| 試験担当者: | 伊藤圭一,大庭耕輔,宮島留美子 |
| 財団法人 食品農医薬品安全性評価センター |
| 〒437-1213 静岡県磐田郡福田町塩新田字荒浜582-2 |
| Tel 0538-58-1266 | Fax 0538-58-1393 | |
| Correspondence |
| Authors: | Ryota Tanaka(Study director),
Keiichi Ito, Kousuke Oba,
Rumiko Miyajima |
| Biosafety Research Center, Foods, Drugs and Pesticides(An-pyo Center) |
| 582-2 Shioshinden Arahama, Fukude-cho, Iwata-gun, Shizuoka, 437-1213, Japan |
| Tel +81-538-58-1266 | Fax +81-538-58-1393 | |
 大塚製薬工場製)に溶解し,6,20および60 mg/mLの濃度になるよう各群の投与液を調製した.調製後は,使用時まで冷暗条件下で密閉保管した.調製液中の被験物質は,6 mg/mL溶液の場合冷暗条件下で少なくとも7日間安定であることを確認した.
大塚製薬工場製)に溶解し,6,20および60 mg/mLの濃度になるよう各群の投与液を調製した.調製後は,使用時まで冷暗条件下で密閉保管した.調製液中の被験物質は,6 mg/mL溶液の場合冷暗条件下で少なくとも7日間安定であることを確認した. 製造,Lot No. 650905,純度99.8 wt%,分子量157.26,融点129℃〕は,白色の顆粒であり,使用時まで室温で遮光下密栓保管した.本ロットは,投与期間中安定であったことを確認した.
製造,Lot No. 650905,純度99.8 wt%,分子量157.26,融点129℃〕は,白色の顆粒であり,使用時まで室温で遮光下密栓保管した.本ロットは,投与期間中安定であったことを確認した. 大塚製薬工場製)に溶解し,6,20および60 mg/mLの濃度になるよう各群の投与液を調製した.調製後は,使用時まで冷暗条件下で密閉保管した.調製液中の被験物質は,6 mg/mL溶液の場合冷暗条件下で少なくとも7日間安定であることを確認した.
大塚製薬工場製)に溶解し,6,20および60 mg/mLの濃度になるよう各群の投与液を調製した.調製後は,使用時まで冷暗条件下で密閉保管した.調製液中の被験物質は,6 mg/mL溶液の場合冷暗条件下で少なくとも7日間安定であることを確認した. から購入した生後8週齢のSprague-Dawley(Crj:CD(SD), SPF)系雌雄ラットを使用した.購入した動物は7日間検疫・馴化飼育した後,一般状態に異常が認められなかったものを10週齢で群分けして試験に用いた.群分け時の体重は,雄で359〜400 g,雌で 227〜282 gの範囲であった.
から購入した生後8週齢のSprague-Dawley(Crj:CD(SD), SPF)系雌雄ラットを使用した.購入した動物は7日間検疫・馴化飼育した後,一般状態に異常が認められなかったものを10週齢で群分けして試験に用いた.群分け時の体重は,雄で359〜400 g,雌で 227〜282 gの範囲であった. 製造のNMF固型飼料(放射線滅菌飼料)を使用し,飼育期間中自由に摂取させた.飲水は,水道水を自由に摂取させた.
製造のNMF固型飼料(放射線滅菌飼料)を使用し,飼育期間中自由に摂取させた.飲水は,水道水を自由に摂取させた. ヤトロン)に血液を採取し,30分間静置後3000 r.p.m. 7分間遠心分離して得た血清について,多項目生化学自動分析装置CentrifiChem ENCORE
ヤトロン)に血液を採取し,30分間静置後3000 r.p.m. 7分間遠心分離して得た血清について,多項目生化学自動分析装置CentrifiChem ENCORE (米国ベーカー社)およびEKTACHEM 700N(米国コダック社)を用いて総蛋白(ビューレット法),アルブミン(B.C.G.法),A/G(計算値),血糖(グルコースオキシダーゼ法),中性脂肪(酵素色素法),総コレステロール(コレステロールオキシダーゼ法),尿素窒素(ウレアーゼアンモニウム指示薬法),クレアチニン(Jaff
(米国ベーカー社)およびEKTACHEM 700N(米国コダック社)を用いて総蛋白(ビューレット法),アルブミン(B.C.G.法),A/G(計算値),血糖(グルコースオキシダーゼ法),中性脂肪(酵素色素法),総コレステロール(コレステロールオキシダーゼ法),尿素窒素(ウレアーゼアンモニウム指示薬法),クレアチニン(Jaff 法),総ビリルビン(ジアゾ法),グルタミン酸オキザロ酢酸トランスアミナーゼ(IFCC法),グルタミン酸ピルビン酸トランスアミナーゼ(IFCC法),γ -グルタミルトランスペプチダーゼ(Orl謡ski法),ナトリウム(電極法),カリウム(電極法),塩素(電極法),カルシウム(アルセナゾ
法),総ビリルビン(ジアゾ法),グルタミン酸オキザロ酢酸トランスアミナーゼ(IFCC法),グルタミン酸ピルビン酸トランスアミナーゼ(IFCC法),γ -グルタミルトランスペプチダーゼ(Orl謡ski法),ナトリウム(電極法),カリウム(電極法),塩素(電極法),カルシウム(アルセナゾ 法)および無機リン(モリブデン酸青法)を測定した.
法)および無機リン(モリブデン酸青法)を測定した. 死亡動物
死亡動物 雄動物
雄動物 自然分娩した雌
自然分娩した雌 交尾の成立しなかった雌
交尾の成立しなかった雌 哺育期間中に全児が死亡した母動物(全児死亡動物)
哺育期間中に全児が死亡した母動物(全児死亡動物) 死亡動物および全児死亡動物
死亡動物および全児死亡動物 妊娠を成立させた雄
妊娠を成立させた雄 自然分娩した雌
自然分娩した雌 交尾の成立しなかった雄雌
交尾の成立しなかった雄雌










 −計画と解析−,"東京大学出版会,東京,1977.
−計画と解析−,"東京大学出版会,東京,1977.