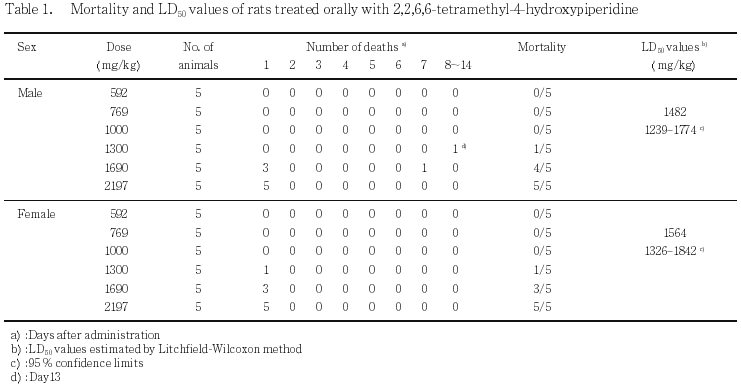
投与量は雌雄ともに592,769,1000,1300,1690 および 2197 mg/kgの6用量とした.
死亡動物は,雌雄とも 1300 mg/kg以上の用量群で投与後3時間以降13日までみられ,その多くが投与翌日に認められた.LD50値(95%信頼限界)は雄が1482(1239〜1774)mg/kg,雌が1564(1326〜1842)mg/kgであった.
一般状態の観察では 雌雄ともすべての用量群で自発運動低下,散瞳および眼瞼下垂がみられ,1300 mg/kg以上の用量群で腹臥位,体温低下,振戦が認められた.さらに雄の 1300 mg/kg群で削痩,腹部膨満および耳介等の蒼白,1690 mg/kg群で立毛,雌の 1690 mg/kg群で腹部膨満,耳介等の蒼白および脱毛が観察された.すべての用量群でみられた自発運動低下,散瞳および眼瞼下垂の多くは投与当日にみられ投与翌日には回復していた.また,2197 mg/kg群の雌雄でみられた散瞳の程度は重度で他の用量群に比較して強いものであった.
生存動物の体重は,1690 mg/kg群の雌雄では投与後7日の測定値が投与前の値に比較して減少したが,その他の用量群においては雌雄とも投与後7および14日の測定で前回の測定値に比較して増加していた.
剖検では,雌雄の死亡動物において腺胃のび漫性出血,十二指腸の赤色斑点が多数認められた.死亡動物の雌雄各1例および観察終了時解剖動物の雌1例について病理組織学検査を行った結果,腺胃に出血,壊死および空胞変性,十二指腸に浮腫,出血,壊死および空胞変性が観察されたことから消化管出血が死因と考えられた.
 )は,白色の顆粒で水に15〜16 %可溶,アセトンに易溶,分子量157.26の物質である.本試験に用いたロット番号6509051の純度は99.8 wt%であった.
)は,白色の顆粒で水に15〜16 %可溶,アセトンに易溶,分子量157.26の物質である.本試験に用いたロット番号6509051の純度は99.8 wt%であった.
 から購入した.動物は検収後,試験環境に馴化し,7週齢で投与した.
から購入した.動物は検収後,試験環境に馴化し,7週齢で投与した.投与時の体重は,雄が 177〜195 g,雌が 139〜153 gであった.
 東京技研サービスの自動水洗式飼育機を使用し,ステンレス製網目飼育ケージに5匹ずつ収容して飼育した.飼育ケージおよび給餌器は週1回取り換えた.動物には,オリエンタル酵母工業
東京技研サービスの自動水洗式飼育機を使用し,ステンレス製網目飼育ケージに5匹ずつ収容して飼育した.飼育ケージおよび給餌器は週1回取り換えた.動物には,オリエンタル酵母工業 製造の固型飼料MFを自由に摂取させ,飲料水としては,水道水を自由に摂取させた.なお,動物飼育期間中の温湿度の実測値は22.4〜23.2℃,51〜61%であり,動物の馴化期間を含め,観察期間中データの信頼性に影響を及ぼしたと思われる環境要因の変化はなかった.
製造の固型飼料MFを自由に摂取させ,飲料水としては,水道水を自由に摂取させた.なお,動物飼育期間中の温湿度の実測値は22.4〜23.2℃,51〜61%であり,動物の馴化期間を含め,観察期間中データの信頼性に影響を及ぼしたと思われる環境要因の変化はなかった.
以上の結果を参考として,本試験では雌雄とも 1000 mg/kgを中心に公比約 1.3で592,769,1000,1300 および 1690 mg/kgの5用量を設定したが,1690 mg/kgの雌雄で生存動物が認められたため,雌雄とも 2197 mg/kgを追加投与し6用量とした.
 大塚製薬工場,ロット番号6B77N)に溶解した.溶液の濃度は,592,769,1000,1300,1690 および 2197 mg/kg群で,それぞれ3.0, 3.8, 5.0, 6.5, 8.5および11.0 w/v%であった.すべての投与群について投与液の濃度分析を
大塚製薬工場,ロット番号6B77N)に溶解した.溶液の濃度は,592,769,1000,1300,1690 および 2197 mg/kg群で,それぞれ3.0, 3.8, 5.0, 6.5, 8.5および11.0 w/v%であった.すべての投与群について投与液の濃度分析を 帝人バイオ・ラボラトリーズで実施した結果,設定濃度の99.6〜104 %の範囲であり,適切に調製されていた.
帝人バイオ・ラボラトリーズで実施した結果,設定濃度の99.6〜104 %の範囲であり,適切に調製されていた.投与経路は経口とし,16時間絶食させた動物に上述の被験物質溶液を注射ポンプおよび胃ゾンデを用い,投与した.投与容量は体重100 gあたり2 mLとし,個体別に測定した体重に基づいて投与容量を算出し,投与した.給餌は被験物質投与3時間後に行った.
全ての用量群でみられた自発運動低下,散瞳および眼瞼下垂の多くは投与日にみられ投与翌日には回復していた.また,2197 mg/kg群の雌雄でみられた散瞳の程度は重度で他の試験群に比較して強いものであった.
その他の用量群においては雌雄とも投与後7および14日の測定で前回の測定値に比較して増加していた.
病理組織学検査は1690 mg/kg群の死亡動物で比較的死後変化の進んでいない雌雄各1例および観察終了時解剖動物の雌1例について胃および十二指腸を対象に行った.その結果,死亡動物の雄では腺胃に出血,壊死および空胞変性,前胃に空胞変性,十二指腸に浮腫,出血および空胞変性が,雌では腺胃に壊死,十二指腸に出血,壊死および空胞変性が観察された.観察終了時解剖動物の雌では腺胃に局所的なびらんが観察され出血および再生像を伴っていた.また,前胃は角化亢進が顕著であったが,十二指腸には異常病変はなかった.
その結果,死亡動物は投与後3時間以降13日までみられ,その多くが投与翌日に認められた.中毒症状として,雌雄とも自発運動低下,散瞳,眼瞼下垂,腹臥位,体温低下,振戦,腹部膨満および耳介等の蒼白,さらに雄で立毛および削痩,雌で脱毛がみられた.これらのうち,自発運動低下,散瞳,眼瞼下垂および振戦は被験物質の直接的な作用,腹臥位および体温低下は死に至る過程でみられた所見と考えられた.
剖検では雌雄の 1690 mg/kg以上の用量群の死亡動物において腺胃のび漫性出血,十二指腸の赤色斑点が多数認められた.1690 mg/kg群の死亡動物の雌雄各1例について病理組織学検査を行った結果,腺胃に出血,壊死および空胞変性,前胃に空胞変性および十二指腸に浮腫,出血,壊死および空胞変性が観察されたことからいずれの動物も消化管出血が死因と考えられた.また,消化管出血を引き起こした原因は本被験物質が強アルカリ性物質(原液;pH 約14,投与液;pH 11.8)であることによるものと考えられた.

| 連絡先 | |||
| 試験責任者: | 山本利男 | ||
| 試験担当者: | 藤島 敦 | ||
| (財)食品農医薬品安全性評価センター | |||
| 〒437-1213 静岡県磐田郡福田町塩新田582-2 | |||
| Tel 0538-58-1266 | Fax 0538-58-1393 | ||
| Correspondence | ||||
| Authors: | Toshio Yamamoto(Study director) Atsushi Fujishima | |||
| Biosafety Research Center, Foods, Drugs and Pesticides(An-Pyo Center) | ||||
| 582-2 Shioshinden, Fukude-cho, Iwata-gun, Shizuoka, 437-1213, Japan | ||||
| Tel +81-538-58-1266 | Fax +81-538-58-1393 | |||