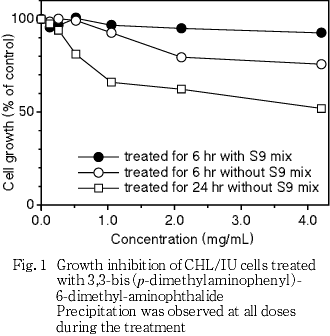
S9 mix非存在下および存在下の短時間処理(6時間処理後18時間の回復時間)ならびに連続処理(24時間処理)において,4.2 mg/mL(10 mmol/L)の濃度においても50 %を越える細胞増殖抑制は認められなかった.従って,すべての処理群で4.2 mg/mL(10 mmol/L)を最高濃度とし,公比2で5濃度設定した.
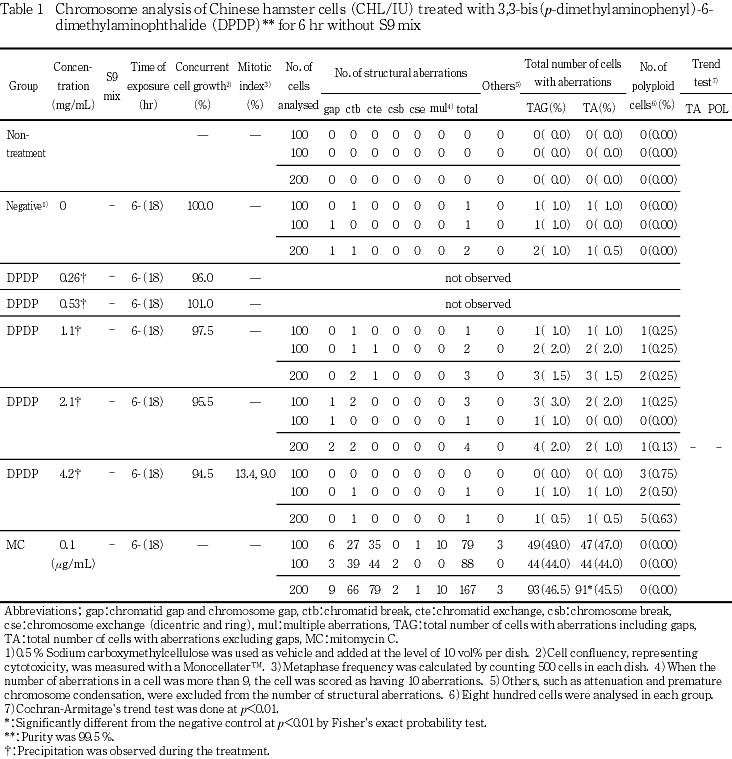
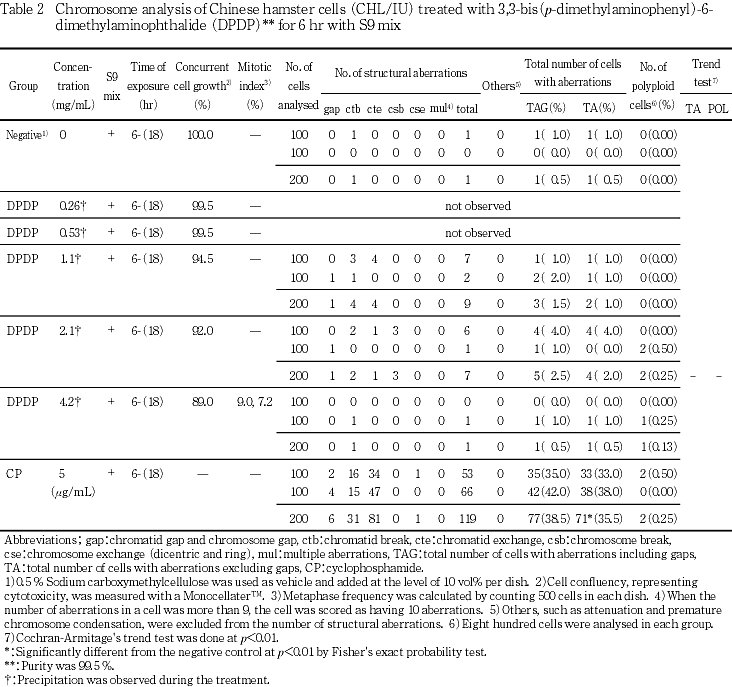
染色体分析はすべての処理系列において1.1〜4.2 mg/mLで行った.その結果,S9 mix非存在下および存在下における短時間処理のいずれの群においても染色体の構造異常および倍数性細胞の誘発作用は認められなかった.
短時間処理で陰性の結果が得られたため,24時間処理を行った.その結果,いずれの群においても染色体の構造異常の誘発作用は認められなかった.倍数性細胞については,高濃度群の4.2 mg/mLにおいて倍数性細胞の有意な増加が認めら得たが,出現頻度は1.93 %と低いことから生物学的には陰性であると判断した.
以上の結果より,本試験条件下で3,3-ビス(p-ジメチルアミノフェニル)-6-ジメチルアミノフタリドは,染色体異常を誘発しない(陰性)と結論した.
その結果,すべての処理系列において最高処理濃度の4.2 mg/mL(10 mmol/L)の濃度においても50 %を越える細胞増殖抑制は認められなかった(Fig. 1).

また,陽性対照物質として用いたマイトマイシンC(MC,協和醗酵工業(株))およびシクロホスファミド(CP,Sigma Chemical Co.)は,日局注射用水((株)大塚製薬工場)に溶解して調製した.それぞれ染色体異常を誘発することが知られている濃度を適用した.
染色体異常試験において,溶媒対照群と処理群では1濃度あたり4枚のディッシュを用いた.このうちの2枚で染色体標本を作製し,残りの2枚については単層培養細胞密度計により細胞増殖率を測定した.無処理対照群および陽性対照群については細胞増殖率測定は行わな かった.
作製したスライド標本のうち,1つのディッシュから得られた異なるスライドを,4名の観察者がそれぞれ処理条件が分からないようにコード化した状態で分析した.染色体の分析は,日本環境変異原学会・哺乳動物試験研究会(MMS)1)による分類法に基づいて行い,染色体型あるいは染色分体型のギャップ,切断,交換などの構造異常の有無と倍数性細胞(polyploid)の有無について観察した.また構造異常については1群200個,倍数性細胞については1群800個の分裂中期細胞を分析した.
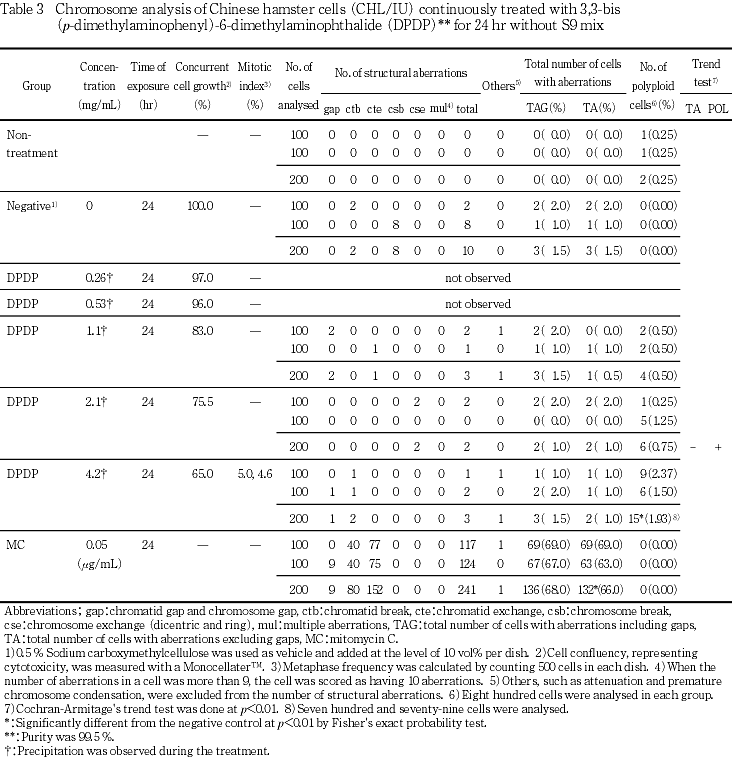
短時間処理で陰性の結果が得られたため,24時間処理を行ったところ,いずれの群(1.1,2.1,4.2 mg/mL)においても染色体の構造異常の誘発作用は認められなかった(Table 3).倍数性細胞については,高濃度群の4.2 mg/mLにおいて倍数性細胞の有意な増加が認められたが,出現頻度は1.93 %と低いことから生物学的には陰性であると判断した.なお,いずれの被験物質処理群においても処理中に沈殿が認められた.
陽性対照物質として用いたMCは,S9 mix非存在下で短時間処理および24時間連続処理した場合において染色体の構造異常を誘発し(Table 1, 3),CPはS9 mix存在下で短時間処理した場合において染色体の構造異常を誘発した(Table 2).これらの陽性対照物質の結果より,本実験系の成立が確認された.
なお,3,3-ビス(p-ジメチルアミノフェニル)-6-ジメチルアミノフタリドは,細菌を用いる復帰変異試験において陰性の結果が得られている4).また関連物質であるN,N,N',N'-テトラメチル-p-フェニレンジアミンについては染色体異常試験で陽性5),無水フタル酸については復帰変異試験で陰性の結果が報告されている6).
以上の結果より,3,3-ビス(p-ジメチルアミノフェニル)-6-ジメチルアミノフタリドは,本試験条件下でCHL/IU細胞に染色体異常を誘発しないと結論した.
| 1) | 日本環境変異原学会・哺乳動物試験分科会編,"化学物質による染色体異常アトラス,"朝倉書店,東京,1988, pp. 16-37. |
| 2) | 吉村功編,"毒性・薬効データの統計解析,事例研究によるアプローチ,"サイエンティスト社,東京,1987, pp. 76-78. |
| 3) | 吉村功,大橋靖夫編,"毒性試験講座14,毒性試験データの統計解析,"地人書館,東京,1992, pp. 218-223. |
| 4) | 原巧ら,化学物質毒性試験報告,10, 203(2003). |
| 5) | 祖父尼俊雄監修,"染色体異常試験データ集改定 1998年版,"エル・アイ・シー,東京,1999, p. 487. |
| 6) | 労働省労動基準局安全衛生部化学物質調査課監修,"労働安全衛生法有害性調査制度に基づく既存化学物質変異原性試験データ集,"日本化学物質安全・情報センター,東京,1996, p. 227. |
| 連絡先 | |||
| 試験責任者: | 佐々木澄志 | ||
| 試験担当者: | 山影康次,高橋俊孝,田中憲穂,若栗 忍,渡辺美香,橋本恵子,三枝克彦,加藤初美 | ||
| (財)食品薬品安全センター秦野研究所 | |||
| 〒257-8523 神奈川県秦野市落合729-5 | |||
| Tel 0463-82-4751 | Fax 0463-82-9627 | ||
| Correspondence | ||||
| Authors: | Kiyoshi Sasaki(Study director) Kohji Yamakage, Toshitaka Takahashi, Noriho Tanaka, Shinobu Wakuri, Mika Watanabe, Keiko Hashimoto, Katsuhiko Saegusa, Hatsumi Kato | |||
| Hatano Research Institute, Food and Drug Safety Center | ||||
| 729-5 Ochiai, Hadano-shi, Kanagawa, 257-8523, Japan | ||||
| Tel +81-463-82-4751 | Fax +81-463-82-9627 | |||