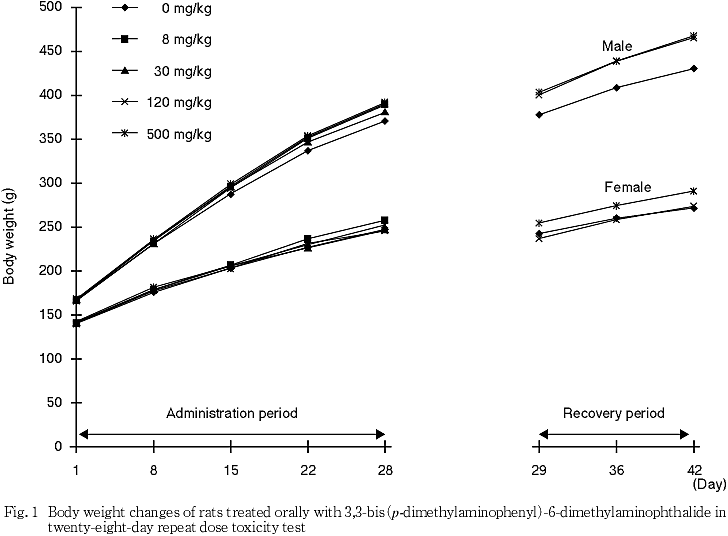
対照群,120および500 mg/kg群については14日間回復群を設けた.
被験物質に起因すると思われる変化が雌雄の甲状腺および雄の上皮小体に認められた.
病理組織学的検査で,雌雄の甲状腺濾胞上皮細胞のび漫性肥大および雄の上皮小体主細胞の肥大が認められた.甲状腺濾胞上皮細胞のび慢性肥大は,雌雄ともに500 mg/kg群で認められ,上皮小体主細胞の肥大は500 mg/kg群の雄で認められた.これらの変化は投与を中止することで消失したことから,容易に回復するものと思われる.
一般状態,体重,摂餌量,血液学検査,血液生化学検査,尿検査,器官重量測定では被験物質に起因すると考えられる変化は認められなかった.
以上,被験物質投与に起因すると考えられる変化が,雌雄とも500 mg/kg群で認められた.従って,本試験条件下における3,3-ビス(p-ジメチルアミノフェニル)-6-ジメチルアミノフタリドの無影響量(NOEL)は雌雄とも120 mg/kg/dayと判断した.
動物入荷後,雌雄とも5日間の検疫期間後,投与開始日まで馴化した.投与開始前日に体重層別無作為抽出法によって群分けした.投与開始時の週齢は5週齢,体重範囲は雄が155〜180 g,雌が129〜153 gであった.
検疫・馴化期間を含む全飼育期間を通じて,温度22 ± 2 ℃(許容範囲19.0〜25.0 ℃),相対湿度55 ± 15 %(許容範囲35.0〜75.0 %),換気約12回/時(オールフレッシュエアー供給),照明12時間/日(7:00-19:00)に自動調節した飼育室を使用した.
動物を滅菌済の実験動物用床敷(ベータチップ,日本チャールス・リバー(株))を敷いたポリカーボネート製ケージに1ケージあたり同性2匹(投与期間中)収容し飼育した.
動物には,実験動物用固型飼料(MF,オリエンタル酵母工業(株))と,5 μmのフィルター濾過後,紫外線照射した水道水をそれぞれ自由に摂取させた.
投与液は被験物質を必要量秤量し,溶媒(0.1 %Tween80[関東化学(株)]添加0.5 %CMC-Na[関東化学(株)]水溶液)を加えながら乳鉢・乳棒で懸濁させ,メートルグラス内で十分に撹拌後定容として50,12,3.0および0.8 mg/mLの投与液とした.調製頻度は週1回とし,投与に供するまで7日間を限度に冷蔵・暗所に保存した.投与液中の被験物質の均一性および冷蔵・暗所保存条件下での8日間の安定性を200および0.4 mg/mLの濃度でHPLC法により確認した.また,初回調製時に各用量群の投与液をHPLC法により分析し,設定濃度± 10 %以内であることを確認した.
対照群と500および120 mg/kg群の雌雄各6匹に,投与期間終了後14日間の回復期間を設けた.
赤血球数(球状化処理二次元レーザーFCM法),ヘモグロビン濃度(シアンメトヘモグロビン法),ヘマトクリット値(球状化処理二次元レーザーFCM法),網赤血球数(RNA染色によるレーザーFCM法),血小板数(球状化処理二次元レーザーFCM法),白血球数(酸性界面活性剤によるレーザーFCM法)を自動血球分析装置(ADVIA120:バイエルメディカル(株))を用いて測定した.さらに平均赤血球容積(MCV),平均赤血球血色素量(MCH),平均赤血球血色素濃度(MCHC)を算出した.白血球百分率(Wright染色塗抹標本について測定)を自動血液細胞分析装置(MICROX HEG-50,HEG-50VF:オムロン(株))を用いて測定した.プロトロンビン時間(PT,光散乱検出方式),活性化部分トロンボプラスチン時間(APTT,光散乱検出方式)を自動血液凝固測定装置(CA-510:シスメックス(株))で測定した.
凝固阻止剤としてプロトロンビン時間および活性化部分トロンボプラスチン時間の測定には,3.2 w/v%クエン酸三ナトリウム水溶液を,その他の項目の測定には,EDTA-2Kを用いた.
AST(GOT; UV-rate法(JSCC改良法)),ALT(GPT; UV-rate法(JSCC改良法)),gGT(γ-グルタミル-ρ-ニトロアニリド基質法(SSCC改良法)),ALP(ρ-ニトロフェニルリン酸基質法(JSCC改良法)),総ビリルビン(酵素法(BOD法)),尿素窒素(酵素-UV法(Urease-LEDH法)),クレアチニン(酵素法(Creatine-Kinase法)),グルコース(酵素法(GlcK-G6PDH法)),総コレステロール(酵素法(CO-HDAOS法)),トリグリセライド(酵素法(GPO-HDAOS法),グリセリン消去法),総蛋白(Biuret法),アルブミン(BCG法),A/G比(総蛋白およびアルブミンより算出),カルシウム(OCPC法),無機リン(酵素法(PNP-XOD-POD法)),ナトリウム(イオン選択電極法),カリウム(イオン選択電極法),クロール(イオン選択電極法)を自動生化学分析装置(TBA-200FR:((株)東芝)により測定した.
 ((株)エイアンドティー)),カリウム(イオン選択電極法; 自動電解質分析装置,PVA-α
((株)エイアンドティー)),カリウム(イオン選択電極法; 自動電解質分析装置,PVA-α ((株)エイアンドティー)),クロール(電量滴定法; 自動電解質分析装置,PVA-α
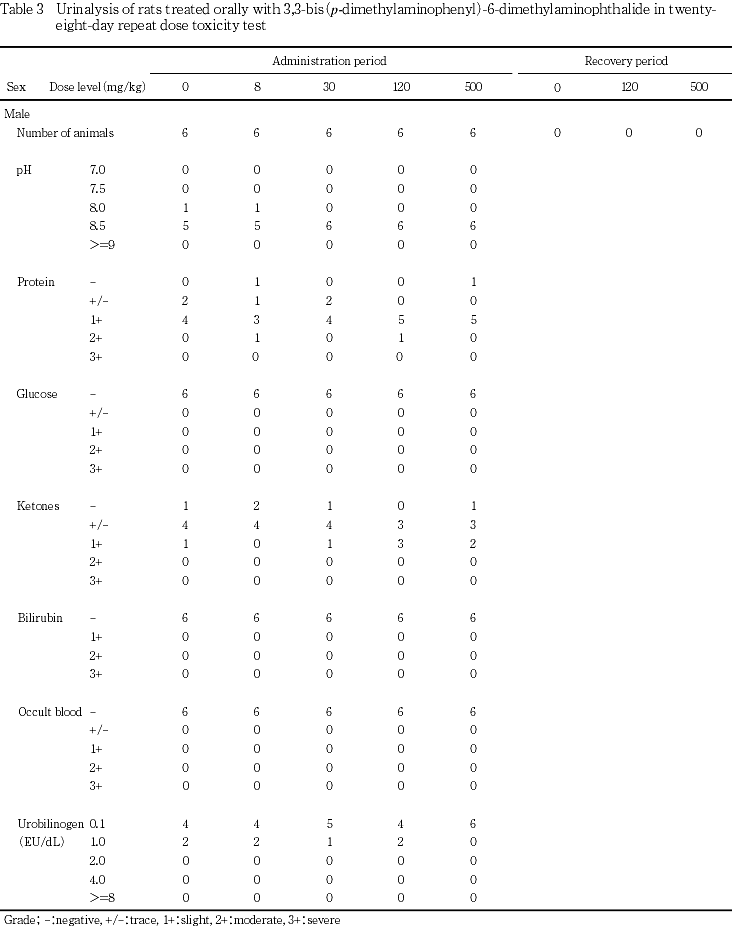
((株)エイアンドティー)),クロール(電量滴定法; 自動電解質分析装置,PVA-α ((株)エイアンドティー))の項目を測定した.回復期間最終週(第37日)にも雌のみ試験紙法による項目を測定した.その結果,被験物質投与の影響を疑わせる変化が認められなかったため,その他の検査は実施しなかった.
((株)エイアンドティー))の項目を測定した.回復期間最終週(第37日)にも雌のみ試験紙法による項目を測定した.その結果,被験物質投与の影響を疑わせる変化が認められなかったため,その他の検査は実施しなかった.
全動物の下記の器官・組織を採取し,10 %中性リン酸緩衝ホルマリン液で固定し,保存した.ただし,精巣はブアン液(Bouin液)で,眼球とハーダー腺はダビドソン液(Davidson液)でそれぞれ固定後,10 %中性リン酸緩衝ホルマリン液で保存した.
投与期間終了後解剖動物の対照群および500 mg/kg群の雌雄全例の器官・組織,ならびに対照群を含む全動物の肉眼的異常部位は常法に従ってヘマトキシリン・エオジン染色標本を作製し,鏡検した.(眼球・ハーダー腺は片側のみ標本作製し,鏡検した.)その結果,500 mg/kg群の雌雄の肝臓,甲状腺,雄の腎臓,上皮小体に被験物質の影響が疑われたため,投与期間終了後解剖動物の8,30および120 mg/kg群と回復期間終了後解剖動物の雌雄の肝臓,甲状腺ならびに雄の腎臓,上皮小体について追加検査した.さらに回復期間終了後解剖動物の器官重量測定の結果,雌の脾臓の相対重量で対照群との間に有意な差がみられたため,回復期間終了後解剖動物の対照群と120および500 mg/kg群の雌の脾臓についても検査した.また全試験動物の肉眼的異常部位についても併せて検査した.

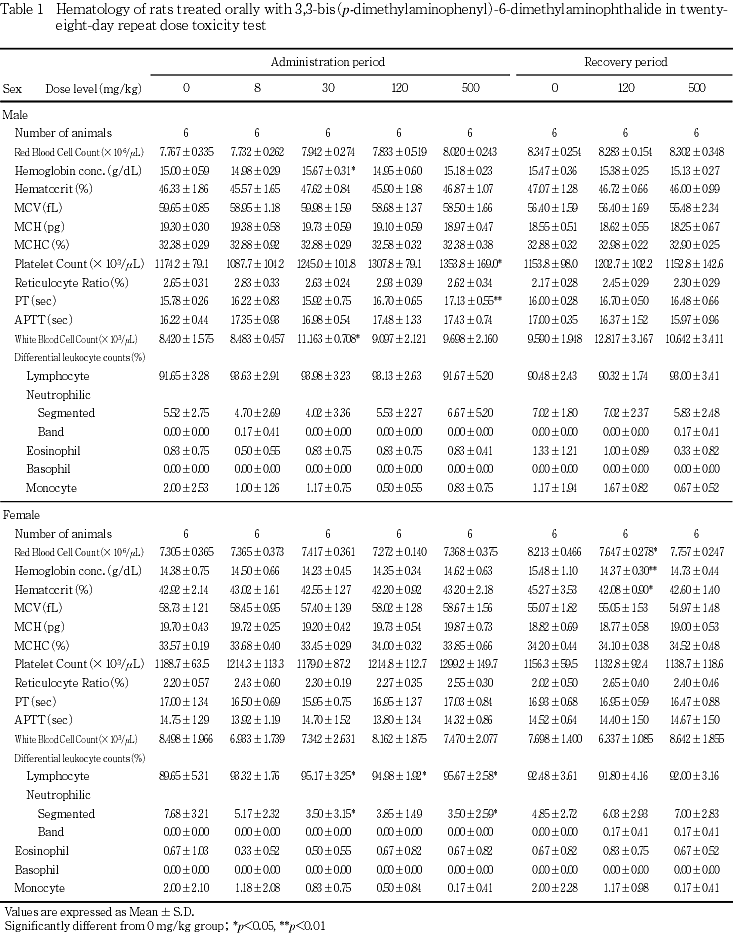
回復期間終了時の検査では,120 mg/kg群の雌で赤血球数,ヘモグロビン濃度およびヘマトクリット値の低値が認められた.
これらの変化のうち,投与期間終了時に認められた30 mg/kg群の雄でのヘモグロビン濃度および白血球数の高値は120および500 mg/kg群では認められていないことから,また回復期間終了時に認められた120 mg/kg群の雌での赤血球数,ヘモグロビン濃度,ヘマトクリット値の低値は投与期間終了時には認められていないことから,被験物質投与とは関連のない偶発的変化と判断した.
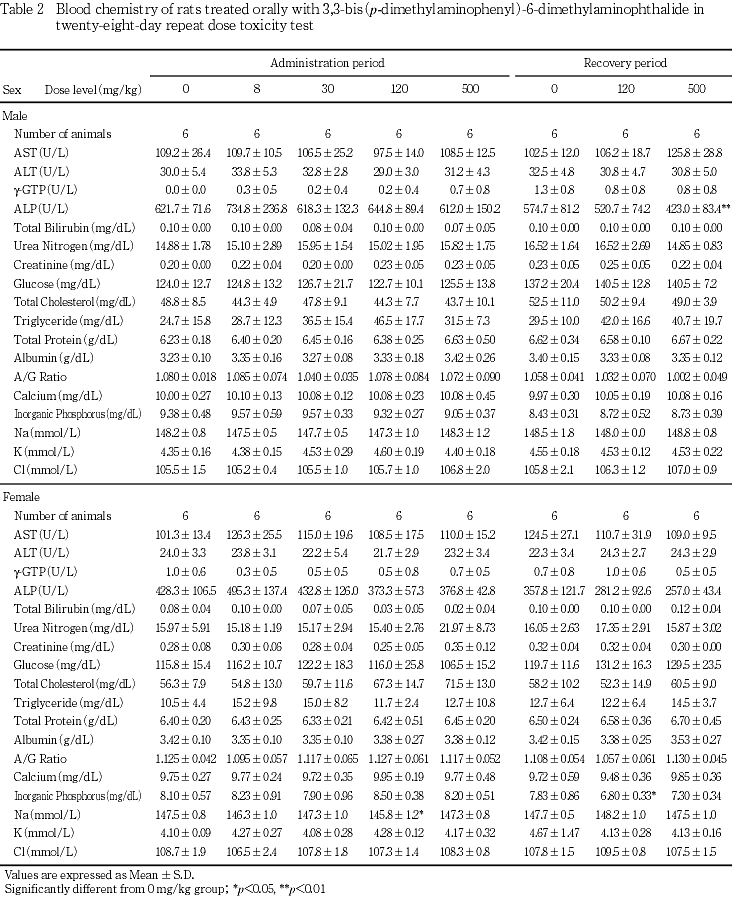
回復期間終了時の検査では,500 mg/kg群の雄でALPの低値,120 mg/kg群の雌で無機リンの低値が認められた.
これらの変化のうち,投与期間終了時に認められた120 mg/kg群の雌におけるナトリウムの低値は,500 mg/kg群では認められていないことから,また回復期間終了時に認められた500 mg/kg群の雄におけるALPの低値,120 mg/kg群の雌における無機リンの低値は投与期間終了時には認められていないことから,いずれも被験物質投与とは関連のない偶発的変化と判断した.
回復期間最終週の雌の検査においては,対照群と被験物質投与群との間に有意な差は認められなかった.

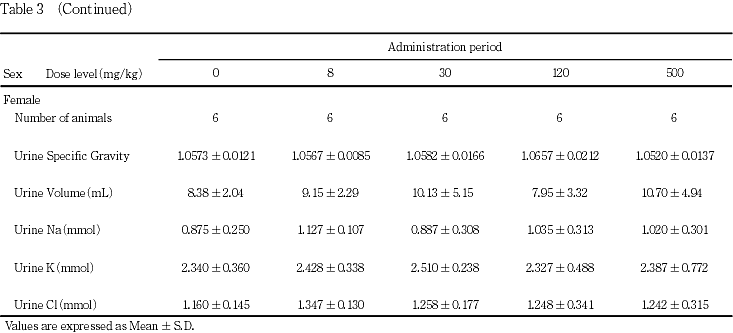
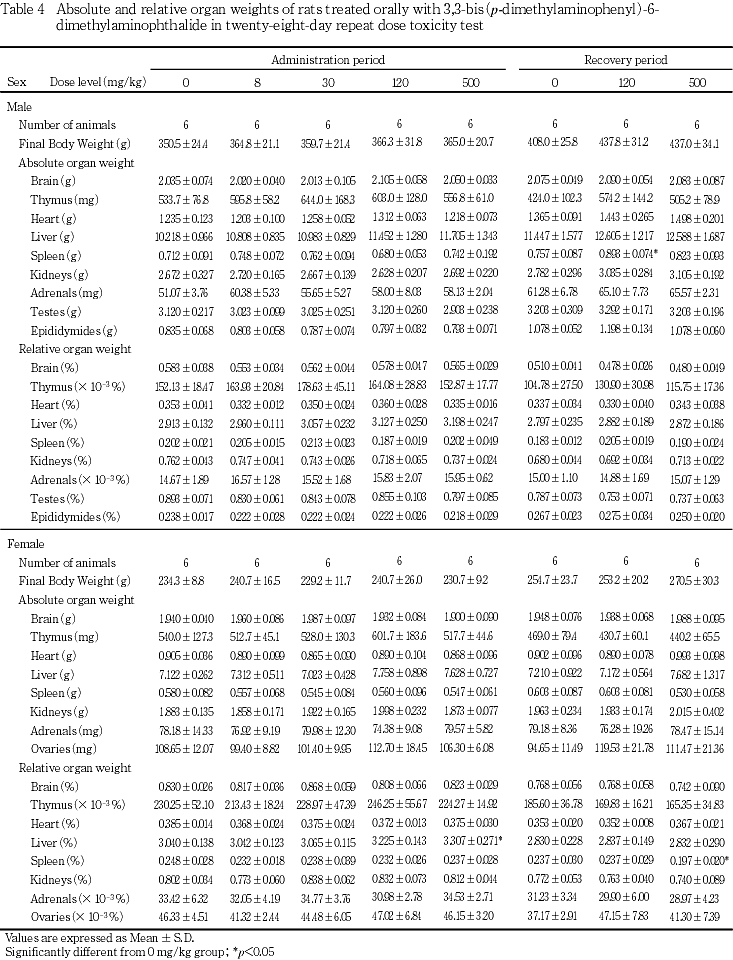
回復期間終了時の検査では,120 mg/kg群の雄で脾臓の絶対重量の高値,500 mg/kg群の雌で脾臓の相対重量の低値が認められた.
これらの変化のうち,回復期間終了時に認められた脾臓の変化は,双方とも投与期間終了時には認められていないことから,被験物質投与とは関連のない偶発的変化と判断した.
偶発的変化として,肺の褐色斑,肝臓の横隔膜面結節,腎臓の嚢胞,腎盂拡張,甲状腺の右側欠損が,投与期間および回復期間終了後解剖動物で用量群と関係なく散発的に認められた.
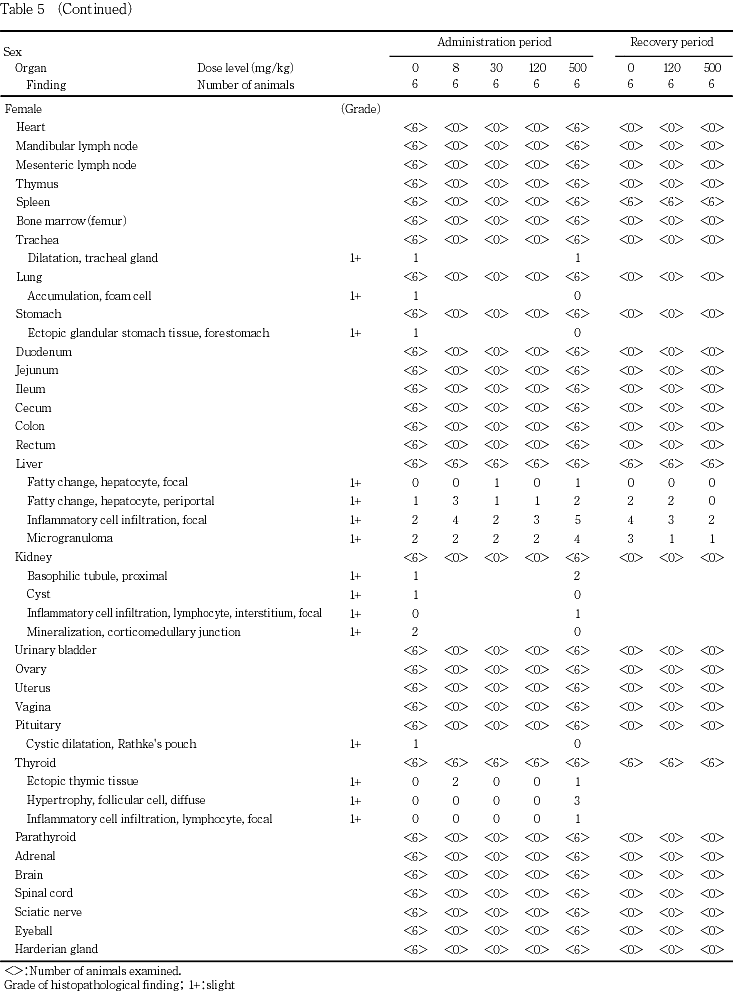
投与期間終了後解剖動物において,甲状腺濾胞上皮細胞のび漫性肥大が,500 mg/kg群の雌雄各3例に認められ,対照群と比較して有意差もみられた.変化のみられた甲状腺では,濾胞腔が狭小化し,濾胞上皮細胞は丈を増していた.上皮小体主細胞の肥大が,500 mg/kg群の雄4例に認められ,対照群と比較して有意差もみられた.肥大した主細胞の細胞質は拡張し淡明化していた.回復期間終了後解剖動物においては甲状腺,上皮小体の変化はともに消失していた.
投与期間終了後解剖動物において,肝臓の小葉中心性肝細胞肥大が,500 mg/kg群の雄1例に認められた.器官重量測定の結果,有意な増加のみられた500 mg/kg群の雌の肝臓では,重量増加に関わるような組織学的変化は認められなかった.30 mg/kg群の雄で,腎臓の腎盂拡張が3例に認められたが,この変化は高用量群では認められなかったため,被験物質とは関連のない変化と判断した.雄の腎臓の近位尿細管上皮の硝子滴発現は,被験物質投与群のみで認められたが,発現状況に一定の傾向が認められなかったため,被験物質とは関連のない変化と判断した.回復期間終了後解剖動物において,器官重量測定の結果,相対重量で対照群と比較して有意な低値のみられた500 mg/kg群の雌の脾臓では,変化は認められなかった.
その他に,心臓の限局性心筋変性/線維化,脾臓の赤血球系髄外造血,肺の泡沫細胞集簇・限局性炎症性細胞浸潤,肝臓の限局性肝細胞脂肪化・門脈周囲性の肝細胞脂肪化・限局性炎症性細胞浸潤・小肉芽腫・限局性肝細胞壊死,腎臓の好塩基性近位尿細管・嚢胞・近位尿細管上皮の硝子滴・集合管上皮細胞の過形成・間質における限局性リンパ球浸潤・皮髄境界部における鉱質沈着,精巣上体の限局性リンパ球浸潤,前立腺の限局性リンパ球浸潤,下垂体のラトケ嚢の嚢胞状拡張,甲状線の異所性胸腺・限局性リンパ球浸潤,気管の気管支腺の拡張,胃の前胃における異所性腺胃組織が認められたが,被験物質投与群で有意に多発したものはなく,いずれも被験物質投与とは関連のない偶発的変化と判断した.
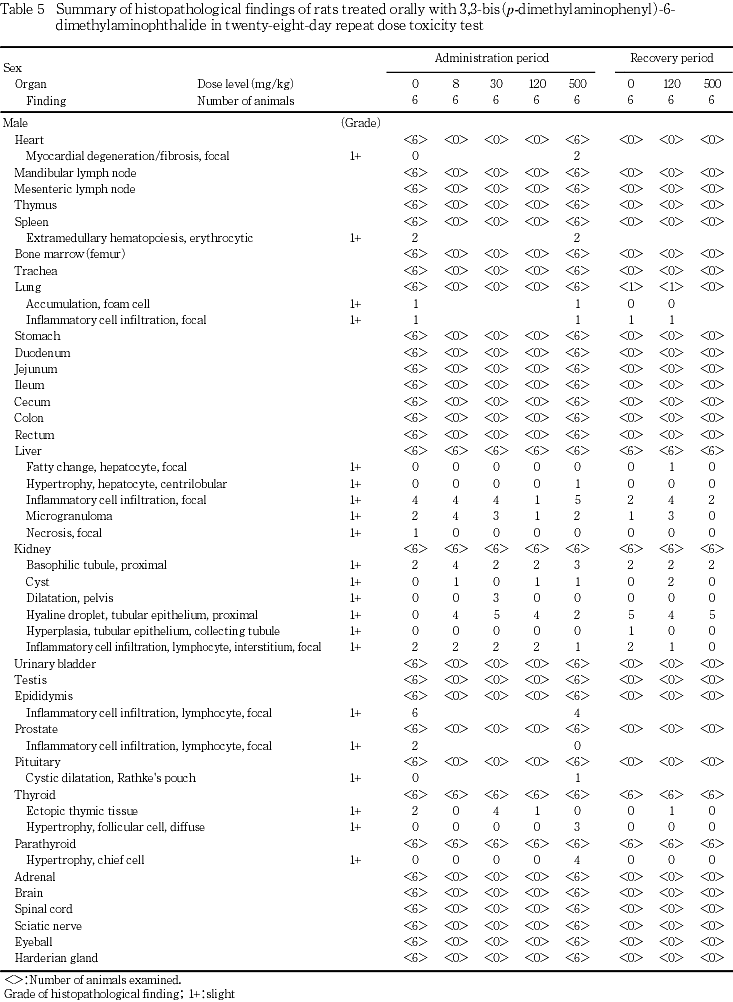
被験物質に起因すると思われる変化が雌雄の甲状腺,雄の上皮小体および肝臓に認められた.
病理組織検査で,500 mg/kg群の雌雄の甲状腺濾胞上皮細胞のび漫性肥大および雄の上皮小体主細胞の肥大が認められ,被験物質に起因する変化と思われた.甲状腺濾胞上皮細胞の肥大は,種々の化学物質投与によってしばしば惹起される変化であり,その多くは循環血液中の甲状腺ホルモン低下によるネガティブフィードバック機構が関与した,持続性の濾胞上皮細胞の刺激が原因となる1, 2).この変化は化学物質の投与を中止することで回復するとされており2),今回の試験でも,被験物質の投与を中止することで変化は消失していた.しかし,今回の検査だけでは濾胞上皮細胞肥大の機序を明らかにすることはできなかった.上皮小体主細胞の肥大は,上皮小体の機能亢進に伴う変化で,慢性腎疾患や,カルシウム欠乏などの栄養障害でも二次的に生じる3).今回の試験では,腎臓,骨などに関連する変化は認められず,血液生化学検査でもカルシウムや無機リン濃度に変化はみられなかったことから,主細胞肥大の原因は明らかにならなかった.
今回の試験では,甲状腺濾胞上皮細胞のび慢性肥大が,雌雄ともに500 mg/kg群で認められ,上皮小体主細胞の肥大が500 mg/kg群の雄に認められた.これらの変化は投与を中止することで消失したことから,容易に回復するものと思われる.
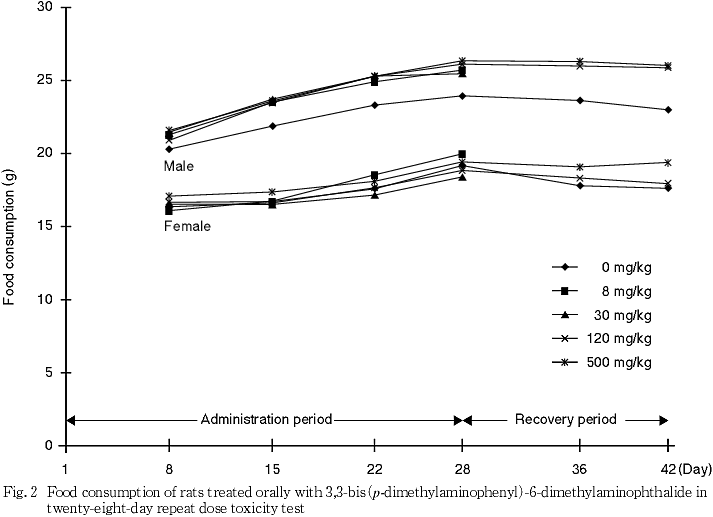
雄で認められた摂餌量の高値は,一般に毒性学的に問題となる低値とは逆の方向への変化であること,体重には異常は認められなかったことから,被験物質投与とは関連のない偶発的変化と判断した.
血液学検査で認められた投与期間終了時の500 mg/kg群の雄における血小板数の高値およびPTの延長は,病理組織検査で骨髄および肝臓に異常は認められなかったこと,他の血球系および凝固系測定値に異常は認められなかったことから,被験物質投与とは関連のない偶発的変化と判断した.また,白血球百分率で認められた雌の500,120および30 mg/kg群での白血球百分率リンパ球比の高値,500および30 mg/kg群の白血球百分率分葉核球比の低値は,白血球数に異常は認められなかったこと,リンパ球増多症を引き起こす感染症等の要因4)や好中球減少症を引き起こす造血臓器疾患等の要因5)は認められなかったことから,被験物質投与とは関連のない偶発的変化と判断した.
投与期間中の尿検査で認められた雌の120および500 mg/kg群のpHの低値(酸性側への変動)は,雄ではpHの異常は認められなかったこと,尿pHが低くなる病態として考えられるいずれにも該当しないこと6)から,被験物質投与とは関連のない偶発的変化と判断した.
一般状態,体重では異常は認められなかった.
以上の結果から,被験物質投与に起因すると考えられる変化が,雌雄とも500 mg/kg群で認められた.従って,本試験条件下における3,3-ビス(p-ジメチルアミノフェニル)-6-ジメチルアミノフタリドの無影響量(NOEL)は雌雄とも120 mg/kg/dayと判断した.
| 1) | C. Gopinath, D. E. Prentice, D. J. Lewis, "The endocrine glands, thyroid, In:Atlas of Experimental Toxicological Pathology," eds. by C. Gopinath, D. E. Prentice, D. J. Lewis, MTP Press, Lancaster, 1987, pp. 112-113. |
| 2) | 前川昭彦 責任編集,"毒性病理組織学,甲状腺/上皮小体,非腫瘍性病変,甲状腺,濾胞上皮細胞のびまん性過形成(びまん性過形成性甲状腺腫),"今井清,広瀬雅雄 編,日本毒性病理学会,名古屋,2000, pp. 436-437. |
| 3) | C. C. Capen, R. A. DeLellis, J. T. Yarrington, "Endocrine system, parathyroid gland, mechanisms of toxicity, modification of parathyroid function associated with metabolic disorders. In:Handbook of Toxicologic Pathology," eds. by W. M. Haschek, C. G. Rousseaux, M. A. Walling, Academic Press, San Diego, 2002, pp. 761-765. |
| 4) | 河合忠ら,"Laboratory medicine異常値の出るメカニズム,リンパ球数とsubpopulation,"医学書院,東京,1986, pp. 43-46. |
| 5) | 河合忠ら,"Laboratory medicine異常値の出るメカニズム,白血球数と好中球数,"医学書院,東京,1986, pp. 39-42. |
| 6) | 河合忠ら,"Laboratory medicine異常値の出るメカニズム,尿検査,尿pH,"医学書院,東京,1986, pp. 7-10. |
| 連絡先 | |||
| 試験責任者: | 須藤雅人 | ||
| 試験担当者: | 松本 忍,大西岳之,友成由紀,豊田直人,高野克代,伯耆淳子,大江みどり,鈴木美江,増田久美子 | ||
| (株)三菱化学安全科学研究所鹿島研究所 | |||
| 〒314-0255 茨城県鹿島郡波崎町砂山14 | |||
| Tel 0479-46-2871 | Fax 0479-46-2874 | ||
| Correspondence | ||||
| Authors: | Masato Sudo(Study director) Shinobu Matsumoto, Takeyuki Oonishi, Yuki Tomonari, Naoto Toyota, Katsuyo Takano, Junko Houki, Midori Ooe, Yoshie Suzuki, Kumiko Masuda | |||
| Mitsubishi Chemical Safety Institute Ltd., Kashima Laboratory | ||||
| 14 Sunayama, Hasaki-machi, Kashima-gun, Ibaraki, 314-0255, Japan | ||||
| Tel +81-479-46-2871 | Fax +81-479-46-2874 | |||