
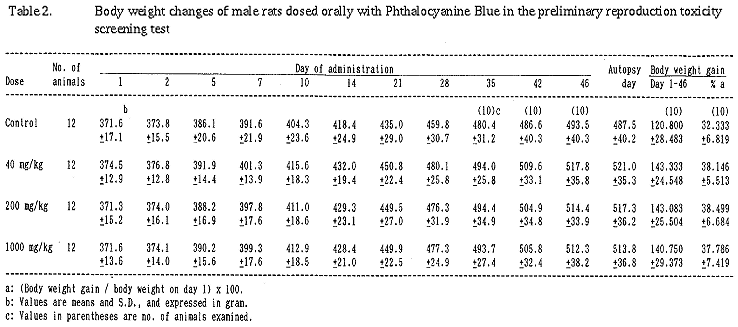
(2)体重推移、摂餌量、器官重量、剖検及び病理組織学的検査では、雌雄ともに被験物質投与による影響は認められなかった。
(3)以上より、本スクリーニング試験における銅フタロシアナートの反復投与による無影響量(NOEL)は雌雄ともに1000 mg/kg/dayであることが示唆された。
(2)以上より、本スクリーニング試験における銅フタロシアナートの雌雄動物の生殖・児動物の発生に対する無影響量 (NOEL) は雌雄ともに1000 mg/kg/dayであることが示唆された。
飼育室内の清掃は1日1回以上、床の清拭消毒は1日1回の頻度で行った。
飼料は固型飼料(CRF-1、オリエンタル酵母工業株式会社)を金属製給餌器を用いて、飲料水は水道水(札幌市水道水)を自動給水装置及びポリプロピレン製給水器を用いて、それぞれ自由に摂取させた。飼料の分析及び飲料水の水質検査の結果、試験施設で定めた基準値の範囲内であった。
動物数は1群あたり雌雄各12匹とした。群分けは、馴化飼育の最終日(投与開始前日)に各群の体重が均一になるように体重別層化無作為抽出法により行った。
動物の識別は、油性フェルトペンあるいはイヤーパンチを用いた。ケージには性別毎に色分けしたカードに試験番号、試験群、グループ番号及び動物番号を明記して標示した。

投与経路は、被験物質が人体に経口的に暴露される可能性があることから、経口投与とした。投与は、胃ゾンデを用いて強制的に胃内に行った。投与容量は、体重1kg当たり10mlとして投与日に最も近い日に測定した体重に基づいて算出した。
投与期間は、雄については交配前14日間及び交尾成立までの交配期間、さらに交尾成立例は投与開始後46日までの期間、雌については交配前14日間及び交尾成立までの交配期間、さらに交尾成立例は妊娠期間及び哺育3日までの期間とした。投与時刻は、午前10時から午後1時の間とした。
投与は10週齢から開始し、投与開始時の平均体重(体重範囲)は雄で372.3g(338〜397g)、雌で232.6g(202〜252g)であった。
全例について、試験期間中1日1回以上の頻度で、視診及び触診により行動、外観などを観察した。
2) 体重測定
全例について、投与1日(投与前)、投与2、5、7、10及び14日、その後は7日毎に(投与終了日を含む)、さらに剖検日に測定した。また、体重増加量及び体重増加率を算出した。
3) 摂餌量測定
全例について、投与1日(投与前)、投与2、5、7、10及び14日、その後は交配期間を除き体重測定日と同じ日(投与終了日を含む)に測定した。
4) 生殖能検査
投与14日の雄と同試験群内の雌を夕方より1対1で最長14日間同居させた。交尾成立は相手雌の腟垢中に精子が確認された場合とし、妊娠成立は相手雌の子宮に着床痕が確認された場合とした。また、交尾率及び受胎率を算出した。
5) 剖検及び器官重量測定
交尾成立例は投与46日の翌日に、交尾不成立例は交配期間終了の翌日に、エーテル麻酔下で放血致死させ、全身の器官・組織を肉眼的に観察した。摘出器官のうち、精巣及び精巣上体(左右)の重量を測定し、器官体重重量比を算出した。
6) 病理組織学的検査
全例について、剖検時に肝臓、腎臓、脾臓、心臓、肺、脳、下垂体、副腎、甲状腺、上皮小体、胸腺、腸間膜リンパ節、膵臓、舌、下顎リンパ節、顎下腺、舌下腺、耳下腺、乳腺、皮膚、眼球、ハーダー腺、胸骨及び大腿骨(骨髄を含む)、脊髄(頸部)、骨格筋(外側広筋)、胸部大動脈、喉頭、気管、気管支、食道、胃(前胃、腺胃)、十二指腸、空腸、回腸、盲腸、結腸、直腸、膀胱、精巣、精巣上体、精嚢(凝固腺を含む)、前立腺及び異常所見部位を10%中性緩衝ホルマリン液で固定し、保存した。なお、眼球及びハーダー腺はデビッドソン液で、精巣及び精巣上体はブアン液で固定・保存した。摘出器官のうち、全例の精巣及び精巣上体について、パラフィン包埋後薄切し、ヘマトキシリン・エオジン染色標本を作製し、鏡検した。
全例について、投与前10日から交尾成立までの連日、ギムザ染色による腟垢塗抹標本を作製し、光学顕微鏡下で性周期段階の判定を行った。
2) 一般状態観察
全例について、試験期間中1日1回以上の頻度で、視診及び触診により行動、外観などを観察した。
3) 体重測定
全例について、投与1日(投与前)、投与2、5、7、10及び14日、妊娠0、1、3、5、7、10、14、17及び20日、哺育1及び4日に測定した。また、投与期間中、妊娠期間中及び哺育期間中の体重増加量及び体重増加率を算出した。
4) 摂餌量測定
全例について、投与1日(投与前)、投与2、5、7、10及び14日、妊娠1、3、5、7、10、14、17及び20日、哺育1及び4日に測定した。
5) 生殖能検査
投与14日の雌と同試験群内の雄を夕方より1対1で最長14日間同居させた。交尾の成立は雌の腟垢中に精子が確認された場合とし、妊娠の成立は子宮に着床痕が確認された場合とした。また、交尾率及び受胎率を算出した。
6) 分娩及び母性行動観察
全例について、分娩状態、母性行動、生存児数及び死亡児数、出産児の性別及び外表を観察した。また、着床率、出産率、分娩率、出生率、哺育率及び性比を算出した。妊娠期間は妊娠21日の午前9時から妊娠22日の午前9時までに分娩が終了した場合を21日間とし、それ以降同様に午前9時から翌日午前9時までを1日として算出した。なお、分娩日を哺育0日として起算した。
7) 剖検及び器官重量測定
交尾成立例は哺育4日に、交尾不成立例は交配期間終了の翌日に、妊娠25日まで分娩の認められない例(不妊例)は妊娠26日に、全哺育児を死亡させた例は直ちにエーテル麻酔下で放血致死させ、全身の器官・組織を肉眼的に観察した。また、子宮の着床痕及び卵巣の妊娠黄体を計数した。摘出器官のうち、卵巣(左右)の重量を測定した。また、器官体重重量比を算出した。
8) 病理組織学的検査
全例について、剖検時に雄と同様な器官・組織の他、卵巣、子宮、腟及び異常所見部位を10%中性緩衝ホルマリン液で固定し、保存した。なお、眼球及びハーダー腺はデビッドソン液で固定・保存した。摘出器官のうち、全例の卵巣、40及び200 mg/kg群の異常所見部位(脾臓及び乳腺)について、パラフィン包埋後薄切し、ヘマトキシリン・エオジン染色あるいはPAS染色標本を作製し、鏡検を行った。
全例について、分娩日から剖検日(哺育4日)まで1日1回、生存及び死亡を確認し、一般状態及び外表について観察した。なお、哺育日数は分娩日を哺育0日として起算した。また、新生児生存率は1腹を単位として算出した。ただし、喰殺を受け死亡あるいは行方不明となった新生児は死亡例として扱った。
2) 体重測定
全例について、哺育1及び4日に測定した。なお、体重値は雌雄別に1腹を単位とした平均値で示した。
3)剖検
予後不良と判断された衰弱例及び死亡例は、直ちに剖検し、whole bodyを10%中性緩衝ホルマリン液で固定し、保存した。その他の例については、哺育4日に体外表(口腔内を含む)を観察し、二酸化炭素吸入法により安楽致死させ、全身の器官・組織を肉眼的に観察した。異常所見部位の認められた例については、whole bodyを10%中性緩衝ホルマリン液で固定・保存した。
交尾率、受胎率、出産率及び哺育率については多試料χ^2検定を行い、その結果、有意な場合は2試料χ^2検定を行った。ただし、2試料χ^2検定あるいは多試料χ^2検定に不適合の場合はFisherの正確確率検定法により行った。
なお、対照群との検定については、危険率5%以下を統計学的に有意とした。
精巣上体において、被膜の肉芽腫が40 mg/kg群の1例で、間質にリンパ球を主とする血管周囲の限局性細胞浸潤が200 mg/kg群の1例で認められた。
妊娠期間中では、40 mg/kg以上の群の全例で糞の青色化が認められた。その他に、40 mg/kg群の1例で自発運動の減少及び血液による腟周囲の被毛汚染が妊娠24日(分娩中)に、200 mg/kg群の1例で右腋下部皮下に腫瘤が妊娠16日以降に認められた。
哺育期間中では、40 mg/kg群の8例中全例、200 mg/kg群の11例中全例、1000 mg/kg群の9例中全例で糞の青色化が認められた。その他に、40 mg/kg群の1例で乳腺の未発達が哺育1日に、同群の他の1例で左眼瞼の腫脹が哺育3日に、200 mg/kg群の1例で右腋下部皮下に腫瘤が哺育期間中に、1000 mg/kg群の1例で胸部、腹部及び腰部の血液による被毛汚染及び乳腺の未発達が哺育1日、眼球の褪色が哺育2〜3日に認められた。

妊娠期間では、対照群と比較して200 mg/kg群で妊娠5日に摂餌量の増加が認められたが、用量依存性を欠く変動であった。
哺育期間では、対照群と比較して有意な差は認められなかった。
その他に、全出産児を死亡させた40 mg/kg群の1例で乳腺の未発達が認められた。また、頸部の瘢痕、脾臓の黄白色腫瘤、眼瞼(左)の腫脹、右腋下部の黄白色皮下腫瘤が、用量依存性なく散発的に認められた。
卵巣に嚢胞形成が1000 mg/kg群の不妊の1例及び対照群の妊娠した1例に認められた。
異常所見部位では、40 mg/kg群の1例に分泌乳腺の未発達が、200 mg/kg群の脾臓に壊死を伴う浸出炎、同群の乳腺に停留嚢胞が認められた。
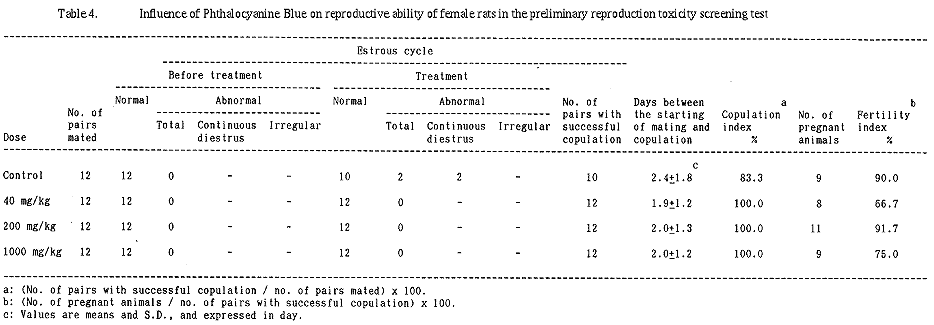
対照群と比較して、交尾までの日数、交尾率及び受胎率に有意な差は認められなかった。なお、交尾不成立例は対照群で2組、不妊例は対照群で1組、40 mg/kg群で4組、200 mg/kg群で1組、1000 mg/kg群で3組に認められた。
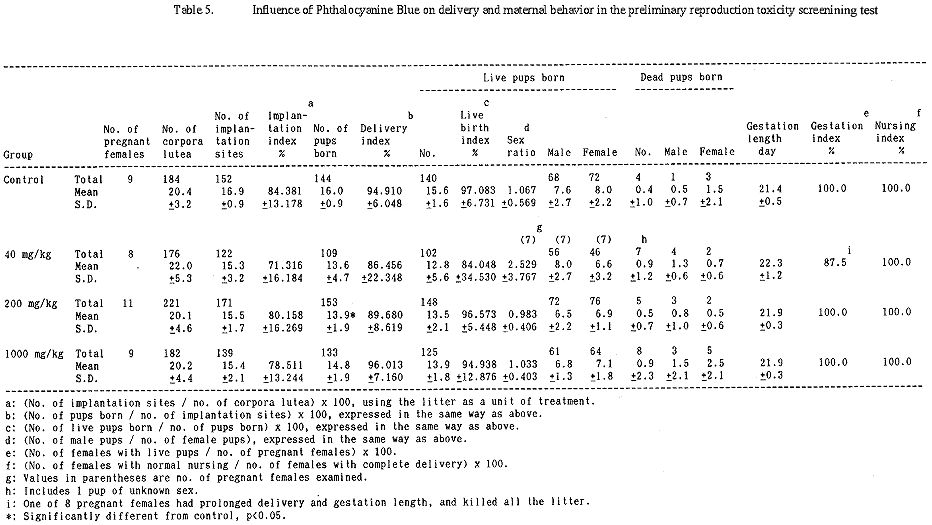
分娩異常として、40 mg/kg群の1例で遷延分娩、妊娠期間の延長及び出産児全例の死亡が認められた。本例は、妊娠24日に分娩を開始し、自発運動の減少、血液による腟周囲の被毛汚染が分娩中に認められた。また、妊娠25日に哺喰などを受けた3匹の死亡児が認められ、妊娠26日の朝には分娩の終了が確認された。なお、本例の分娩終了時の乳腺は未発達であった。一方、200 mg/kg群の1例で乳腺に停留嚢胞が認められたが、分娩や哺育は正常であった。また、1000 mg/kg群の1例で出産後一時的に症状や出産児に多数の死亡が認められたが、全児の死亡に至らず、哺育2日以降は正常な哺育が認められた。
対照群では、哺育1〜3日の死亡が雄68例雌72例中、雌6例に認められた。分娩日(出産後)に胸部及び腹部皮膚の剥離、自発運動の減少あるいは下唇の暗赤色化が雌各1例に認められ、そのうち皮膚剥離のみられた例は衰弱のため同日屠殺した。40 mg/kg群では、哺育2日死亡が雄56例雌46例中、雄1例に認められた。200 mg/kg群では、分娩日(出産後)〜哺育1日の死亡が雄72例雌76例中、雌2例に、哺育4日に尾先端部の欠落が雄1例に認められた。1000 mg/kg群では哺育2日死亡が雄61例雌64例中、雄5例雌3例に認められた。
死亡例のうち、40 mg/kg群の雌1例で背部皮膚の剥離が認められた。衰弱のため屠殺した対照群の雌1例で、胸部及び腹部の皮膚剥離が認められた。哺育4日に屠殺した例のうち、対照群の雄1例で肝臓の内側右葉の黄白色化が、200 mg/kg群の雄1例で尾先端部の欠落が認められた。
被験物質投与により、雌雄ともに、糞の青色化が40 mg/kg以上の群の全例に、胃や腸管の内容物の青緑色あるいは灰青色化が200 mg/kg群の少数例及び1000 mg/kg群のほぼ全例に認められた。これらは被験物質が青色を呈していることに起因するものと考えられ、剖検では消化管を含め器官・組織自体に着色や異常は認められなかった。
その他に一般状態観察では、体重推移及び摂餌量においても被験物質投与による影響は認められなかった。
以上より、本スクリーニング試験における銅フタロシアナートの反復投与による無影響量(NOEL)は雌雄ともに1000 mg/kg/dayであることが示唆された。
生殖能検査では、雌の性周期、雌雄の交尾及び受胎に対して被験物質投与による影響は認められなかった。また、生殖器(精巣、精巣上体及び卵巣)の重量や病理組織学的検査においても、被験物質投与による影響は認められなかった。なお、交尾不成立例及び不妊例の生殖器にそれらの原因を示唆する病理組織学的所見は認められなかった。
分娩及び母性行動観察では、分娩異常として40 mg/kg群の1例で遷延分娩、妊娠期間の延長及び出産児全例の死亡が認められた。同例では自発運動の減少や血液による腟周囲の被毛汚染が認められ、分娩が困難であったことが推測された。しかしながら、同様な分娩異常が中間及び高用量群に認められないことから、本例は偶発的な出現と判断され、被験物質投与との関連性はないものと考えられた。
新生児の観察では、生存性、一般状態観察、体重推移及び剖検において被験物質投与による影響は認められなかった。
以上より、本スクリーニング試験における銅フタロシアナートの雌雄動物の生殖・児動物の発生に対する無影響量 (NOEL) は雌雄ともに1000 mg/kg/dayであることが示唆された。
| 連絡先: | |||
| 試験責任者 | 釜田悟 | ||
| (株)化合物安全性研究所 | |||
| 〒 004 北海道札幌市豊平区真栄 363 番 24 | |||
| Tel 011-885-5031 | Fax 011-885-5313 | ||
| Correspondence: | |||
| Kamada, Satoru | |||
| Safety Research Institute for Chemical Compounds Co., Ltd., Japan | |||
| 363-24 Shin-ei, Toyohira-ku, Sapporo, Hokkaido, 004, Japan | |||
| Tel 81-11-885-5031 | Fax 81-11-885-5313 | ||