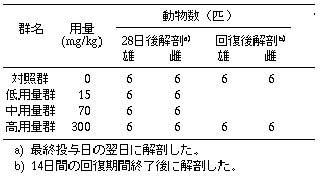
なお、本試験は化審法ガイドライン(1986年)に従って実施した。また化審法GLP(1984年)を満足している。
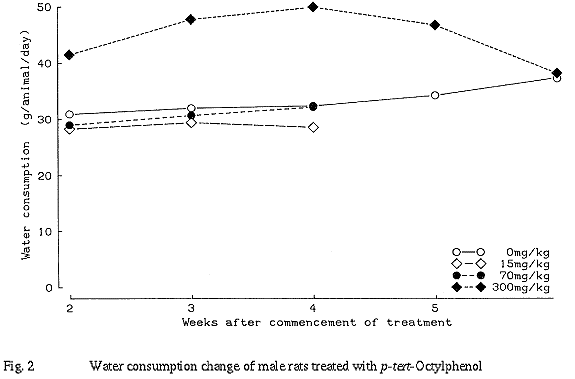
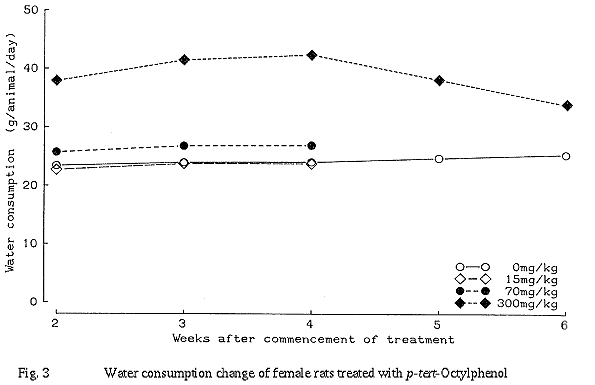
300 mg/kg群において、雌雄ともに流涎、飲水量の増加、血清ナトリウムの増加、尿量の増加および尿比重の低下、尿中電解質の変化、腎臓の重量増加および灰白色斑が認められた。病理組織学的検査で腎臓の尿細管上皮に再生性変化が認められた。その他、雄で体重増加抑制および血清アルブミンの減少、雌で血中総コレステロールの減少、A/G比の低下、尿素窒素の増加、トリグリセライドの増加および肝重量の軽度の増加が認められた。
70 mg/kg群でも流涎が雌雄で、A/G比の低下が雌で認められた。
これら被験物質投与に起因する変化は投与休止により消失あるいは回復傾向を示した。
以上の結果より、本試験条件下におけるp-tert-オクチルフェノールの無影響量は雌雄とも15 mg/kgと考えられる。
今回、ラットを用いてp-tert-オクチルフェノールの経口投与による28日間反復投与毒性試験を実施し、生体への毒性学的影響について検討したので報告する。
動物入荷後5日間馴化し、健康状態が良好なことを確認した後、5週齢で投与を開始した。
投与開始前に動物を体重別層化無作為抽出法により群分けした後、イヤーパンチを用いて群および個体を識別した。投与開始時の体重範囲は、雄が128〜148g、雌が118〜146gであった。
実験動物用床敷(ベータチップ:日本チャールス・リバー株式会社)を敷いたポリカーボネート製ケージ(265W×426D×200Hmm)に1ケージ当り2匹(同性)で収容し、スチール製架台上で飼育した。ステンレス製の固型飼料用給餌器およびポリカーボネート製の給水瓶(700 ml)を用いた。
ケージ(含床敷)、給餌器および給水瓶は、週1回の頻度でオートクレーブ滅菌したものと交換した。
投与液の安定性については本研究所において分析し、冷暗所保存下で調製後14日間は安定であることを確認した。

| a) | 赤血球数 | レーザー光散乱法 |
| b) | 白血球数 | 同上 |
| c) | 血小板数 | 同上 |
| d) | ヘモグロビン濃度 | シアンメトヘモグロビン法 |
| e) | ヘマトクリット値 | ミクロヘマトクリット法 |
| f) | 白血球百分率 | ライト染色塗抹標本について測定 |
| g) | 網状赤血球数 | ニューメチレンブルー染色後ライト染色した塗抹標本について測定 |
| h) | プロトロンビン時間(PT) | Quick一段法 |
| i) | 活性化部分トロンボ(APTT)プラスチン時間 | 活性化セファロプラスチン法 |
| j) | 平均赤血球容積(MCV) | a)、e)より算出 |
| k) | 平均赤血球血色素量(MCH) | a)、d)より算出 |
| l) | 平均赤血球血色素濃度(MCHC) | d)、e)より算出 |
a)〜d)は自動血液分析装置(ELT-8/ds:オルソインスツルメンツ社)、e)はヘマトクリット用遠心機(MC-201:株式会社日立製作所)、f)、g)は血液細胞自動分析装置(MICROX HEG-70A:立石電機株式会社)、h)、i)は血液凝固計(KC-10:アメルング社)により測定した。
| a) | 総蛋白 | Biuret法 |
| b) | アルブミン | BCG法 |
| c) | A/G比 | a)およびb)より算出 |
| d) | グルコース | 酵素-UV法(GK-G6PDH法) |
| e) | トリグリセライド | 酵素法(LPL-GK-G3PO-POD法) |
| f) | 総コレステロール | 酵素法(CES-CO-POD法) |
| g) | 尿素窒素 | 酵素-UV法(Urease-GLDH法) |
| h) | クレアチニン | Jaffe法 |
| i) | カルシウム | O-CPC法 |
| j) | 無機リン | UV法 |
| k) | GOT(AST) | UV-Rate法(SSCC改良法) |
| l) | GPT(ALT) | UV-Rate法(SSCC 改良法) |
| m) | γ-GTP | γ−グルタミル・p−ニトロアニリド基質法(SSCC改良法) |
| n) | ALP | p−ニトロフェニルリン酸基質法(GSCC改良法) |
| o) | ナトリウム | イオン選択電極法 |
| p) | カリウム | イオン選択電極法 |
| q) | クロライド | イオン選択電極法 |
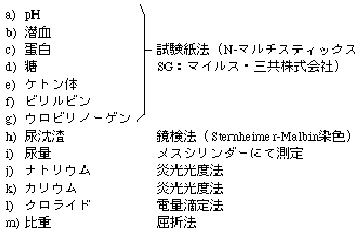
a)〜g)は尿分析器(クリニテック10:株式会社マイルス・三共)、j)、k)は全自動炎光光度計(FLAME30-C/AD-3型:日本分光メディカル)、l)はクロライドメーター(Model 925:コーニングメディカル株式会社)、m)は尿比重計(ユリコン-S:株式会社アタゴ)により測定した。
各計画殺時の生存動物について採血後に腹大動脈を切断して放血し、致死させ剖検を行った。
(2)器官重量
各計画殺時の全生存動物について以下の器官の重量を測定した。測定には電子上皿天秤(ED-H60:株式会社島津製作所)を用いた。更に、解剖日の体重を基に対体重比についても算出した。
脳、肝臓、腎臓、副腎、精巣または卵巣
(3)病理組織学的検査
全動物について以下の器官を採取し、10%中性リン酸緩衝ホルマリン液にて固定後保存した。ただし、眼球およびハーダー腺はDavidsonの溶液にて固定した。
脳、下垂体、眼球(付属腺を含む)、肺、胃、甲状腺(上皮小体を含む)、心臓、肝臓、脾臓、腎臓、副腎、膀胱、精巣または卵巣、骨髄(大腿骨)
採取した器官のうち、28日後解剖動物の対照および高用量群の心臓、肝臓、腎臓、副腎および脾臓を対象に、常法に従いヘマトキシリン・エオジン染色標本を作製し鏡検した。この結果、腎臓で被験物質の影響が認められたため、低、中用量群および回復後解剖動物についても検査した。また剖検時に肉眼的変化の認められた器官についても同様に処理して鏡検した。
 の方法により平均値あるいは順位の多重比較検定を行った。尿の定性検査および尿沈渣については、Armitageのχ^2検定を用いた。
の方法により平均値あるいは順位の多重比較検定を行った。尿の定性検査および尿沈渣については、Armitageのχ^2検定を用いた。
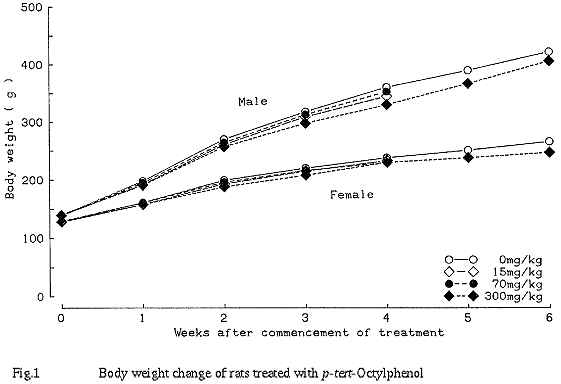
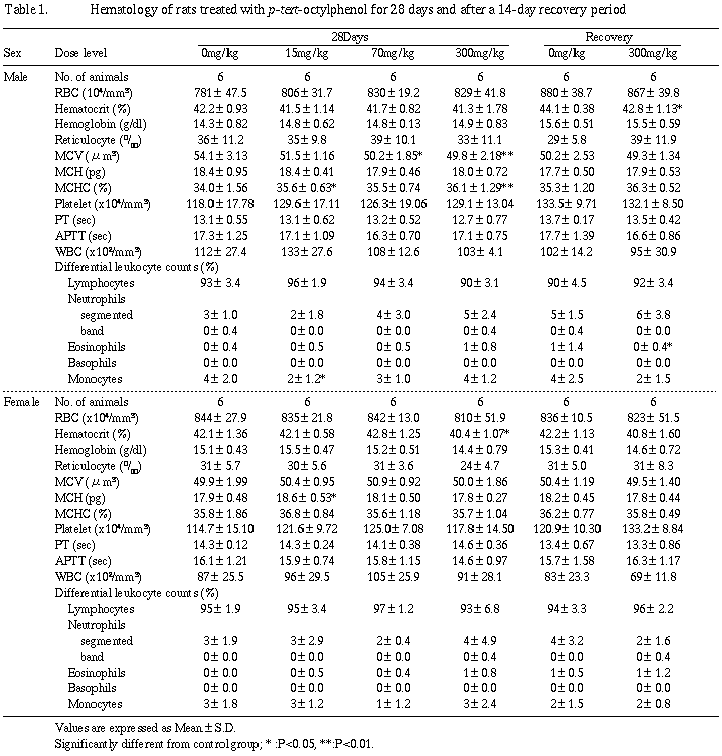
その他、総蛋白およびアルブミンの増加が15 mg/kg群の雌に、GPTの低下が70 mg/kg群の雌にみられたが、これらはいずれも用量依存性のない変化であるため、偶発的変化と判断した。
回復期間終了時の検査では、300 mg/kg群の雄に血中カリウムの減少がみられたが、生理的変動範囲内の変化であるため被験物質投与とは関連のない偶発的変化と判断した。
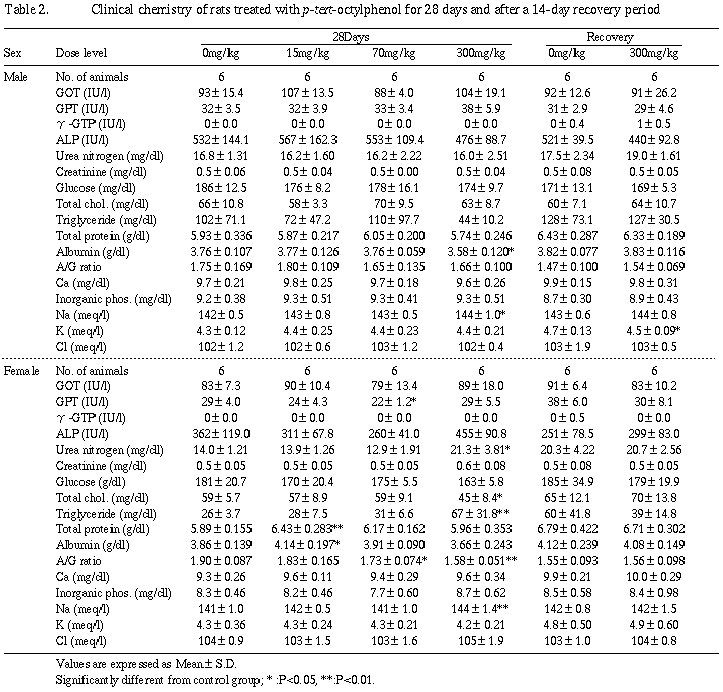
ケトン体の減少が300 mg/kg群の雌雄に、尿蛋白の減少が雌に、また、尿沈渣でリン酸アンモニウムマグネシウムの減少が15および300 mg/kg群の雄に、赤血球数の減少が300 mg/kg群の雄でみられたが、これらは尿量増加により希釈されたために得られた二次的変化と考えられる。その他、カリウムおよびクロライドの減少が15 mg/kg群の雄に、またpHの低下が70 mg/kg群の雌にみられたが、用量依存性がなく偶発的なものと考えられる。
回復期間終了前での検査では異常は認められなかった。
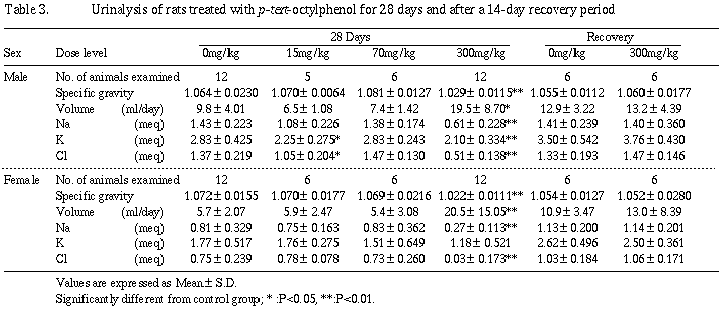
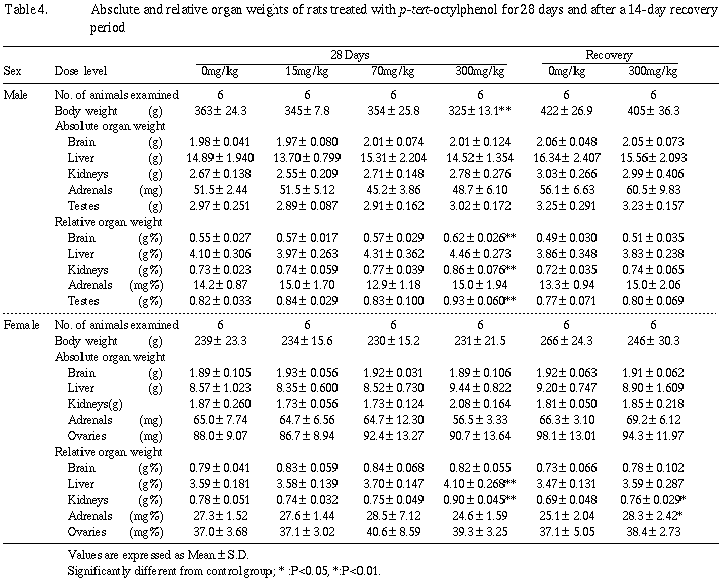
その他、300 mg/kg群の雄で脳および精巣の対体重比に増加がみられたが、実重量ではほとんど差がないことから、体重差が反映した見掛け上の変化と考えられる。
回復期間終了時の検査では、300 mg/kg群の雌に腎臓および副腎の対体重比で増加が認められたが、実重量では差がなかった。
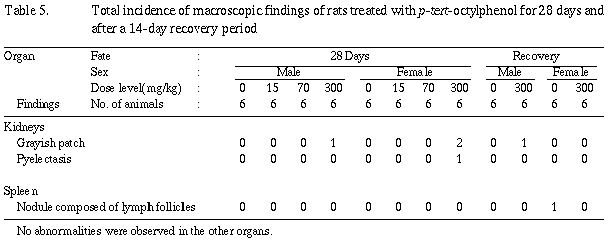
その他、片側腎臓の腎盂腔の拡張が投与終了時解剖動物の300 mg/kg群の雌に1例、脾臓のろ胞の集合による直径5 mm大の結節形成が回復期間終了時解剖動物の対照群の雄に1例認められたが、その発現状況から偶発病変と判断した。
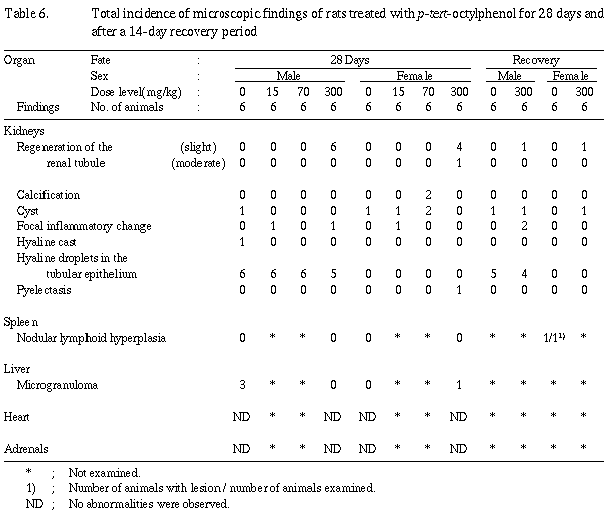
その他、腎臓の尿細管上皮内の硝子滴の出現が投与終了時および回復期間終了時解剖動物の雄の各群で高頻度に認められたが、群間で程度の差はなかった。各群の少数例に肝臓の微小肉芽腫、腎臓の皮髄境界部間質における石灰沈着、限局性炎症性変化、硝子円柱およびのう胞が散見された。また肉眼所見に対応する変化として脾臓のリンパ球の結節性過形成および片側性の腎盂腔の拡張が認められた。これらは用量相関性を欠く変化であり、ラットを用いた毒性試験ではしばしば自然発生病変として認められることから、被験物質投与とは無関係と考えられる。
300 mg/kg群において流涎、飲水量の増加、体重増加抑制が認められた。また、血液生化学的検査、尿検査および器官重量においても被験物質投与に起因すると考えられる変化が認められた。さらに病理学的検査においては腎臓に尿細管上皮の障害が認められた。70 mg/kg群においても流涎など毒性徴候が観察された。
腎臓の尿細管でみられた形態変化は変性や脱落に対する再生性増殖を示唆する上皮の腫大や好塩基性変化であり、被験物質は尿細管上皮に対して障害性を有するものと考えられる。雌の1例にみられた間質の炎症性細胞浸潤は尿細管に対する障害性がより強く、基底膜を越えて間質にまで波及したことを表している。また、回復期間終了後の2例にみられた尿細管周囲の線維化も同様に障害が間質に及んだことを意味するが、一定の炎症性過程を経た修復の像と理解される。回復期間終了後の多くの例ではこのような所見は観察されなかったことから、被験物質の影響が尿細管上皮だけにとどまった場合には2週間の回復期間を設けることによって完全に回復することが示された。
300 mg/kg群の雌雄で尿量の増加とともに尿中電解質の減少が認められた。通常、尿量の増加に伴い尿中電解質は増加あるいは変化しないことが多い。そこで本試験とは別に雌ラットに300 mg/kgの用量で28日間投与し尿の変化を調べたところ(以下補足試験)、被験物質投与後6時間までに多量の尿と電解質が排泄されていることが判明した。本試験で得られた尿は投与後7時間以降のものであったことから、投与後の電解質排泄に対して代償的に再吸収が亢進し、その結果尿中電解質が減少したと考えられる。
一方、腎臓の近位尿細管で障害が認められたため、補足試験にて尿中酵素(N-Acetyl-β-D-glucosaminidase)を測定したが、明らかな尿量増加を認めたにもかかわらず、尿中酵素の変化は明確でなかった。このことから、尿量の増加は尿細管障害に直接起因するものではなく、被験物質の利尿作用によるものである可能性が示唆される。
300 mg/kg群の雌で肝臓重量に軽度の増加がみられたが、病理組織学的変化はなかった。雌で認められた血中総コレステロールおよびトリグリセライド等の脂質の変化は本所見と関連したものである可能性が考えられる。しかしながら、いずれもわずかな変化であり、毒性学的重要性は少ないものと考えられる。
被験物質に起因する変化は、回復期間終了後には消失あるいは回復傾向がみられることから、投与休止により回復性を示す変化と考えられる。
以上の結果から、本試験条件下におけるp-tert-オクチルフェノールの無影響量は雌雄とも15 mg/kgと考えられる。
| 連絡先: | |||
| 試験責任者 | 松浦郁夫 | ||
| (株)三菱化成安全科学研究所鹿島研究所 | |||
| 〒314 -02 茨城県鹿島郡波崎町砂山 14 | |||
| Tel 0479-46-2871 | Fax 0479-46-2874 | ||
| Correspondence: | |||
| Matsuura, Ikuo | |||
| Mitsubishi-Kasei Institute of Toxicological and Environmental Sciences, Japan | |||
| 14 Sunayama, Hasaki-machi, Kashima-gun, Ibaraki, 314-02, Japan | |||
| Tel 81-479-46-2871 | Fax 81-479-46-2874 | ||