トリリン酸アルミニウム塩のチャイニーズ・ハムスター培養細胞を用いる染色体異常試験
In Vitro Chromosomal Aberration Test of Triphosphoric acid aluminium salt
in Cultured Chinese Hamster Cells
要約
トリリン酸アルミニウム塩の培養細胞に及ぼす細胞遺伝学的影響について,チャイニーズ・ハムスター培養細胞(CHL/IU)を用いて染色体異常試験を実施した.
細胞増殖抑制試験の結果をもとに,短時間処理法のS9 mix存在下においては250,500,1000,1500,2000 μg/mL,S9 mix非存在下においては100 μg/mLを最高濃度として公比2で5濃度をそれぞれ設定した.
短時間処理法のS9 mix存在下の2000 μg/mLにおいて,染色体構造異常細胞の出現頻度は33.0 %であり,出現頻度が最高濃度のみで急激に増加していた.
この結果より,用量依存性を検討するために,S9 mix存在下について1600,1800,2000 μg/mLを設定して確認試験を実施した.その結果,2000 μg/mLにおいて,染色体構造異常細胞の出現頻度は11.0 %となり,染色体異常誘発の再現性が認められた.
倍数性細胞の出現頻度は,いずれの処理群においても5 %未満であった.
以上の結果より,本試験条件下ではトリリン酸アルミニウム塩は,染色体異常を誘発する(陽性)と結論した.
方法
1. 使用した細胞
大日本製薬(株)から入手(2001年2月,入手時:継代14代,凍結時:16代)したチャイニーズ・ハムスター肺由来のCHL/IU細胞を,解凍後4週間以内で試験に用いた.
2. 培養液の調製
培養には,非働化した仔牛血清(GIBCO BRL,ロット番号1027934,296130)を10 vol%添加したイーグルMEM(日水製薬(株))培養液を用いた.
3. 培養条件
2 × 104個のCHL/IU細胞を,培養液5 mLを入れたディッシュ(径6 cm,Becton Dickinson and Company)に播き,37 ℃のCO2インキュベーター(5 % CO2)内で培養した.
短時間処理法では,細胞播種3日目にS9 mix存在下および非存在下で6時間処理し,処理終了後新鮮な培養液でさらに18時間培養した.また連続処理法では,細胞播種3日目に被験物質を加え,24時間処理した.
4. 被験物質
トリリン酸アルミニウム塩(ロット番号:10101,テイカ(株)(大阪)提供)は,純度94.7 %(不純物としてZnO:2.1 %,Cd:1 ppm以下,Pb:2 ppm,Cr:1 ppm以下,As:0.05 ppm以下,Hg:0.01 ppm以下を含有)の白色粉末である.被験物質は使用時まで室温で保存した.
被験物質原体は安定であり,反応しない.
5. 被験物質懸濁液の調製
被験物質懸濁液は,用時調製した.媒体はジメチルスルホキシド(関東化学(株),ロット番号:210G1441)を用いた.原体を媒体に懸濁して原液を調製し,ついで原液を媒体で順次希釈して所定の濃度の被験物質懸濁液を作製した.被験物質秤量の際は,純度換算(94.7 %)を実施した.被験物質懸濁液は,すべての試験において培養液の1 vol%になるように加えた.
6. 細胞増殖抑制試験
染色体異常試験に用いる被験物質の処理濃度を決定するため,被験物質の細胞増殖に及ぼす影響を調べた.被験物質のCHL/IU細胞に対する増殖抑制作用は,血球計算盤を用いて各群の細胞を計数し,陰性対照群に対する割合をもって指標とした.
その結果,トリリン酸アルミニウム塩の約50 %の増殖抑制を示す濃度を,生存曲線において細胞増殖率が50 %前後を示す2点を結ぶ直線式より算出したところ,短時間処理法のS9 mix存在下で1251 μg/mL,S9 mix非存在下で55 μg/mL,連続処理法24時間処理で33 μg/mLであった(Fig. 1).
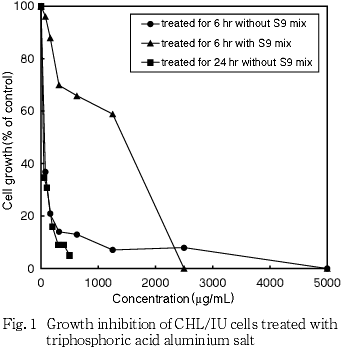
7. 実験群の設定
細胞増殖抑制試験の結果より,短時間処理法のS9 mix存在下においては250,500,1000,1500,2000 μg/mL,S9 mix非存在下においては100 μg/mLを最高濃度として公比2で5濃度をそれぞれ設定した.
さらにS9 mix存在下については1600,1800,2000 μg/mLを設定して確認試験を実施した.
陽性対照として,短時間処理法のS9 mix存在下では,ベンゾ[a]ピレン(東京化成工業(株),ロット番号:GG01)の濃度を20 μg/mL,S9 mix非存在下では,マイトマイシンC(協和発酵工業(株),ロット番号:328AJF)の濃度を0.1 μg/mLに設定した.
各濃度2枚のディッシュに処理した.
8. 染色体標本作製法
培養終了の2時間前に,コルセミドを最終濃度が約0.1 μg/mLになるように培養液に加えた.染色体標本の作製は常法に従って行った.スライド標本は各ディッシュにつき2枚作製した.作製した標本を,3 vol%ギムザ溶液で20分間染色した.
9. 染色体分析
作製したスライド標本のうち,1枚のディッシュから得られたスライドを処理条件が分からないようにコード化した状態で分析した.染色体の分析は,日本製薬工業協会・医薬品評価委員会・基礎研究部会・第3分科会・遺伝毒性ワーキンググループによる分類法1)に基づいて行い,染色体型あるいは染色分体型の切断,交換などの構造異常およびギャップの有無と倍数性細胞(polyploid)の有無について観察した.ギャップは構造異常には含めなかった.また,構造異常および倍数性細胞については1群200個の分裂中期細胞を分析した.
10. 記録と測定
媒体および陽性対照群と被験物質処理群についての分析結果は,観察した細胞数,構造異常の種類と数,倍数性細胞の数について集計し,各群の値を記録用紙に記入した.被験物質の染色体異常誘発性についての判定は,石館ら2)の判定基準に従い,染色体異常を有する細胞の頻度が5 %未満を陰性,5 %以上10 %未満を疑陽性,10 %以上を陽性とした.
11. 細胞増殖率の測定
染色体標本作製と同一のサンプルにおける細胞増殖率を測定した.標本作製時に剥離した細胞の一部を採取し,血球計算盤で細胞を計数した.
結果および考察
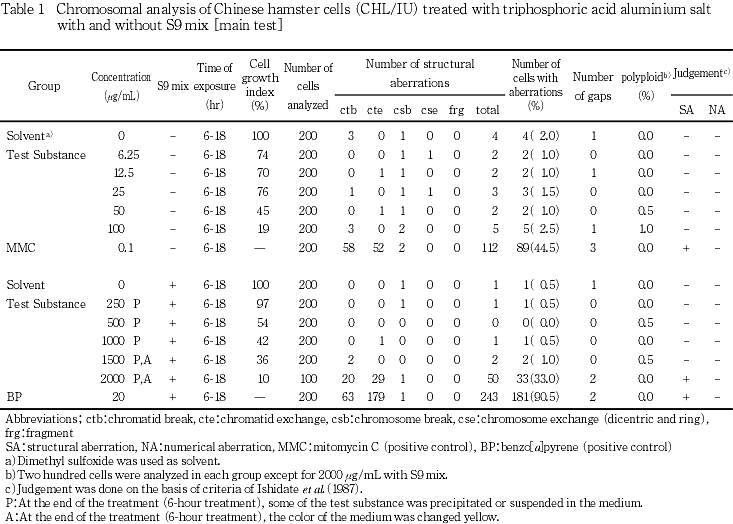
短時間処理法による染色体分析の結果をTable 1および2に示した.トリリン酸アルミニウム塩を加えてS9 mix存在下および非存在下で6時間処理した結果,短時間処理法のS9 mix存在下の2000 μg/mLにおいて,染色体構造異常細胞の出現頻度は33.0 %であり,出現頻度が最高濃度のみで急激に増加していた.
この結果より,用量依存性を検討するために,S9 mix存在下について1600,1800,2000 μg/mLを設定して確認試験を実施した.その結果,2000 μg/mLにおいて,染色体構造異常細胞の出現頻度は11.0 %となり,染色体異常誘発の再現性が認められた.
いずれの処理群においても,倍数性細胞の出現頻度は5 %未満であった.
以上の結果から,トリリン酸アルミニウム塩は本試験条件下において,染色体異常を誘発すると結論した.
なお,類似化合物であるトリポリリン酸ナトリウム2)は,連続処理法で陰性の結果が報告されている.

文献
| 1) | 日本製薬工業協会・医薬品評価委員会・基礎研究部会・第3分科会・遺伝毒性ワーキンググループ編,"医薬品のための遺伝毒性試験Q&A,"サイエンティスト社,東京,2000. |
| 2) | 祖父尼俊雄監修,"染色体異常試験データ集<改訂1998年版>,"エル・アイ・シー,東京,1999. |
| 連絡先 |
| 試験責任者: | 中川宗洋 |
| 試験担当者: | 太田絵律奈,成見香瑞範,石毛裕子,堀 一成,長友弘子 |
| (株)三菱化学安全科学研究所 鹿島研究所 |
| 〒314-0255 茨城県鹿島郡波崎町砂山14 |
| Tel 0479-46-2871 | Fax 0479-46-2874 | |
| Correspondence |
| Authors: | Munehiro Nakagawa(Study director)
Erina Ohta, Kazunori Narumi, Yuko Ishige, Kazushige Hori, Hiroko Nagatomo |
| Mitsubishi Chemical Safety Institute Ltd., Kashima Laboratory |
| 14 Sunayama, Hasaki-machi, Kashima-gun, Ibaraki, 314-0255 Japan |
| Tel +81-479-46-2871 | Fax +81-479-46-2874 | |



