2-ペンチルアントラキノンは,アントラキノン類の1つで,光重合用増感剤,アントラキノン法過酸化水素製造用水素キャリアーなどに使用されている化学物質である.2-ペンチルアントラキノンの28日間反復経口投与毒性試験(回復14日間)を雌雄のSprague-Dawley系ラットを用いて実施した.雌雄とも3.75,15および60 mg/kgの用量の被験物質投与群ならびに媒体(コーン油)を投与する対照群の計4群を設定し,28日間の反復強制経口投与を行った.試験には雌雄とも各群5匹の他,対照群および60 mg/kg投与群には回復試験として各5匹を加え,計60匹の動物を使用した.
その結果,一般状態の変化として,投与直後の一過性の流涎が60 mg/kg投与群の雌雄で散見された.
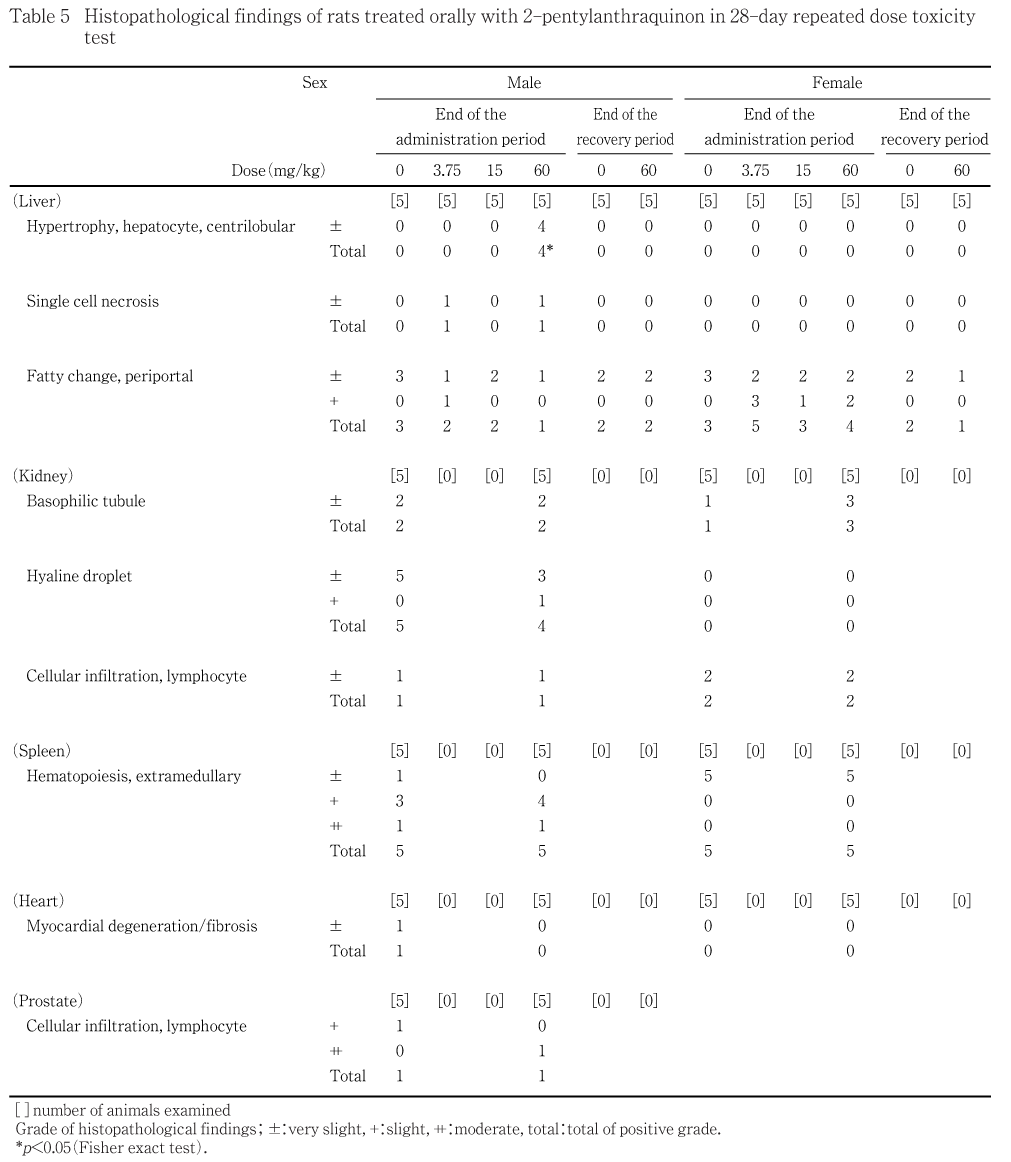
投与期間終了時の血液学検査では,プロトロンビン時間の有意な延長が15および60 mg/kg投与群の雄で観察された.また,投与期間終了時の剖検では前胃粘膜の肥厚が60 mg/kg投与群の雄で認められ,同群の雄では,肝臓の実重量および相対重量が有意に増加し,組織学検査では軽微な小葉中心性の肝細胞肥大が観察された.
回復試験期間終了時では,投与期間終了時にみられた上記の変化は観察されず,被験物質投与の影響は14日間の休薬により回復することが示唆された.
その他,体重,摂餌量,尿検査および血液生化学検査に被験物質投与の影響は認められなかった.また,詳細な症状観察および機能検査に異常は認められず,神経毒性を示唆する所見はみられなかった.
以上の結果から,本試験条件下における2-ペンチルアントラキノンの無毒性量は雄では3.75 mg/kg/day,雌では15 mg/kg/dayであると考えられた.
被験物質として,山本化成(東京)より提供された2-ペンチルアントラキノン(ロット番号01-13001-50,含量98.6 %)を使用した.被験物質は,密閉容器に入れ冷所(冷蔵)で保管した.山本化成において,動物試験前後に被験物質の品質試験を実施し,試験期間中の被験物質の安定性を確認した.
投与検体は,被験物質を秤量し,メスシリンダーを用いて媒体であるコーン油(ナカライテスク)を加えて,1.2 w/v%溶液を調製した.この1.2 w/v%溶液を段階希釈して0.3および0.075 w/v%溶液を作製した.調製後の投与検体はガラス瓶に分取し,冷蔵保管した.また,0.05および5 w/v%の調製検体について,冷蔵条件下における8日間の安定性がHPLC法で確認されたため,投与検体の調製は投与前8日以内に行った.さらに,初回調製時の投与検体について含量測定をHPLC法で実施した結果,被験物質の平均含量は所定濃度であったことが確認された.
4週齢のSprague-Dawley(SD)系〔Crj:CD(SD)IGS,SPF〕の雌雄ラット(日本チャールス・リバー)を購入し,検疫と飼育環境への馴化を兼ねて,入荷日を含め8日間予備飼育した.試験には雌雄各30匹を使用し,検疫終了時の体重を基に,体重別層化無作為抽出法により群分けした.投与開始時の週齢は5週齢であった.
動物は,温度21.0〜25.0℃,湿度40.0〜75.0 %,換気回数約15回/時間,照明12時間(7時〜19時点灯)に制御された飼育室内で,金属製金網床ケージに1匹ずつ収容し,固型飼料(CE-2,日本クレア)と水道水(秦野市水道局給水)を自由に摂取させて飼育した.
投与用量は,本試験に先立って実施した予備試験の結果を基に決定した.即ち,2-ペンチルアントラキノンを62.5,250および1000 mg/kgの用量で,雌雄各群3匹のラットに7日間反復投与した結果,1000 mg/kg投与群では雌雄各1例が死亡し,体重減少,軟便,被毛の汚れ,皮膚蒼白,自発運動の低下,褐色尿等が認められた.また,同投与群の雌雄では血液学検査で赤血球数,血色素量およびヘマトクリット値の減少が認められ,剖検所見では肝臓および腎臓の大型化,前胃粘膜の肥厚,剥離および潰瘍が認められた.250 mg/kg投与群では投与初期に軽度の体重増加抑制がみられ,62.5および250 mg/kg投与群では肝臓,腎臓および脾臓の大型化,前胃粘膜の肥厚が観察され,低用量群でも被験物質投与の影響が認められた.以上の結果から,60 mg/kgの用量を28日間反復投与した場合でも被験物質投与の影響が認められると予想されたことから,60 mg/kgを本試験の高用量とし,以下公比4で除して,中用量および低用量をそれぞれ15および3.75 mg/kgに設定した.各群の動物数は,雌雄とも対照群および高用量群を各10匹,低および中用量群を各5匹とし,対照群および高用量群の雌雄各5匹は回復試験に用いた.
投与は1日1回,28日間,ラット用胃管を用いて強制的に経口投与した.投与容量は5 mL/kgとし,各投与時の最近時の体重を基に個体別に投与液量を算出した.なお,回復試験は14日間とした.
毎日(投与期間中は投与前および投与後1回以上,回復試験期間中は1日1回),生死を含む一般状態を観察した.
毎週1回の頻度で,毎回13時〜16時にスコアリング法を用いた詳細な症状観察を行った.まず,ケージ越しでの観察(姿勢・体位,自発運動,発声,振戦,痙攣)を行った後,動物をケージから取り出して外表を観察し(取り出し易さ,扱い易さ,心拍動,体温,被毛,皮膚色,可視粘膜,流涙,眼球突出,瞳孔径,流涎),作業台上での観察(体位・姿勢,探索行動,身づくろい,発声,挙尾反応,歩行,常同行動,奇妙な行動,振戦,痙攣,呼吸数,立毛,眼裂,排尿回数,排便回数,接触に対する反応,撤去反応,耳介反射)を行った.投与量および動物番号の情報はブラインドにして実施した.また,投与第4週および回復第2週の詳細な症状観察時に機能検査を行った.機能検査は聴覚刺激に対する反応(驚愕反応),視覚刺激に対する反応(視覚定位,瞳孔反射),固有感覚刺激に対する反応(正向反射)を観察した.
体重は,投与第1週は3回,それ以降は毎週2回の頻度で測定した.また,投与期間終了日(投与第28日),回復試験期間終了日(回復第14日)および剖検日にも体重を測定した.摂餌量は,毎週1回の頻度で1日あたりの摂餌量を測定した.
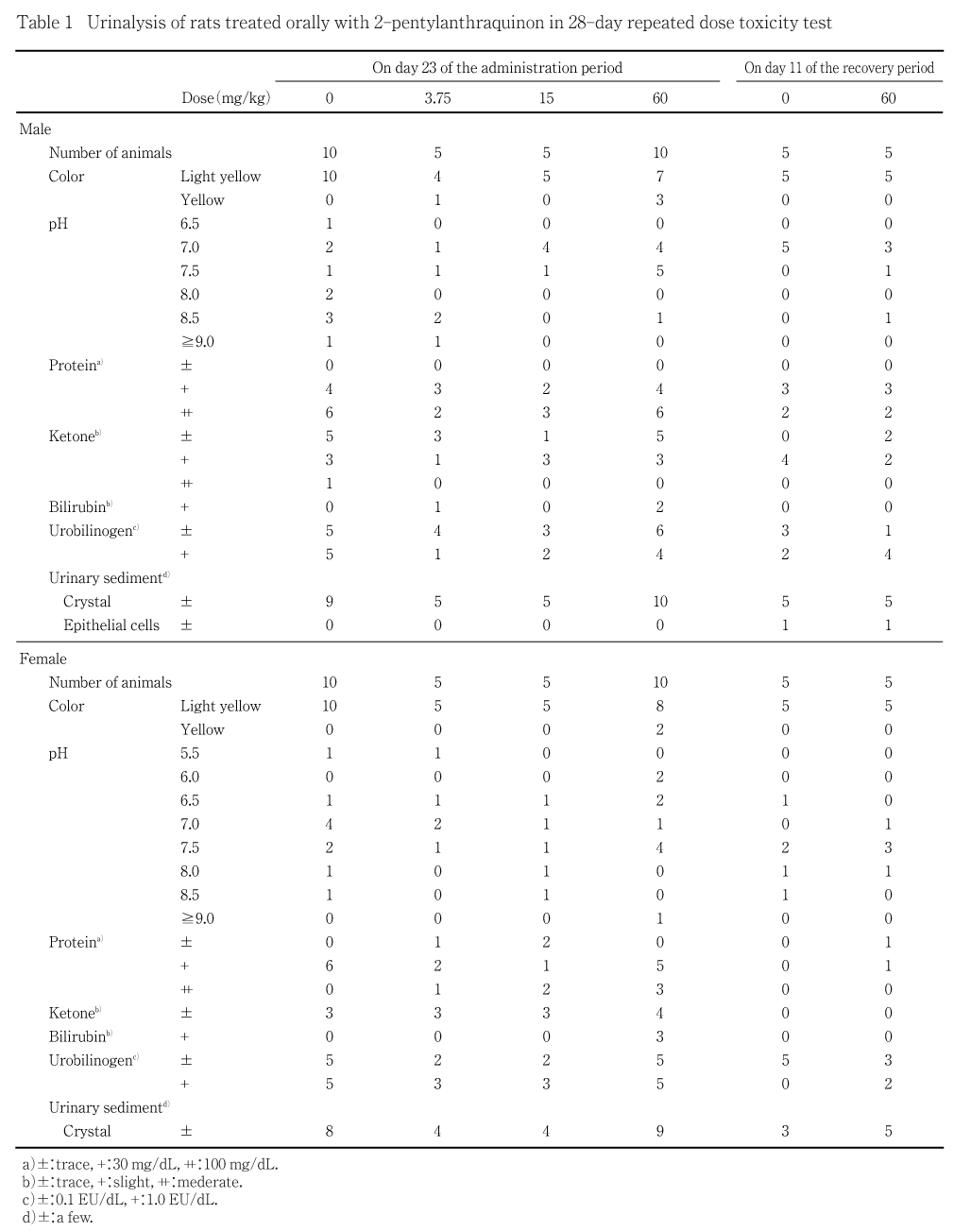
投与第4週(投与後)および回復第2週に動物を代謝ケージに収容し,採尿開始後4時間の時点で尿を採取し,視診により色調および濁度を,試験紙法(クリニテック200+,バイエル・三共)によりpH,潜血,蛋白,ブドウ糖,ケトン体,ウロビリノーゲンおよびビリルビンを,光学顕微鏡を用いて沈渣を検査した.
投与期間あるいは回復試験期間終了日から翌日の剖検日にかけて,動物を18〜21時間絶食させた.その後,ペントバルビタールナトリウム麻酔下で,腹部後大静脈から,プロトロンビン時間および活性部分トロンボプラスチン時間の測定にはクエン酸ナトリウムを抗凝固剤として,その他の血液学検査用にはEDTA-2Kを抗凝固剤として採血し,血液生化学検査用にはヘパリンを抗凝固剤として採血した.採血は可能な限り対照群から低,中,高用量群の順に各群1匹ずつ,動物番号の若いほうから選抜して行った.
血液自動分析装置(CELL-DYN3500,ダイナボット)を用いて,電気抵抗法により赤血球数(RBC),平均赤血球容積(MCV)および血小板数,フローサイトメトリー・レーザー光散乱法/電気抵抗法により白血球数(WBC),フローサイトメトリー・レーザー光散乱法により白血球分類,吸光度法により血色素量を測定し,これらを基にヘマトクリット値,平均赤血球血色素量(MCH)および平均赤血球血色素濃度(MCHC)を算出した.また,全自動血液凝固測定装置(CA-1000,東亜医用電子)を用いて,光散乱検出法によりプロトロンビン時間(PT)および活性部分トロンボプラスチン時間(APTT)を測定した.さらに,光学顕微鏡を用いたBrecher法により,網状赤血球比率を算出した.
生化学自動分析装置(COBAS MIRA plus,ロシュ・ダイアグノスティックス)を用いて,ビウレット法により総蛋白濃度,BCG法によりアルブミン濃度,コレステロールオキシダーゼ・HDAOS法により総コレステロール濃度,GPO・HDAOS(グリセリン消去)法によりトリグリセライド濃度,ヘキソキナーゼ・G-6-PDH法によりグルコース濃度,ウレアーゼ・GlDH法により尿素窒素濃度(BUN),Jaff事@によりクレアチニン濃度,アゾビリルビン法により総ビリルビン濃度,GSCC法によりアルカリフォスファターゼ(ALP)活性,IFCC法によりアスパラギン酸アミノトランスフェラーゼ(AST)活性,アラニンアミノトランスフェラーゼ(ALT)活性およびg-グルタミルトランスペプチダーゼ(g-GTP)活性,OCPC法によりカルシウム濃度,モリブデン酸直接法により無機リン濃度を測定し,アルブミン/グロブリン(A/G)比を算出した.また,全自動電解質分析装置(EA05,エイアンドティー)を用いたイオン電極法によりナトリウムイオン濃度,カリウムイオン濃度および塩素イオン濃度を測定した.
採血後,必要に応じて腋窩動脈を切断して放血屠殺し,器官および組織の肉眼的観察を実施した.また,各動物の肝臓,腎臓,副腎,精巣,精巣上体,卵巣,胸腺,脾臓,脳,心臓および甲状腺の重量(実重量)を測定したほか,各器官の重量を剖検日の体重で除して比体重値(相対重量)を算出した.肉眼的観察に引き続き,全例の肉眼的病変部,脳,脊髄,胃,小腸(十二指腸,空腸,回腸),大腸(結腸,直腸),肝臓,腎臓,副腎,脾臓,心臓,胸腺,甲状腺,気管,肺(気管支を含む),生殖腺(精巣,卵巣),副生殖器(精巣上体,前立腺,子宮,精嚢,腟),膀胱,リンパ節(腸間膜リンパ節,下顎リンパ節),坐骨神経(腓腹筋を含む),大腿骨および骨髄,大動脈,舌,食道,膵臓,顎下腺,舌下腺,下垂体,上皮小体および眼球を0.1 Mリン酸緩衝10 %ホルマリン溶液に固定した.ただし,精巣および精巣上体はブアン液に固定した.次いで,投与期間終了時の対照群および高用量群の固定した器官および組織(ただし,十二指腸,空腸,直腸,精嚢,腟,大腿骨,大動脈,舌,食道および上皮小体を除く)をパラフィン包埋して薄切し,ヘマトキシリン・エオジン染色標本を作製した後,光学顕微鏡を用いて病理組織学的に検査した.この検査の結果,肝臓に被験物質投与に起因した可能性のある変化が認められたため,回復試験群を含む全例の肝臓の組織学的検査を実施した.
体重,摂餌量,血液学検査および血液生化学検査値ならびに器官重量の各測定値については,群ごとに平均値および標準偏差を求めた.検定対象が対照群を含めて4群の場合,Bartlettの方法により分散の一様性について検定を行い,一元配置型の分散分析およびDunnett法,あるいはKruskal-Wallisの順位検定およびDunnett型の検定法で多重比較を行った.検定対象が対照群を含めて2群の場合,F検定を行い,Studentのt検定あるいはAspin-Welchのt検定を行った.
尿の試験紙による検査成績,尿の色調および濁度については,投与第4週に得られた各検査値は,列の累積または分割表を用いるx^2検定を行い,Dunnett型の検定法により多重比較を行った.回復第2週に得られた各検査値は,Wilcoxonの順位和検定を行った.
病理組織所見のグレード分けしたデータはMann- WhitneyのU検定により,また陽性グレードの合計値はFisherの直接確率の片側検定を行った.
なお,いずれの場合も有意水準は5 %とした.
死亡例および切迫屠殺例はいずれの群にもみられなかった.
投与期間中,60 mg/kg投与群の雄3例,雌4例で,投与直後の一過性の流涎が投与第3週以降に散見された.その他,15 mg/kg投与群の雌1例では解剖当日に爪をケージ等に引っかけたためと思われる爪剥がれによる出血が認められた.
回復試験期間中には,いずれの群にも一般状態の変化は認められなかった.
投与期間中および回復試験期間中ともに,いずれの群にも詳細な症状観察に特記すべき変化は認められず,神経毒性を示唆する所見は観察されなかった.また,投与第4週および回復第2週の機能検査でも,いずれの群においても異常は認められなかった.
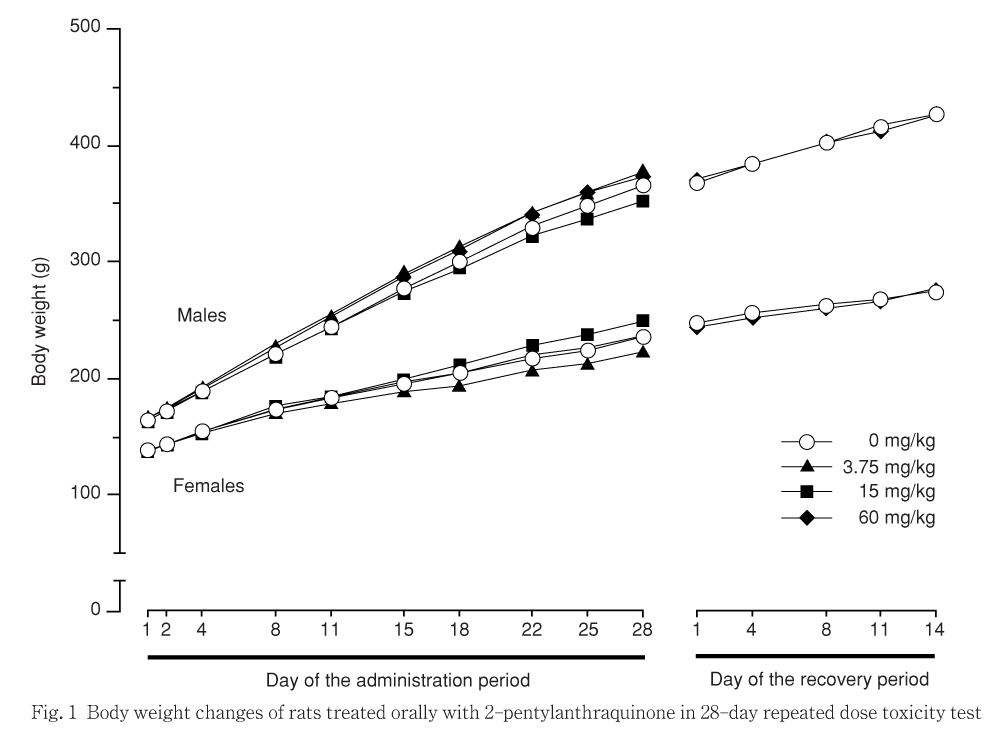
投与期間中および回復試験期間中ともに,各被験物質投与群の体重および体重増加量は対照群との間に差は認められなかった.

投与期間中および回復試験期間中ともに,各被験物質投与群の摂餌量は対照群との間に差は認められなかった.

投与第4週および回復第2週の検査ともに,いずれの群においても異常は認められず,対照群と各被験物質投与群との間に差は認められなかった.
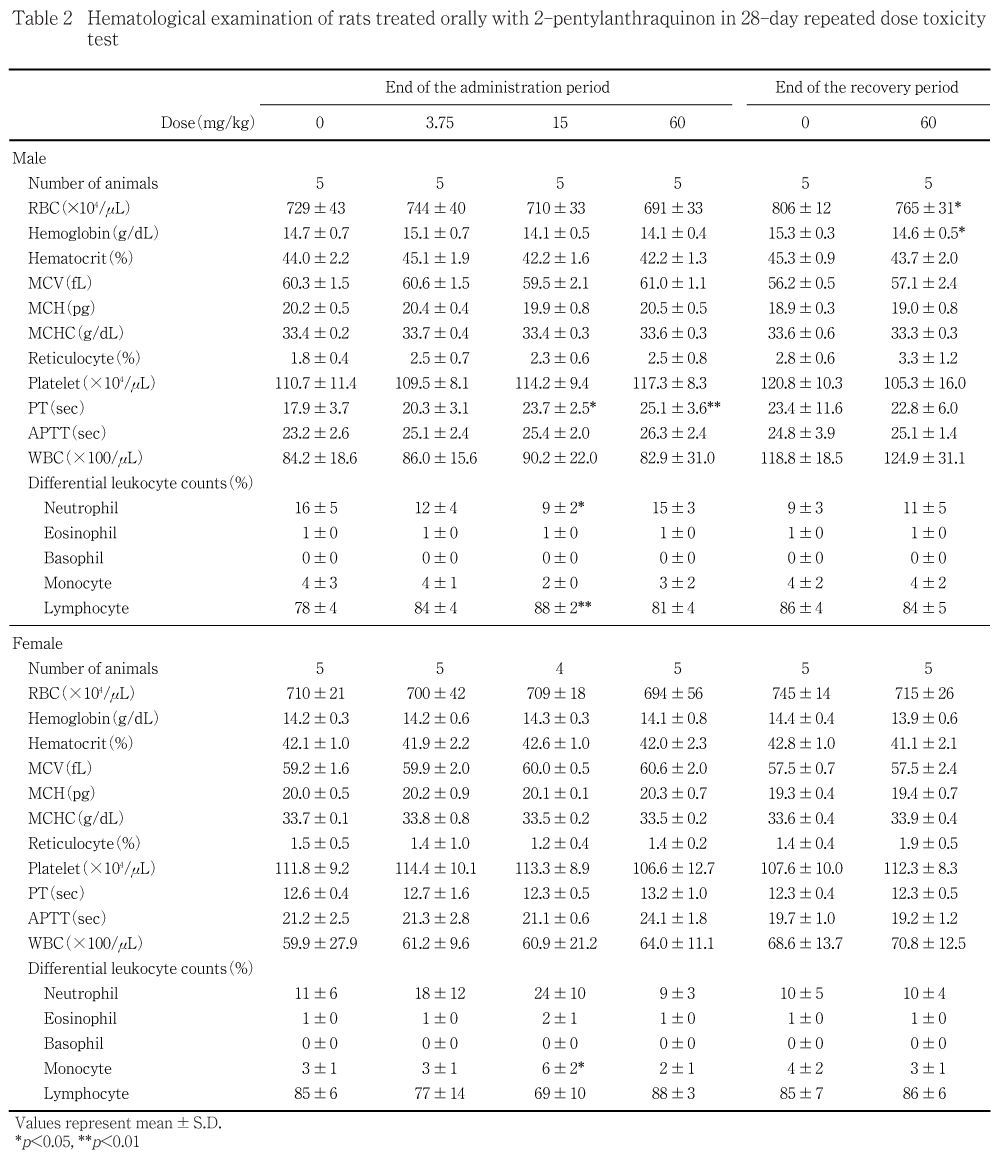
投与期間終了時の検査では,プロトロンビン時間の有意な延長が15および60 mg/kg投与群の雄でみられた.また,60 mg/kg投与群の雄では赤血球数が低い傾向がみられた.その他,好中球比率の減少およびリンパ球比率の増加が15 mg/kg投与群の雄で,単球比率の増加が15 mg/kg投与群の雌でそれぞれ有意に認められた.白血球百分比を絶対数に換算して比較すると,各被験物質投与群の各白血球数は対照群との間に差は認められなかったことから,白血球百分比の変化は被験物質投与による影響ではないと判断した.
回復試験期間終了時の検査では,赤血球数および血色素量の有意な減少が60 mg/kg投与群の雄でみられた.
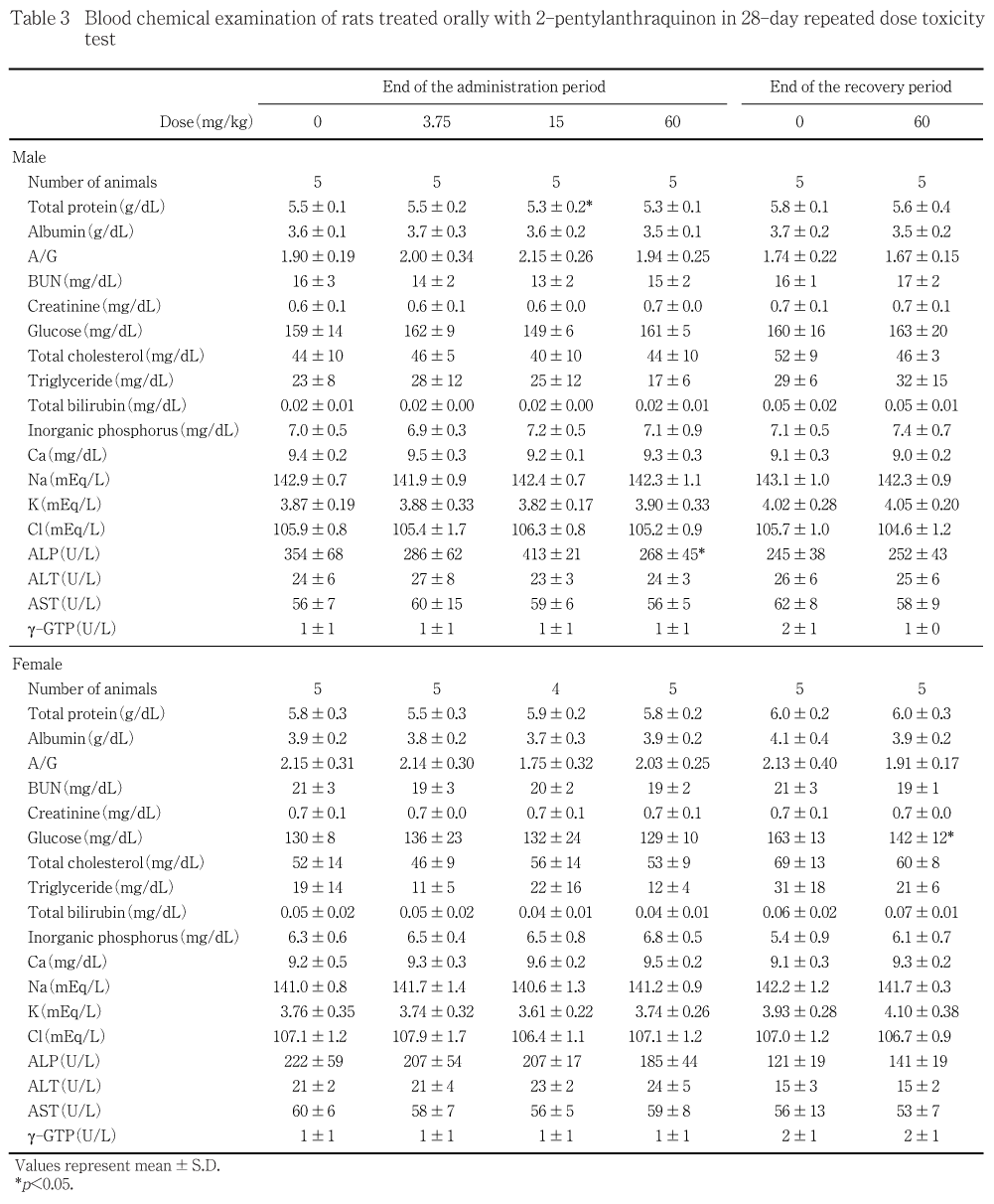
投与期間終了時の検査では,アルカリフォスファターゼ活性の有意な低下が60 mg/kg投与群の雄でみられた.また,総蛋白濃度の有意な減少が15 mg/kg投与群の雄で認められたが,アルブミン濃度やA/G比に変化はみられず,60 mg/kg投与群では有意差が認められなかったことから,被験物質投与による影響ではないと判断した.
回復試験期間終了時の検査では,グルコース濃度の有意な減少が60 mg/kg投与群の雌で認められた.
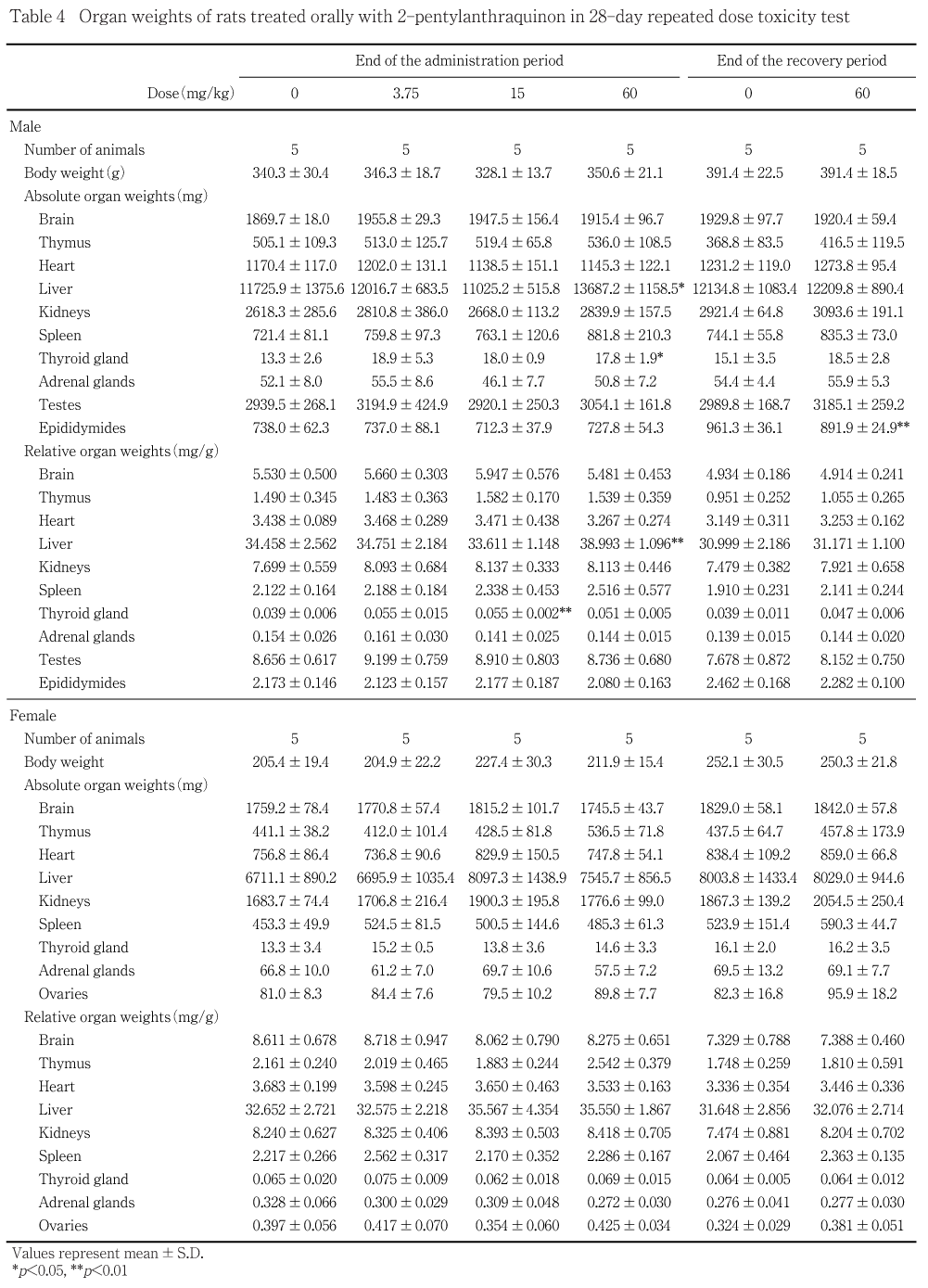
投与期間終了時剖検例では,肝臓の実重量および相対重量の有意な増加が60 mg/kg投与群の雄でみられた.また,甲状腺の実重量の有意な増加が60 mg/kg投与群の雄で,甲状腺の相対重量の有意な増加が15 mg/kg投与群の雄で認められた.
回復試験期間終了時剖検例では,精巣上体の実重量の有意な減少が60 mg/kg投与群の雄でみられたが,相対重量に変化は認められなかったこと,投与期間終了時剖検例の精巣上体重量や組織学的変化はみられなかったことから,被験物質投与による影響ではないと判断した.
投与期間終了時剖検例において,前胃粘膜の肥厚が60 mg/kg投与群の雄1例で観察された.回復試験期間終了時剖検例では,肉眼的異常所見は認められなかった.
肝臓では,軽微な小葉中心性の肝細胞肥大が60 mg/kg投与群の雄4例でみられ,この所見の発現頻度は対照群と比較して有意に高かった.また,軽微な単細胞壊死が3.75および60 mg/kg投与群の各雄1例で,軽微あるいは軽度の門脈周囲性の肝細胞脂肪化が対照群を含む雌雄の各群で認められたが,いずれの変化も対照群に比較して差はなかった.
腎臓では,軽微な好塩基性尿細管およびリンパ球浸潤が対照群および60 mg/kg投与群の雌雄で,軽微あるいは軽度の硝子滴が対照群および60 mg/kg投与群の雄で認められたが,いずれの変化も対照群に比較して差はなかった.
脾臓では,軽微から中等度の髄外造血が対照群および60 mg/kg投与群の雌雄全例で認められたが,対照群に比較して差はなかった.
前立腺では,軽度あるいは中等度のリンパ球浸潤が対照群および60 mg/kg投与群の各雄1例で認められたが,対照群に比較して差はなかった.
心臓では,軽微な心筋の変性/線維化が対照群の雄1例で観察された.
剖検で前胃粘膜の肥厚が観察された60 mg/kg投与群を含め,胃には組織学的異常所見は認められなかった.
病理組織学検査を実施したその他の器官には,組織学的異常所見は認められなかった.
肝臓では,軽微な門脈周囲性の肝細胞脂肪化が対照群および60 mg/kg投与群の雌雄で認められたが,対照群に比較して差はなかった.
2-ペンチルアントラキノンを3.75,15および60 mg/kg の用量で雌雄のSprague-Dawley系ラットに28日間反復経口投与し,その後14日間の回復試験を実施した.
その結果,高用量群の雄では,投与期間終了時に肝臓の実重量および相対重量が有意に増加し,組織学検査では軽微な小葉中心性の肝細胞肥大が認められた.本被験物質と同じアントラキノン類である2-エチルアントラキノン1)やアントラキノン2)の28日間経口投与試験あるいは1-アミノ-2,4-ジブロモアントラキノンの13週間混餌投与試験 3)でも,肝臓に同様の変化が観察されていることから,本試験でみられた肝臓の変化は被験物質投与の影響であると考えられた.
また,高用量群の雄1例では投与期間終了時に前胃粘膜の肥厚が観察された.予備試験でも2-ペンチルアントラキノン1000 mg/kg投与群で前胃粘膜の肥厚,剥離および潰瘍がみられ,62.5および250 mg/kg投与群でも前胃粘膜の肥厚が観察されたことから,被験物質が刺激性物質であり,前胃粘膜に軽度の傷害を生じたものと考えられた4).また,高用量群の雌雄で投与期間中に散見された投与直後の一過性の流涎も,被験物質の刺激によって生じたと考えられた.
血液学検査では,投与期間終了時に15および60 mg/ kg投与群の雄で用量依存的なプロトロンビン時間の延長がみられた.アントラキノン類である2-ペンチルアントラキノンとp-ナフトキノンの誘導体であるビタミンKは同じキノン化合物であることから,肝臓でプロトロンビン生成や血液凝固因子形成促進の役割を果たしているビタミンKの作用に被験物質が影響を及ぼしている可能性は十分にある.よって,プロトロンビン時間の延長は被験物質投与による影響であると考えられた.また,高用量群の雄で,投与期間終了時に赤血球数の減少傾向が,回復試験期間終了時に赤血球数および血色素量の有意な減少がみられた.予備試験の血液学検査でも貧血所見がみられたほか,脾臓の大型化が認められた.また,前述したアントラキノン類 1-3)のほか1-アミノアントラキノンの反復経口投与毒性・生殖発生毒性併合試験 5)でも貧血所見が認められており,溶血性貧血の可能性が示唆されている.一方,本試験では網状赤血球の増加や骨髄の造血亢進像,脾臓の髄外造血増強は認められておらず,尿検査および血液生化学検査でも溶血を示唆する所見はみられていない.また,出血所見もみられず血液生化学検査から血液希釈の可能性も考えられない.従って,赤血球数および血色素量の減少と被験物質投与との関連も疑われたが,その原因を明らかにすることはできなかった.
その他,血液生化学検査では,アルカリフォスファターゼ活性の有意な低下が投与期間終了時に高用量群の雄でみられたが,血中カルシウム濃度に変動はみられないことから,被験物質投与による影響ではないと判断した.また,回復試験期間終了時にグルコース濃度の有意な減少が高用量群の雌で認められたが,投与期間終了時ではグルコースに変動はみられず,膵臓,副腎および甲状腺に器質的変化は認められなかったことから,被験物質との関連はないと考えられた.さらに,投与期間終了時に甲状腺の実重量の有意な増加が60 mg/kg投与群の雄で,甲状腺の相対重量の有意な増加が15 mg/kg投与群の雄で認められたが,甲状腺に組織学的な変化は認められなかった.また,これらの甲状腺重量の変化と背景データを比較すると大きな差は認められなかったことから,被験物質投与による影響ではないと判断した.
体重,摂餌量および尿検査に被験物質投与の影響は認められなかった.詳細な症状観察および機能検査でも異常は認められず,2-ペンチルアントラキノンの神経毒性を示唆する所見は観察されなかった.
以上の結果から,2-ペンチルアントラキノン投与によりプロトロンビン時間の延長,肝重量の増加および肝細胞肥大が認められ,また,被験物質の刺激による流涎や前胃粘膜の肥厚が観察された.これらの変化は14日間の休薬により回復することが示唆された.従って,本試験条件下における2-ペンチルアントラキノンの無毒性量は雄では3.75 mg/kg/day,雌では15 mg/kg/dayであると考えられた.
| 1) | 畔上二郎ら: 2-エチルアントラキノンのラットを用いる28日間反復経口投与毒性試験.化学物質毒性試験報告,8:179-188(2001). |
| 2) | IUCLID(International Uniform Chemical Infor-mation Data Base)Data Sheet, Substance ID:84- 65-1. EU(2000). |
| 3) | Fleischman RW, Esber HJ, Hagopian M, Lilja HS, Huff J:Thirteen-week toxicology studies of 1-amino-2,4-dibromoanthraquinone in Fischer 344/N rats and B6C3F1 mice. Toxicol Appl Pharmacol, 82: 389-404(1986). |
| 4) | 高橋道人(監訳):「毒性病理学の基礎」第1版,ソフトサイエンス社,東京(1992) pp.85-93. |
| 5) | 長尾哲二ら:1-アミノアントラキノンのラットを用いる反復経口投与毒性・生殖発生毒性併合試験.化学物質毒性試験報告,3:87-101(1996). |
| 連絡先 | |||
| 試験責任者: | 立花滋博 | ||
| 試験担当者: | 田子和美,野口早苗,加藤博康, 関 剛幸,古谷真美,永田伴子, 堀内伸二,稲田浩子,三枝克彦, 安生孝子 | ||
| (財)食品薬品安全センター秦野研究所 | |||
| 〒257-8523 神奈川県秦野市落合729-5 | |||
| Tel 0463-82-4751 | Fax 0463-82-9627 | ||
| Correspondence | |||
| Authors: | Shigehiro Tachibana (Study Director) Kazumi Tago, Sanae Noguchi, Hiroyasu Kato, Takayuki Seki, Mami Furuya, Tomoko Nagata, Shinji Horiuchi, Hiroko Inada, Katsuhiko Saegusa, Takako Anjo |
||
| Hatano Research Institute, Food and Drug Safety Center 729-5 Ochiai, Hadano-shi, Kanagawa, 257-8523, Japan | |||
| Tel +81-463-82-4751 | Fax +81-463-82-9627 | ||