| AF-2 | : | 2-(2-フリル)-3-(5-ニトロ-2-フリル)アクリルアミド(和光純薬工業 ) ) |
| 2-AA | : | 2-アミノアントラセン(和光純薬工業 ) ) |
| SA | : | アジ化ナトリウム(和光純薬工業 ) ) |
| 9-AA | : | 9-アミノアクリジン(Aldrich Chemical Co.) |
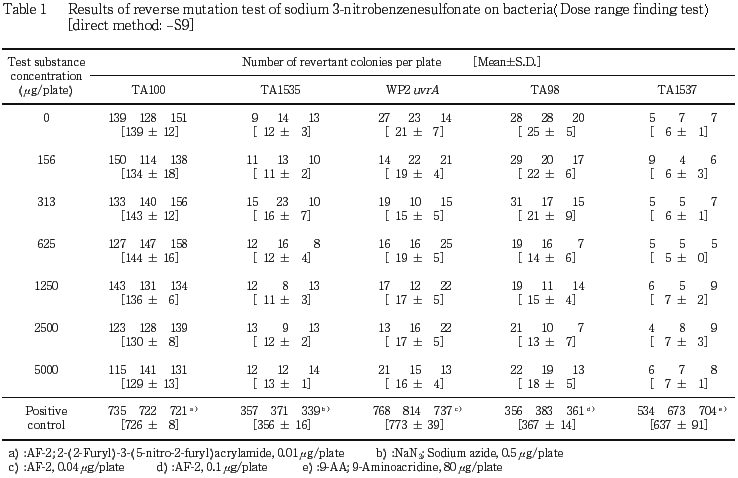
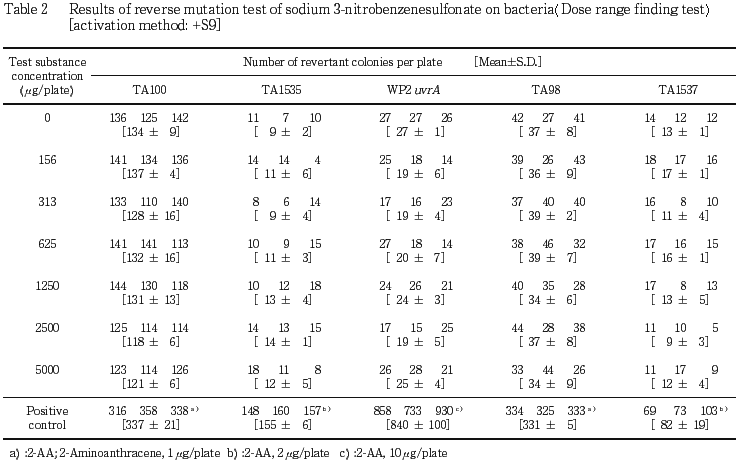
試験は,指標菌株としてSalmonella typhimurium TA100,TA1535,TA98,TA1537およびEscherichia coli WP2 uvrAを用い,S9 mix非存在(直接法)および存在(代謝活性化法)下でプレインキュベーション法により行った.
156,313,625,1250,2500および5000 μg/プレート濃度を設定して行った濃度設定試験では,代謝活性化の有無にかかわらず,全ての菌株において生育阻害は認められず,いずれの濃度においても溶媒対照と比較して2倍以上の復帰変異コロニー数の増加は認められなかった.したがって,本試験は,濃度設定試験と同じ濃度を用いて同様に行った.
試験の結果,濃度設定試験と同様,全ての菌株において代謝活性化の有無にかかわらず,復帰変異コロニー数の増加は認められず,また,菌の生育阻害も認められなかった.
以上の成績から,本実験条件下では,3-ニトロベンゼンスルホン酸ナトリウムは,細菌に対し遺伝子突然変異を誘発しない(陰性)と結論した.
試験に際して,各凍結菌株を解凍後,その30 μLをニュートリエントブロス(Bacto nutrient broth dehydrated,Difco Laboratories)液体培地15 mLに接種し,37℃で12時間振盪培養した.培養後の菌懸濁液は,濁度を測定し,濁度と生菌数の換算式より1 mLあたり1×10^9 以上の生菌数が得られていることを確認し,試験菌液とした.
各菌株の遺伝的特性検査は,凍結保存菌の調製時並びに各実験ごとに行い,本試験に用いた菌株が規定の特性を保持していることを確認した.
 提供)は,淡黄色の粉末で,水に対しては20%(20℃)溶け,ジメチルスルホキシド(DMSO)に易溶,アセトンに対しては難溶であり,分子式 C6H4NNaO5S,分子量225.15,純度98.8%(不純物として,芒硝0.63%,食塩0.04%,水分0.86%,3,3'-ジニトロジフェニルスルホン0.04%を含む)の物質である.
提供)は,淡黄色の粉末で,水に対しては20%(20℃)溶け,ジメチルスルホキシド(DMSO)に易溶,アセトンに対しては難溶であり,分子式 C6H4NNaO5S,分子量225.15,純度98.8%(不純物として,芒硝0.63%,食塩0.04%,水分0.86%,3,3'-ジニトロジフェニルスルホン0.04%を含む)の物質である.実験終了後,被験物質提供元において残余被験物質を分析した結果,安定性に問題はなかった.
 大塚製薬工場)を用い,被験物質を溶解して最高濃度の供試液(原液)を調製した.この原液の一部を溶媒で順次希釈して所定濃度の供試液を調製した.供試液は,用時調製した.
大塚製薬工場)を用い,被験物質を溶解して最高濃度の供試液(原液)を調製した.この原液の一部を溶媒で順次希釈して所定濃度の供試液を調製した.供試液は,用時調製した.
| AF-2 | : | 2-(2-フリル)-3-(5-ニトロ-2-フリル)アクリルアミド(和光純薬工業 ) ) |
| 2-AA | : | 2-アミノアントラセン(和光純薬工業 ) ) |
| SA | : | アジ化ナトリウム(和光純薬工業 ) ) |
| 9-AA | : | 9-アミノアクリジン(Aldrich Chemical Co.) |
AF-2および2-AAはDMSO( 同仁化学研究所)に,SAおよび9-AAは蒸留水(
同仁化学研究所)に,SAおよび9-AAは蒸留水( 大塚製薬工場)に溶解した.
大塚製薬工場)に溶解した.
 )を購入し,使用した.培地1 Lあたりの組成は下記のとおりであり,径90 mmのシャーレ1枚あたりに30 mLを分注したものである.
)を購入し,使用した.培地1 Lあたりの組成は下記のとおりであり,径90 mmのシャーレ1枚あたりに30 mLを分注したものである.
| 硫酸マグネシウム・七水塩 | 0.2 g |
| クエン酸・一水塩 | 2 g |
| リン酸水素二カリウム | 10 g |
| リン酸一アンモニウム | 1.92 g |
| 水酸化ナトリウム | 0.66 g |
| グルコース | 20 g |
| 寒天(OXOID Agar No.1) | 15 g |
 )を購入し,使用した.S9は,誘導剤としてフェノバルビタールおよび5,6-ベンゾフラボンを投与したSprague-Dawley系雄ラットの肝臓から調製されたものである.
)を購入し,使用した.S9は,誘導剤としてフェノバルビタールおよび5,6-ベンゾフラボンを投与したSprague-Dawley系雄ラットの肝臓から調製されたものである.
試験管に使用溶媒,被験物質供試液あるいは陽性対照物質溶液を0.1 mL,次いで直接法では0.1 Mリン酸ナトリウム緩衝液(pH 7.4)を0.5 mL,代謝活性化法ではS9 mixを0.5 mL加え,続いて試験菌液0.1 mLを分注し,37℃で20分間振盪培養した.培養終了後,45℃に保温したトップアガー2 mLを加えた混合液をプレート上に重層した.37℃で48時間培養後,復帰変異コロニーを計数し,同時に指標菌株の生育阻害の有無を実体顕微鏡を用いて観察した.プレートは,各濃度とも3枚を使用した.
| 1) | 被験物質処理群において溶媒対照値の2倍以上の復帰変異コロニー数が出現する. |
| 2) | 被験物質濃度の増加とともに復帰変異コロニー数が増加する(濃度依存性). |
| 3) | 濃度設定試験および本試験の結果から,復帰変異コロニー数の増加に再現性が認められる. |
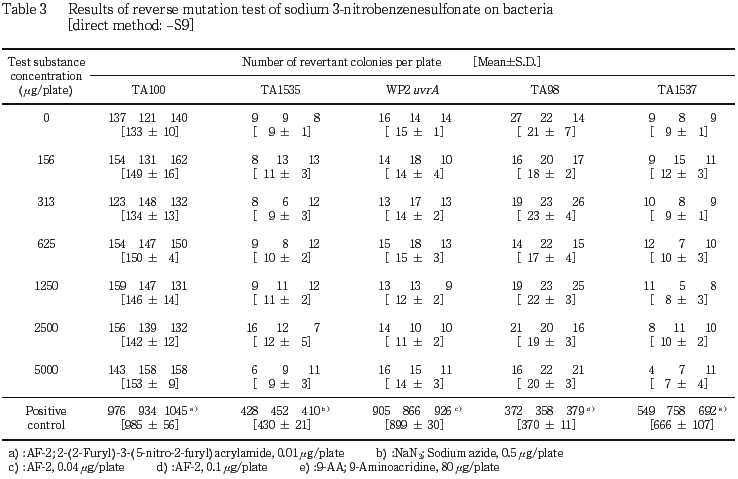
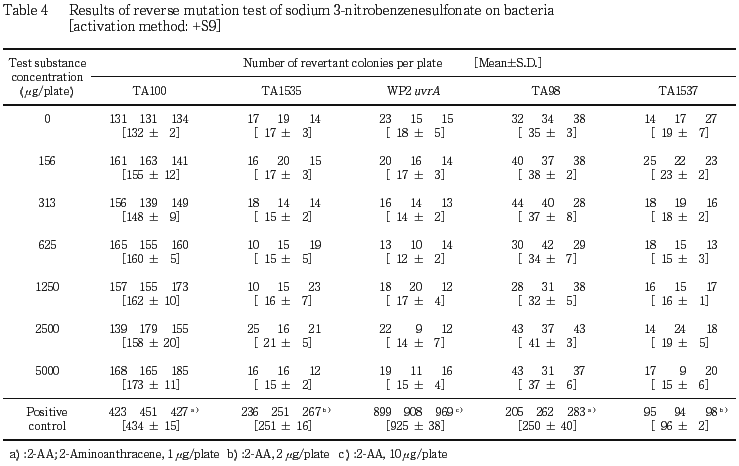
本試験の結果(Table 3,4)は,濃度設定試験と同様,直接法および代謝活性化法のいずれの場合も,供試した全ての菌株における復帰変異コロニー数は,溶媒対照値の2倍を越えるものではなかった.また,いずれの菌株においても生育阻害は認められなかった.
以上の成績から,本実験条件下では,3-ニトロベンゼンスルホン酸ナトリウムの遺伝子突然変異誘発性は陰性と判定した.
なお,類縁化合物である2-ニトロベンゼンスルホン酸,3-ニトロベンゼンスルホン酸,4-ニトロベンゼンスルホン酸の変異原性については,いずれもS. typhimurium TA98,TA100を用いた復帰突然変異試験で陰性3)と報告されている.
| 1) | D.M. Maron, B.N. Ames, Mutat. Res., 113, 173 (1983). |
| 2) | M.H.L. Green, "Handbook of Mutagenicity Test Procedures,"1, Vol.3, eds. by B.J. Kilbey, M. Legator, W. Nichols, C. Ramel, Elsevier, Amsterdam, New York, Oxford, 1984, pp. 161-187. |
| 3) | 河合昭宏,後藤純雄,松本由美子,松下秀鶴,産業医学,29,34(1987). |
| 連絡先 | |||
| 試験責任者: | 野田 篤 | ||
| 試験担当者: | 野田 篤,昆 尚美 | ||
| (財)畜産生物科学安全研究所 | |||
| 〒229-1132 神奈川県相模原市橋本台3-7-11 | |||
| Tel 042-762-2775 | Fax 042-762-7979 | ||
| Correspondence | ||||
| Authors: | Atsushi Noda(Study director) Naomi Kon | |||
| Research Institute for Animal Science in Biochemistry and Toxicology | ||||
| 3-7-11 Hashimotodai, Sagamihara-shi, kanagawa, 229-1132, Japan | ||||
| Tel +81-42-762-2775 | Fax +81-42-762-7979 | |||