メタクリロニトリルの培養細胞に及ぼす細胞遺伝学的影響について,チャイニーズ・ハムスター培養細胞(CHL/IU)を用いて染色体異常試験を実施した.
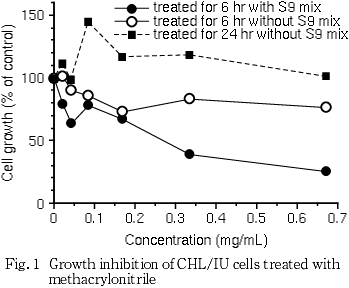
連続処理(24時間)およびS9 mix非存在下の短時間処理(6時間)では,0.67 mg/mL(10 mM)の濃度においても50 %を越える細胞増殖抑制は認められなかった.S9 mix存在下の短時間処理における50 %細胞増殖抑制濃度は,0.27 mg/mLであった.従って,連続処理およびS9 mix非存在下での短時間処理では,0.67 mg/mL(10 mM)を最高濃度とし,公比2で3濃度設定した.S9 mix存在下での短時間処理では,50 %細胞増殖抑制濃度の約2倍濃度を最高処理濃度とし,公比2で5濃度設定した.連続処理では,24時間処理後,短時間処理ではS9 mix非存在下および存在下で6時間処理し,新鮮培地で更に18時間培養後,標本を作製し,検鏡することにより染色体異常誘発性を検討した.染色体分析が可能な最高濃度は,24時間連続処理およびS9 mix非存在下の短時間処理では0.67 mg/mL(10 mM),S9 mix存在下での短時間処理では0.27 mg/mLであったことから,これらの濃度を高濃度群として3濃度群を観察対象とした.
CHL/IU細胞を24時間連続処理およびS9 mix非存在下で短時間処理したいずれの処理群においても,染色体の構造異常および倍数性細胞の誘発作用は認められなかった.S9 mix存在下の短時間処理では,すべての処理群(0.068-0.27 mg/mL)で染色体異常の誘発作用が認められ,その誘発頻度は7.5-62.0 %(gapを除く)であった.倍数性細胞の誘発作用は低濃度群(0.068 mg/mL)および中濃度(0.14 mg/mL)で観察され,出現頻度はそれぞれ3.13 %および1.88 %であった.傾向性検定では有意差(p<0.01)が認められなかったが,それは分裂遅延による可能性が考えられた.
以上の結果より,本試験条件下でメタクリロニトリルは,染色体異常を誘発する(陽性)と結論した.
その結果,連続処理およびS9 mix非存在下での短時間処理では,最高処理濃度の0.67 mg/mL (10 mM)においても50 %を越える細胞増殖抑制作用は認められなかった.S9 mix存在下の短時間処理における50 %細胞増殖抑制濃度は0.27 mg/mLであった(Fig. 1).

染色体異常試験において,溶媒対照群と処理群では1濃度あたり2フラスコを用い,染色体標本の作製およびコールターカウンターによる細胞増殖率測定を行った.無処理対照群および陽性対照群についてはコールターカウンターによる細胞増殖率測定は行わなかった.
作製したスライド標本のうち,1つのフラスコから得られた異なるスライドを,4名の観察者がそれぞれ処理条件が分からないようにコード化した状態で分析した.染色体の分析は,日本環境変異原学会・哺乳動物試験研究会(MMS)1)による分類法に基づいて行い,染色体型あるいは染色分体型のギャップ,切断,交換などの構造異常の有無と倍数性細胞(polyploid)の有無について観察した.また構造異常については1群200個,倍数性細胞については1群800個の分裂中期細胞を分析した.
染色体異常を有する細胞の出現頻度について,溶媒対照群と被験物質処理群および陽性対照群間でフィッシャーの直接確率法2)により,有意差検定を実施した (p<0.01).また,用量依存性に関してコクラン・アーミテッジの傾向性検定3) (p<0.01)を行った.これらの検定結果を参考とし,生物学的な観点からの判断を加味して染色体異常誘発性の評価を行った.
短時間処理による染色体分析の結果をTable 2に示した.メタクリロニトリルを加え,S9 mix非存在下で処理したいずれの処理群においても,染色体の構造異常および倍数性細胞の誘発作用は認められなかった.一方,S9 mix存在下で短時間処理したすべての処理群(0.068〜0.27 mg/mL)において,染色体の構造異常の誘発が見られ,その出現頻度は7.5〜62.0 %(gapを除く)であった.また,低濃度群(0.068 mg/mL)および中濃度群(0.14 mg/mL)で倍数性細胞の有意な(p<0.01)増加が認められ,その出現頻度は3.13 %および1.88 %であったが,傾向性検定の結果,濃度依存性は認められなかった(p<0.01).これは,高濃度群(0.27 mg/mL)では細胞増殖率が57.5 %と高い値であったにもかかわらず,分裂指数が低下していることや毒性のため800細胞観察できなかった(観察細胞数:733細胞)ことから,分裂遅延により倍数性細胞の頻度が濃度依存的に減少した可能性が考えられた.
メタクリロニトリルのメチル基が水素に置換しているアクリロニトリルは,代謝活性化の有無に関係なく染色体の構造異常を誘発するが,倍数性細胞を誘発しないことが報告されている4).また,メタクリロニトリルのニトリル基がメチルエステルに置換しているメチルメタクリラートは染色体の構造異常を誘発するが,その作用は弱い5).これらのことから,化学構造が類似したこれらの3物質は,ともに染色体の構造異常を誘発するがその作用機序が異なる可能性が示唆された.
なお.メタクリロニトリルやメチルメタクリラートについては,復帰変異試験およびショウジョウバエを用いた伴性劣性致死試験において陰性の結果が報告されている6-9)が,アクリロニトリルは,復帰変異試験で陽性の結果が得られている4).

| 1) | 日本環境変異原学会・哺乳動物試験分科会編,“化学物質による染色体異常アトラス,”朝倉書店,東京,1988, pp.16-37. |
| 2) | 吉村功編,“毒性・薬効データの統計解析,事例研究によるアプローチ,”サイエンティスト社,東京,1987, pp. 76-78. |
| 3) | 吉村功,大橋靖夫編,“毒性試験講座14,毒性試験データの統計解析,”地人書館,東京,1992, pp. 218-223. |
| 4) | 石舘基監修,“改訂増補 染色体異常試験データ集,”株式会社エル・アイ・シー,東京,1987,p. 9. |
| 5) | C. L. Doerr et al., Mutat. Res., 222, 191(1989). |
| 6) | E. Zeiger et al., Environ. Mutagen., 9, 1(1987). |
| 7) | S. Zimmering et al., Environ. Mol. Mutagen., 14, 245 (1989) |
| 8) | T. H. J. M. Waegemaekers and M. P. M. Bensink, Mutat. Res., 137, 95(1984) |
| 9) | H. Schweikl et al., Mutat. Res., 415, 119(1998) |
| 連絡先 | |||
| 試験責任者: | 田中憲穂 | ||
| 試験担当者: | 山影康次,日下部博一,佐々木澄志,高橋俊孝,若栗 忍,橋本恵子 | ||
| (財)食品薬品安全センター 秦野研究所 | |||
| 〒257-8523 神奈川県秦野市落合729-5 | |||
| Tel 0463-82-4751 | Fax 0463-82-9627 | ||
| Correspondence | ||||
| Authors: | Noriho Tanaka(Study director) Kohji Yamakage, Hirokazu Kusakabe, Kiyoshi Sasaki, Toshitaka Takahashi, Shinobu Wakuri, Keiko Hashimoto | |||
| Hatano Research Institute, Food and Drug Safety Center | ||||
| 729-5 Ochiai, Hadano, Kanagawa, 257-8523, Japan | ||||
| Tel +81-463-82-4751 | Fax +81-463-82-9627 | |||