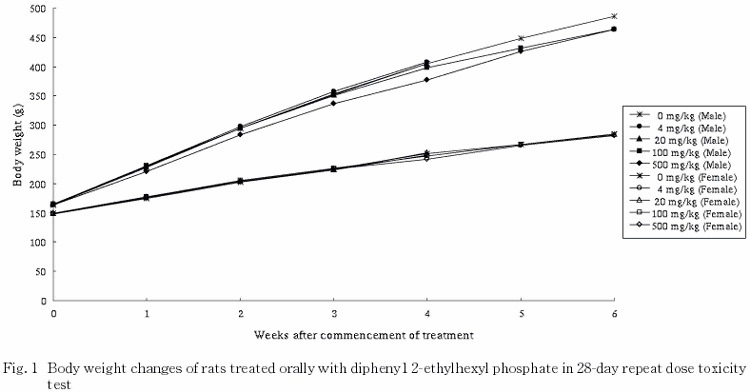
摂餌量の低値が500 mg/kg群の雌で認められた.血液学検査では,活性化部分トロンボプラスチン時間の延長が500 mg/kg群の雌で認められた.血液生化学検査では,血漿コリンエステラーゼの低値が500 mg/kg群の雌雄,血球コリンエステラーゼの低値が100 mg/kg群の雌と500 mg/kg群の雌雄,総コレステロールの高値が500 mg/kg群の雌,総タンパクの高値が100 mg/kg群の雄と500 mg/kg群の雌雄,アルブミンの高値が100 および500 mg/kg群の雄,GOT の低値が500 mg/kg群の雌,アルカリフォスファターゼの低値が100 および500 mg/kg群の雌で認められた.尿検査では,異常は認められなかった.病理学検査では,肝臓の変化として相対重量の高値が100 mg/kg群の雄,絶対重量および相対重量の高値が500 mg/kg群の雌雄,褐色化が100 および500 mg/kg群の雌雄,腫大が500 mg/kg群の雌雄,小葉中心性の肝細胞肥大が100および500 mg/kg群の雌雄で認められた.腎臓の変化として,近位尿細管上皮内の硝子滴の増強が500 mg/kg群の雄で認められ,一部の動物では好酸性小体の発現も伴われていた.甲状腺の変化として,腫大が100 mg/kg群の雄と500 mg/kg群の雌雄,ろ胞上皮細胞の肥大が100 および500 mg/kg群の雌雄で認められた.副腎の変化として,絶対重量と相対重量の高値が100 mg/kg群の雌と500 mg/kg群の雌雄,腫大が100 および500 mg/kg群の雌雄,束状帯の脂肪滴の増加が500 mg/kg群の雌雄で認められた.これらの変化は,投与を止めることにより軽減ないし回復していた.20 mg/kg 群では雌雄いずれも被験物質に起因した変化は認められなかった.
以上の結果より,本試験条件下におけるリン酸(2-エチルヘキシル)ジフェニルエステルの無影響量は雌雄いずれも20 mg/kg/day であると判断した.
検疫・馴化期間を含めた全飼育期間中,温度20〜25℃,湿度40〜70%,換気約12回/時,照明12時間(7:00〜19:00)に自動調節された飼育室を使用した.動物は,実験動物用床敷(ベータチップ:日本チャールス・リバー(株))を敷いたポリカーボネート製ケージに1ケージあたり2匹で収容し飼育した.
動物には,実験動物用固型飼料(MF:オリエンタル酵母工業(株))および5μmのフィルター濾過後,紫外線照射した水道水を,それぞれ自由に摂取させた.
 法),総蛋白(Biuret法),アルブミン(BCG法),A/G比(総蛋白およびアルブミンより算出),カルシウム(O-CPC法),無機リン(UV法),ナトリウム,カリウム,クロール(イオン選択電極法)を自動分析装置(日立736-10形:(株)日立製作所)により測定した.
法),総蛋白(Biuret法),アルブミン(BCG法),A/G比(総蛋白およびアルブミンより算出),カルシウム(O-CPC法),無機リン(UV法),ナトリウム,カリウム,クロール(イオン選択電極法)を自動分析装置(日立736-10形:(株)日立製作所)により測定した.
全例の血漿コリンエステラーゼ(アセチルチオコリン-DTNB法)を自動分析装置(日立736-10形:(株)日立製作所),血球コリンエステラーゼ(アセチルチオコリン-DTNB法)を自記分光光度計(日立U-3200形:(株)日立製作所)および脳コリンエステラーゼ(アセチルチオコリン-DTNB法)を自動分析装置(COBAS FARA:F.Hoffmann La Roche & Co.)により測定した.
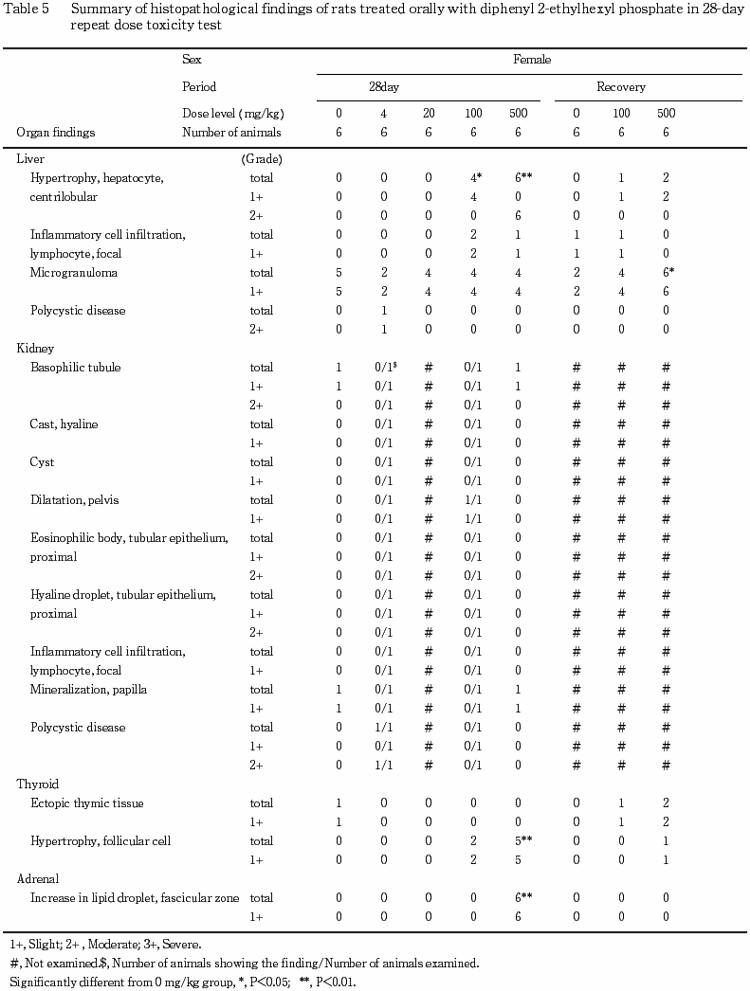
投与期間終了時解剖動物の対照群および500 mg/kg群の雌雄の心臓,肝臓,脾臓,腎臓,副腎,脳,坐骨神経,脊髄,甲状腺,下垂体および全動物の肉眼的異常部位を対象に,常法に従いヘマトキシリン・エオジン染色標本を作製し鏡検した.その結果,雌雄の肝臓,副腎,甲状腺と雄の腎臓に被験物質投与に起因すると考えられる変化が認められたため,投与期間終了時解剖動物の他の群と回復試験終了時解剖動物の当該器官(腎臓は雄のみ)を検査した.また,代表例の肝臓および副腎についてオイルレッドO染色と甲状腺の渡辺鍍銀染色を行い,鏡検した.
 法により検定した.分散が一様でない場合はKruskal-Wallisの検定を行い,Dunnett型またはScheff
法により検定した.分散が一様でない場合はKruskal-Wallisの検定を行い,Dunnett型またはScheff 型の順位和検定を行った.計数データおよび病理組織所見については,Armitageのχ^2検定を行った.有意水準は 5% 未満とした.
型の順位和検定を行った.計数データおよび病理組織所見については,Armitageのχ^2検定を行った.有意水準は 5% 未満とした.

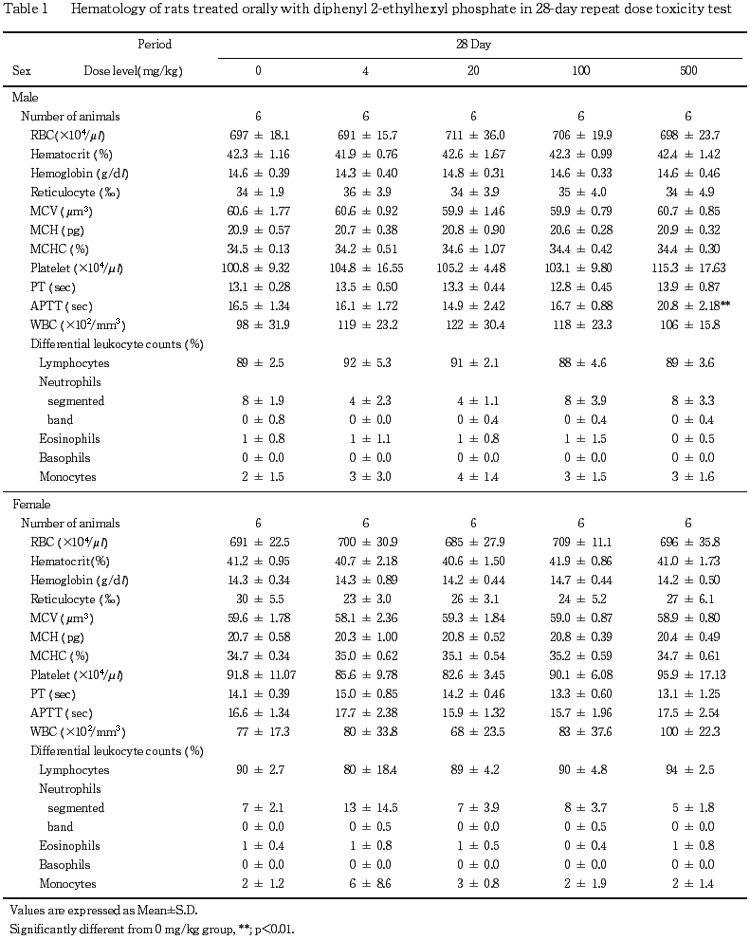
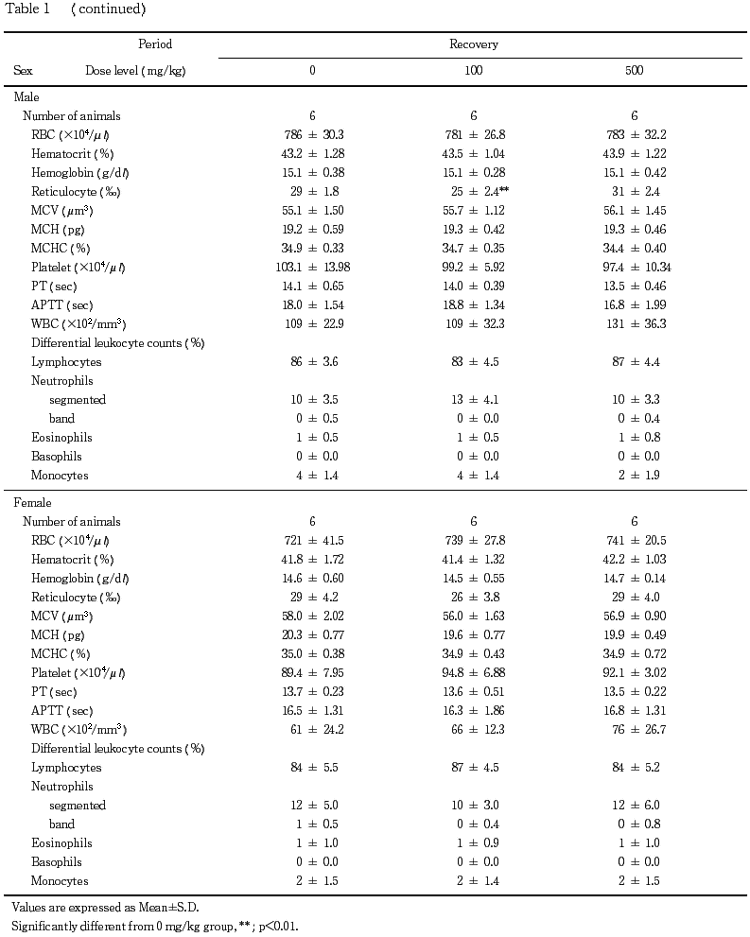
なお,回復期間終了時の検査で網状赤血球数の低値が100 mg/kg群の雄で認められたが,軽微な変動であることやその発現状況から被験物質に起因した変化ではないと判断した.
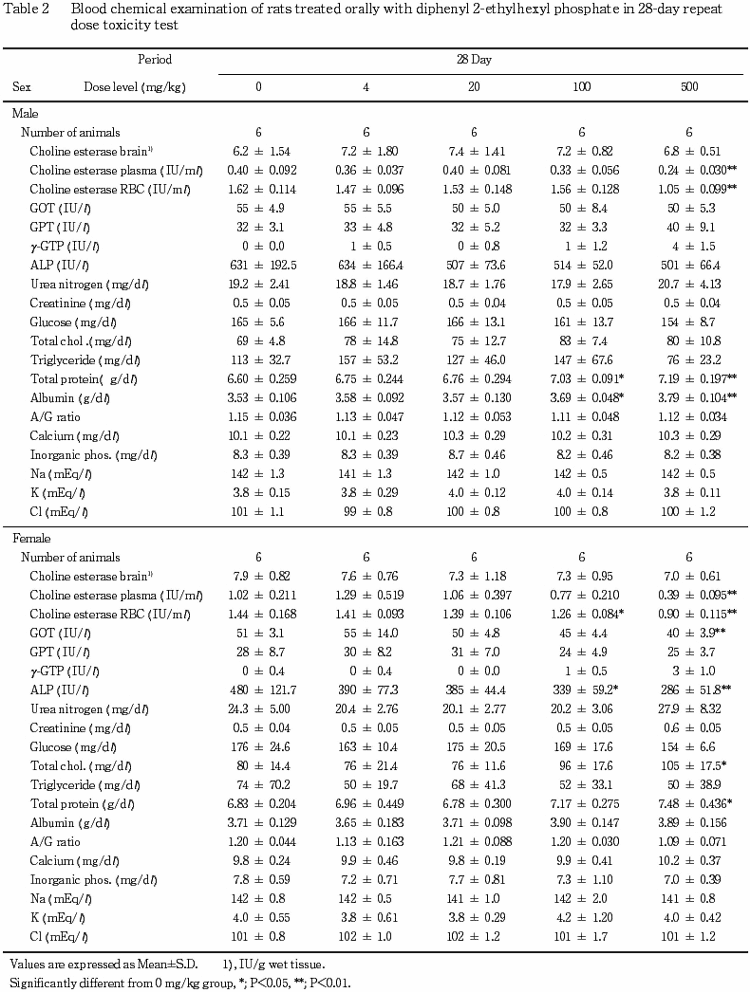
なお,回復期間終了時の検査で A/G比と無機リンの高値が500 mg/kg群の雄で認められたが,いずれも軽微な変動であることやその発現状況から被験物質に起因した変化ではないと判断した.
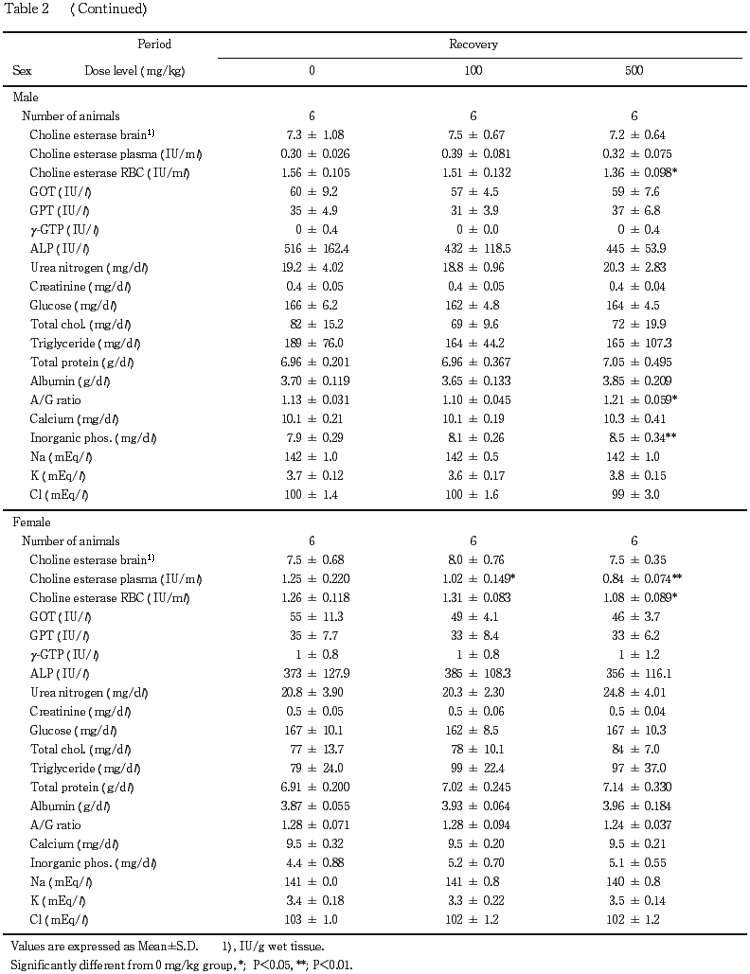

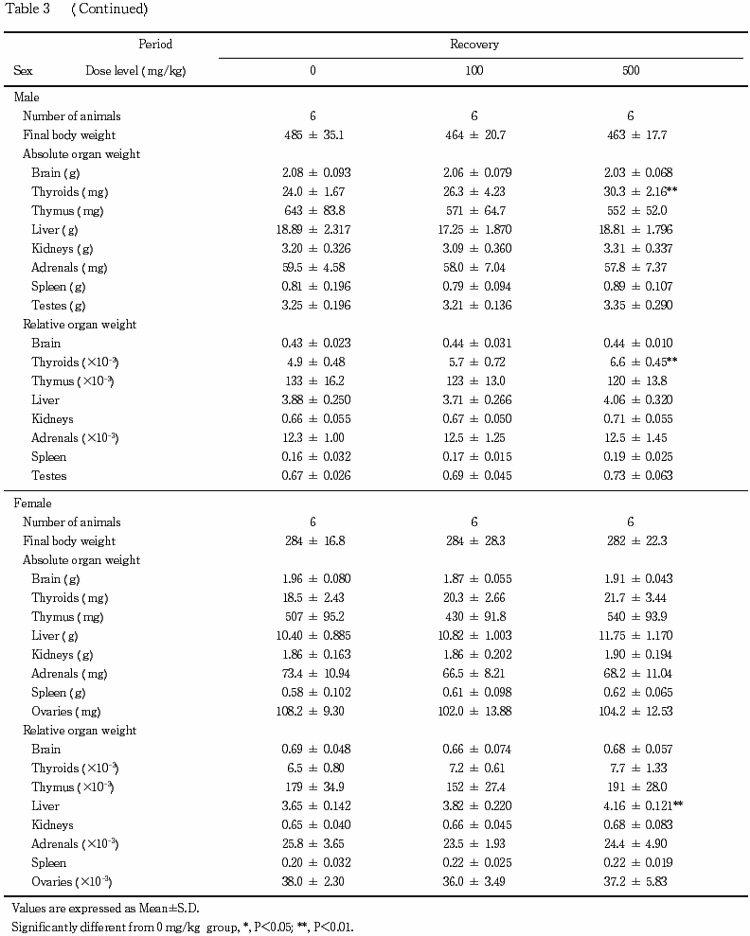
その他,被験物質投与群に種々の変化が認められたが,その発現状況からいずれも被験物質に起因した変化ではないと判断した.
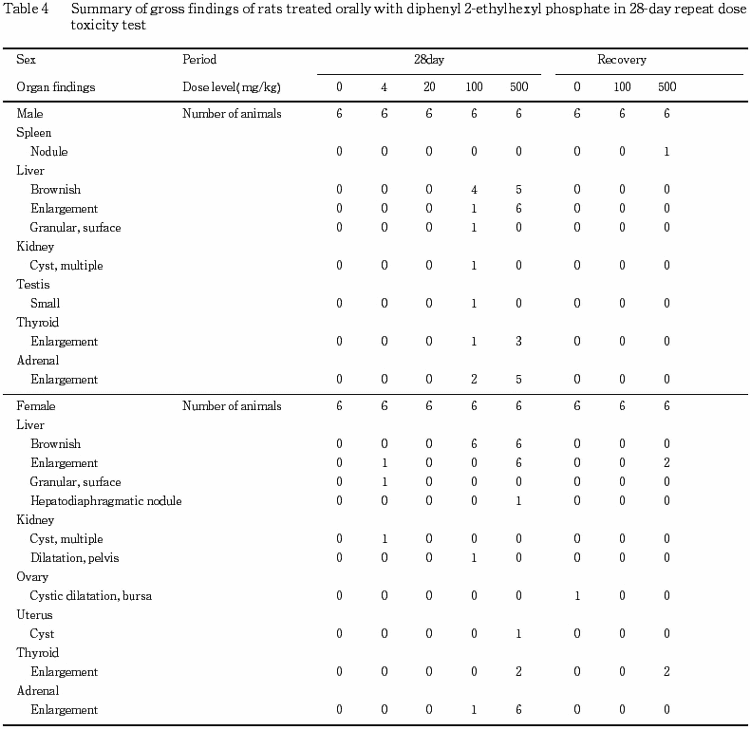
その他,被験物質投与群で種々の変化が認められたが,その発現状況からいずれも被験物質に起因した変化ではないと判断した.
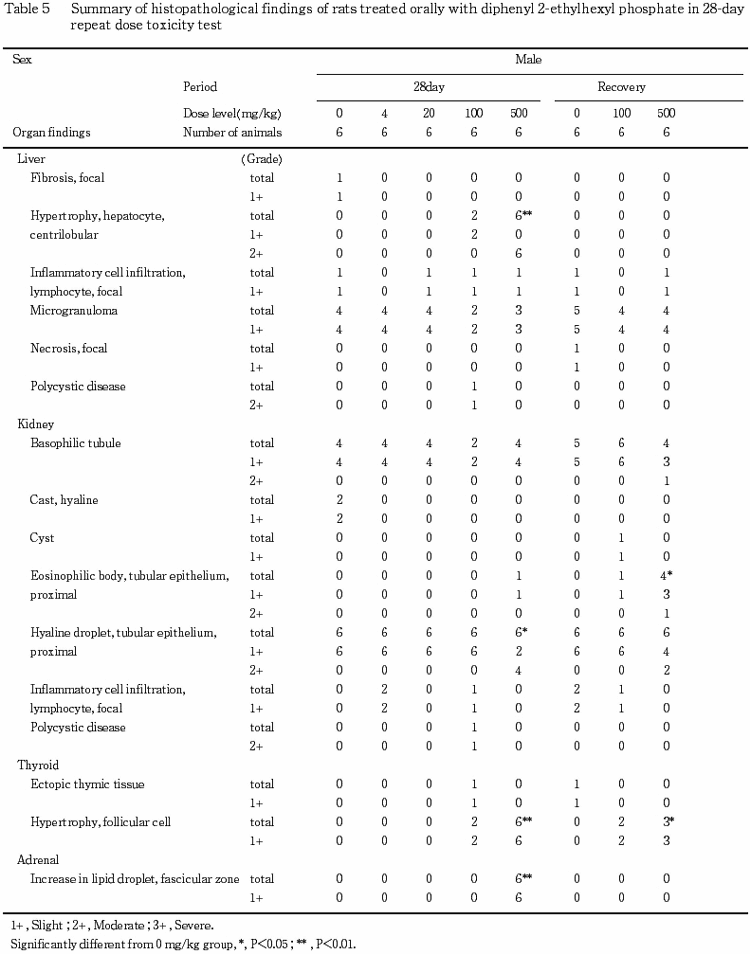
一般症状として,投与前後の流涎が100および500 mg/kg群の雌雄で認められた.しかし,投与後の流涎は投与直後に発現する一過性の変化であり,投与前の流涎は動物の体に触れることによって発現する条件反射的な変化であることや,これらの変化は投与を止めることにより発現しないことから,被験物質の味等に起因した変化であり,毒性学的意義はないと判断した.従って,流涎は無影響量の評価の対象からは除外した.
体重に変化はみられなかったが,摂餌量の低値が500 mg/kg群の雌で認められた.本変化は投与を止めることにより回復した.
血液学検査で,活性化部分トロンボプラスチン時間の延長が500 mg/kg群の雄で認められた.しかし,軽微な変化であることやプロトロンビン時間に異常がないことや肝傷害性の変化がないことなどから本変化の毒性学的意義は低いと思われる.本変化は投与を止めることにより回復した.
血液生化学検査で,血漿あるいは血球コリンエステラーゼの低値が100 mg/kg群の雌と500 mg/kg群の雌雄で認められた.被験物質はコリンエステラーゼ活性の阻害作用を有することが知られている有機リン化合物の一種であることから,同様のコリンエステラーゼ活性の阻害が惹起されたものと思われる.また,総コレステロール,総蛋白あるいはアルブミンの高値が100 mg/kg群の雄と500 mg/kg群の雌雄で認められたが,これらの変化はコリンエステラーゼ活性阻害に伴い代償性に肝臓でのタンパク質や脂質の合成が亢進した結果生じたものと思われる.回復期間終了時には,上記変化のうち血漿あるいは血球コリンエステラーゼの低値が100および500 mg/kg群で認められたが,その程度は明らかに軽減していた.なお,投与期間終了時にGOTの低値が500 mg/kg群の雌,アルカリフォスファターゼの低値が100および500 mg/kg群の雌で認められたが,一般的に問題となる値の上昇ではなく,減少であることから毒性学的には意義の乏しい変化と思われる.
病理学検査では,肝臓の絶対重量あるいは相対重量の増加が100 mg/kg群の雄と500 mg/kg群の雌雄,褐色化が100および500 mg/kg群の雌雄,小葉中心性の肝細胞肥大が500 mg/kg群の雌雄で認められた.小葉中心性の肝細胞肥大はくもり硝子様変化を特徴としており,これらの肝肥大性の変化は薬物代謝酵素誘導によるものと思われる.腎臓の近位尿細管上皮の硝子滴の増強が500 mg/kg群の雄で認められた.近位尿細管上皮の硝子滴はα2uグロブリンを含む蛋白の再吸収像であり,正常な成熟ラットでしばしばみられる変化である.そして,種々の化学物質投与により硝子滴の増数を特徴としたα2uグロブリン腎症が雄ラットに特異的に発現することが知られている2,3).被験物質投与により同様のα2uグロブリン腎症が惹起されたものと思われる.また,近位尿細管上皮の好酸性小体あるいは好塩基性尿細管は硝子滴の過剰な蓄積に伴う変化と思われる.甲状腺の腫大が 100 mg/kg 群の雄と500 mg/kg群の雌雄,ろ胞上皮細胞の肥大が100 および500 mg/kg群の雌雄で認められた.薬物代謝酵素誘導を起こす化学物質は,肝臓での甲状腺ホルモンの代謝を促進し,二次的に視床下部-下垂体系を介して甲状腺ろ胞上皮細胞の肥大を惹起することが知られている4,5).前述のように本試験でも薬物代謝酵素誘導の発現を示唆する肝肥大が認められることから,同様の機序でろ胞上皮細胞の肥大が生じた可能性が考えられる.一方,被験物質の甲状腺への直接作用の可能性も考えられるが,本試験の結果のみからでは明らかにはできなかった.副腎の絶対重量および相対重量の高値が100 mg/kg群の雌と500 mg/kg群の雌雄,腫大が100および500 mg/kg群の雌雄,束状帯の脂肪滴の増加が500 mg/kg群の雌雄で認められた.束状帯の脂肪滴の増加は,ステロイド合成阻害によって発現する脂質増生(lipid hyperplasia)の組織像と類似していた6).回復期間終了後解剖動物では,これらの変化は回復あるいは軽減していた.
なお,被験物質は有機リン化合物であり,ネコおよびサルに運動神経麻痺と脊髄の脱髄を起こすことが知られているトリフェニルフォスフェートが不純物として含まれている7,8).しかし,本試験では神経症状や中枢神経系の病理組織変化は認められなかった.
これらの試験結果から,本試験条件下におけるリン酸(2-エチルヘキシル)ジフェニルエステルの無影響量は雌雄いずれも20 mg/kg/dayと結論した.
| 1) | 化学工業日報社編,“12093 の化学商品,”化学工業日報社,東京,1993,pp.911-914. |
| 2) | C.L. Alden, C.H. Frith, "Handbook of Toxicologic Pathology," eds. by W. M. Haschek, C.G. Rousseaux, Academic Press, San Diego, 1991, pp.340-342. |
| 3) | P. Greaves, "Histopathology of Preclinical Toxicity Studies," ed.by P. Greaves, Interpretation and Relevance in Drug Safety Evaluation, Elsevier, Amsterdam, 1990, pp.532-538. |
| 4) | C.C. Capen, R.A. DeLellis, and J.T. Yarrington, "Handbook of Toxicologic Pathology," eds.by W.M. Haschek, C.G. Rousseaux, Academic Press, San Diego, 1991, pp.723-725. |
| 5) | G.O. Lumb and J.H. Rust, Toxicol. Pathol. 13, 315 (1985). |
| 6) | F. Zak, "Endocrine System. Monographs on Pathology of Laboratory Animals," eds. by T.C. Jones, U. Mohr, R.D. Hunt, Springer-Verlag, Berlin, 1983, pp.80-84. |
| 7) | W.L. Sutton, C.J. Terhaar, F.A. Miller, R.F. Scherberger, E.C. Riley, R.L. Roudabush and D.W. Fassett, Arch. Environmental Health, 1, 33(1960). |
| 8) | D. Tanaka, S.J. Bursian, E.J. Lehning and R.J. Aulerich, Brain Research, 531, 294(1990). |
| 連絡先 | |||
| 試験責任者: | 須藤雅人 | ||
| 試験担当者: | 清水優子,土谷 稔,勝田 修,豊田直人, 高野克代 | ||
| (株)三菱化学安全科学研究所 鹿島研究所 | |||
| 〒314-02 茨城県鹿島郡波崎町砂山14 | |||
| Tel 0479-46-2871 | Fax 0479-46-2874 | ||
| Correspondence | ||||
| Authors: | Masato Sudo(Study director) Yuko Shimizu,Minoru Tsuchitani,Osamu Katsuta,Naoto Toyota,Katsuyo Takano | |||
| Mitsubishi Chemical Safety Institute Ltd., Kashima Laboratory | ||||
| 14 Sunayama, Hasaki-machi, Kashima-gun, Ibaraki, 314-02 Japan | ||||
| Tel +81-479-46-2871 | Fax +81-479-46-2874 | |||