トリメチル亜リン酸のラットを用いる経口投与簡易生殖毒性試験
Preliminary Reproduction Toxicity Screening Test of Trimethoxyphosphine by Oral Administration in Rats
要約
トリメチル亜リン酸は,有機リン系アルキル化剤で,有機リン系殺虫剤として広く使用されている.ラットを用いた単回経口投与毒性試験1)では,LD50値が2000 mg/kg以上であること,トリメチル亜リン酸の164 mg/kg/dayを妊娠ラットに経口投与すると,胎児に口蓋裂や無顎を誘発すること2)が報告されている.今回,Sprague-Dawley系雌雄ラットの交配前14日から交配を経て,雄では連続42日間,雌では妊娠期間を通して哺育3日まで,トリメチル亜リン酸の0,5,20および80 mg/kgを経口投与し,雌雄ラットに対する生殖毒性について検討した.
その結果,いずれの投与群においても死亡動物はみられなかった.一般状態の変化として,投与直後に流涎が,雄の20 mg/kg以上および雌の80 mg/kg投与群に観察された.体重推移および摂餌量には,トリメチル亜リン酸の影響は認められなかった.剖検・病理組織学検査では,前胃粘膜の肥厚が20 mg/kg以上の投与群で雌雄ともに観察されたが,内部生殖器にはトリメチル亜リン酸の投与に起因したと考えられる変化は認められなかった.
生殖毒性に関しては,性周期,交尾および受胎能にはトリメチル亜リン酸の影響はみられなかった.また,妊娠期間,分娩および哺育状態にも,トリメチル亜リン酸の投与に起因したと考えられる変化は認められなかった.出生児に関しても,生存性および体重には,トリメチル亜リン酸の影響は認められなかった.80 mg/kg投与群の死亡児1例に自然発生奇形と考えられる異常が認められたが,その他の出生児に形態異常は観察されなかった.
以上の結果から,本試験条件下におけるトリメチル亜リン酸の雌雄動物に対する無作用量は5 mg/kg/day,生殖毒性に対する無作用量は80 mg/kg/day,出生児に対する無作用量は80 mg/kg/dayと判断された.
方法
1. 被験物質
トリメチル亜リン酸は,融点-78 ℃,沸点111 ℃の無色透明の液体であり,皮膚,気道,眼等に対して刺激性がある.試験には,呉羽化学工業(株)(東京)より提供された被験物質(ロット番号:86001,純度:99.53 %)を使用した.受領した被験物質は酸化防止のため窒素を充填して,使用時まで冷蔵庫内に保管した.試験終了後は提供元で再分析し,試験期間中の安定性を確認した.
被験物質は水と激しく反応し,爆発の危険があることから,媒体はコーン油を選択した.被験物質は,各濃度ごとに秤量し,コーン油(製造番号:V8P7069,ナカライテスク(株)に溶解して調製した.調製した検体は,酸化を防止する目的で窒素を充填後,冷蔵,遮光の条件下で保存し,調製後1週間以内に使用した.調製検体は,冷蔵,窒素充填,遮光条件下で8日間安定であり,初回調製した各濃度の投与検体について,被験物質の含量測定を実施した結果,いずれも所定量の被験物質が含有されていることを確認した.
2. 使用動物および飼育方法
試験には,7週齢のSprague-Dawley系(Crj:CD(SD)IGS, SPF)雌雄ラットを日本チャールス・リバー(株)の筑波飼育センターから購入し,飼育環境への馴化と検疫を兼ねて入荷後12日間予備飼育した.予備飼育中に雌は毎日腟スメアを採取し,性周期が4日周期を示した動物のみを試験に供した.群分けは,雌雄とも検疫終了日の体重を基にして体重別層化無作為抽出法により行い,雌雄とも1群13匹からなる4群に分けた.投与開始時の週齢は,雌雄ともに9週齢であった.
動物は,温度24 ± 1℃,湿度50〜65 %,換気回数約15回/時,照明12時間(7時〜19時点灯)に制御された飼育室で,金属製金網床ケージに1匹ずつ収容し,固型飼料(CE-2,日本クレア(株)および水道水(秦野市水道局給水)を自由に摂取させて飼育した.交尾した雌については,妊娠14日から哺育4日まで,紙パルプ製チップ (ALPHA-dri加商(株)を入れたプラスチック製ラット用繁殖ケージに収容した.
3. 投与量の設定および投与方法
投与量は,予備試験の結果をもとに設定した.すなわち,トリメチル亜リン酸の0,40,80および160 mg/kgを雌雄ラットの交配前14日から交配を経て,雄では連続21日間,雌では妊娠6日まで反復経口投与した結果,一般状態,体重,摂餌量,交尾および受胎能力に投与の影響はみられなかったが,剖検時に80 mg/kg以上の投与群で前胃部粘膜の白濁,肥厚および剥離が認められ,160 mg/kg 投与群ではそれらの病変が重度であったことから,高用量には80 mg/kgを設定し,公比4で減じて中用量には20 mg/kgを,低用量には5 mg/kgを設定した.対照群には,トリメチル亜リン酸の媒体であるコーン油を用いた.
投与期間は,雄に対しては交配前14日から交配を経て連続42日間,雌に対しては交配前14日から交配および妊娠期間を通して哺育3日(分娩日=哺育0日)までとし,1日1回,一定の時刻に投与した.なお,分娩しなかった雌は剖検日前日まで投与を継続した.投与容量は体重1 kg当たり5 mLとし,雄および交配前,交配期間中の雌では,週1回測定した体重を基に,交尾した雌では,最新の測定体重を基に算出した.
4. 観察および検査
1) 親動物
(1) 一般状態
飼育期間中,毎日1回以上観察した.
(2) 体重測定
投与期間中週1回〔雄:投与1,8,15,22,29,36,43日,雌:投与1,8,15,22日(雌の投与22日における体重測定は,交配中の動物のみを対象とした)〕および解剖日に測定した.交尾した雌は妊娠0,7,14,20日に,分娩した雌は哺育0および4日に測定した.
(3) 摂餌量測定
投与期間中(交配期間を除く)週1回,体重測定日と同じ日に餌重量を測定し,1週間の摂餌量を算出した.交尾した雌は妊娠0〜7,7〜14,14〜20日,分娩した雌は哺育0〜4日の摂餌量を測定した.
(4) 性周期および交配
予備飼育中に引き続き投与開始日以降も,毎日,腟スメアを採取して,性周期を観察した.交配は,投与15日の夕方から最長2週間,同群内の雌雄を1対1で連続同居方式で行った.交尾の確認は,腟スメア中の精子および腟栓の確認により行い,交尾が確認された雌については,その日を妊娠0日として起算し,雄から分離して個別に飼育した.交配結果および妊娠の成否により,各投与群における交尾率〔(交尾動物数/同居動物数)× 100〕,受胎率〔(妊娠動物数/交尾動物数)× 100〕,同居開始から交尾日までの日数およびその間に回帰した発情期の回数を求めた.
(5) 分娩および哺育状態の観察
交尾した雌は,全て自然分娩させた.分娩状態の直接観察は可能な動物についてのみ行い,分娩状態が直接観察できなかった動物は,分娩後の徴候から分娩障害の有無を判断して記録した.分娩の確認は,午前9時〜11時に行い,分娩が完了していることを確認した動物については,その日を分娩日(哺育0日)として妊娠期間(妊娠0日〜分娩日の日数)を算出した.分娩後は,哺育状態を毎日観察した.
(6) 剖検・病理組織学検査
雄動物は,投与42日の翌日に,致死量のペントバルビタールナトリウム麻酔下で放血・致死させ,剖検した.その際,精巣および精巣上体の重量を測定した.また,胃,精巣および精巣上体はブアン液に固定し,高用量群および対照群の全例について病理組織学検査を実施した.ただし,高用量群の動物で異常が認められた胃については,その他の投与群についても病理組織学検査を実施した.剖検時に異常を認めた器官は,0.1 Mリン酸緩衝10 vol%ホルマリン溶液に固定し,病理組織学検査を実施した.
雌動物のうち,分娩した雌は哺育4日に,交尾は確認されたが分娩しなかった雌は妊娠26日相当日に,それぞれ致死量のペントバルビタールナトリウム麻酔下で放血・致死させ,剖検した.その際,卵巣および子宮を摘出して,卵巣については実体顕微鏡下で妊娠黄体数を,子宮については着床数を数え,着床率〔(着床数/黄体数)× 100〕を算出した.胃および卵巣についてはブアン液に固定し,高用量群および対照群の全例について,病理組織学検査を実施した.ただし,高用量群の動物で異常が認められた胃については,その他の投与群についても病理組織学検査を実施した.
2) 出生児
(1) 産児数および死亡児
哺育0日に産児数(生存児+死亡児)を数えて,分娩率〔(産児数/着床痕数)× 100〕および生児出産率〔(出産生児数/着床痕数)× 100〕を求めた.また,出産率〔(生児出産雌数/妊娠動物数)× 100〕を算出した.生存児は外表を観察し,性別および外表奇形(矮小児を含む)の有無を検査した.
哺育0日以降は生児数を毎日調べ,出生率〔(出産生児数/総産児数)× 100〕および新生児生存率〔(哺育4日の生児数/哺育0日の生児数)× 100〕を求めた.死亡児は剖検し,異常の認められた器官は,10 vol%ホルマリン溶液に固定して保存した.
(2) 体重
哺育0および4日に個体別に測定し,各腹ごとに雌雄別の平均値を算出した.
(3) 剖検
出生児は哺育4日に剖検し,外表および内部器官の異常の有無を観察した.
5. 統計解析
交尾率,受胎率および出生児の形態異常出現頻度についてはFisherの直接確率検定を行った.病理組織学所見では,グレード分けしたデータは,Mann-WhitneyのU検定を,陽性グレードの合計値はFisherの直確率の片側検定を行った.その他のデータは,個体ごとに得られた値あるいは各腹ごとの平均値を1標本として,Bartlett法により各群の分散の一様性について検定を行い,分散が一様である場合には一元配置型の分散分析を,分散が一様でない場合にはKruskal-Wallisの順位検定を行った.群間に有意性が認められた場合は,Dunnett法により多重比較を行った.なお,有意水準は5 %とした.
結果
1. 親動物
1) 一般状態
投与後に流涎が20 mg/kg投与群の雄1例,80 mg/kg投与群の雄全例,雌11例に観察された.流涎は投与10日からみられ,いずれの場合も投与直後にのみ観察された.その他,脱毛が対照群を含む各投与群で散見され,眼周囲の被毛の汚れが80 mg/kg投与群の雄1例,分娩後に排泄口周囲の被毛の汚れが対照群の1例に観察された.
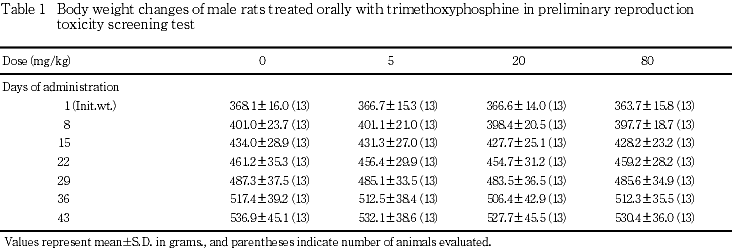
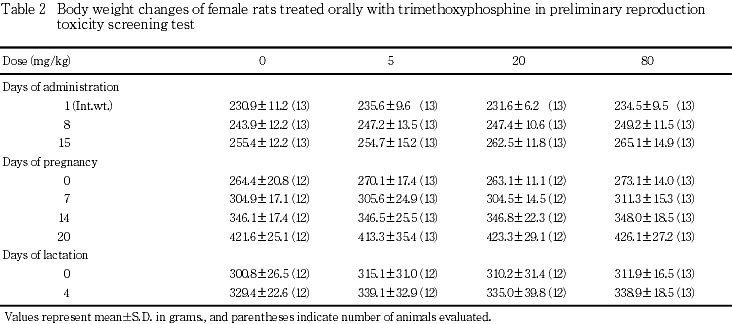
2) 体重(Tables 1, 2)
雌雄とも,全投与期間を通して,対照群とトリメチル亜リン酸各投与群との間に有意差は認められなかった.
3) 摂餌量(Table 3, 4)
投与8〜15日の摂餌量が,雌の80 mg/kg投与群で有意に増加したが,雌の20 mg/kg以下および雄のトリメチル亜リン酸各投与群においては,対照群との間に有意差は認められなかった.


4) 剖検所見
精巣および精巣上体の小型化が,20 mg/kg投与群の1例に観察された.前胃粘膜では,肥厚が80 mg/kg投与群の雄11例,雌4例,20 mg/kg投与群の雌2例,対照群の雌1例に観察され,淡色部が80 mg/kg投与群の雄1例,雌2例,20 mg/kg投与群の雌雄各1例に,剥離が80 mg/kg投与群の雌1例に認められた.
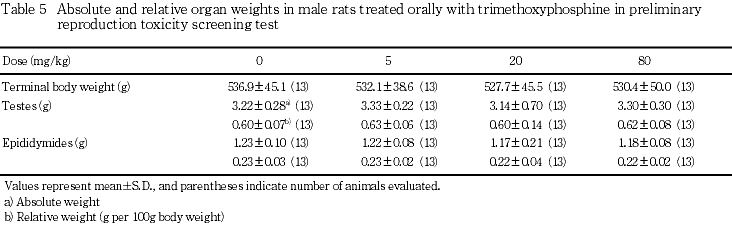
5) 器官重量 (Table 5)
精巣および精巣上体の実重量および比体重値には,対照群とトリメチル亜リン酸各投与群との間に有意差は認められなかった.
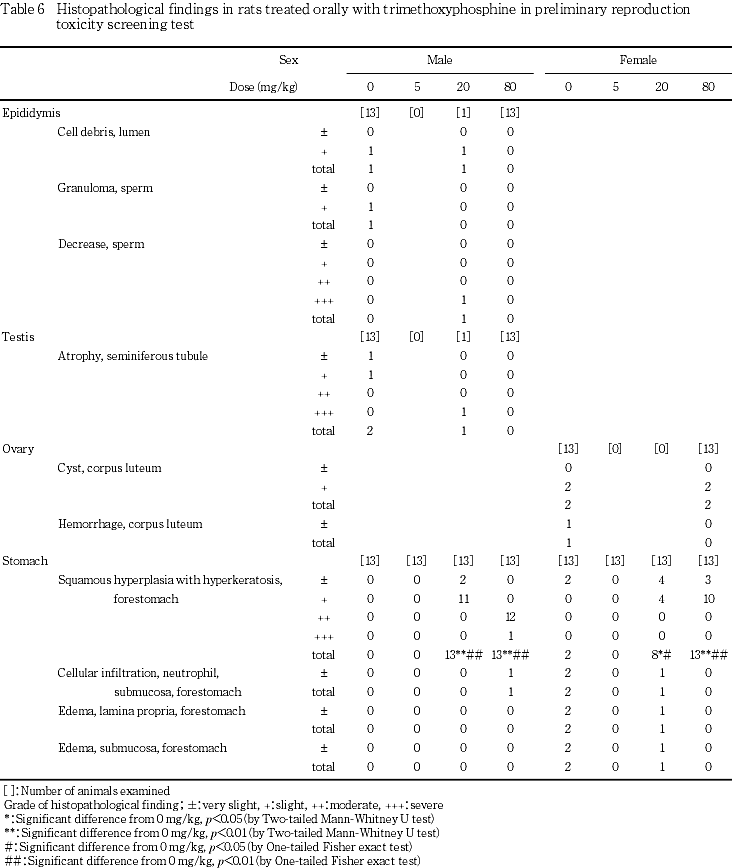
6) 病理組織学検査(Table 6)
精巣および精巣上体には,剖検時に精巣および精巣上体の小型化がみられた20 mg/kg投与群の1例に,精巣上体の精子減少および腔内細胞残屑,さらには精細管の萎縮が観察された.その他,精巣上体の腔内細胞残屑および精子肉芽腫が対照群で各1例,精細管の萎縮が対照群の2例に観察されたが,80 mg/kg投与群では精巣および精巣上の異常は観察されなかった.
卵巣には,黄体嚢胞が80 mg/kg投与群および対照群のそれぞれ2例に,黄体の出血が対照群の1例に観察された.
前胃には扁平上皮の過形成および過角化症が80 mg/kg投与群の雌雄全例,20 mg/kg投与群の雄全例,雌8例および対照群の雌2例に観察され,粘膜下織の好中球浸潤が80 mg/kg投与群の雄1例,20 mg/kg投与群の雌1例,対照群の雌2例に,粘膜固有層および粘膜下織の浮腫が20 mg/kg投与群の雌1例,対照群の雌2例に観察された.
7) 性周期および交配成績(Table 7)
性周期にはトリメチル亜リン酸の影響を示唆する変化はみられなかった.交配検査の結果,交尾率および受胎率にもトリメチル亜リン酸の影響は認められなかった.また,交尾までの日数およびその間の発情数に,対照群とトリメチル亜リン酸各投与群との間に有意差は認められなかった.

8) 出産率および妊娠期間(Table 8)
出産率には,トリメチル亜リン酸の影響を示唆する変化はみられなかった.妊娠期間は80 mg/kg投与群において有意に短縮したが,20 mg/kg以下の投与群では対照群との間に有意差は認められなかった.
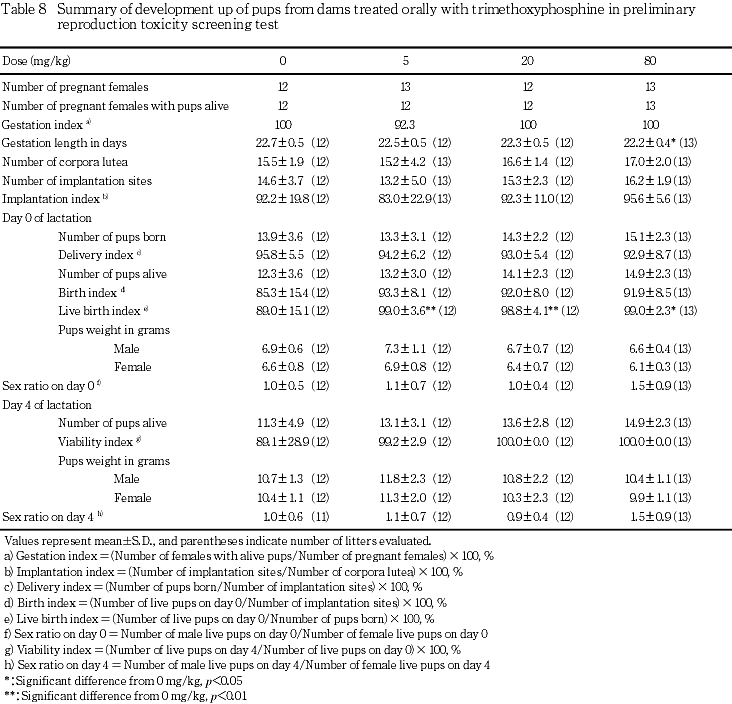
9) 黄体数,着床数および着床率(Table 8)
黄体数,着床数および着床率にトリメチル亜リン酸の影響を示唆する変化はみられなかった.
10) 分娩および哺育状態
分娩状態の観察では,腟出血が対照群および5 mg/kg投与群の各1例に観察された.その他,分娩後に胎盤を食べない例が対照群の1例に観察された.同例では哺育状態の観察でも児を集めない,乳頭突出不良,児の体表温低下,児のミルクスポットが確認されない等の異常が観察され,哺育2日に全児が死亡した.その他,児を集めない,乳頭突出不良,児の体表温低下,児のミルクスポットが確認されない例が20 mg/kg投与群の1例にも観察されたが,80 mg/kg投与群では分娩および哺育状態に異常は認められなかった.
2. 出生児
1) 生存性(Table 8)
出生率がトリメチル亜リン酸各投与群で有意に増加したが,総産児数,分娩率,出産生児数,生児出産率,哺育4日の生児数,新生児生存率および性比には,対照群とトリメチル亜リン酸各投与群との間に有意差は認めらなかった.
2) 体重(Table 8)
哺育0および4日における出生児の体重には,対照群とトリメチル亜リン酸各投与群との間に有意差は認められなかった.
3) 形態
哺育0日における生存児に,矮小を含む外表奇形は観察されなかった.死亡児の剖検では,無顎,耳介の低位,小眼および水腎が80 mg/kg投与群の1例(哺育0日死亡児)に観察された.哺育4日の剖検では,出生児の形態異常は観察されなかった.
考察
トリメチル亜リン酸の5,20および80 mg/kgをSprague-Dawley系雌雄ラットの交配前14日から交配を経て,雄では連続42日間,雌では妊娠期間を通して哺育3日まで経口投与し,生殖毒性について検討した.
その結果,いずれの投与群においても死亡動物はみられなかった.一般状態の変化として,流涎が雄の20 mg/kg以上および雌の80 mg/kg投与群で観察された.流涎はいずれも投与直後に一過性にみられたこと,トリメチル亜リン酸は皮膚,気道,眼等に対して刺激作用を有することから,本試験でみられた流涎は被験物質の刺激性によって惹起された変化と推察される.雌では,80 mg/kg投与群の摂餌量が有意に増加したが,体重には雌雄ともに有意な変化はみられなかった.先に実施された28日間反復投与毒性試験3)においても,摂餌量の増加はみられていないことから,本試験でみられた摂餌量の変化は,トリメチル亜リン酸の毒性を示唆するものではないと考えられる.剖検および病理組織学検査では,20 mg/kg以上の投与群の前胃に上皮の肥厚が観察された.前胃は刺激性の変化が発現しやすい部位であり,28日間反復投与毒性試験3)においても同様の変化が認められていることから,トリメチル亜リン酸の投与によって誘発されたものと推定される.なお,内部生殖器には,被験物質の投与に起因したと考えられる変化は観察されなかった.
雌の性周期,雌雄の交尾および受胎能には,トリメチル亜リン酸の影響はみられなかった.また,分娩および哺育状態についても,被験物質の投与に起因したと考えられる異常は観察されなかった.妊娠期間は80 mg/kg投与群で有意に短縮したが,いずれの動物も妊娠22または23日に分娩していることから,妊娠維持の異常を示唆する変化ではないと考えられる.出生児の生存性および体重には,トリメチル亜リン酸の影響を示唆する変化は認められなかった.なお,トリメチル亜リン酸投与群の出生率が対照群より有意に増加したが,対照群の値が背景値より低下したことによるもので,被験物質の投与に起因した変化ではないと判断した.出生児の形態観察では,80 mg/kg投与群の死亡児1例に無顎,耳介の低位,小眼および水腎がみられた.Sprague-Dawley系ラットを用いた催奇形性試験2)では,164 mg/kg/dayのトリメチル亜リン酸を妊娠6〜15日に経口投与した結果,約半数の母動物で胎児に口蓋裂または無顎が発現していることから,本試験でみられた奇形は,トリメチル亜リン酸に無関係であると断定はできない.しかしながら,今回みられた奇形はSprague-Dawley系ラットにおいて自然発生的にもみられる型であり4),その他の出生児には奇形は観察されていないことから,被験物質の投与により誘発されたと考えるよりも,Sprague-Dawley系ラットの自然発生奇形と考える方が妥当と思われる.
以上の結果から,本試験条件下におけるトリメチル亜リン酸の雌雄動物に対する無作用量は5 mg/kg/day,生殖毒性に対する無作用量は80 mg/kg/dayと考えられ,出生児に対する無作用量も80 mg/kg/dayと考えられた.
文献
| 1) | 榎並倫宣ら,化学物質毒性試験報告,7, 445(1999). |
| 2) | M. A. Mehlman, P. H. Craig, M. A. Gallo, Toxicol. Appl. Pharmacol., 72, 119(1984). |
| 3) | 榎並倫宣ら,化学物質毒性試験報告,7, 447(1999). |
| 4) | T. Nakatsuka, et al. Cong. Anom., 37, 47(1997).
|
| 連絡先 |
| 試験責任者: | 太田 亮 |
| 試験担当者: | 渡辺千朗,永田伴子,堀内伸二,稲田浩子,三枝克彦,安生孝子 |
| (財)食品薬品安全センター 秦野研究所 |
| 〒257-8523 神奈川県秦野市落合729-5 |
| Tel 0463-82-4751 | Fax 0463-82-4751 | |
| Correspondence |
| Authors: | Ryo Ohta(Study director)
Chiaki Watanabe, Tomoko Nagata, Shinji Horiuchi, Katsuhiko Saegusa, Hiroko Inada, Takako Anjo |
| Hatano Research Institute, Food and Drug Safety Center |
| 729-5 Ochiai, Hadano, Kanagawa 257-8523, Japan |
| Tel +81-463-82-4751 | Fax +81-463-82-9627 | |








