
雌においては,いずれの群とも死亡および瀕死例は認められなかった.一般状態では,投与による変化はみられなかった.体重は,200 mg/kg群で哺育期に増加抑制が,800 mg/kg群で妊娠期および哺育期に増加抑制がみられた.摂餌量は,200および800 mg/kg群で交配前,妊娠期および哺育期に低値がみられた.剖検,器官重量および病理組織学検査では,投与による変化はみられなかった.
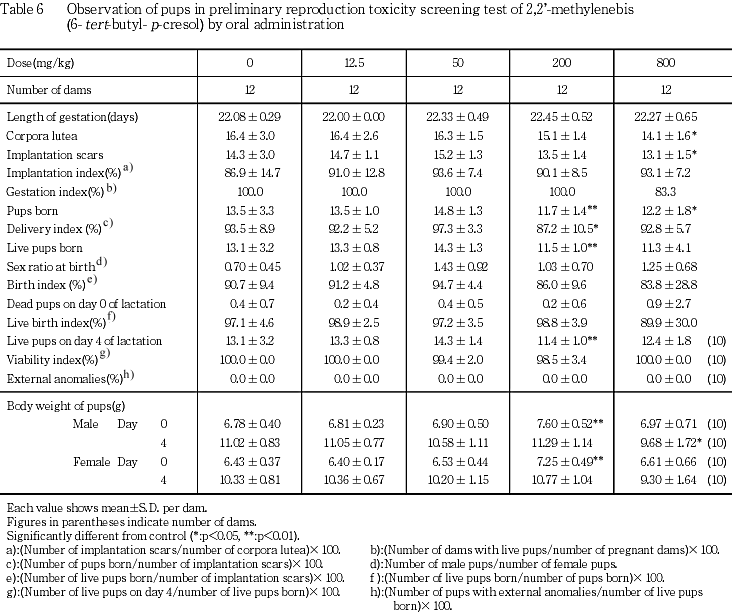
発情回数,交尾率,交尾所要日数,受胎率,妊娠期間,分娩状態,哺育状態では,投与による変化はみられなかった.800 mg/kg群では,新生児を分娩できなかった雌および哺育期に新生児が全例死亡した母動物が各1例認められた.また,800 mg/kg群では,黄体数,着床痕数,総出産児数,哺育0および4日の新生児数,出生率,哺育4日に雌雄別体重の低値あるいは低値傾向が,死産児数の高値傾向がみられた.200 mg/kg群では,黄体数,着床痕数,総出産児数,哺育0および4日の新生児数の低値あるいは低値傾向がみられた.新生児の外表,一般状態および剖検では,投与による変化はみられなかった.
以上のように,2,2'-メチレンビス(6-tert-ブチル-ρ-クレゾール)の一般毒性学的無影響量は,雄では50 mg/kg投与により精子検査成績および精巣の病理組織学検査成績に影響が認められたことから12.5 mg/kg/day,雌では200 mg/kg投与により体重の増加抑制および摂餌量の低値が認められたことから50 mg/kg/dayと考えられる.また,生殖発生毒性学的な無影響量は,雄では50 mg/kg投与により精子検査成績および精巣の病理組織学検査成績に影響が認められたことから12.5 mg/kg/day,雌では200 mg/kg投与により黄体数および着床痕数の低値傾向が認められたことから50 mg/kg/day,児動物では200 mg/kg投与により哺育0日および4日の新生児数の低値が認められたことから50 mg/kg/dayと考えられる.
被験物質は,5 %アラビアゴム水溶液で懸濁して調製した.被験物質は純度換算を行い,投与量は原体重量で表示した.なお,調製液は,調製後冷蔵・遮光条件下で7日間,さらに室温・遮光条件下で4時間保存しても安定性に問題のないことが確認されていたため,各濃度の調製液は調製後,冷蔵・遮光条件下で保管し,調製後7日以内に使用した.また,投与開始日および雄の投与期間終了日に使用した各濃度の投与液中の被験物質濃度を確認した結果,被験物質濃度に問題はなかった.
動物は,室温20〜26℃,湿度40〜70 %,明暗各12時間(照明:午前6時〜午後6時),換気回数12回/時に維持されている飼育室で飼育した.検疫・馴化期間中はステンレス製ケージを用いて1ケージ当たり5匹までの群飼育とし,群分け後はステンレス製ケージを用いて個別飼育した.母動物は,妊娠18日にオートクレーブ処理した床敷(サンフレーク,日本チャールス・リバー(株))を入れたプラスチック製ケージに個別に移し,自然分娩および哺育をさせた.飼料は固型飼料(CRF-1,オリエンタル酵母工業(株))を,飲料水は水道水をいずれも自由に摂取させた.
投与開始日の週齢は雌雄とも10週齢であり,体重範囲は雄が332〜383 g,雌が206〜238 gであった.
投与量は,ラットにおける28日間反復経口投与毒性試験1) (投与段階:0,50,200および800 mg/kg)の結果により決定した.すなわち,800 mg/kg群でも一般状態,体重,摂餌量,尿検査および血液生化学検査成績に影響はみられないものの,50 mg/kg以上の群で肝臓重量の増加またはその傾向が,200 mg/kg以上の群で精巣のセルトリ細胞の空胞化および精子分化の障害が認められた.そこで,当試験の投与量は,一般状態,体重および摂餌量に影響はみられないものの,精巣に明らかな影響が認められると考えられる800 mg/kgを最高用量とし,以下公比4で除して200,50および12.5 mg/kgとした.また,対照として被験物質投与群の投与液と同一容量の媒体(5 %アラビアゴム水溶液)のみを投与する群を設けた.
投与期間は,雄では交配前14日間とその後36〜38日間の合計50〜52日間とし,雌では交配前14日間,交配期間中(最長8日間),妊娠期間中および哺育3日までの合計40〜48日間とした.なお,投与開始日を投与1日とした.
精子の活動性は,精子原液を精子培養液で希釈し,約30分間培養(培養条件:37 ℃,5 %炭酸ガス,95 %空気)後に精子希釈液をHTM-IVOS(Hamilton Thorne Research)を用いて,活動精子率を求め,活動精子について基準点移動速度,最短距離移動速度,総移動速度および頭部の横切り回数を算出した.
精子の生存性として,加藤らの方法2)に従い,マイクロウェルプレート内で精子原液を精子培養液にて約3倍希釈した後,16 μMのcalcein acetoxy methyl esterと8 μMのethidium homodimer-1とで約2時間培養・染色(培養条件:37℃,5 %炭酸ガス,95 %空気)した後,蛍光顕微鏡下で精子を生存精子,途中死亡精子と死滅精子に分類し,生存精子率と生き残り精子率を求めた.なお,生存,途中死亡および死滅精子の判定は,頭部〜尾部にかけて緑色の蛍光発色が認められるものを生存精子,頭部には赤色の蛍光発色が,尾部には緑色の蛍光発色が認められるものを途中死亡精子,頭部には赤色の蛍光発色が認められるが,尾部には蛍光発色が認められないものを死滅精子とした.
精子の形態は,精子原液と10 %エオジン染色液を混和後,塗抹標本を作製し,顕微鏡下で観察した.
精子数は,左精巣上体尾部をホモジナイズ後,HTM-IVOS(Hamilton Thorne Research)を用いて算出した.なお,左精巣上体尾部1 g当たりの精子数も算出した.
対照群および800 mg/kg群の精巣および精巣上体の頭部,ならびに剖検時に異常の認められた精嚢(800 mg/kg群の6例)についてH-E染色組織標本を作製し,病理組織学検査を実施した.800 mg/kg群の検査で対照群と比べて異常を示す動物数に差があると考えられた精巣および精巣上体の頭部については,12.5,50および200 mg/kg群も同様に検査した.
対照群および800 mg/kg群の卵巣についてH-E染色組織標本を作製し,病理組織学検査を実施した.
交尾確認は毎朝ほぼ一定時刻に行い,腟垢内に精子または腟栓を確認した雌を交尾成立動物として,その日を妊娠0日として起算した.
交尾率,受胎率および出産率は,χ^2検定により行った.
なお,病理組織学検査において,800 mg/kg群で毒性学的影響が示唆され他の群についても検査を実施した器官・組織の所見については,対照群との群間比較を順位を利用したDunnett型の検定法を用いて行った.そこで対照群との間に有意差が認められた場合は,Cochran・Armitageの傾向検定を用いて用量反応性の検定を行った.
一般状態観察において,200および800 mg/kg群で一過性の流涎がみられた.その他には,対照群を含む各群で軟便が散見されたが,投与量との関連は認められなかった.


12.5および50 mg/kg群では,対照群と比べていずれの器官の絶対および相対重量にも有意差はみられなかった.200および800 mg/kg群では,対照群と比べて精巣および精巣上体の絶対ならびに相対重量の有意な低値がみられた.
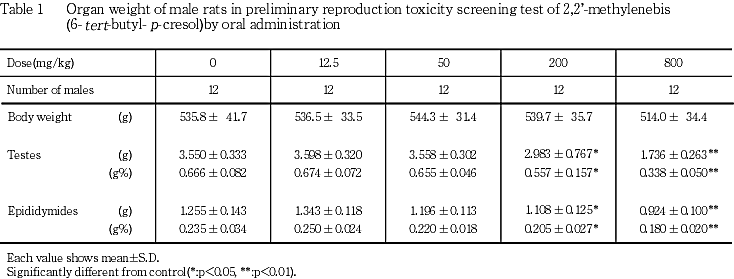
50 mg/kg群では,対照群と比べて活動精子率,生存精子率,生き残り精子率,精子数および精巣上体尾部1 g当たりの精子数の有意な低値,奇形精子率の有意な高値がみられた.なお,50 mg/kg群では,対照群と比べて頭部の横切り回数の有意な高値がみられたが,投与量に関連した変化ではないことから,投与によるものではないと判断された.
200 mg/kg群では,対照群と比べて活動精子率,生存精子率,生き残り精子率,精子数および精巣上体尾部1 g当たりの精子数の有意な低値がみられた.また,200 mg/kg群では,6例の活動精子率は0 %であったが,算出できた動物の基準点移動速度,最短距離移動速度および総移動速度に有意差はみられなかった.なお,200 mg/kg群では,対照群と比べて頭部の横切り回数の有意な低値がみられたが,ごく軽度な差であった.また,同群では,精子の形態観察が可能であった7例で対照群と比べて奇形精子率の有意な高値がみられた.
800 mg/kg群では,対照群と比べて精子数および精巣上体尾部1 g当たりの精子数の有意な低値がみられた.800 mg/kg群では,いずれの動物とも活動精子率は0 %であり,対照群と比べて有意差が認められ,基準点移動速度,最短距離移動速度,総移動速度および頭部の横切り回数の測定はできなかった.また,800 mg/kg群では,精子の形態観察が可能な動物は1例のみであったが,その大部分は奇形精子であった.なお,同群では,観察可能な精子が得られなかったため,生存精子率および生き残り精子率の算出ができなかった.

精巣上体においては,精子の減少が200 mg/kg群で9例,800 mg/kg群で12例全例みられた.
なお,精巣における精細管の萎縮および精巣上体における精子の減少は,200および800 mg/kg群で対照群と比べて有意差が認められ,用量相関性も確認された.
剖検時に萎縮の認められた精嚢(800 mg/kg群の6例)では,異常はみられなかった.

一般状態観察において,200および800 mg/kg群で一過性の流涎がみられた.その他には,対照群を含む各群で軟便が散見されたが,投与量との関連は認められなかった.
妊娠期間中において,12.5,50および200 mg/kg群では対照群と比べていずれの測定日の体重にも有意差はみられなかった.800 mg/kg群では,対照群と比べて妊娠0〜21日に体重の有意な低値がみられた.
哺育期間中において,12.5および50 mg/kg群では対照群と比べていずれの測定日の体重にも有意差はみられなかった.200および800 mg/kg群では,対照群と比べて哺育4日に体重の有意な低値がみられた.
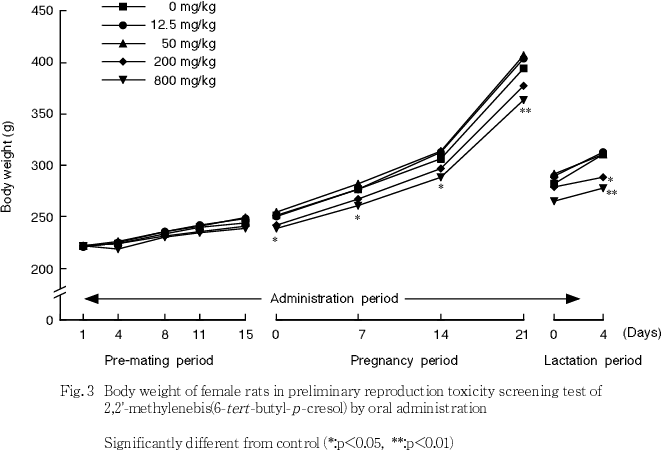
妊娠期間中において,12.5および50 mg/kg群では対照群と比べていずれの測定日の摂餌量にも有意差はみられなかった.200および800 mg/kg群では,対照群と比べて妊娠2日に摂餌量の有意な低値がみられた.
哺育期間中において,12.5および50 mg/kg群では対照群と比べて摂餌量に有意差はみられなかった.200および800 mg/kg群では,対照群と比べて哺育4日に摂餌量の有意な低値がみられた.
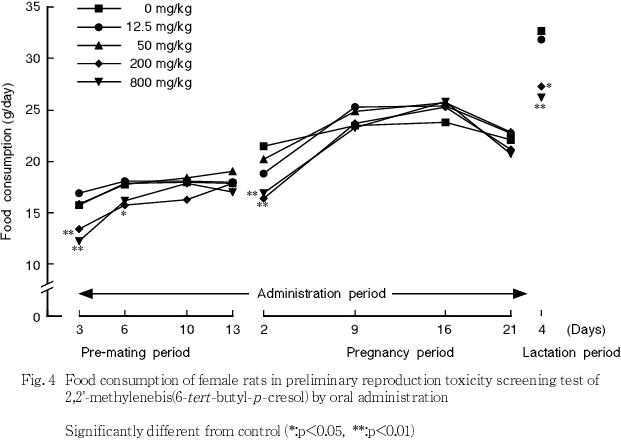
各投与群とも,対照群と比べて卵巣の絶対および相対重量に有意差はみられなかった.
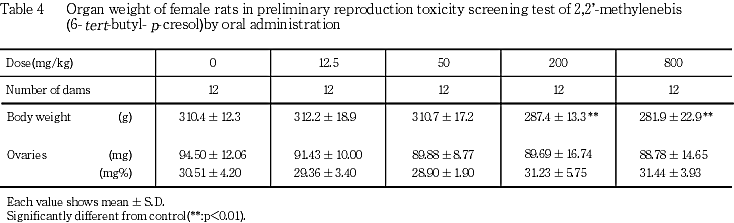
交配に用いた全例で交尾が確認されたため,各群の交尾率はいずれも100 %であった.交尾所要日数は,各投与群とも対照群との間に有意差はみられなかった.
不受胎雌は200 mg/kg群で1例みられたが,受胎率には各投与群と対照群との間に有意差は認められなかった.

12.5および50 mg/kg群では,対照群と比べて黄体数,着床痕数および着床率に有意差はみられなかった.200 mg/kg群では,対照群と比べて有意差は認められないものの,黄体数および着床痕数の低値傾向がみられた.800 mg/kg群では,対照群と比べて黄体数および着床痕数の有意な低値がみられた.
対照群,12.5,50および200 mg/kg群では出産率は100 %であった.800 mg/kg群では,2母動物で新生児が得られなかったため出産率は83.3 %であった.対照群および各投与群とも,哺育状態に異常はみられなかった.
新生児の外表観察では,各群とも異常はみられなかった.
新生児の一般状態では,各群とも異常はみられなかった.
雄に関しては,死亡および瀕死例はいずれの群にも認められなかった.200 mg/kg以上の群で投与直後に一過性の流涎がみられたが,被験物質の刺激性に基づく変化と判断され,毒性症状とはみなさなかった.摂餌量において,800 mg/kg群で投与3日に一過性の低値がみられたが,体重推移に異常は認められない軽微な変化と考えられる.剖検において,200 mg/kg群で精巣および精巣上体の萎縮が,800 mg/kg群で精巣,精巣上体および精嚢の萎縮がみられた.また,器官重量では,200 mg/kg以上の群で精巣および精巣上体の絶対ならびに相対重量の低値がみられた.精子検査において50および200 mg/kg群で活動精子率,生存精子率,生き残り精子率,精子数および精巣上体尾部1 g当たりの精子数の低値,奇形精子率の増加がみられた.800 mg/kg群では,活動精子は認められず,奇形精子の増加傾向,精子数および精巣上体尾部1 g当たりの精子数の低値がみられた.また,病理組織学検査において50 mg/kg群で精巣に巨細胞形成が,200 mg/kg群で精巣に精細管の萎縮,精細管の変性,精子減少と巨細胞形成ならびに精巣上体に精子減少が,800 mg/kg群で精巣に精細管の萎縮ならびに精巣上体に精子減少がみられた.なお,800 mg/kg群で精巣に巨細胞形成がみられなかったのは,精細管の萎縮が顕著で,生殖細胞がほとんど脱落しているため,形成された細胞も同様に脱落し認められなくなったものと考えられた.したがって,50 mg/kgの投与で精巣の精子形成に影響を及ぼすと考えられる.なお,ラットにおける28日間反復経口投与毒性試験1)では,800 mg/kg投与しても精巣重量に変化は認められず,200 mg/kg以上の群で精巣のセルトリ細胞の空胞化および精子分化の障害が認められているが,精細管の萎縮はみられていない.したがって,2,2'-メチレンビス(6-tert-ブチル-ρ-クレゾール)では,投与期間が長くなると精巣に及ぼす影響は強くなることが示唆された.
雌に関しては,死亡および瀕死例はいずれの群とも認められなかった.一般状態観察において,雄の場合と同様に200 mg/kg以上の群で認められた流涎は毒性症状とはみなさなかった.体重では,200 mg/kg群で哺育期に増加抑制が,800 mg/kg群で妊娠期および哺育期に増加抑制がみられた.また,摂餌量では,200および800 mg/kg群で交配前,妊娠期および哺育期に低値がみられた.しかし,剖検および卵巣重量では,投与による変化はみられなかった.
したがって,当試験条件下における2,2'-メチレンビス(6-tert-ブチル-ρ-クレゾール)の一般毒性学的無影響量は,雄が12.5 mg/kg/day,雌が50 mg/kg/dayと考えられる.
親動物の生殖発生に対しては,前述したように50 mg/kg以上の群で精子検査成績に影響がみられ,精巣に病理組織学変化が認められた.しかし,交配開始日までの14日間の投与では,いずれの群とも交尾率および受胎率に影響は認められなかった.
発情回数,交尾所要日数,受胎雌数,妊娠期間,分娩状態および哺育状態では,投与に起因すると思われる変化はみられなかった.しかし,200 mg/kg群で黄体数および着床痕数の低値傾向が,800 mg/kg群で黄体数および着床痕数の低値がみられた.また,800 mg/kg群で新生児を分娩できなかった雌および哺育期に新生児が全例死亡した母動物が各1例認められた.なお,着床痕数の低値は黄体数の低値に伴う変化と考えられる.
新生児に対しては,200 mg/kg群では総出産児数,哺育0および4日の新生児数の低値がみられた.800 mg/kg群では,総出産児数,出生率,哺育0および4日の新生児数の低値あるいは低値傾向,死産児数の高値傾向がみられた.また,800 mg/kg群では,哺育4日に雌雄別体重の低値あるいは低値傾向がみられた.外表観察では,各投与群とも投与による影響はみられなかった.一般状態では,各投与群とも投与による異常はみられなかった.
したがって,当試験条件下における2,2'-メチレンビス(6-tert-ブチル-ρ-クレゾール)の生殖発生毒性学的な無影響量は,雄の生殖に関しては12.5 mg/kg/day,雌の生殖に関しては50 mg/kg/day,児動物に関しては50 mg/kg/dayと推察される.
以上のように,2,2'-メチレンビス(6-tert-ブチル-ρ-クレゾール)の一般毒性学的無影響量は,雄では50 mg/kg投与により精子検査成績および精巣の病理組織学検査成績に影響が認められたことから12.5 mg/kg/day,雌では200 mg/kg投与により体重の増加抑制および摂餌量の低値が認められたことから50 mg/kg/dayと考えられる.また,生殖発生毒性学的な無影響量は,雄では50 mg/kg投与により精子検査成績および精巣の病理組織学検査成績に影響が認められたことから12.5 mg/kg/day,雌では200 mg/kg投与により黄体数および着床痕数の低値傾向が認められたことから50 mg/kg/day,児動物では200 mg/kg投与により哺育0および4日の新生児数の低値が認められたことから50 mg/kg/dayと考えられる.
| 1) | 厚生省生活衛生局企画課生活化学安全対策室監修,"化学物質毒性試験報告,"Vol. 4,化学物質点検推進連絡協議会,東京,1996, p. 413. |
| 2) | M. Kato, Cong. Anom., 35, 394(1995). |
| 連絡先 | |||
| 試験責任者: | 古橋忠和 | ||
| 試験担当者: | 長瀬孝彦,藤村高志,内藤一嘉,今枝知子,吉島賢一,加藤真之,牧野浩平 | ||
| (株)日本バイオリサーチセンター 羽島研究所 | |||
| 〒501-6251 岐阜県羽島市福寿町間島6-104 | |||
| Tel 058-392-6222 | Fax 058-392-1284 | ||
| Correspondence | ||||
| Authors: | Tadakazu Furuhashi(Study director) Takahiko Nagase, Takashi Fujimura, Kazuyoshi Naitou, Tomoko Imaeda, Ken-ichi Yoshijima, Masashi Katou and Kohei Makino | |||
| Nihon Bioresearch Inc. Hashima Laboratory | ||||
| 6-104 Majima, Fukuju-cho, Hashima, Gifu, 501-6251, Japan. | ||||
| Tel +81-58-392-6222 | Fax +81-58-392-1284 | |||