
毒性予備試験を行った結果,雄および雌マウスにおける最大耐量は,いずれも 2000 mg/kgであった.小核予備試験において,2000 mg/kgを雄マウスに投与し,投与後24,48および72時間に骨髄の塗抹標本を作製した.小核出現頻度は,24時間群と他の群との間に明瞭な差は認められなかった.また,赤血球中に占める幼若赤血球の比率を指標とした骨髄細胞の増殖抑制も認められなかった.これらの結果から,雄雌ともに小核本試験でのN-(アミノエチル)エタノールアミンの最高用量を2000 mg/kgとし,標本作製時期を投与後24時間に決定した.
N-(アミノエチル)エタノールアミンの500,1000および2000 mg/kgを雄および 雌マウスにそれぞれ投与し,投与後24時間目に標本を作製した.小核出現頻度は,雄においては,いずれの投与群においても,溶媒対照群と比較して統計学的に有意な増加は認められず,用量依存性も認められなかった.しかし,雌においては,小核出現頻度は,用量に依存して増加し,2000 mg/kg投与群において溶媒対照群と比較して統計学的に有意に増加した.しかし,その小核出現頻度は溶媒対照群の背景データをわずかに上回っていたのみであった.また,全赤血球中に占める幼若赤血球の比率は,いずれの投与群においても,溶媒対照群との間に有意差は認められなかった.
小核本試験において,雌のみで用量に依存して小核の誘発が認められたので,その結果を確認するために,雌マウスを用いて,小核本試験と同様の実験群を設定し,追加試験を実施した.その結果,小核出現頻度は,いずれの投与群においても,溶媒対照群と比較して統計学的に有意な増加は認められず,用量依存性も認められなかった.また,全赤血球中に占める幼若赤血球の比率は,雄雌ともにいずれの投与群においても,溶媒対照群との間に有意差は認められず,被験物質が標的細胞を暴露した証拠は得られなかったが,雄雌ともに最高用量を 2000 mg/kgで試験を実施したことから,充分評価に耐えうる試験結果であると考えられる.
以上の結果から, N-(アミノエチル)エタノールアミンは,本試験条件下でCrj:BDF1雄および雌マウスの骨髄細胞において,小核誘発作用を示さないと結論した.
動物は,床敷としてホワイト・フレーク (R)(CRJ)を入れたTPX樹脂製ケージ(CRJ)に1匹ずつ収容し,バリアーシステムの飼育室(設定温度:23±1℃,設定湿度:55±5%,換気回数:約15回/時間,明暗サイクル:午前7時点灯,午後7時消灯)で,マウス繁殖用固型飼料(NMF)と水道水を自由に摂取させて飼育した.動物の群分けは自由群分け(無作為抽出)により行った.
調製溶液の安定性について, 2.50 mg/ml溶液は秦野研究所で実施した染色体異常試験で調製したものについて,また200 mg/ml溶液(2000 mg/kg群)は,本試験で調製したものについて,室温遮光条件下で調べた.その結果,調製4時間後における各濃度の平均含量は,それぞれ初期値(0時間)の平均値に対して,103および99.3%であった.また,投与検体について含量測定試験を行った.その結果,500 mg/kg群および2000 mg/kgの投与検体について,含量はそれぞれ95.4および102%であった.
また,陽性対照物質 , サイクロフォスファミド(CPA, Sigma Chemical Co.,) は,局方生理食塩液に溶解して所定の濃度に調製し,50 mg/kgの用量を単回強制経口投与した.
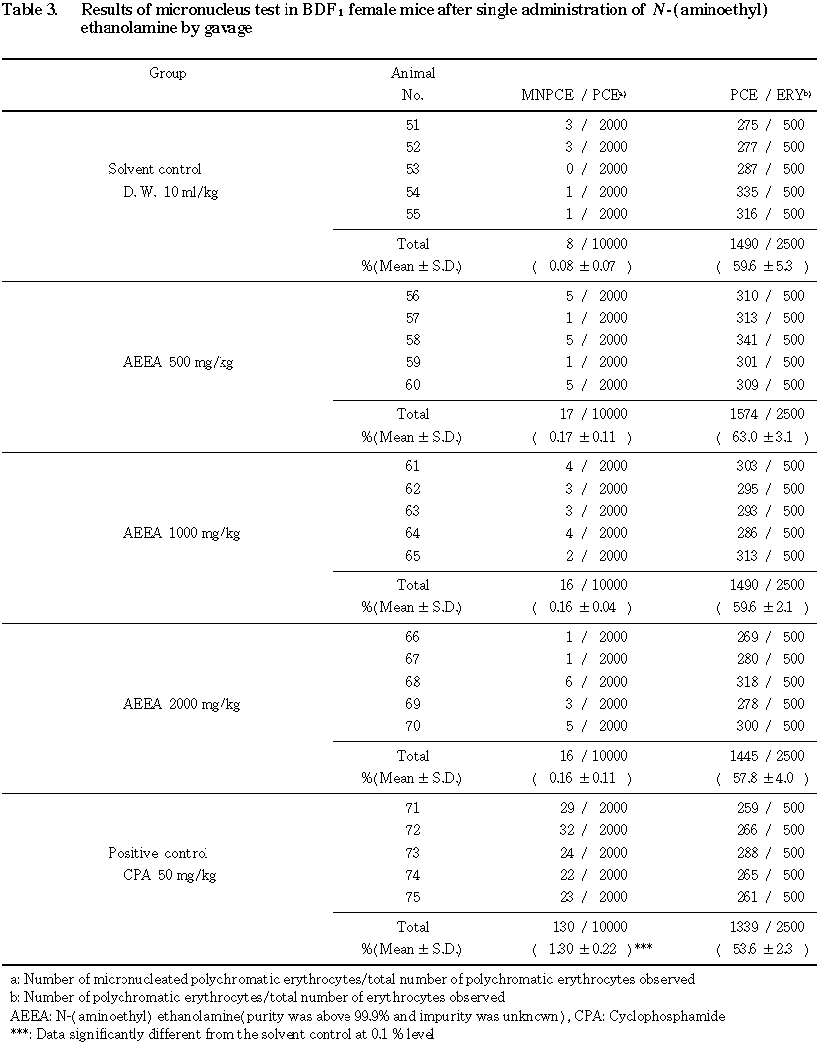
骨髄標本はそれぞれの個体について, 2名の観察者によりブラインド法で観察した.1個体あたり2000個の幼若赤血球(polychromatic erythrocytes)を観察し,その中の小核を有するものの数を記録した.また赤血球を1個体あたり500個観察し,その中の幼若赤血球の比率を調べて,骨髄細胞の増殖抑制の指標とした.
その結果,すべての投与群において,毒性徴候および死亡例は認められなかった.したがって, N-(アミノエチル)エタノールアミンの強制経口投与によるCrj:BDF1雄および雌マウスの最大耐量は,2000 mg/kgであると判断し,それを小核予備試験に用いる投与用量とした.
一方,雌の投与群における小核出現頻度は, Fisher の正確確率検定法(Bonferroniの補正)による有意差検定の結果,2000 mg/kg群において,溶媒対照群と比較して統計学的に有意な増加を示した.また,Cochran-Armitageの傾向検定でも,用量に依存した有意な増加傾向を示した.一方,CPAを50 mg/kg投与した陽性対照群での小核出現頻度は,5%水準で有意な増加がみられた.さらに,2000 mg/kg投与群における小核出現頻度は,秦野研究所における溶媒対照群の背景データのばらつきの範囲内(1994年11月〜1995年4月までの7試験における0.01〜0.27)をわずかに上回った.
雌の追加試験の結果を Table 3に示す.溶媒対照群および陽性対照群の小核出現頻度は,それぞれ背景データのばらつきの範囲内 (平均値±3×標準偏差)であった.N-(アミノエチル)エタノールアミン投与群の小核出現頻度は,Fisherの正確確率検定法(Bonferroniの補正)による有意差検定の結果,いずれの投与群においても,溶媒対照群と比較して統計学的に有意な増加は認められなかった.さらに,Cochran-Armitageの傾向検定においても,用量に依存した有意な増加傾向は認められなかった.一方,CPAを50 mg/kg投与した陽性対照群での小核出現頻度は,5%水準で有意な増加がみられた.赤血球中に占める幼若赤血球の比率は,いずれの検体投与群および陽性対照群においても,溶媒対照群との間に有意差は認められなかった.
全赤血球中に占める幼若赤血球の比率は,いずれの投与群においても,雄雌ともに溶媒対照群との間に有意差は認められず,被験物質が標的細胞を充分暴露した証拠は得られなかった.しかし,雄および雌において,最高用量を 2000 mg/kgとして試験を実施しているので,充分評価に耐えうる試験結果であると考えられる.
N-(アミノエチル)エタノールアミンの変異原性については,Zeiger8)は,S. thphimurium TA1535の代謝活性化によって,弱い陽性の結果を得ている.また,Fouremanら9)もショウジョウバエの伴性劣性致死試験で擬陽性の結果を得ている.一方,Leung10)は,6種のアルキレンアミンについて,変異原性を多種の試験系によって調べ,S. thphimuriumの4菌株では,代謝活性化の有無に関わらず陰性,チャイニーズ・ハムスターのCHO細胞を用いる遺伝子突然変異試験および姉妹染色体交換試験においても,代謝活性化の有無に関わらず陰性,さらに生体内のラットの肝細胞の不定期DNA合成試験でも陰性の結果を得ている.このように,N-(アミノエチル)エタノールアミンの変異原性は,それほど強くないものと推察される.
小核本試験において,雄では小核出現頻度の増加は認められなかったが,雌では,最高用量の 2000 mg/kg投与群で溶媒対照群の背景データの範囲をわずかに上回る小核の誘発が認められた.雌における結果を確認するために同一用量での追加試験を行ったところ,小核出現頻度の増加は認められなかった.
以上の結果と報告されている他の変異原性試験の結果を併せて考察すると,マウスの小核試験については,雄雌ともに陰性であると判断される.


| 1) | W. Schmid, Mutat. Res., 31, 9, (1975) |
| 2) | W. Schmid, "Chemical Mutagens," Vol. 4, ed. by A. Hollander, Plenum Press, New York, London, 1976, pp. 76-78. |
| 3) | M. Hayashi, T. Sofuni, M. Ishidate, Jr., Mutat. Res., 120, 241, (1983). |
| 4) | 林 真, "小核試験," サイエンティスト社,東京, 1991, pp. 44-55. |
| 5) | 吉村 功 編, "毒性・薬効データの統計解析," サイエンティスト社,東京, 1987, pp. 76-78. |
| 6) | 吉村 功,大橋靖雄 責任編集,"毒性試験講座14, 毒性試験データの統計解析," 地人書館,東京,1992,pp.18-222. |
| 7) | 吉村 功 編, "毒性・薬効データの統計解析," サイエンティスト社,東京,1987,pp. 67-69. |
| 8) | E. Zeiger, B. Anderson, S. Howorth, T. Lawlor, K. Mortelmans, W. Speck, Env. Mutag., 9(Supple. 7), 1(1987). |
| 9) | P. Foureman, J. M. Mason, R. Valencia, S. Zimmerings, Env. Mol. Mutag., 23, 51(1994). |
| 10) | H-W. Leung, Mutat. Res., 320, 31(1994). |
| 連絡先 | |||
| 試験責任者: | 澁谷 徹 | ||
| 試験担当者: | 堀谷尚古,加藤基恵,原 巧,
関野早苗,松木容彦, 飯田さやか,中込まどか | ||
| Correspondence | |||
| Authors: | Tohru Shibuya(Study Director)
Naoko Horiya, Motoe Katoh, Hara Takumi, Sanae Sekino, Yasuhiko Matsuki, Sayaka Iida, Madoka Nakagomi | ||
| Hatano Research Institute, Food and Drug Safety Center | |||
| 729-5, Ochiai, Hadano-shi, Kanagawa 257 Japan | |||
| Tel +81-463-82-4751 | Fax +81-463-82-9627 | ||