 死亡動物
死亡動物
投与後の一般状態の変化として,雌雄の150 mg/kg以上の投与群で流涎が,雌雄の500 mg/kg群および雌の150 mg/kg群で流涙が認められた.
体重および摂餌量では,雌雄とも被験物質投与の影響は認められなかった.臨床検査では被験物質投与の影響を示唆する変化として,雄の150 mg/kg以上の投与群および雌の全ての投与群で総胆汁酸の高値,雄の500 mg/kg群で中性脂肪の低値が認められた.しかし,いずれも機序については不明であった.
病理学検査では,剖検所見および組織所見に被験物質投与の影響と考えられる変化は認められなかった.器官重量では雄の500 mg/kg群で腎臓の相対重量が高値を示した.この所見に対応する組織変化は認められなかったが,被験物質投与の影響が疑われた.
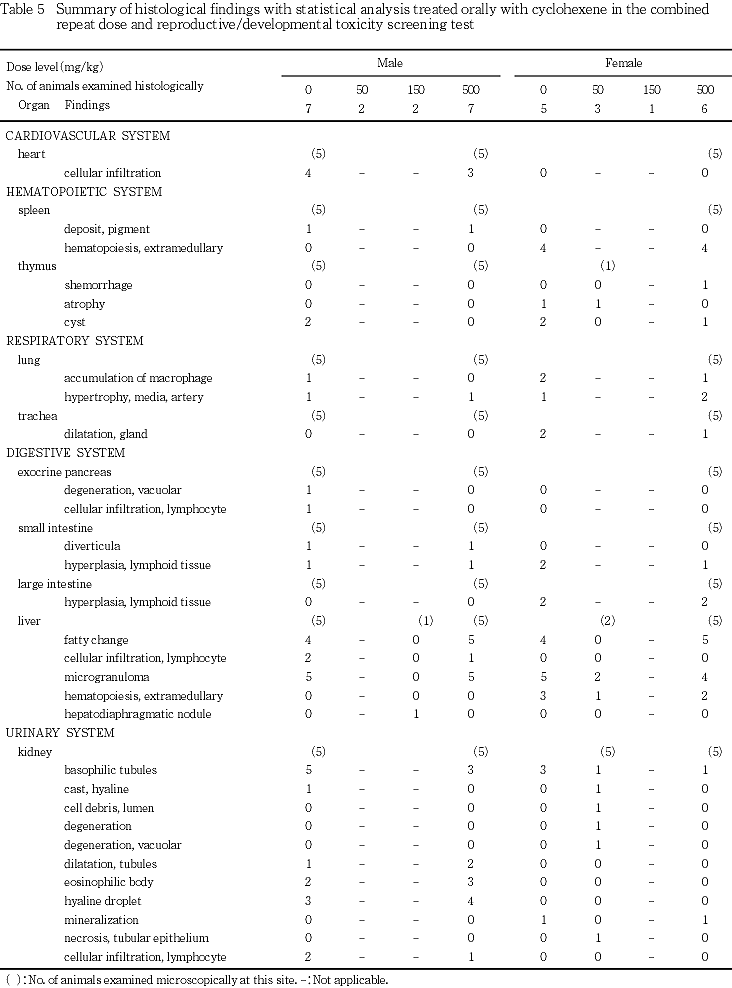
また,分娩状態,妊娠期間にも被験物質投与の影響は認められなかった.
新生児の外表検査では,被験物質投与の影響と考えられる異常は認められず,体重変化にも影響は認められなかった.
死亡児および哺育4日の剖検でも被験物質投与の影響と考えられる異常所見は観察されなかった.
以上の結果から,本試験条件下ではシクロヘキセンの反復投与毒性に関する無影響量(NOEL)は雄では50 mg/kg/dayと判断された.
雌雄の生殖能および児動物の発生・発育に及ぼす無影響量はともに500 mg/kg/dayと判断された.
被験物質はコーンオイル(ナカライテスク(株))に溶解し,10,30および100 mg/mLの濃度になるよう各群の投与液を調製した.また,コーンオイル中の被験物質は,3および200 mg/mLの濃度では室温(約25 ℃)保存下24時間および冷蔵(約4 ℃)保存下7日間安定であることを確認した.
投与液の濃度分析は,調製開始時に調製した全ての試験群の投与液について行った.その結果,表示濃度に対する誤差が+1.4から+1.9 %の範囲であり,基準範囲内(± 10 %以内)であった.したがって,使用した投与液にはほぼ所定量のシクロヘキセンが含有されていたことが確認された.
動物は,温度24 ± 3 ℃,湿度55 ± 20 %,換気回数15回/時間,照度150〜300 lux,照明時間12時間(午前7時点灯,午後7時消灯)に管理されたバリアシステムの飼育室でアルミ製前面・床ステンレス網目飼育ケージに1匹ずつ収容し飼育した.妊娠18日以降の母動物は哺育4日までアルミ製前面・床ステンレス網目飼育ケージに哺育トレーおよび巣作り材料(サンフレーク,日本チャールス・リバー(株)製造)を入れて飼育した.
飼料は,オリエンタル酵母(株)製造のCRF-1固形飼料(放射線滅菌飼料)を使用し,飼育期間中自由に摂取させた.飲水は,水道水を自由に摂取させた.
投与液量は,体重100 gあたり0.5 mLとし,交配前および交配期間中の雌雄および交尾不成立の雌では,個体別に測定した最新体重に基づいて算出を行った.また,妊娠および哺育期間中の雌は,妊娠0,7,14,20および哺育0日に測定した個体別体重に基づいて算出を行った.胃ゾンデを用いて毎日1回(7日/週)強制経口投与した.対照群にはコーンオイルのみを同様に投与した.
投与期間は,雄は交配前14日間と交配期間14日間および交配期間終了後20日間の連続48日間とした.雌は交配前14日間と交配期間中(最長14日間)および交尾成立雌は妊娠期間を通じて分娩後の哺育4日まで(42〜53日間)とした.交尾不成立の雌は交配期間終了後24日間の連続52日間とした.また,交尾後分娩しなかった雌は妊娠25日の解剖前日まで(40〜43日間)とした.
雌は投与1(投与開始日),8および15日に測定し,投与1から15日までの体重増加量を算出した.交尾が確認されなかった雌はそれ以降の投与22,29,36,43,50および53日に測定した.また,交尾が確認された雌は,妊娠0,7,14および20日に,分娩した雌は哺育0,4および5日(剖検日)に測定し,それぞれ妊娠0から20日および哺育0から4日までの体重増加量を算出した.死亡動物については発見時にも測定した.
雌は投与1(投与開始日),8および15日に餌重量を測定し,測定日から次の測定日までの摂餌量を求め平均1日摂餌量を算出するとともに投与1から15日までの累積摂餌量を算出した.交尾が確認されなかった雌はそれ以降の投与29,36,43,50および52日に餌重量を測定し,測定日から次の測定日までの摂餌量を求め平均1日摂餌量を算出した.また,交尾が確認された雌は妊娠0,7,14および20日に,分娩した雌は哺育0および4日に餌重量を測定し,測定日から次の測定日までの摂餌量を求め平均1日摂餌量を算出するとともに妊娠0から20日までの累積摂餌量を算出した.
なお,交配期間中の雌雄同居動物は摂餌量を測定しなかった.
性周期観察は交尾確認日まで行い,発情期から次の発情期までの間の日数を性周期日数として平均性周期を算出した.また,性周期観察期間中の異常性周期(4または5日以外の性周期)発現率[(異常性周期を示す雌動物数/観察雌動物数)× 100]を算出した.
交配結果から各群について交尾率[(交尾動物数/同居動物数)× 100]を算出した.
新生児は哺育0日に出産児数(生存児+死亡児)を調べ,性別を判定し,性比(雄/雌)を算出するとともに,外表異常の有無を調べた.また,哺育0および4日に雌雄個体別の体重を測定し,1腹の雌雄別平均体重を算出した.哺育4日の体重測定後,エーテル麻酔下で放血安楽死させ,器官・組織の肉眼的観察を行った.死産児および哺育期間中の死亡児はブアン氏液に固定し,器官・組織の肉眼的観察を実施した.また,新生児の4日の生存率[(哺育4日生児数/出産生児数)× 100]を算出した.
a) 血液学検査
抗凝固剤(EDTA-2K)入り採血管インセパック-E(積水化学工業(株))に新鮮血を採取し,総合血液学検査装置ADVIA120(バイエル社)を用いて白血球数(WBC:フローサイトメトリー法),赤血球数(RBC:暗視野板法),ヘモグロビン量(HGB:シアンメトヘモグロビン法),ヘマトクリット値(HCT:RBC,MCVより算出),平均赤血球容積(MCV:暗視野板法),平均赤血球血色素量(MCH:HGB,RBCより算出),平均赤血球色素濃度(MCHC:HGB,HCTより算出),血小板数(PLT:暗視野板法),白血球百分率(フローサイトメトリー法)および網赤血球率(Reticulocyte:RNA染色法)を測定した.
b) 血液凝固能検査
抗凝固剤(3.13 %クエン酸ナトリウム水溶液)入り採血管ベノジェクト・(テルモ(株))に血液を採取した後,3000 r.p.m.で13分間遠心分離して得た血漿を検査に用いた.血液凝固測定装置KC-40(アメルング社)を用いてプロトロンビン時間(PT:Quick一段法)および活性化部分トロンボプラスチン時間(APTT:クロット法)を測定した.
c) 血液生化学検査
インセパック-SQ(積水化学工業(株))に血液を採取した後,3000 r.p.m.で7分間遠心分離して得た血清を検査に用いた.多項目生化学自動分析装置日立7170((株)日立製作所)を用いて総蛋白(T. protein:Biuret法),アルブミン(Albumin:BCG法),A/G(計算値),血糖(Glucose:HK-G-6-PDH法),中性脂肪(Triglyceride:GK-GPO遊離グリセロール消去法),総コレステロール(T. cholesterol:コレステロールオキシダーゼ・HDAOS法),尿素窒素(BUN:ウレアーゼ・GLDH法),クレアチニン(Creatinine:酵素法),総ビリルビン(T. bilirubin:バナジン酸酸化法),アスパラギン酸アミノトランスフェラーゼ(AST:酵素-UV法),アラニンアミノトランスフェラーゼ(ALT:酵素-UV法),アルカリホスファターゼ(ALP:P-ニトロフェニルリン酸基質法),カルシウム(Calcium:MXB法),無機リン(I. phosphorus:PNP-XDH法)および総胆汁酸(T. bile acid:酵素サイクリング法)を,電解質測定装置EA06R((株)エイ アンド ティー)を用いてナトリウム(Sodium:イオン選択電極法),カリウム(Potassium:イオン選択電極法)および塩素(Chloride:イオン選択電極法)を測定した.
d) 尿検査
投与期間終了週に,各群それぞれ5例の雄動物について給餌・給水の条件下で採尿ケージを用いて3時間尿および24時間尿を採取した.3時間尿を用いてpH,潜血,糖および蛋白を検査した.検査にはN-マルティスティックスSG(バイエル・三共(株))を用い,判定は尿分析装置CLINITEK500(バイエル社)で行った.24時間尿を用いて尿量(計量)および色調(目視)を検査した後,尿を室温,1500 r.p.m.で5分間遠心し,上清および残渣に分離した.上清を用いてAuto&stat OM-6030((株)アークレイファクトリー)で尿浸透圧(氷点降下法)を測定した.
 死亡動物
死亡動物
剖検では器官・組織の肉眼的観察を行い,皮膚,乳腺,リンパ節(腸間膜リンパ節,下顎リンパ節),胸骨,大腿骨,骨髄(胸骨,大腿骨),胸腺,気管,肺および気管支,心臓,甲状腺,上皮小体,舌,食道,胃および十二指腸,小腸(パイエル板を含む),大腸(パイエル板を含む),肝臓,膵臓,脾臓,腎臓,副腎,膀胱,精嚢,前立腺,眼球,ハーダー腺,脳(大脳,小脳,橋を含む),下垂体,脊髄(頸部,胸部,腰部),坐骨神経(筋肉近位端を含む)を10 vol%中性緩衝ホルマリン液に,精巣および精巣上体をブアン氏液に固定した.
 雄動物
雄動物
48日間投与した翌日,採血安楽死させ,器官・組織の肉眼的観察を行った後,脳,胸腺,肝臓,腎臓,脾臓,副腎,精巣および精巣上体重量を測定した.解剖日の体重を基に器官重量・体重比(相対重量)を算出した.また,全動物について皮膚,乳腺,リンパ節(腸間膜リンパ節,下顎リンパ節),胸骨,大腿骨,骨髄(胸骨,大腿骨),胸腺,気管,肺および気管支,心臓,甲状腺,上皮小体,舌,食道,胃および十二指腸,小腸(パイエル板を含む),大腸(パイエル板を含む),肝臓,膵臓,脾臓,腎臓,副腎,膀胱,精嚢,前立腺,眼球,ハーダー腺,脳(大脳,小脳,橋を含む),下垂体,脊髄(頸部,胸部,腰部),坐骨神経(筋肉近位端を含む)を10 vol%中性緩衝ホルマリン液に,精巣および精巣上体をブアン氏液に固定した.
 自然分娩した雌
自然分娩した雌
哺育5日に,採血安楽死させ,器官・組織の肉眼的観察を行った後,脳,胸腺,肝臓,腎臓,脾臓,副腎および卵巣重量を測定した.解剖日の体重を基に相対重量を算出した.また,全動物について皮膚,乳腺,リンパ節(腸間膜リンパ節,下顎リンパ節),胸骨,大腿骨,骨髄(胸骨,大腿骨),胸腺,気管,肺および気管支,心臓,甲状腺,上皮小体,舌,食道,胃および十二指腸,小腸(パイエル板を含む),大腸(パイエル板を含む),肝臓,膵臓,脾臓,腎臓,副腎,膀胱,卵巣,子宮,腟,眼球,ハーダー腺,脳(大脳,小脳,橋を含む),下垂体,脊髄(頸部,胸部,腰部),坐骨神経(筋肉近位端を含む)を10 vol%中性緩衝ホルマリン液に固定した.なお,剖検時に黄体数および着床痕数を調べた.
 交尾の成立しなかった雌
交尾の成立しなかった雌
52日間投与の翌日,エーテル麻酔下で放血安楽死させ,器官・組織の肉眼的観察を行った後, に示した全ての固定器官を同様に固定した.
に示した全ての固定器官を同様に固定した.
 自然分娩の認められない雌
自然分娩の認められない雌
妊娠25日に,エーテル麻酔下で放血安楽死させ,器官・組織の肉眼的観察を行った後, に示した全ての固定器官を同様に固定した.着床痕が認められない動物は妊娠不成立と判定した.
に示した全ての固定器官を同様に固定した.着床痕が認められない動物は妊娠不成立と判定した.
 全児死亡の認められた雌
全児死亡の認められた雌
生存児全ての死亡または喰殺が確認された日にエーテル麻酔下で放血安楽死させ,器官・組織の肉眼的観察を行った後, に示した全ての固定器官を同様に固定した.なお,剖検時に黄体数および着床痕数を調べた.
に示した全ての固定器官を同様に固定した.なお,剖検時に黄体数および着床痕数を調べた.
 死亡動物および全児死亡動物
死亡動物および全児死亡動物
全固定器官について実施した.
 妊娠を成立させた雄
妊娠を成立させた雄
対照群と高用量群の各5例については全固定器官,および全群の剖検時に認められた異常病変部組織について実施した.
 自然分娩した雌
自然分娩した雌
対照群と高用量群の各5例については全固定器官,および全群の剖検時に認められた異常病変部組織について実施した.
 交尾の成立しなかった雌雄
交尾の成立しなかった雌雄
腟,子宮,卵巣,精巣,精巣上体,精嚢,前立腺および異常病変部組織について実施した.
 妊娠を成立させなかった雄および妊娠不成立の雌
妊娠を成立させなかった雄および妊娠不成立の雌
腟,子宮,卵巣,精巣,精巣上体,精嚢および前立腺について実施した.
なお,精巣についてはPAS・ヘマトキシリン染色およびヘマトキシリン・エオジン染色した後,ヘマトキシリン・エオジン染色標本で一般的病変を検査し,PAS・ヘマトキシリン染色標本で精子形成サイクル(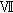 または
または )を検査した1).
)を検査した1).
出産率,交尾率および受胎率についてはχ2検定を用いた.
異常性周期発現率,剖検所見および病理組織所見の発生率についてはFisherの直接確率検定法で検定した.
有意水準はBartlettの等分散検定については5 %,その他の検定は5および1 %の両側検定で実施した.但し,供試動物数が1群につき2例以下の場合,有意差検定は行わなかった.なお,哺育期間中の出生児に関する成績は1母体当たりの平均を1標本として集計した.
一般状態の観察で,雄では,被験物質投与の影響と考えられる症状として流涎が150および500 mg/kg群でそれぞれ3および12例(全例),流涙が500 mg/kg群で2例に認められた.その他,鼻分泌物が50および150 mg/kg群でそれぞれ2および1例,軟便が対照群,50および500 mg/kg群でそれぞれ1,2および1例,脱毛が50,150および500 mg/kg群でそれぞれ1,1および4例,痂皮が150および500 mg/kg群で各1例,外傷が500 mg/kg群で1例に観察された.150 mg/kg群で観察された流涎の多くは投与直後から投与後5分程度までの一過性の変化であった.一方,500 mg/kg群での流涎は投与後30から60分まで継続していた.
雌では交配前,交配,妊娠および哺育期間を通じて流涎が150および500 mg/kg群で2および12例(全例),流涙が150および500 mg/kg群で各1例に観察された.その他,鼻分泌物,眼分泌物が500 mg/kg群でそれぞれ1例,脱毛が50,150および500 mg/kg群でそれぞれ2例,痂皮が50,150および500 mg/kg群でそれぞれ1,1および2例に観察された.流涎は150 mg/kg群では投与直後から投与後5分程度までの一過性の変化であった.一方,500 mg/kg群では投与後6時間まで継続する動物も数例認められた.
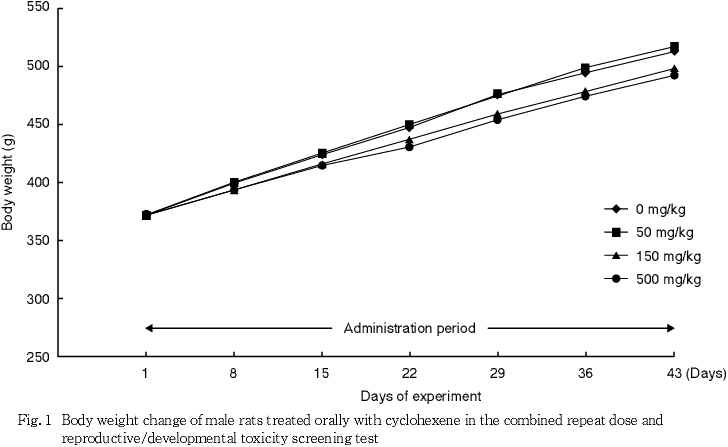
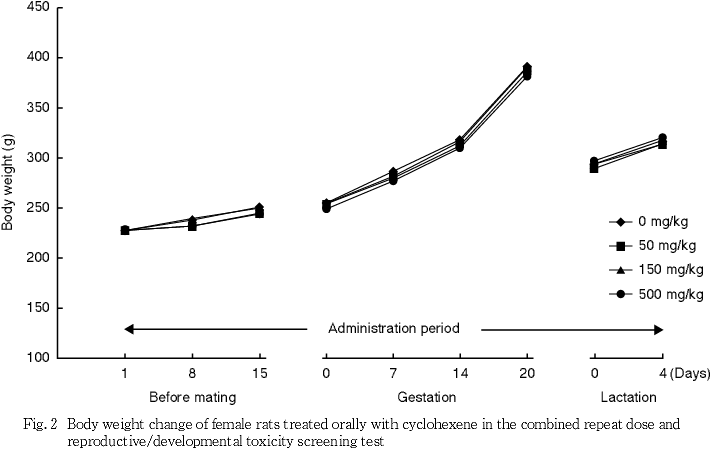
雌では対照群と被験物質投与群との間で有意な差は認められなかった.
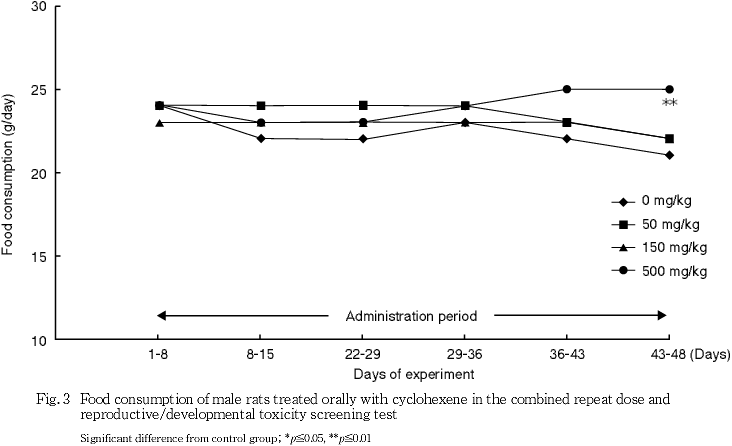
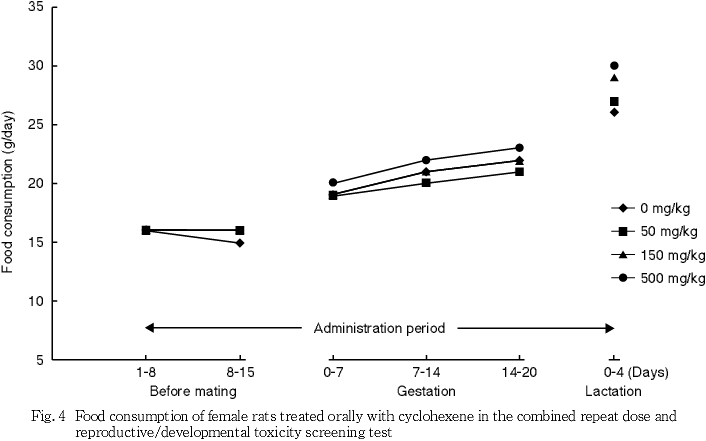
血液凝固能検査において,雄では対照群に比べ500 mg/kg群で活性化部分トロンボプラスチン時間が有意な短縮を示した.雌では500 mg/kg群でプロトロンビン時間が有意な延長を示したが,軽微な変化であり被験物質投与の影響とは判断しなかった.
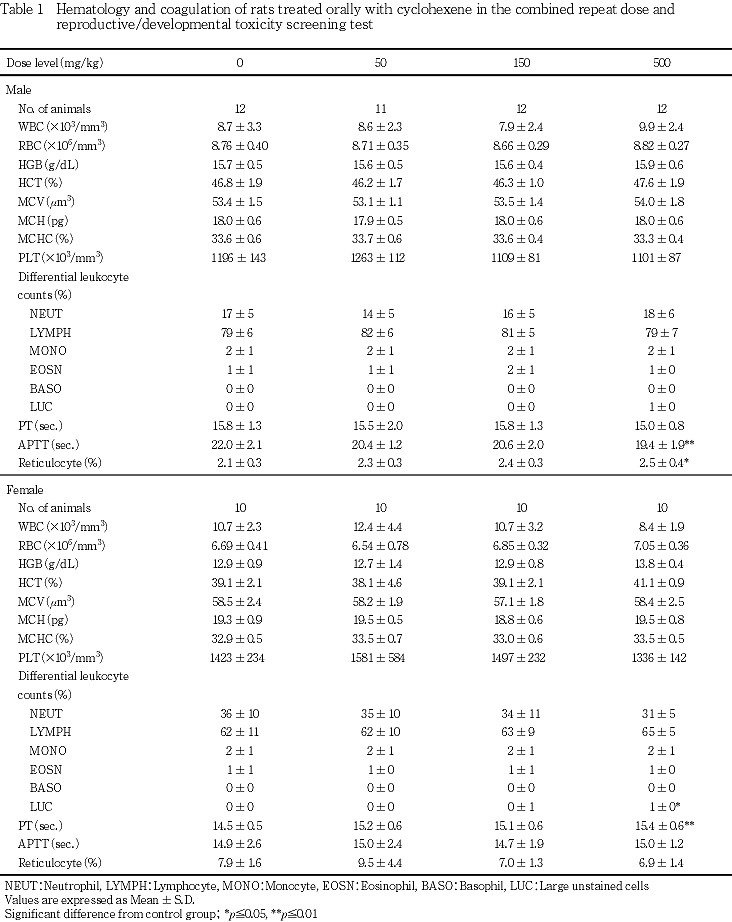
雌では,全ての被験物質投与群で総胆汁酸が有意あるいは統計学的に有意差が認められないものの高値を示した.さらに,500 mg/kg群でALTが有意な低値を示した.
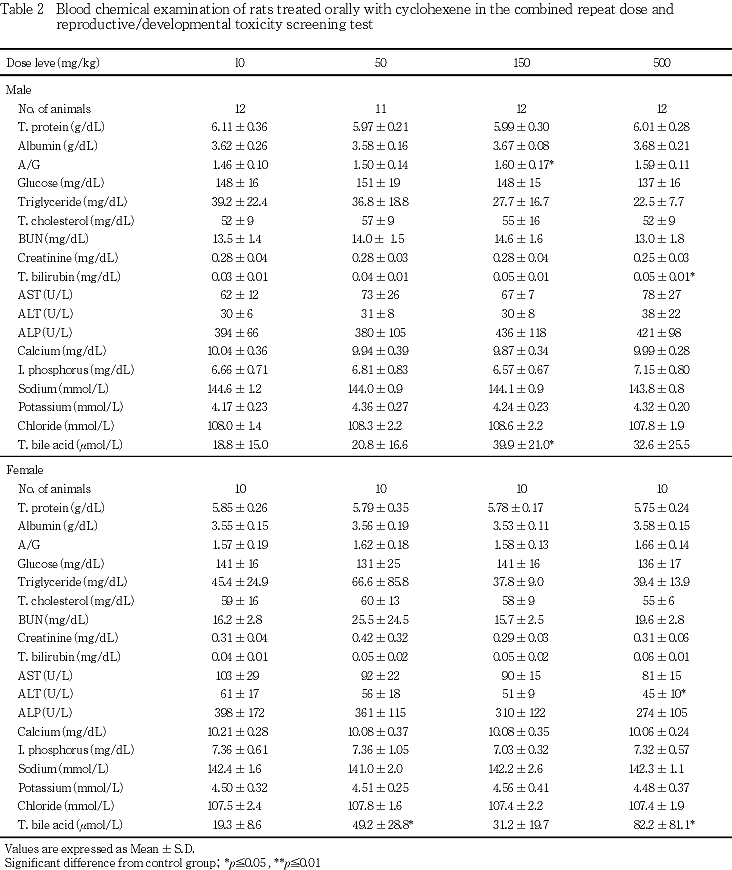
他の検査項目には,対照群と被験物質投与群との間に有意な差は認められなかった.
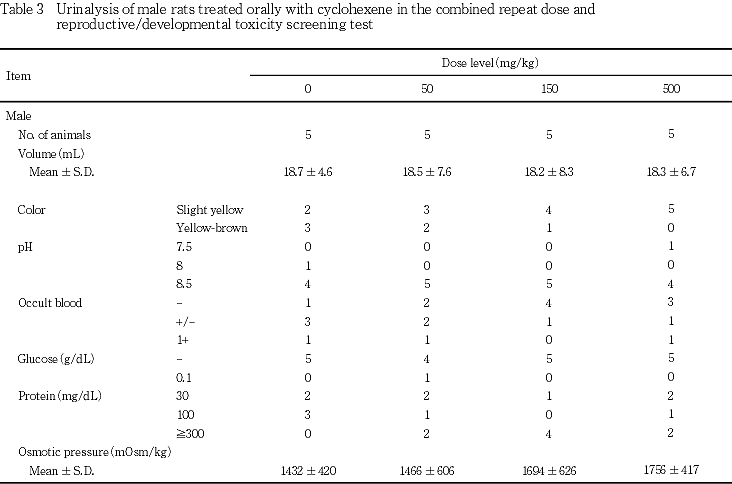
雌ではいずれの測定器官にも対照群と被験物質投与群との間に有意な差は認められなかった.
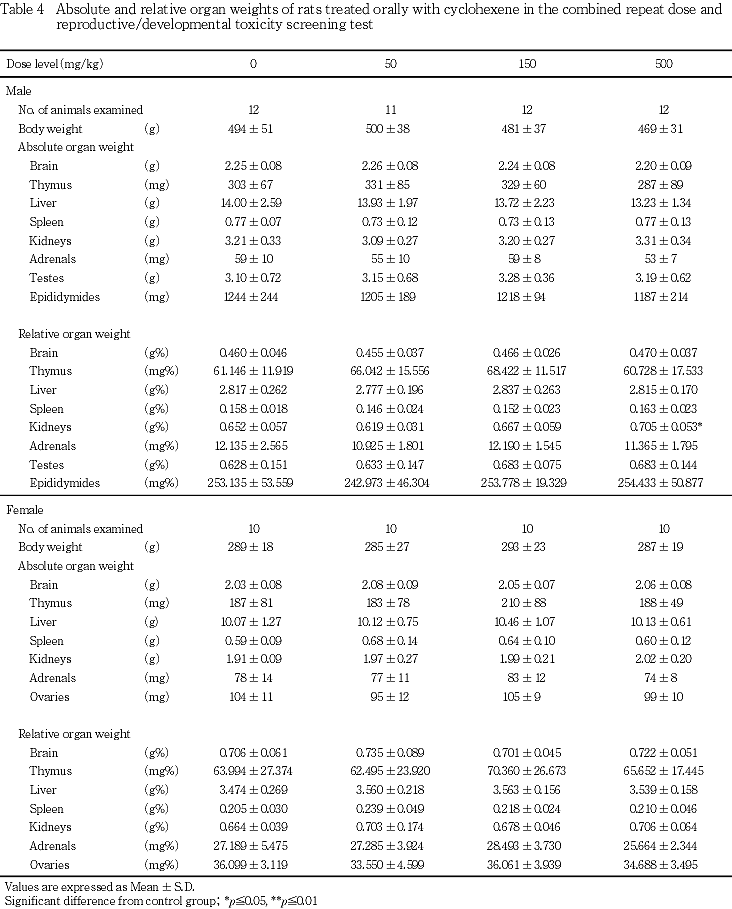
計画解剖した雄では,小腸の憩室が対照群および500 mg/kg群で各1例,横隔膜結節が150 mg/kg群で1例,精巣および精巣上体の萎縮が対照群,50および500 mg/kg群で各1例,精巣上体の結節が対照群,50および500 mg/kg群で2,2および1例,脱毛が150および500 mg/kg群で各1例に観察された.
計画解剖した雌では胸腺の萎縮,肝臓の白色斑点および黄色斑点,腎臓の淡色化および皮膚の痂皮が50 mg/kg群で各1例,胸腺の赤色化が500 mg/kg群で1例,脱毛が150および500 mg/kg群で各1例に観察された.50 mg/kg群の交尾が確認されなかった雌1例の解剖では,腎臓の腎盂拡張および尿管の内腔拡張が観察された.対照群,50,150および500 mg/kg群でそれぞれ1,1,2および2例に認められた妊娠不成立雌の剖検では,子宮の嚢胞が対照群で1例に観察された.
妊娠を成立させた雄では,対照群と比較して被験物質投与群に多く発生した所見は認められなかった.所見としては心臓の細胞浸潤,肝臓の脂肪化および小肉芽腫,腎臓の尿細管好塩基化および硝子滴,前立腺のリンパ球浸潤が対照群および500 mg/kg群で多数例に観察された.その他,認められた所見は単発性あるいは散発性の発現であった.また,肉眼所見の異常病変に相当して肝横隔膜結節および精巣上体の精子肉芽腫が観察された.
対照群および500 mg/kg群の妊娠を成立させた雄各5例の精巣について精子形成サイクルのステージ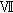 -
- における精細管の精上皮細胞数を測定した結果,いずれの細胞数も対照群と同程度であった.なお,交尾が確認されなかった雄(50 mg/kg の1例)および妊娠を成立させなかった雄3例(150 mg/kg の2例および500 mg/kg群の1例)における精上皮細胞数も,妊娠を成立させた雄の精上皮細胞数と差がみられなかった.他の妊娠を成立させなかった雄3例は,組織学的に精細管が萎縮しており,精子形成サイクルの測定は不可能であった.
における精細管の精上皮細胞数を測定した結果,いずれの細胞数も対照群と同程度であった.なお,交尾が確認されなかった雄(50 mg/kg の1例)および妊娠を成立させなかった雄3例(150 mg/kg の2例および500 mg/kg群の1例)における精上皮細胞数も,妊娠を成立させた雄の精上皮細胞数と差がみられなかった.他の妊娠を成立させなかった雄3例は,組織学的に精細管が萎縮しており,精子形成サイクルの測定は不可能であった.
自然分娩した雌では,対照群と比較して被験物質投与群に多く発生した所見は認められなかった.所見としては脾臓の髄外造血,肝臓の脂肪化および小肉芽腫,乳腺の増生,子宮の分娩後病変が対照群および500 mg/kg群で多数例に観察された.その他,認められた所見は単発性あるいは散発性の発現であった.また,肉眼所見の異常病変に相当して胸腺の出血,萎縮(中等度),肝臓の小肉芽腫および髄外造血,腎臓の尿細管好塩基化,硝子円柱,管内細胞残屑,近位尿細管の変性,空胞変性および管上皮壊死,皮膚の潰瘍が観察された.
50 mg/kg群の交尾が確認されなかった雌雄1組では,雄に前立腺のリンパ球浸潤,雌に腎臓の尿細管好塩基化および腎盂拡張(中等度)および子宮の内腔拡張が観察された.
妊娠を成立させなかった雄では,精巣の精細管の萎縮(中等度)および間細胞増生が対照群,50および500 mg/kg群で各1例,精巣の多核巨細胞出現が50および500 mg/kg群で各1例,精巣上体の精子減少が対照群,50および500 mg/kg群で各1例観察された.
妊娠不成立の雌では,子宮の腺腔拡張が観察された.
全児死亡の認められた対照群の雌では,脾臓の色素沈着および髄外造血,胸腺の嚢胞,肺のマクロファージ集簇,肝臓のリンパ球浸潤,小肉芽腫および髄外造血,腎臓の尿細管好塩基化およびリンパ球浸潤,ハーダー腺の小肉芽腫が観察された.
性周期観察では,平均性周期に対照群と被験物質投与群との間に有意な差は認められなかった.異常性周期を示す動物が150および500 mg/kg群で1および2例認められたが,異常性周期発現率には対照群と被験物質投与群との間に差は認められなかった.
哺育0および4日の体重では,雌雄ともに対照群と被験物質投与群との間に有意な差は認められなかった.
哺育期間中の死亡児の剖検では,腎盂拡張が150 mg/kg群の雄で1例に認められた.
哺育4日の剖検では,胸腺頸部残留が雌雄の150および雄の500 mg/kg群でそれぞれ1例,肝臓の白色斑点が雄の500および雌の50 mg/kg群で各1例,腎臓の腎盂拡張が雄の50,150および500 mg/kg群でそれぞれ4,3および1例,雌の対照群,50,150および500 mg/kg群でそれぞれ4,4,2および1例,尿管拡張が雄の50,150および500 mg/kg群でそれぞれ4,3および1例,雌の対照群,50,150および500 mg/kg群でそれぞれ1,3,5および4例,尾の痂皮が雌雄の150 mg/kg群でそれぞれ3例,尾の壊疽が対照群の雌で1例,無尾,鎖肛および肝臓の白色化が500 mg/kg群の雌で1例および皮膚の痂皮が500 mg/kg群の雄で1例に観察された.
体重および摂餌量では,雌雄とも被験物質投与の影響は認められなかった.
臨床検査では血液学検査において,雄の500 mg/kg群で網赤血球率の高値が認められたが僅かな変化であり,他の赤血球項目に変化が認められなかったため,毒性学的には意義のない変化であったと考えた.雌では被験物質投与の影響は認められなかった.
血液凝固能検査では,雄の500 mg/kg群で活性化部分トロンボプラスチン時間の短縮が認められたが,同項目の短縮は毒性学的に意味のない変化と考えた.雌では被験物質投与の影響は認められなかった.
血液生化学検査において,雄の150および500 mg/kg群,雌の全ての被験物質投与群で認められた総胆汁酸の高値,雄の500 mg/kg群で認められた中性脂肪の低値については被験物質投与の影響と考えられたが,機序については不明であった.その他,雄の150および500 mg/kg群でA/G比の高値が認められたが僅かな変化であり,総蛋白およびアルブミン量には変化が認められなかったことから毒性学的には意義のない変化と判断した.また,雌の500 mg/kg群でALTの低値が認められたが,この項目の低値は毒性学的に意味のない変化と考えた.
雄の尿検査では,用量に関連して黄褐色尿例が減少したが,異常を示唆する尿色ではないことから被験物質投与の影響とは考えなかった.
病理学検査では,妊娠を成立させた雄および自然分娩した雌において,剖検および組織所見とも被験物質の影響と考えられる所見は観察されなかった.認められた所見はいずれも対照群と500 mg/kg群で同程度の発生数であるか,少数または単発性の発生であることから自然発生性と考えた.対照群および500 mg/kg群の精巣について実施した精子形成サイクルにおける精細管の精上皮細胞数を測定したところ,被験物質投与の影響は認められなかった.また,腎臓の相対重量の増加が雄の500 mg/kg群において認められ,組織所見で対応する変化は認められなかったが,被験物質投与の影響が疑われた.なお,事故により死亡した50 mg/kg群の雄動物の剖検時に観察された肝臓の瘢痕と脳の赤色斑点は,組織学的には肝臓の出血,脳および脊髄の出血に相当した.
以上のことから,シクロヘキセンの反復投与による一般毒性学的影響として,雌雄の150 mg/kg以上の投与群で流涎および流涙が観察された.また,血液生化学検査で雄の150 mg/kg以上,雌の50 mg/kg以上の投与群で総胆汁酸が高値,雄の500 mg/kg群で中性脂肪が低値を示した.したがって,本試験条件下におけるシクロヘキセンの反復投与による無影響量は雄では50 mg/kg/dayと判断された.しかし,雌では確認できなかった.
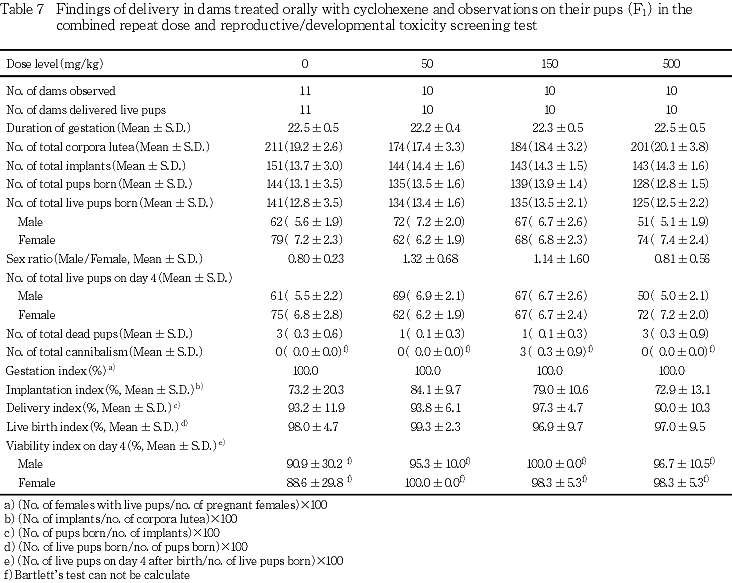
分娩時観察では交尾動物のうち(対照群を含め)83.3〜91.7 %が正常に分娩し,妊娠期間にも被験物質投与の影響は認められなかった.妊娠不成立の動物において,雄では肉眼所見において精巣および精巣上体の萎縮が観察された.そのうち対照群,50および500 mg/kg群の数例では組織学的に精巣の精細管萎縮と間細胞増生および精巣上体の精子減少が観察され,これらの動物では妊娠不成立の原因に精巣の精細管萎縮が関与していると考えられた.その他の雄と雌においては,妊娠不成立の原因は剖検および組織所見から明らかにできなかった.しかし,不妊動物は対照群でも認めれられており,被験物質投与とは関連のない現象と考えた.
また,対照群で哺育期間中に全児死亡が1例に認められたが,剖検および組織所見から,その原因は不明であった.
その他,妊娠黄体数,着床痕数,出産児数,出産生児数,性比,哺育4日生児数,出産率,着床率,出生率,生後4日生存率,雌雄新生児の哺育0および4日の平均体重に被験物質投与の影響は認められなかった.
新生児の外表検査では,500 mg/kg群で鎖肛および無尾を伴った児が観察されたが,1例のみの発現であることから被験物質投与の影響とは考えなかった.
死亡児および哺育4日の剖検では,被験物質投与によると考えられる異常所見は観察されなかった.
以上のことから,シクロヘキセンの生殖能および次世代児に対する影響はいずれも500 mg/kg/day投与によっても認められず,無影響量はともに500 mg/kg/dayと判断された.
| 1) | 高橋道人,"精巣毒性評価のための精細管アトラス,"ソフトサイエンス社,東京,1994, pp.15-20. |
| 2) | K, Kobayashi,産業衛生学雑誌,42, 125(2000). |
| 3) | M, Yoshida, J. Japanese Soc. Comp. Stat., 1, 111(1988). |
| 4) | R. G. D. Steel, Biometrics, 15, 560(1959). |
| 連絡先 | |||
| 試験責任者: | 伊藤圭一 | ||
| 試験担当者: | 森山知通,伊賀達也,木原 亨 | ||
| (財)食品農医薬品安全性評価センター | |||
| 〒437-1213 静岡県磐田郡福田町塩新田字荒浜582-2 | |||
| Tel 0538-58-1266 | Fax 0538-58-1393 | ||
| Correspondence | ||||
| Authors: | Keiichi Ito(Study director) Tomomichi Moriyama, Tatsuya Iga, Tohru Kihara | |||
| Biosafety Research Center, Foods, Drugs and Pesticides(An-pyo Center) | ||||
| 582-2 Shioshinden Arahama, Fukude-cho, Iwata-gun, Shizuoka, 437-1213, Japan | ||||
| Tel +81-538-58-1266 | Fax +81-538-58-1393 | |||