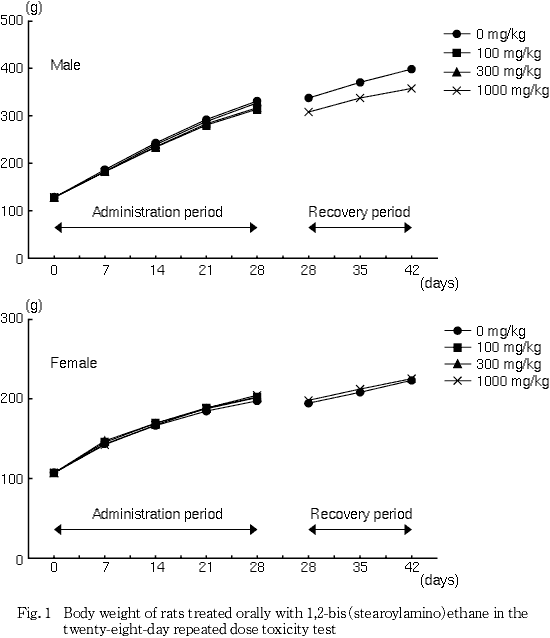
雌雄いずれの投与群にも被験物質に起因すると考えられる異常動物は認められず死亡例もみられなかった.体重および摂餌量測定の結果,雌雄いずれの投与群とも被験物質に起因すると考えられる変化は認められなかった
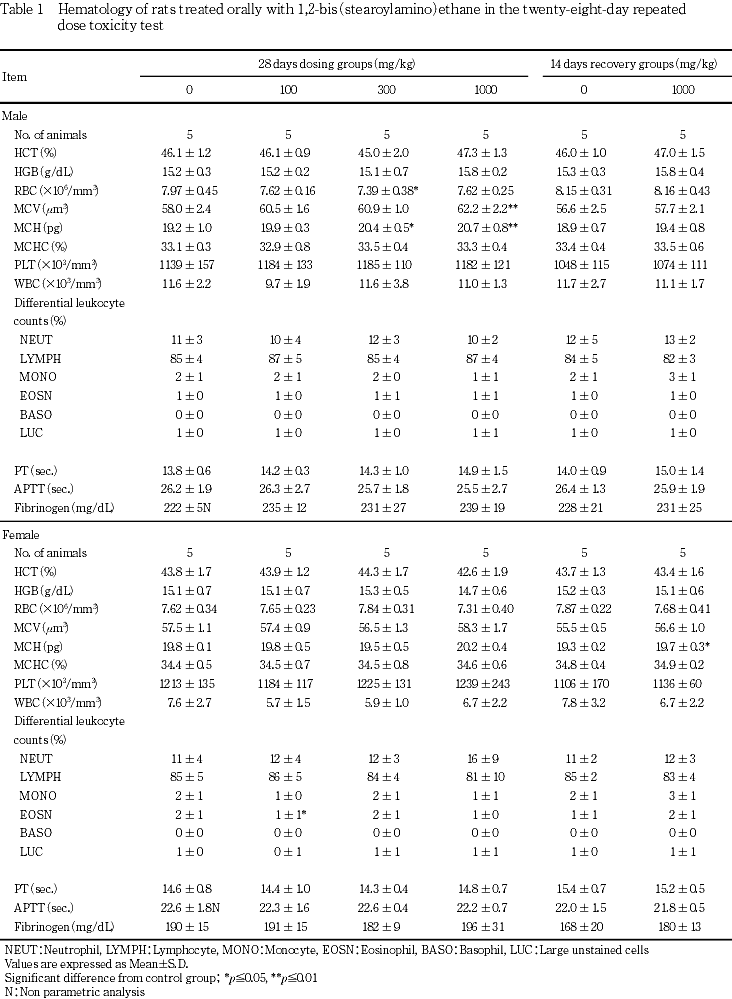
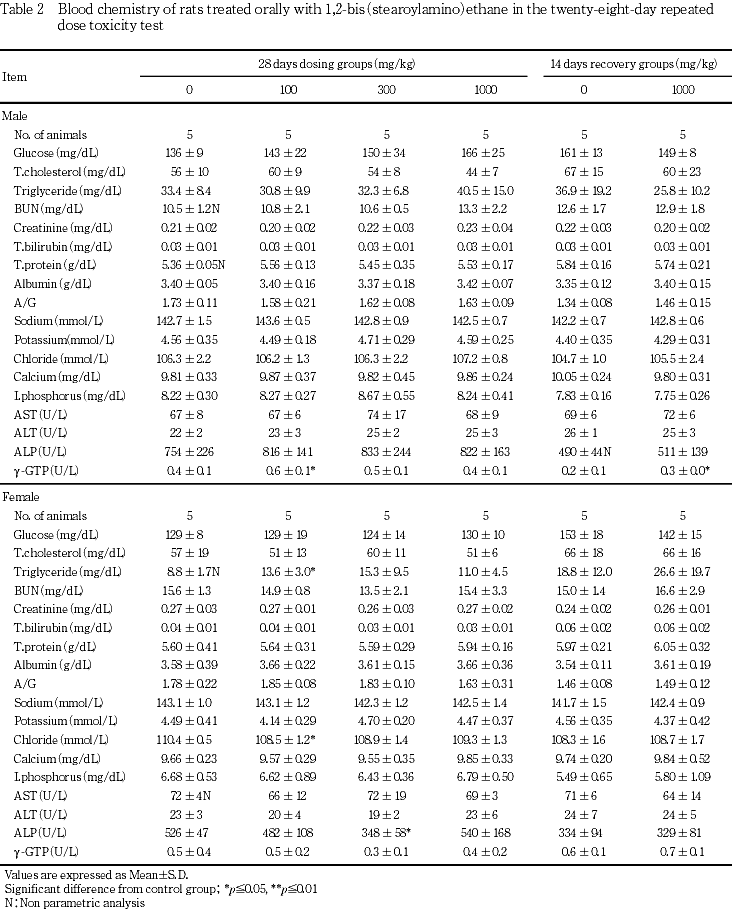
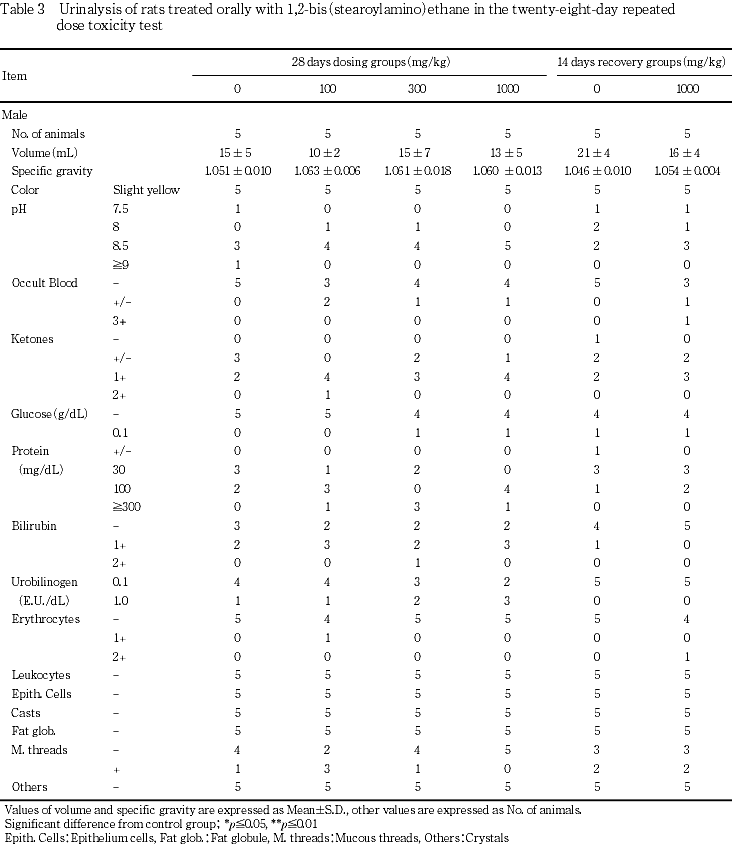
血液学検査,血液凝固能検査,血液生化学検査,尿検査およびの器官重量測定の結果,雌雄いずれの投与群とも被験物質に起因すると考えられる変化は認められなかった.
病理学検査の結果,肉眼所見および組織学所見ともに被験物質の影響を示唆する所見は認められなかった.
以上の結果から,本試験条件下における1,2-ビス(ステアロイルアミノ)エタンの無影響量は,雌雄とも被験物質に起因する変化が認められなかった1000 mg/kg/dayと考えられた.
[用量設定理由]
用量設定のための2週間反復投与試験を0,100,300および1000 mg/kgの4用量で実施した結果,雌雄とも全ての投与群で被験物質に起因すると考えられる変化は認められなかった.従って,28日間反復投与毒性試験の最高用量を1000 mg/kgとし,以下公比約3で除し,中用量を300 mg/kg,低用量を100 mg/kgと設定した.
器官重量は脳,肝臓,腎臓,副腎,胸腺,脾臓,精巣,精巣上体および卵巣について重量を測定した.投与28日または回復14日の測定体重および器官重量から器官重量/体重比(相対重量)を算出した.また,脳(大脳,小脳,橋を含む),脊髄,下垂体,眼球,唾液腺(顎下腺,舌下腺),甲状腺,上皮小体,心臓,胸腺,肺(気管支を含む),気管,肝臓,腎臓,脾臓,副腎,胃,小腸(パイエル氏板を含む),大腸,精巣,精巣上体,精嚢,前立腺,卵巣,子宮,腟,膀胱,末梢神経(坐骨神経),リンパ節(下顎リンパ節,腸間膜リンパ節),骨髄(大腿骨),大動脈および皮膚を十分な量の10 %中性緩衝ホルマリン液で固定した.但し,精巣および精巣上体はブアン液で前固定した後,10 %中性緩衝ホルマリン液で固定した.
病理組織学検査は固定した器官・組織のうち,投与期間終了時に解剖した対照群および高用量群の胸腺,心臓,肝臓,脾臓,腎臓,副腎,精巣,精巣上体,子宮,卵巣,骨髄(大腿骨)について実施した.また,肝臓および腎臓については低用量および中用量群も組織学検査を実施した.皮下部の腫瘤についても組織学検査を行った.なお,回復期間終了時の病理組織学検査は,投与期間終了時の解剖動物において対照群と被験物質投与群間に有意に増減を示した所見が認められなかったことから,実施しなかった.組織標本は,常法に従ってパラフィン包埋,薄切後,ヘマトキシリン・エオジン染色を施した.鏡検では,病変の種類および程度を含む各所見について記録した.

雄では,対照群に比較して300および1000 mg/kg群でMCHが高値を示した.また,1000 mg/kg群ではMCVが高値を示した.いずれも生理的変動の範囲(対照群の平均値± 2SD)内での変化であった.その他,300 mg/kg群で赤血球数が僅かに低値を示したが,用量に関連しない変化であった.
雌では,対照群に比較して100 mg/kg群で好酸球比率が僅かに低値を示したが,用量に関連しない変化であった.
[回復期間終了時の検査結果]
雌では,対照群と比較して1000 mg/kg群でMCHが僅かな高値を示したが,投与終了時の結果においてはみられなかった変化であった.
雌雄とも,対照群と比較して各投与群で差がみられなかった.
[回復期間終了時の検査結果]
雌雄とも対照群と1000 mg/kg群で差が認められなかった.
雄では,対照群に比較して100 mg/kg群でγ-GTPが僅かに高値を示した.
雌では,対照群に比較して100 mg/kg群で中性脂肪が高値および塩素が僅かに低値を示した.また,300 mg/kg群ではアルカリホスファターゼが低値を示した.しかし,雌雄いずれの変化も用量に関連しない変化であった.
[回復期間終了時の検査結果]
雄では,対照群に比較して1000 mg/kg群でγ-GTPが僅かに高値を示したが,軽微で毒性学的に意義のある変化ではなかった.
雌雄とも,対照群に比較して各投与群で差が認められなかった.
[回復期間終了時の検査結果]
雌雄とも,対照群に比較して1000 mg/kg群で差が認められなかった.
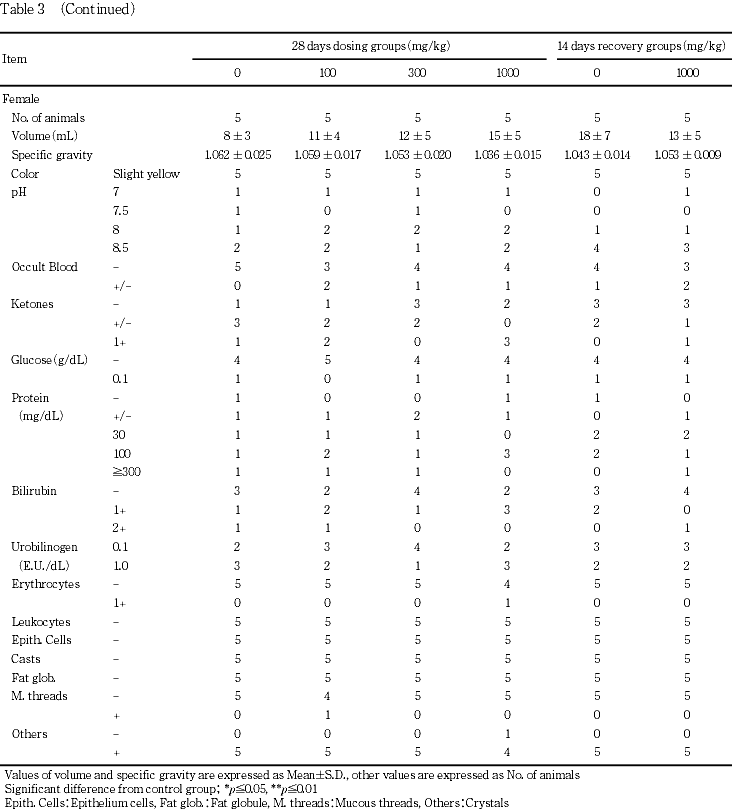
雌雄とも,対照群に比較して各投与群の全ての器官において差が認められなかった.
[回復期間終了時の検査結果]
雄では,対照群に比較して1000 mg/kg群で胸腺実重量が低値を示したが,投与終了時の結果ではみられなかった変化であった.
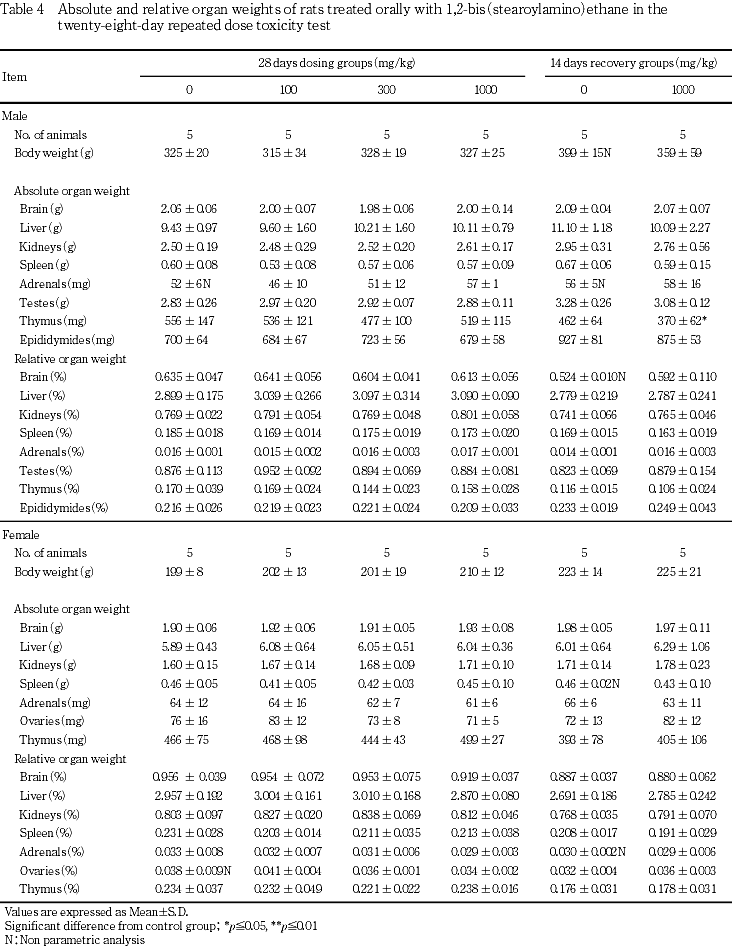
雌雄とも,対照群に比較して各投与群の全ての器官において差が認められなかった.
[回復期間終了時の検査結果]
雌雄とも,対照群に比較して1000 mg/kg群の全ての器官において差が認められなかった.
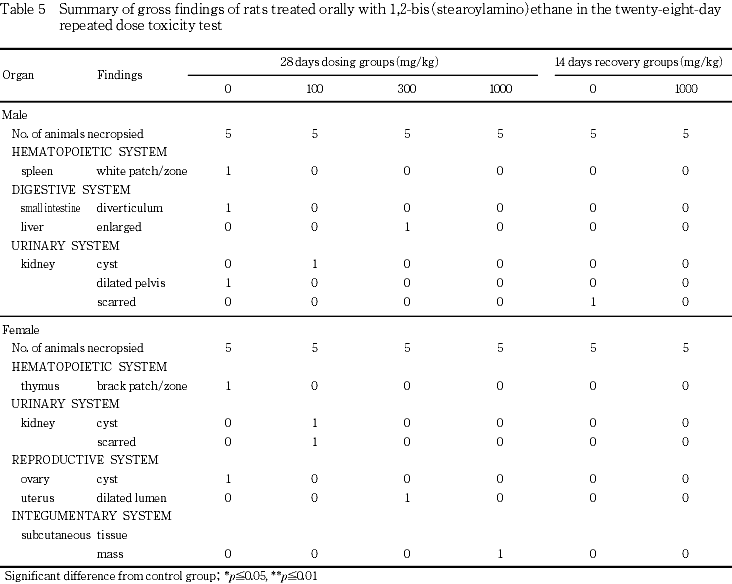
剖検所見では,脾臓の白色斑/区域が雄の対照群で,胸腺の黒色斑/区域が雌の対照群で,小腸の憩室が雄の対照群で,肝臓の肥大が雄の300 mg/kg群で,腎臓の嚢胞が雌雄の100 mg/kg群で,腎臓の腎盂拡張が雄の対照群で,瘢痕が雌の100 mg/kg群で,卵巣の嚢胞が対照群で,子宮の内腔拡張が300 mg/kg群で,皮下部の腫瘤が雌の1000 mg/kg群で,それぞれ単発的に観察された.
[回復期間終了時の検査結果]
剖検所見では,腎臓の瘢痕が雄の対照群に単発的に観察された.
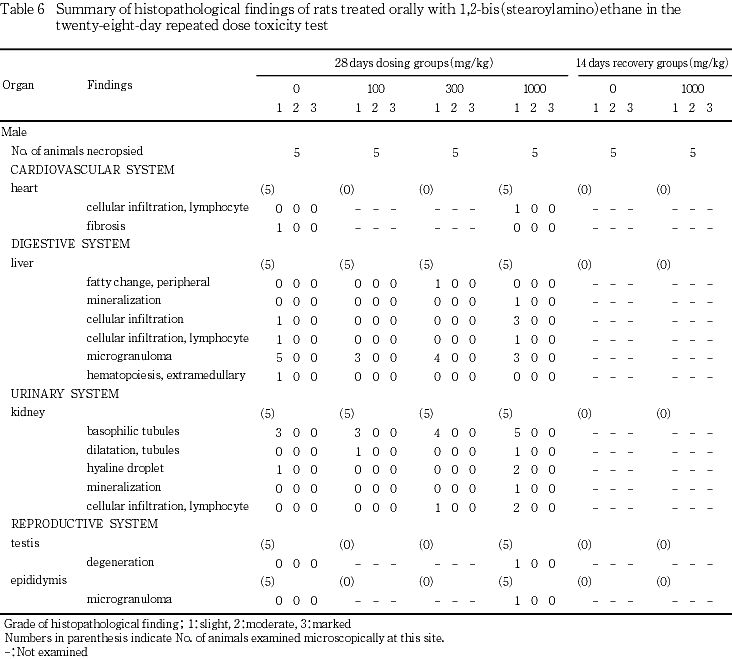
心臓のリンパ球浸潤が雄の1000 mg/kg群に1例,線維化が雄の対照群に1例,胸腺のケルスタイナー氏嚢胞が雌の対照群および1000 mg/kg群にそれぞれ1例認められた.肝臓では周辺性脂肪化が雄の300 mg/kg群で1例,雌の対照群,100および1000 mg/kg群にそれぞれ1例,鉱質沈着が雄の1000 mg/kg群に1例,壊死が雌の300 mg/kg群で1例,細胞浸潤が雄の対照群および1000 mg/kg群に1および3例,リンパ球浸潤が雄の対照群および1000 mg/kg群にそれぞれ1例,雌の対照群および1000 mg/kg群に2および1例,小肉芽腫が雄の対照群,100,300および1000 mg/kg群に5,3,4および3例,雌の対照群,100,300および1000 mg/kg群に5,4,2および5例,髄外造血が雄の対照群に1例それぞれ認められた.腎臓では尿細管好塩基化が雄の対照群100,300および1000 mg/kg群に3,3,4および5例,雌の対照群および1000 mg/kg群に1および3例,嚢胞が雌の100 mg/kg群に1例,管腔拡張が雄の100および1000 mg/kg群でそれぞれ1例,雌の100,300および1000 mg/kg群で1,2および1例,硝子滴変性が雄の対照群および1000 mg/kg群に1および2例,雌の1000 mg/kg群に1例,鉱質沈着が雄の1000 mg/kg群に1例,雌の対照群に2例,リンパ球浸潤が雄の300および1000 mg/kg群で1および2例,雌の対照群,300および1000 mg/kg群にそれぞれ1例が認められた.精巣の変性と精巣上体の小肉芽腫が1000 mg/kg群でそれぞれ1例,子宮の内腔拡張が雌の対照群で1例に認められた.
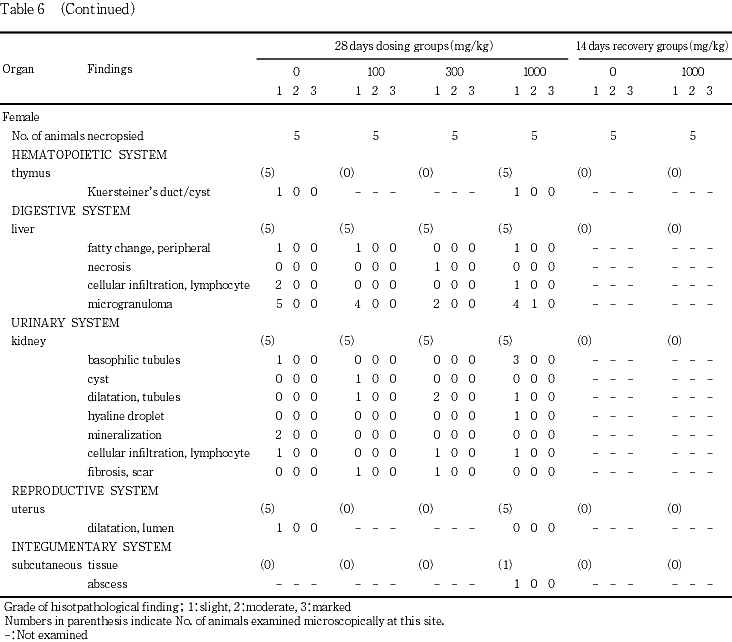
一般状態の観察では,雌の1000 mg/kg群の1例に外傷と皮下部の腫瘤が認められた.外傷は自傷であり,同部位に観察された皮下部の腫瘤は外傷に起因する膿瘍であり,被験物質に起因する変化とは考えられなかった.
体重および摂餌量おいては,雌雄とも対照群と被験物質投与群とに差が認められなかった.
血液学検査および血液凝固能検査の結果,雌雄とも被験物質の影響は認められなかった.
血液生化学検査の結果,雌雄とも被験物質の影響は認められなかった.
尿検査の結果,雌雄とも被験物質の影響は認められなかった.
器官重量測定の結果,雌雄の各投与群とも対照群と比較して測定した全ての器官において差が認められず,被験物質の影響はみられなかった.
病理学検査の結果,剖検所見には被験物質の影響と考えられる変化は認められなかった.組織学検査において腎臓で観察された所見は対照群と比較して有意差がなかったことから自然発生性のものと考えられた.また,肝臓の細胞浸潤は低用量および中用量群では観察されず,高用量群での発生も対照群と比較して有意差が認められないことから自然発生性の変化と考えられた.
以上の結果から,本試験における1,2-ビス(ステアロイルアミノ)エタンの無影響量は雌雄とも被験物質に起因する変化が認められなかった1000 mg/kg/dayと判断された.
| 1) | 佐野正樹,岡山佳弘,医薬安全性研究会会報,32, 21(1990). |
| 2) | M. Yoshida, J. Japanese Soc. Comp. Stat. 1, 111(1988). |
| 3) | 倍味繁,稲葉太一,医薬安全性研究会会報,40, 33(1994). |
| 連絡先 | |||
| 試験責任者: | 渡 修明 | ||
| 試験担当者: | 各務 進,伊賀達也,向井大輔, 宮島留美子,大橋信之 | ||
| (財)食品農医薬品安全性評価センター | |||
| 〒437-1213 静岡県磐田郡福田町塩新田字荒浜582-2 | |||
| Tel 0538-58-1266 | Fax 0538-58-1393 | ||
| Correspondence | ||||
| Authors: | Nobuaki Watari(Study director) Susumu Kakamu, Tatsuya Iga, Daisuke Mukai, Rumiko Miyajima, Nobuyuki Oohashi | |||
| Biosafety Research Center, Foods, Drugs and Pesticides(An-pyo Center) | ||||
| 582-2 Arahama, Shioshinden, Fukude-cho, Iwata-gun, Shizuoka, 437-1213, Japan | ||||
| Tel +81-538-58-1266 | Fax +81-538-58-1393 | |||