
以上により,当試験条件下における一般毒性学的な無影響量は雌雄とも2.4mg/kg未満と推察された.また,12mg/kg以上の群で授乳期(哺育行動)の母動物に対する影響が,さらに300mg/kg群では周産期(分娩)の母動物に対する影響および新生児の発育に対する影響がうかがわれた.したがって,生殖発生毒性学的な無影響量は雄の生殖に関しては300mg/kg,雌の生殖に関しては2.4mg/kg,児動物の発生に関しては60mg/kgと推察された.
投与検体液は,被験物質をコーンオイルに用時溶解し,調製後は速やかに投与に用いた.投与開始前および投与終了前の2回,各投与検体液中の被験物質濃度を測定した.その結果,いずれの投与検体液も適正範囲内の値を示した.コーンオイル中の2mg/mlおよび60mg/ml濃度の被験物質は,室温・遮光・気密条件下で調製後3時間まで,0.48mg/ml濃度では調製後1時間までの安定性が確認された.そこで,投与検体液の使用はそれぞれの安定性が確認された時間以内とした.
動物は,室温20〜24℃,湿度40〜70%,明暗各12時間,換気回数12回/時に設定した飼育室で飼育した.検疫・馴化期間中はステンレス製懸垂式ケージを用いて1ケージあたり4匹までの群飼育とし,群分け後はステンレス製五連ケージを用いて個別飼育した.ただし,交配はステンレス製懸垂式ケージ内で行った.また,母動物は妊娠18日に床敷[サンフレーク,日本チャールス・リバー(株)]を入れたプラスチック製ケージに個別に移し,自然分娩および哺育させた,床敷の分析成績は,当試験施設で定めた基準値の範囲内であった.
飼料は,固型飼料[CRF-1,オリエンタル酵母工業(株)]を給餌器に入れ,自由に摂取させた.飲料水は,水道水を給水瓶を用いて自由に摂取させた.飼料および飲料水の検査の結果,いずれも試験成績は当試験施設で定めた基準値の範囲内であった.
群構成は,以下の如くとした.一群の動物数は,雌雄各12例とした.
投与量設定の理由:投与量設定のための雄ラットを用いた2週間経口投与による予備試験(投与段階:0,10,30,100,300および1000mg/kg,一群5例)の結果を参考にして決定した.すなわち,1000mg/kg群では全例が投与5日までに死亡した.一方,300 mg/kg群では投与3日以降に1〜5例で流涎がみられ,体重は増加抑制傾向であり剖検日には有意差が認められた.また,100mg/kg群でも投与7日以降には1〜4例で流涎がみられた.したがって,当試験では2週間投与試験で一般状態観察および体重に影響がみられた300mg/kgを最高用量とし,以下公比5で60,12および2.4mg/kg群を設定した.対照として,被験物質と同一容量の媒体(コーンオイル)を投与する群を設けた.
投与期間は,雄では交配前14日間とその後35日間の合計49日間とし,雌では交配前14日間,交配期間中(最長7日間),妊娠期間および哺育4日の剖検前日(41〜46日間)までとした.投与は1日1回で連日とした.

(2)体重:1週間に2回および剖検日に測定した.
(3)摂餌量:交配開始前14日間および交配期間終了後に,連続2日間量を測定して1日量に換算し,1週間に2回測定した.
(4)剖検:投与期間(49日間)終了の翌日に,エーテル麻酔下で腹大動脈の切断により放血致死させた後に,器官・組織の肉眼的観察を行った.精巣および精巣上体を摘出後に重量を測定し,ブアン液に固定し,保存した.
(5)病理組織学的検査:精巣および精巣上体は,全例について常法に従ってパラフィン包埋標本を作製した.対照群および300mg/kg群についてはH-E染色組織標本を作製し,病理組織学的検査を行った.
(2)性周期:投与開始日から交尾確認日まで毎日1回観察した.なお,発情期が連続2日間にわたって観察される場合は1回と数えた.
(3)体重:交配開始前14日間および交配期間中は毎週2回,妊娠期間中は妊娠0,7,14および21日に,哺育期間は哺育0および4日にそれぞれ測定した.
(4)摂餌量:交配開始前14日間までは毎週2回,連続2日間量を測定して1日量に換算し,1週間に2回測定した.また,妊娠期間中は妊娠0,7,14および19日からの連続2日間量を,哺育期間中は哺育0〜4日の累積量を測定し,それぞれ1日量に換算した.
(5)分娩状態の態察:自然分娩させ,分娩状態の異常の有無,分娩終了の確認を妊娠 21日から妊娠25日の午前9時まで毎日行った.午前9時までに分娩が終了していた場合,その日を哺育0日とした.
(6)交尾確認後25日の午前9時までに分娩しない動物:エーテル麻酔下で腹大動脈から放血致死させた後に剖検し,妊娠の成否を確認した.交尾が確認されたものの,着床痕がみられなかった雌(No.352)は不妊動物とした.当例では,子宮および卵巣を摘出して10%中性緩衝ホルマリン液に固定し,保存した.
(7)哺育状態の観察および剖検:哺育4 日まで毎日観察し,哺育4日にエーテル麻酔下で腹大動脈から放血致死させた後に剖検し,着床痕数および黄体数を数えた.子宮,卵巣および剖検で異常の認められた器官・組織を摘出して10%中性緩衝ホルマリン液に固定し,保存した.
(8)全新生児が死亡した母動物の処置:全新生児が死亡した母動物(No.251,356)は,発見後速やかにエーテル麻酔下で腹大動脈から放血致死させた後に剖検し,着床痕数および黄体数を数えた.その後,子宮および卵巣を摘出して10%中性緩衝ホルマリン液に固定し,保存した.
(9)病理組織学的検査:全例の卵巣について,常法に従ってパラフィン包埋標本を作製した.対照群および300mg/kg群の卵巣はH-E染色組織標本を作製し,病理組織学的検査を行った.また,剖検で異常が認められた器官・組織(300mg/kg群の胃および小腸)についても同様に病理組織学的検査を行った.さらに,一部の例の胃については鉄染色(Ber-lin blue stain)組織標本を作製し,観察した.
なお,交尾確認は毎朝ほぼ一定時刻に行い,腟垢内に精子または腟栓を確認した雌を交尾成立動物として,その日を妊娠0日として起算した.
(2)新生児について,一般状態および死亡の有無を,生存期間中毎日1回観察した.
(3)体重:哺育0(出生日)および4日に測定した.
(4)剖検:哺育4日にエーテル麻酔下で腹大動脈から放血致死させた後,剖検した.
検定では,Bartlett法による等分散性の検定を行い,等分散の場合には一元配置法による分散分析を行い,有意ならば対照群との群間比較はDunnett法(例数が等しい場合)またはScheff 法(例数が等しくない場合)により行った.一方,等分散と認められなかった場合は,順位を利用した一元配置法による分析(Kruskal-Wallisの検定)を行い,有意ならば対照群との群間比較は順位を利用したDunnett法(例数が等しい場合)またはScheff
法(例数が等しくない場合)により行った.一方,等分散と認められなかった場合は,順位を利用した一元配置法による分析(Kruskal-Wallisの検定)を行い,有意ならば対照群との群間比較は順位を利用したDunnett法(例数が等しい場合)またはScheff 法(例数が等しくない場合)を用いて行った.
法(例数が等しくない場合)を用いて行った.
対照群では,観察期間を通じて異常症状は観察されなかった.
2.4,12および60mg/kg群では,投与7〜10日から最終投与日まで少数例あるいは約半数例で流涎がみられる日があった.300mg/kg群では,投与6日から最終投与日まで少数例〜全例で流涎がみられた.当症状は,投与後約2〜5分からみられ,投与後約30〜60分まで継続した.高用量群では低用量群に比して発現日が早く,投与後の症状発現までの時間が短く,症状持続時間が長く,また発現例数が多い傾向がうかがえた.なお,翌日の投与前には異常はみられなかった.
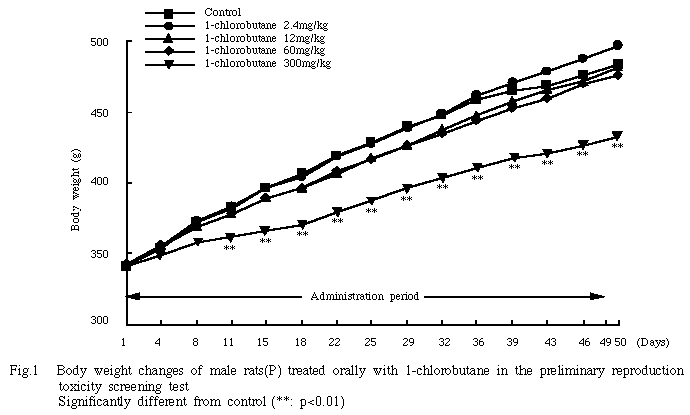
2)体重(Fig.1)
300mg/kg群では投与2週目頃から対照群に比して体重増加抑制がみられ,投与11日から剖検日まで有意差が認められた.一方,60mg/kg以下の投与群は対照群とほぼ同様の推移を示し,有意差は認められなかった.
3)摂餌量
300mg/kg群の摂餌量は対照群に比して低値傾向であり,投与6日には有意差が認められた.60mg/kg以下の投与群は対照群とほぼ同程度かやや低値傾向であったが,いずれの測定日とも有意差は認められなかった.
4)剖検所見
対照群および各投与群のいずれの例とも,著変はみられなかった.
5)器官重量(Table1)
300mg/kg群では,対照群に比して精巣相対重量が有意な高値を示した.精巣上体は,各投与群とも絶対重量および相対重量ともに対照群との間に有意差は認められなかった.

6)病理組織学的検査
精巣:巨細胞を伴う精細管の中等度の変性が,300mg/kg群の1例にみられた.その他には,著変はみられなかった.
精巣上体:ごく軽度の被膜における動脈炎が対照群の1例に,ごく軽度の間質の細胞浸潤および中等度の精子減少が300mg/kg群の各1例にみられた.その他には,著変はみられなかった.
交配開始前および交配期間中:対照群では,交配開始前および交配期間中を通じて異常症状は観察されなかった.2.4mg/kg群では投与10日に,12mg/kg群では投与15日に各1例で1回のみ,流涎がみられた.また,60mg/kg群では投与7日から少数例に交配終了日まで,300mg/kg群では投与7日から少数例〜約半数例に交配終了前日まで流涎がみられた.
妊娠期間中:対照群および2.4mg/kg群では,妊娠期間中に異常症状は観察されなかった.12および60mg/kg群では妊娠0〜4日から分娩前日まで,少数例で流涎がみられる日があった.300mg/kg群では,妊娠0日から分娩日まで,少数例〜過半数例で流涎がみられた.300mg/kg群の1例(No.455)は妊娠22日に死亡したが,前日までは他の例と同様の流涎がみられたのみで,その他には異常症状は観察されなかった.
哺育期間中:対照群,2.4,12および60mg/kg群では,哺育期間を通じて異常症状は観察されなかった.300mg/kg群では,哺育0〜3日に少数例〜約半数例で流涎がみられた.なお,300mg/kg群では哺育4日の朝に1例(No.456)が死亡していたが,前日まで流涎がみられた以外には異常症状は観察されなかった.さらに,哺育4日の観察後から剖検前までの間に同群の他の1例(No.458)が死亡したが,哺育2,3日に流涎がみられた以外には異常症状は観察されなかった.また,生存例の1例(No.459)では,哺育3,4日には立毛および被毛光沢不良が観察された.
流涎は,いずれの場合も投与後約2〜5分からみられ,投与後約30〜60分まで継続した.高用量群では,低用量群に比して投与後の症状発現までの時間が短く,症状持続時間が長く,また発現例数が多い傾向がうかがえた.なお,翌日の投与前には異常はみられなかった.
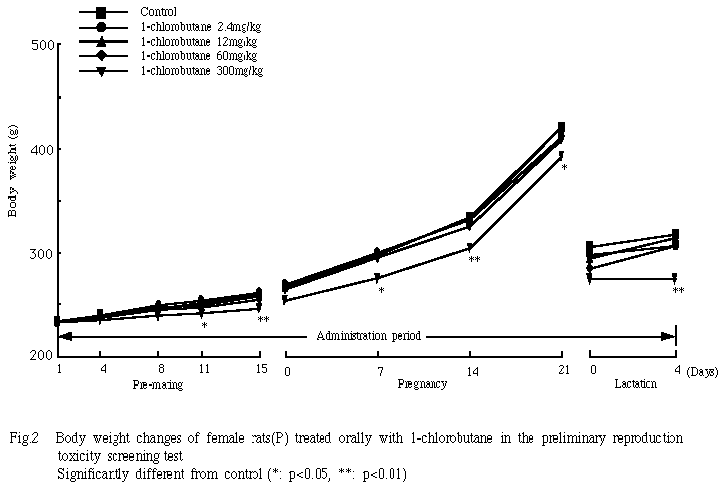
2)体重(Fig.2)
300mg/kg群では投与2週目頃から対照群に比して体重増加抑制傾向がみられ,交配開始前の投与11および15日,妊娠期間の妊娠7,14および21日ならびに哺育4日には有意差が認められた.同群では,哺育4日には哺育0日に比して10例中4例で10g以上の体重減少がみられ,とくに1例(No.459)は47gの減少を示した.一方,60mg/kg以下の投与群は交配開始前,妊娠期間中および哺育期間とも対照群とほぼ同様の推移を示し,有意差は認められなかった.
3)摂餌量
300mg/kg群の摂餌量は,交配開始前,妊娠期間中および哺育期間とも対照群に比してやや低値傾向であり,妊娠2日には有意差が認められた.なお,生存例の1例(No.459)では哺育期間中の摂餌量が他の例に比して低値であった.一方,60mg/kg以下の投与群では対照群とほぼ同程度かやや低値を示す日もみられたが,有意差は認められなかった.
4)剖検所見
生存例:対照群および2.4mg/kg群の各12例,12mg/kg群の11例ならびに60mg/kg群の10例では,剖検で著変はみられなかった.一方,300mg/kg群(9例)では腺胃粘膜の暗赤色斑が1例(No.454)に,白色化が2例(No.457,461)に,水腫・黒色斑および小腸の黒色化が1例(No.459)にみられた.
哺育2日までに全新生児が死亡した母動物(12mg/kg群:No.251,60mg/kg群:No.356)では,著変はみられなかった.
不妊例:60mg/kg群の1例(No.352)では,著変はみられなかった.
死亡例:300mg/kg群の3例の内で,哺育4日に死亡していた1例(No.456)および妊娠22日に死亡した1例(No.455)では腺胃粘膜に黒色点散在がみられた.哺育4日の剖検前に死亡した1例(No.458)では,著変はみられなかった.
5)病理組織学的検査
(1)生存例
卵巣:対照群および300mg/kg群のいずれの例とも著変はみられなかった.
胃:剖検で腺胃の白色化がみられた300mg/kg群の2例(No.457,461)では腺胃に軽度の粘液分泌増加および上皮の剥離が,暗赤色斑がみられた1例(No.454)ではごく軽度のびらんがみられた.また,水腫および黒色斑がみられた1例(No.459)では腺胃に中等度のびらんならびに粘膜下織に中等度の水腫がみられた.なお,当例では粘膜上に褐色物質の付着がみられたが,鉄染色は陰性であった.
小腸:剖検で黒色化がみられた300mg/kg群の1例(No.459)で,粘膜の高度の菲薄化がみられた.
(2)死亡例
剖検で腺胃粘膜に黒色点散在がみられた300mg/kg群の2例では,いずれも腺胃にびらんがみられた.変化の程度は,哺育4日に死亡していた1例(No.456)が高度であり,妊娠22日に死亡した1例(No.455)ではごく軽度であった.その他に,卵巣および胃に死後変化が観察された.
検疫・馴化期間中の7日間および投与期間の14日間(交配前)の発情回数は,各投与群とも対照群とほぼ同程度であり,有意差は認められなかった.

2)交尾率,受胎雌数および受胎率
対照群を含む各群の動物とも,同居開始後7日までに全例で交尾が確認された.交尾率は,対照群および各投与群とも100%であった.交尾成立までの平均日数は,対照群に比して各投与群ではやや延長傾向がうかがえたが,投与用量に関連した変動はみられず,また各投与群とも有意差は認められなかった.
受胎雌数は,対照群,2.4,12および300mg/kg群では12例中12例ずつ,60mg/kg群では12例中11例であった.したがって,受胎率は対照群,2.4,12および 300mg/kg群が100%,60mg/kgが91.7%であった. 3)妊娠期間,分娩状態および哺育行動
妊娠期間は,各投与群とも対照群とほぼ同程度であった.これらの母動物では,いずれも分娩状態に異常はみられなかった.
哺育期間中の母動物の観察では,対照群および2.4mg/kg群では異常はみられなかった.一方,12mg/kg群の1例(No.251)では哺育0,1,2日に,60mg/kg群の1例(No.356)では哺育1,2日に,300mg/kg群の1例(No.459)では哺育3,4日には乳頭発達不良があり,授乳行動および巣作り行動が観察されないなどの哺育行動不良がみられた.
4)着床痕数
着床痕数は,対照群に比して各投与群ではやや高値傾向がうかがえたが,有意差は認められず,また投与用量に関連した変動もみられなかった.
5)出産率
新生児出産雌数は対照群,2.4および12mg/kg群で12例中12例,60mg/kg群で11例中11例で,出産率はいずれも100%であった.300mg/kg群では1例(No.455)が妊娠22日に死亡したため,新生児出産雌数は12例中11例で出産率は91.7%であった.
総出産児数は,対照群に比して各投与群はほぼ同程度 かあるいはやや高値傾向であった.また,分娩率は各投与群はやや低値傾向であった.死産児数は,各投与群はやや低値傾向がうかがえた.一方,新生児数は各投与群はやや高値傾向であった.出生率は,各投与群はやや高値傾向であった.しかしながら,いずれの項目も対照群との間に有意差は認められず,また投与用量に関連した変動もみられなかった.
2)性比および外表異常の観察
性比は,各投与群とも対照群とほぼ同程度であった.新生児の外表観察では,いずれの例も異常はみられなかった.
3)新生児の一般状態,哺育4日の生存率および剖検所見
新生児の一般状態観察では,対照群および2.4mg/kg群は,いずれも異常はみられなかった.一方,12および60mg/kg群の哺育行動不良が観察された母動物(No.251,356)の新生児では,哺育1日に表皮温下降が観察された.また,300mg/kg群では,1母動物(No.456)の新生児で哺育4日に,他の1母動物(No.459)の新生児で哺育3,4日に表皮温下降が観察された.
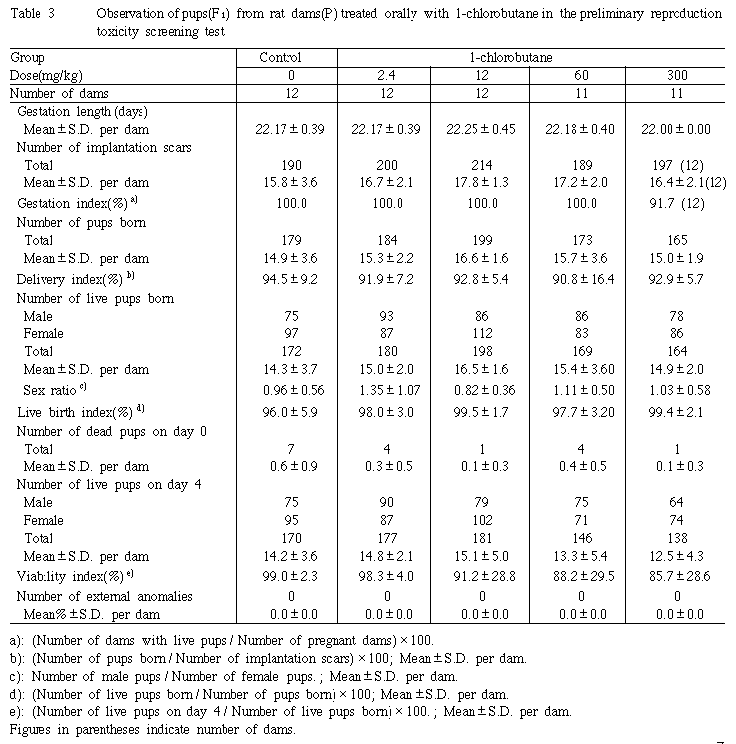
哺育4日の剖検日までに,対照群では2母動物で2例,2.4mg/kg群では2母動物で3例の新生児が死亡した.一方,12mg/kg群では1母動物で1例と,さらに哺育行動不良がみられた1母動物(No.251)で哺育2日までに新生児の全例が,60mg/kg群では4母動物で5例と,さらに哺育行動不良がみられた1母動物(No.356)で新生児の全例が哺育2日までに死亡した.その他に,300mg/kg群では2母動物で3例,哺育4日に死亡していた1母動物(No.456)で哺育4日までに8例,さらに哺育期間中に摂餌量の低値および哺育行動不良がみられ,哺育4日に最大の体重減少を示した1母動物(No.459)では哺育4日に15例の新生児が死亡した.したがって,哺育4日の生存率は,対照群が99.0%に対して2.4mg/kg群は98.3%であり,ほぼ同程度であった.また,12および60mg/kg群ではそれぞれ91.2および88.2%とやや低値傾向であった.一方,300mg/kg群では有意差は認められなかったものの85.7%と低値を示した.なお,60mg/kg以下の投与群では哺育0日の新生児数が対照群に比してやや多かったため,哺育4日の生存児数は対照群よりも多いかあるいはほぼ同程度であった.また,300mg/kg群では哺育0日の新生児数は対照群よりもやや多かったものの,哺育期間中の死亡児が多かったため,哺育4日の生存児数が低値であった.
哺育4日の剖検では,いずれの生存児にも著変はみられなかった.
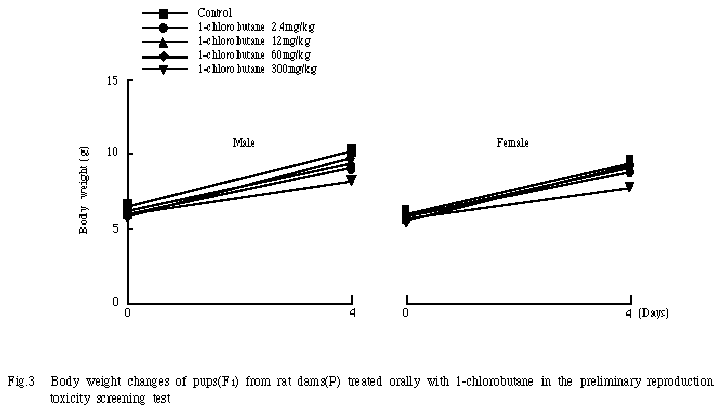
4)新生児の体重(Fig.3)
各投与群の哺育0日の体重は,雌雄とも対照群とほぼ同程度かやや低値傾向であった.哺育4日には,60mg/kg以下の投与群では対照群に比してやや低値傾向が持続してみられた.一方,300mg/kg群では哺育4日の体重は雌雄ともに対照群との間に有意差は認められなかったものの,低値であった.
5)未分娩胎児および死産児
前述の如く,300mg/kg群の母動物1例(No.455)は妊娠22日に死亡し,剖検により死亡胎児19例が確認された.
死産児は対照群で7例,2.4,12,60および300mg/kg群でそれぞれ4例,1例,4例および1例であった.死産児数には,投与用量に関連した変動は認められなかった.
雄(P)に対しては,各投与群で投与後に流涎がみられたが,翌日には消失しており,一過性の症状であった.当症状の発現までの投与日数,発現までの時間,持続時間,発現動物数にはほぼ用量依存性がうかがえた.しかしながら,症状発現動物数は投与開始後2〜3週目頃を頂点とし,その後は投与を継続しても必ずしも増加する傾向はみられなかった.体重は,300mg/kg群で投与期間の初期から増加抑制が認められ,摂餌量の低値傾向に起因した変動と思われた.また,器官重量では精巣相対重量が高値を示したが,体重増加抑制に伴った二次的な変動と考えられた.剖検では著変はみられなかった.また,病理組織学的検査では300mg/kg群で精巣の精細管上皮の変性と精巣上体の精子数減少がみられたが,発現例数が1例のみであり,その他の例には同様の所見が全くみられなかったことから,被験物質投与との関連性のない偶発性変化と思われた.なお,当例では交尾および授胎が可能であり,精巣の組織変化は交尾あるいは授胎などの生殖機能への影響がみられない程度のものであることが知られた.
雌(P)に対しては,交配開始前および交配期間中の症状は,雄の同量投与群の場合と同様で各投与群で投与後に流涎がみられたが,発現例数は雄に比して少なかった.また,妊娠期間中では2.4mg/kg群で,さらに哺育期間中では60mg/kg以下の投与群で流涎はみられず,これらの期間中でも流涎の発現例数は雄の同時期に比して少なかった.体重は,300mg/kg群で投与2週目,妊娠期間および哺育期間には低値であり,摂餌量の低値傾向に起因した変動と考えられた.剖検では300mg/kg群で胃および小腸に黒色斑,黒色化あるいは暗赤色斑などがみられ,病理組織学的検査により胃粘膜のびらん,上皮の剥離,水腫,小腸の粘膜菲薄化などが観察された.したがって,哺育期間中の摂餌量の低値傾向,体重増加抑制あるいは減少は,これらの消化管障害が一因と推測された.なお,胃の鉄染色は陰性であった.
以上のように,一般毒性学的には2.4mg/kg以上の群で雌雄の一般状態(流涎),300mg/kg群で雌雄の体重,摂餌量に影響がみられ,雌の剖検および病理組織学的検査(胃,小腸)に異常所見が得られた.したがって,当試験条件下における1-クロロブタンの一般毒性学的な無影響量は雌雄とも2.4mg/kg未満と推察された.
親動物(P)の生殖発生に関しては,交尾率,発情回数,受胎雌数,受胎率,新生児出産雌数,妊娠期間,着床痕数および出産率は,各投与群で被験物質投与の影響はみられなかった.しかしながら,妊娠22日には300mg/kg群の1母動物が死亡した.当動物では,上記のように消化管障害に加えて妊娠による負荷が死亡原因と推測された.剖検では死亡胎児が19例認められたが,早期あるいは後期吸収胚はみられなかったことから,1-クロロブタンが周産期(分娩)の母動物に対して影響を及ぼした結果と考えられた.さらに,12,60および300mg/kg群の各1例で哺育行動不良が観察され,新生児の多くが哺育4日までに死亡した.したがって,12mg/kg以上では授乳期(哺育行動)の母動物に対して影響を及ぼした可能性が推察された.
新生児に対しては,総出産児数,分娩率,死産児数,新生児数,出生率,性比に被験物質投与の影響はみられなかった.また,哺育4日の剖検では異常はみられなかった.一方,新生児の一般状態では12および60mg/kg群の各1母動物ならびに300mg/kg群の2母動物の新生児で表皮温下降が観察され,300mg/kg群の当該例の体重は同群の他の新生児に比して低値であった.この内の1母動物(No.456)は哺育4日に死亡しており,また他の1母動物(No.459)は一般状態の異常,哺育行動不良を示した動物であったことから,授乳が充分にできなかったことに起因したものと思われた.この2例を含めて,300mg/kg群では哺育4日までに新生児の死亡例数が多かったため,有意差は認められなかったものの,哺育4日の生存率が低値を示した.また,哺育4日の体重は300mg/kg群で雌雄とも有意差は認められなかったものの低値であり,新生児の発育にも影響を及ぼしている可能性が考えられた.12および60mg/kg群でも,哺育行動不良がみられた母動物で哺育2日までに全新生児が死亡したが,これらの投与群ではその他の母動物には300mg/kg群にみられたような影響は観察されず,哺育4日の生存率がやや低値であったが生存児の体重は対照群と大きな差がみられないことから,新生児に対する影響はないと推察された.
したがって,生殖発生毒性学的には12mg/kg以上の投与群で授乳期(哺育行動)の母動物に対して,300mg/kg群ではさらに周産期(分娩)の母動物に対して影響を及ぼした可能性が考えられた.また,300mg/kg群では新生児の死亡数が多く,哺育4日の生存率が低値であり,哺育4日の雌雄の生存児の体重が低値であった.したがって,当試験条件下における生殖発生毒性学的な無影響量は,雄の生殖に関しては300mg/kg,雌の生殖に関しては2.4mg/kg,児動物の発生に関しては60mg/kgと推察された.
以上により,当試験条件下における一般毒性学的な無影響量は雌雄とも2.4mg/kg未満と推察された.また,生殖発生毒性学的な無影響量は,雄の生殖に関しては300mg/kg,雌の生殖に関しては2.4mg/kg,児動物の発生に関しては60mg/kgと推察された.
| 連絡先 | |||
| 試験責任者: | 和田 浩 | ||
| 試験担当者: | 小林吉一,藤村高志,岡田雅昭, 古橋忠和,山本明義 | ||
| (株)日本バイオリサーチセンター羽島研究所 | |||
| 〒 501-62 岐阜県羽島市福寿町間島 6-104 | |||
| Tel 058-392-6222 | Fax 058-392-1284 | ||
| Correspondence | |||
| Authors: | Hiroshi Wada (Study director ), Yoshikazu Kobayashi, Takashi Fujimura, Masaaki Okada, Tadakazu Furuhashi and Akiyoshi Yamamoto | ||
| Nihon Bioresearch Inc. Hashima Laboratory | |||
| 6-104 Majima, Fukuju-cho, Hashima, Gifu, 501-62, Japan | |||
| Tel +81-58-392-6222 | Fax +81-58-392-1284 | ||