3-メチルフェノールのラットを用いる28日間反復経口投与毒性試験
Twenty-eight-day Repeat Dose Oral Toxicity Test of 3-Methylphenol in Rats
要約
3-メチルフェノールは,合成樹脂,消毒剤,薬品原料として使用されている1).3-メチルフェノールを0(オリブ油),100,300および1000 mg/kgの投与量で,1群当たり雌雄各7あるいは14匹のCrj:CD(SD)IGSラットに28日間反復経口投与してその毒性を検討した.さらに,0および1000 mg/kg群の雌雄各7匹を用いて投与終了の翌日から14日間観察を継続して投与期間終了時にみられた毒性の回復性についても併せて検討した.
100 mg/kg群では,いずれの検査項目にも変化はみられなかった.
300 mg/kg群では,投与期間終了時の雌の肝臓の相対重量が有意な高値であった.その他の検査項目には異常はみられなかった.
1000 mg/kg群では,一般状態の変化として,雌雄とも投与期間を通して投与後に振戦または流涎が観察された.回復期間中には異常は観察されなかった.体重は,雄では投与2日から28日,雌では投与7日から28日に有意な低値を示した.回復期間中は,雌雄とも体重は対照群と比較して低値であったが,体重増加率は対照群を上回り,回復傾向がみられた.摂餌量は,雄では投与2日,雌では投与2日および14日,ならびに回復1日に有意な低値がみられた.投与4週の尿検査では,雌雄の尿pHの低下,尿蛋白陰性例の増加または増加傾向,ならびに雄の尿量および飲水量の高値がみられたが,回復2週の検査では変化はみられなかった.血液生化学検査では,投与期間終了時に雌雄の総コレステロールが高値または高値傾向であった.血液学検査および剖検では,被験物質の投与に起因すると考えられる変化は認められなかった.器官重量は,投与期間終了時に雌雄の肝臓の相対重量,雌の腎臓の相対重量に有意な高値がみられ,回復期間終了時には,雌雄の肝臓の絶対重量または相対重量に有意な低値がみられた.病理組織学検査では,投与期間終了時に雄の1例に肝臓の小葉中心性肝細胞肥大がみられた.
以上のことから,本試験条件下における無影響量(NOEL)は,雄で300 mg/kg/day,雌で100 mg/kg/dayであると結論される.
方法
1. 被験物質および投与液の調製
3-メチルフェノール(純度:99.13 %,Lot No. 981006,本州化学工業(株),和歌山)は,常温において無色ないし淡黄色液体で,融点が11〜12℃,沸点が202.7℃,水に難溶,アセトンおよびアルコールに易溶である.入手後の被験物質は遮光気密容器に入れ,冷所で保存した.残余被験物質を製造業者が分析し,投与期間中の被験物質の安定性を確認した.投与液の調製は,投与量ごとに被験物質を精秤し,所定の濃度となるように溶媒である日本薬局方オリブ油(ヤクハン製薬(株))を加えて溶解することによって行った.調製液は,室温で3時間,冷暗所保存条件下で8日間安定であることが確認されていることから,調製後直ちに遮光気密容器に入れて冷蔵庫内(2〜8 ℃)に保存し,調製後7日以内に使用した.投与に用いる初回および最終調製時の各濃度の調製液について被験物質の濃度を分析した結果,含有率は設定値の98.4〜102 %であり,調製液は規定の濃度を含有することを確認した.
2. 試験動物および飼育条件
日本チャールス・リバー(株)よりSprague-Dawley系ラット(Crj:CD(SD)IGS)の雌雄を4週齢で購入して雄は7日間,雌は8日間の検疫・馴化を行った後,健康な動物を雌雄各42匹選択して5週齢で試験に供した.投与開始日の体重範囲は雄が135〜152 g,雌が122〜141 gであった.動物は,温度22〜23 ℃,湿度36〜64 %,換気回数10〜15回/時間および照明時間12時間(8:00から20:00まで点灯)に制御されたバリアシステムの飼育室で,ブラケット式金属製金網床ケージに群分け前は5匹以内,群分け後は個別で飼育した.飼料はg線照射固型飼料(CRF-1,オリエンタル酵母工業(株))を金属製給餌器を用いて,飲料水は札幌市水道水を自動給水装置を用いてそれぞれ自由に摂取させた.
3. 投与量および投与方法
投与量設定試験では,0,125,250,500および1000 mg/kgの投与量で1群雌雄各5匹のSD系ラットに14日間経口投与した.その結果,1000 mg/kg群では雌雄に振戦,腹臥,横臥または流涎などの症状の発現,雄の体重と摂餌量の低値,雌雄の肝臓の相対重量および雄の腎臓の相対重量に有意な高値がみられた.500 mg/kg群では雌雄とも肝臓の相対重量に有意な高値がみられた.血液生化学検査では,雌の500および1000 mg/kg群で総コレステロールが有意な高値であった.250および125 mg/kg群には3-メチルフェノール投与によると考えられる変化は認められなかった.以上のことから,28日間反復経口投与毒性試験の本試験では,雌雄のラットに確実に毒性が認められると予測される1000 mg/kgを最高用量とし,以下公比約3で除して300および100 mg/kgの3用量群とし,これに溶媒(オリブ油)のみを同様に投与する対照群を含めた計4群を設定した.1群の動物数は雌雄とも7または14匹とし,投与前々日の体重に基づいて層化無作為抽出法により群分けを行った.
投与に際しては,ラット用胃ゾンデを用いて1日1回,28日間の計28回,強制的に胃内に投与した.投与容量を5 mL/kgとし,各動物の投与液量は投与日に最も近い測定日の体重に基づいて算出した.
4. 検査項目
1) 一般状態観察
投与期間および回復期間中,全例について1日1回以上の頻度で観察した.
2) 体重および摂餌量測定
体重は全例について,投与1日(投与前),投与2,7,14,21および28日(投与終了日),回復1,7および14日ならびに剖検日に測定し,投与1日から28日,回復1日から14日の体重増加量および体重増加率を算出した.また,摂餌量は剖検日を除いて体重と同じ日に測定した.
3) 尿検査
投与4週および回復2週に全例を代謝ケージに収容して非絶食下で採尿を行い,同時に採尿中の飲水量(重量)も測定した.約3時間の蓄尿についてpH,蛋白,糖,ケトン体,ウロビリノーゲン,ビリルビン,潜血反応(以上,マルティスティックス,バイエル・三共)および色調(肉眼観察)ならびに沈渣(鏡検)を検査し,21時間蓄尿について尿量(容量)および比重(屈折計法,アタゴ)を測定した.
4) 血液学検査
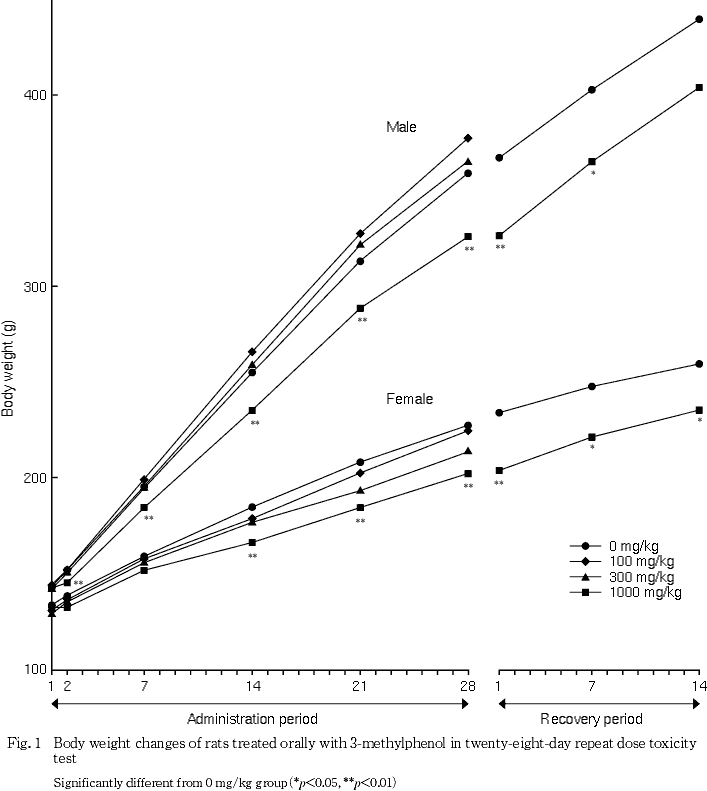
全例について剖検時に16〜20時間絶食させた後,エーテル麻酔下で腹部大動脈より採血し,EDTA・2Kで処理した血液を用いて赤血球数,ヘマトクリット値,血小板数,白血球数(以上,電気抵抗法),ヘモグロビン量(シアンメトヘモグロビン法)(以上,自動血球計数装置F-820,シスメックス),平均赤血球容積(赤血球数,ヘマトクリット値より算出),平均赤血球ヘモグロビン量(赤血球数,ヘモグロビン量より算出),平均赤血球ヘモグロビン濃度(ヘマトクリット値,ヘモグロビン量より算出),網赤血球数(Brecher法)および白血球百分比(May-Gr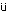 nwald-Giemsa染色)を測定した.また,3.8 %クエン酸ナトリウムで処理した後,3000 回転/分で10分間遠心分離して得られた血漿を用いて,プロトロンビン時間(トロンボプラスチン法)および活性化部分トロンボプラスチン時間(エラジン酸法)(以上,血液凝固自動測定装置アメルングKC-10A,バクスター)を測定した.
nwald-Giemsa染色)を測定した.また,3.8 %クエン酸ナトリウムで処理した後,3000 回転/分で10分間遠心分離して得られた血漿を用いて,プロトロンビン時間(トロンボプラスチン法)および活性化部分トロンボプラスチン時間(エラジン酸法)(以上,血液凝固自動測定装置アメルングKC-10A,バクスター)を測定した.
5) 血液生化学検査
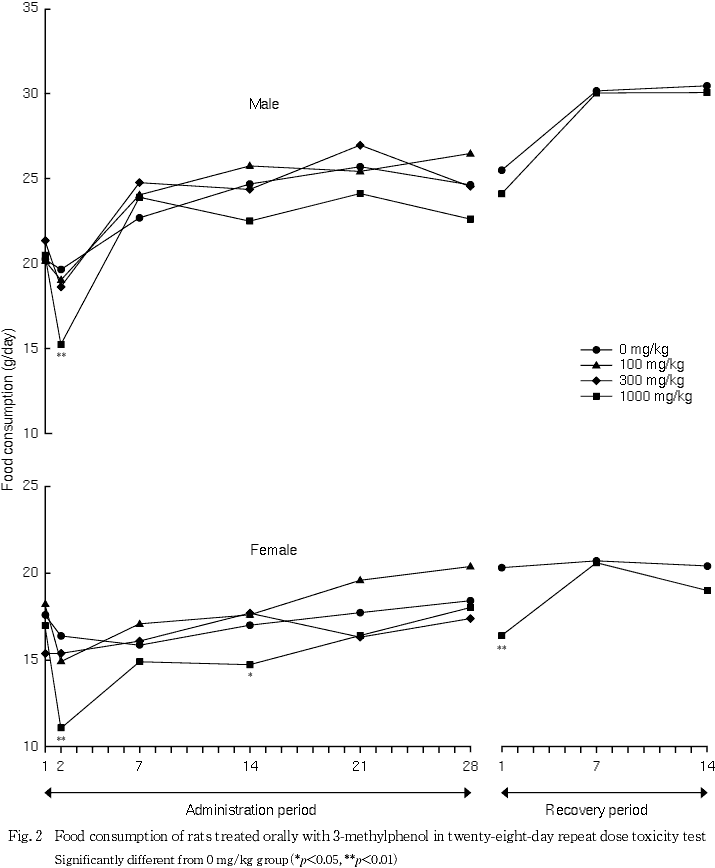
血液学検査と同様に,全例について腹部大動脈より採血し,ヘパリン処理した後,3000回転/分で10分間遠心分離して得られた血漿を用いてGOT(IFCC法),乳酸脱水素酵素(Wr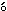 blewski & La Due法)およびグルコース(ヘキソキナーゼ法)を測定し,無処理血液を3000回転/分で10分間遠心分離して得られた血清を用いてGPT(IFCC法),アルカリホスファターゼ(Bessey-Lowry法),γ-GTP(包接L-γ-グルタミル-ρ-ニトロアニリド基質法),総コレステロール(酵素法),トリグリセリド(遊離グリセロール消去法),総ビリルビン(アゾビリルビン法),尿素窒素(ウレアーゼ・インドフェノール法),クレアチニン(Jaff
blewski & La Due法)およびグルコース(ヘキソキナーゼ法)を測定し,無処理血液を3000回転/分で10分間遠心分離して得られた血清を用いてGPT(IFCC法),アルカリホスファターゼ(Bessey-Lowry法),γ-GTP(包接L-γ-グルタミル-ρ-ニトロアニリド基質法),総コレステロール(酵素法),トリグリセリド(遊離グリセロール消去法),総ビリルビン(アゾビリルビン法),尿素窒素(ウレアーゼ・インドフェノール法),クレアチニン(Jaff 法),カルシウム(OCPC法),無機リン(Fiske-SubbaRow法),総蛋白(ビウレット法)(以上,自動分析装置7150形,日立製作所),ナトリウム,カリウム(以上,炎光光度法,自動炎光光度計480型,コーニング),クロール(電量滴定法,クロライドカウンターCL-6M,平沼産業),蛋白分画およびA/G比(以上,セルロースアセテート膜電気泳動法,全自動電気泳動装置CTE-150,常光)を測定した.
法),カルシウム(OCPC法),無機リン(Fiske-SubbaRow法),総蛋白(ビウレット法)(以上,自動分析装置7150形,日立製作所),ナトリウム,カリウム(以上,炎光光度法,自動炎光光度計480型,コーニング),クロール(電量滴定法,クロライドカウンターCL-6M,平沼産業),蛋白分画およびA/G比(以上,セルロースアセテート膜電気泳動法,全自動電気泳動装置CTE-150,常光)を測定した.
6) 剖検および器官重量測定
投与28日および回復14日の翌日に全例について,体外表を観察し,エーテル麻酔下で採血後放血致死させ剖検した.また,脳,肺,心臓,肝臓,腎臓,脾臓,副腎,下垂体,胸腺,甲状腺(上皮小体含む),精巣,精巣上体および卵巣の重量を測定するとともに,絶対重量を剖検日の体重で除し100を乗じて相対重量を算出した.
7) 病理組織学検査
全例について脳(大脳および小脳),下垂体,胸腺,甲状腺,上皮小体,副腎,脾臓,心臓,胸部大動脈,舌,食道,胃(前胃および腺胃),肝臓,膵臓,十二指腸,空腸,回腸(パイエル板含む),盲腸,結腸,直腸,喉頭,気管,肺(気管支含む),腎臓,膀胱,前立腺,精嚢(凝固腺含む),卵巣,子宮(角部および頸部),膣,乳腺(原則として右腹部,雌のみ),皮膚(腹部),胸骨(骨髄含む),大腿骨(骨髄含む),脊髄(頸部),骨格筋(大腿部),腸間膜リンパ節,下顎リンパ節,顎下腺,舌下腺,耳下腺および坐骨神経を10 %中性緩衝ホルマリン液で,眼球およびハーダー腺をデビッドソン液で固定・保存し,精巣および精巣上体をブアン液で固定後70 %エタノールで保存した.これらの器官・組織を常法に従ってパラフィン包埋後,薄切してヘマトキシリン・エオジン染色標本を作製し,対照群および高用量群の全例を鏡検した.さらに肝臓は,その他の用量群の雌雄の動物についても全例鏡検した.
5. 統計解析
体重,体重増加量,体重増加率,摂餌量,尿検査の定量的項目,血液学検査,血液生化学検査,器官の絶対重量および相対重量の結果についてBartlettの検定法を行い,等分散性を解析した.等分散の場合は一元配置分散分析法で解析し,不等分散の場合はKruskal-Wallisの検定法で解析した.一元配置分散分析の結果,有意差がみられた場合は,Dunnettの検定法で解析した.Kruskal-Wallis法の解析の結果,有意差がみられた場合は,Mann-WhitneyのU-検定法で解析した.
尿比重および尿検査の定性的項目の結果については,Kruskal-Wallisの検定法で解析し,有意差がみられた場合は,Mann-WhitneyのU-検定法を用いて解析した.
これら対照群と被験物質投与群との間の検定においては,いずれも有意水準を5 %とした.
結果
1. 一般状態
1000 mg/kg群において,振戦が投与1日に雄9例,雌11例に発現し,2日以降も投与終了日まで雌雄に散見された.また,流涎が投与期間を通して雌雄に散見された.さらに腹臥または横臥が,投与1日に雌雄各1例と7日に雌で1例にみられた.これらの症状は,投与後数分から約30分の間に発現し,発現後2時間以内に回復した.その他に,外尿道口周囲被毛汚染が雌で2例に観察された.回復期間にはいずれの動物にも変化は認められなかった.
2. 体重(Fig. 1)
投与期間中,100および300 mg/kg群では雌雄とも対照群と比較して有意な差は認められなかった.1000 mg/kg群では,雄は投与期間を通して,雌は投与14日から28日まで対照群より有意に低く,体重増加量および体重増加率も雌雄とも有意な低値であった.
回復期間には,1000 mg/kg群の体重は期間を通して雌雄とも低く,雄の回復14日の値を除いて有意な低値であった.しかし,雌雄とも対照群を上回る体重の増加が認められた.
3. 摂餌量(Fig. 2)
投与期間中,100および300 mg/kg群では雌雄とも対照群と比較して有意な差は認められなかった.1000 mg/kg群では,雄で投与2日に,雌で投与2日および14日に有意な低値が認められた.
回復期間における1000 mg/kg群の摂餌量は,雌の回復1日に有意な低値がみられた.
4. 尿検査および飲水量
投与4週の検査では,1000 mg/kg群において,雌雄の尿pHの有意な低下,雄の飲水量および尿量の有意な高値,雌の尿蛋白陰性例の有意な増加,ならびに雄の尿蛋白陰性例の増加傾向がみられた.
回復2週の検査では,1000 mg/kg群の雌雄とも,いずれの検査項目にも変化は認められなかった.
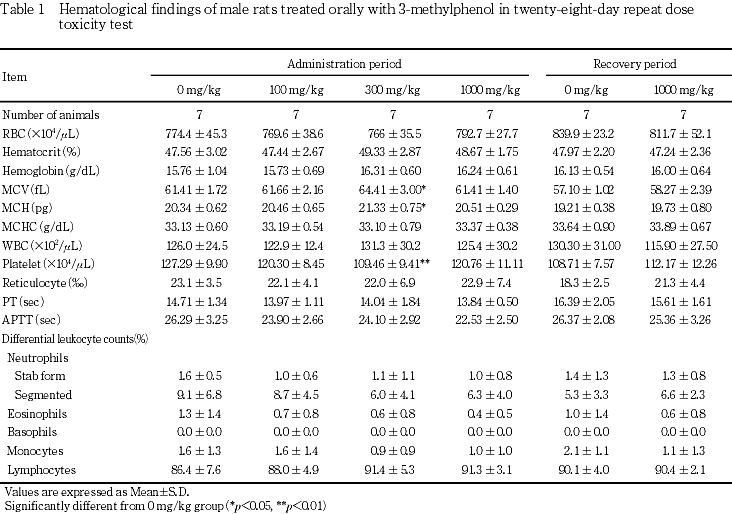
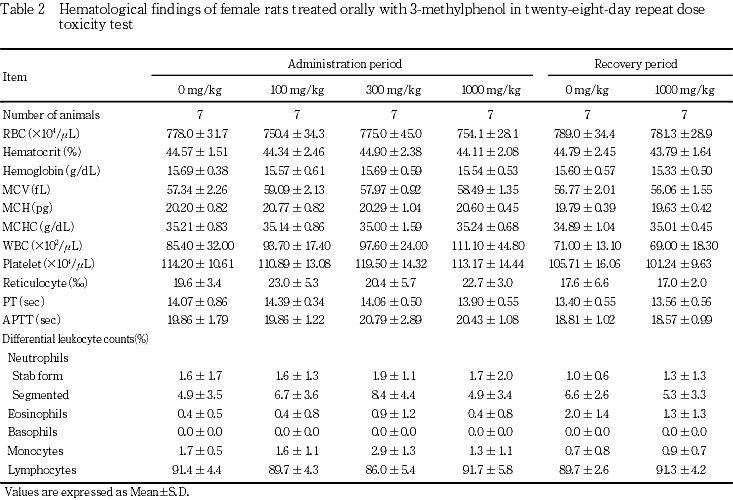
5. 血液学検査(Table 1, 2)
投与期間終了時の検査では,雄の300 mg/kg群において,平均赤血球容積および平均赤血球ヘモグロビン量に有意な高値,血小板数に有意な低値がみられたが,1000 mg/kg群におけるそれらの値は対照群とほぼ同じであったことから,いずれも偶発的な変動と考えられた.雌では,いずれの投与群においても変化は認められなかった.
回復期間終了時には,1000 mg/kg群の雌雄とも対照群と比較して有意な差は認められなかった.
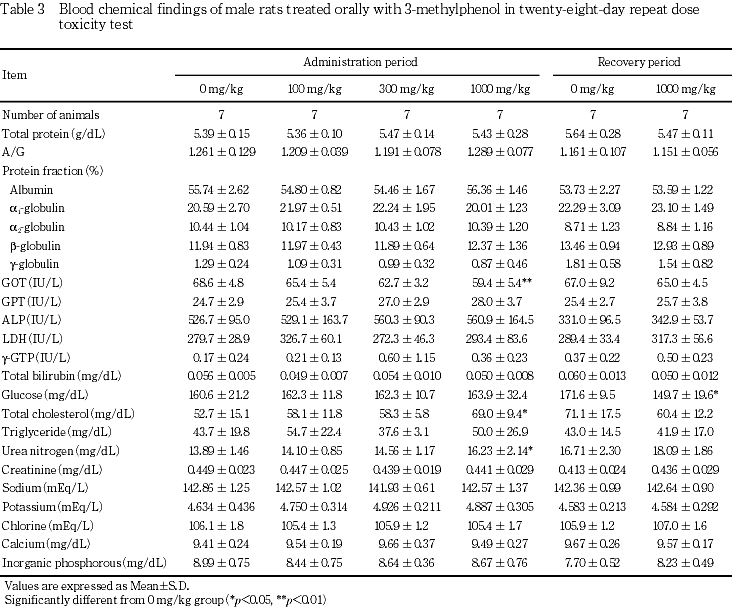
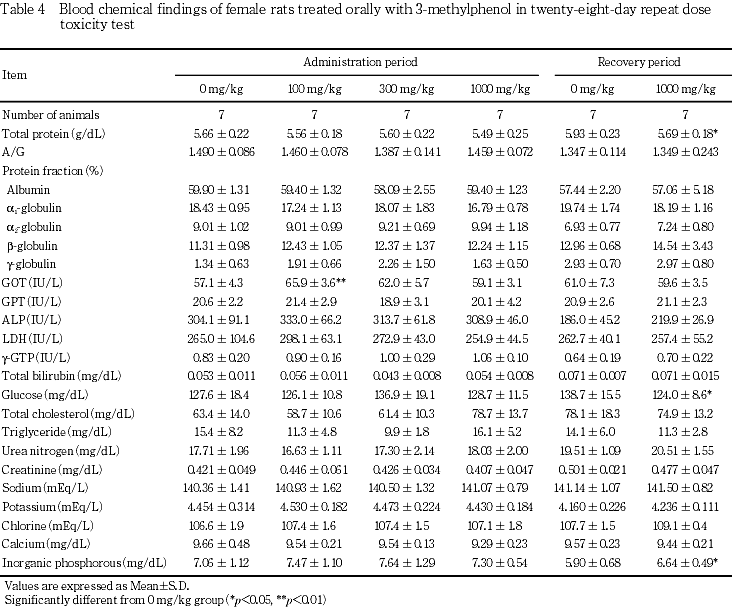
6. 血液生化学検査(Table 3, 4)
投与期間終了時の検査では,雄の1000 mg/kg群において,総コレステロールが有意な高値であった.また,GOTの有意な低値および尿素窒素の有意な高値がみられたが,いずれも軽度な変化であり,対照群の変動範囲内であった.雌では,100 mg/kg群でGOTに有意な高値がみられたが,300 mg/kg以上の用量群では認められない変化であった.1000 mg/kg群では,総コレステロールが高値傾向を示した.その他の検査項目には,対照群と比較して有意な差は認められなかった.
回復期間終了時の1000 mg/kg群では,雌雄のグルコースに有意な低値がみられた.雌では,総蛋白に有意な低値および無機リンに有意な高値がみられたが,いずれも軽度な変化であり,関連項目に明らかな変化がみられないことから偶発的な変動と考えられた.
7. 剖検
投与期間終了時および回復期間終了時の剖検では,いずれの投与群の雌雄にも被験物質投与によると考えられる変化は認められなかった.
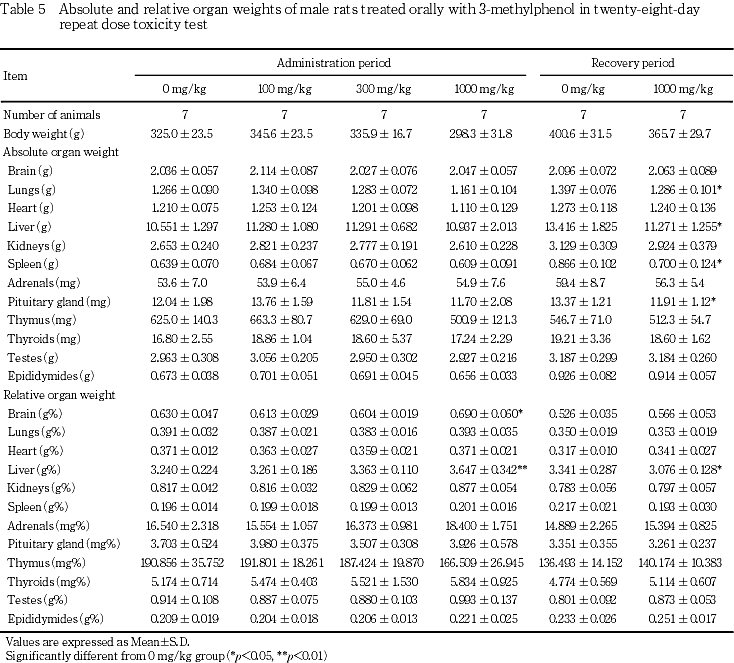
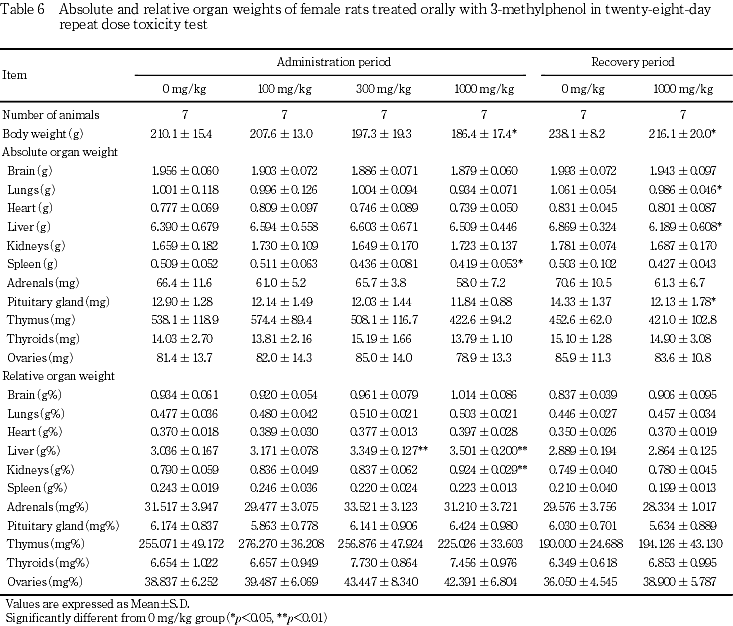
8. 器官重量(Table 5, 6)
投与期間終了時に,雄では,1000 mg/kg群において,剖検日の体重に低値傾向がみられ,肝臓および脳の相対重量が有意な高値を示した.雌の器官重量は,100 mg/kg群ではいずれの器官にも対照群と比較して有意な差は認められなかったが,300 mg/kg群では肝臓の相対重量が有意な高値であった.1000 mg/kg群では,剖検日の体重が有意に低く,肝臓および腎臓の相対重量が有意な高値を示した.また,脾臓の絶対重量が有意な低値であったが,相対重量には有意差はみられなかった.
回復期間終了時に,1000 mg/kg群の雄では,肝臓の絶対重量および相対重量が有意な低値であった.また,剖検日の体重に低値傾向がみられ,脾臓,肺,下垂体の絶対重量が有意な低値であったが,相対重量には有意差はみられなかった.雌では,剖検日の体重が有意に低く,肝臓,肺,下垂体の絶対重量が有意な低値であったが,相対重量には有意差はみられなかった.
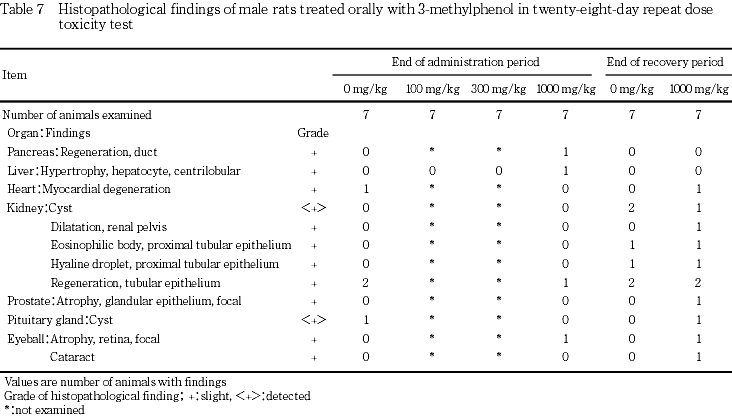
9. 病理組織学検査(Table 7, 8)
投与期間終了時の検査において,1000 mg/kg群の雄で,膵臓の導管の再生,肝臓の小葉中心性肝細胞肥大,腎臓の尿細管上皮の再生および眼球の限局性網膜萎縮が各1例みられた.100 mg/kg群では,雌で肝臓の門脈周囲性の肝細胞脂肪化が1例みられたが,300および1000 mg/kg群には認められない変化であった.
回復期間終了時には,1000 mg/kg群の雄で,心臓の心筋変性,腎臓の嚢胞,腎盂拡張,近位尿細管上皮の好酸性小体,近位尿細管上皮の硝子滴,前立腺の腺上皮の限局性萎縮,下垂体の嚢胞,眼球の限局性網膜萎縮および白内障が各1例,腎臓の尿細管上皮の再生が2例みられた.雌では,肺の泡沫細胞集簇,肝臓の小肉芽腫および腎臓の尿細管上皮の再生が各1例みられた.

考察
1000 mg/kg群では,一般状態の変化として雌雄とも振戦または流涎が,投与期間を通して,投与後数分から2時間の間に観察された.これらの症状は回復期間中にはみられなかった.体重は雌雄とも投与期間中増加が抑制され,低値を示した.回復期間には雌雄とも体重は対照群と比較して低値であったが,回復期間の体重増加率は対照群を上回っており,回復傾向がみられた.摂餌量は投与期間中雌雄で低値がみられ,回復期間には雌で低値がみられた.
投与4週の尿検査では,雄の飲水量および尿量が増加した.また,雌雄の尿pHの低下および尿蛋白陰性例の増加または増加傾向がみられた.これらの原因として,体重増加が抑制されたことから,低栄養状態による有機酸の産生の増加ならびに蛋白の合成や排泄の低下が考えられた.回復2週の検査では同じ変化はみられなかった.
投与期間終了時の血液生化学検査では,雌雄に総コレステロールの高値または高値傾向がみられた.その増加の程度は軽度であり,アルカリホスファターゼ,総ビリルビン,GPTあるいはGOTに高値がみられていないことから,肝障害性の変化ではなく,肝臓での合成あるいは異化・排泄などの機能的変化であることが推察された.回復期間終了時にみられた雌雄のグルコースの低値については,トリグリセリド,総コレステロールあるいは内分泌器官に異常のないことから,その原因は不明であった.
器官重量では,投与期間終了時に雌雄とも肝臓の相対重量に有意な高値がみられ,病理組織学検査では,雄の1例に小葉中心性肝細胞肥大が認められた.肝細胞肥大は毒性変化のみならず生体の適応反応として捉えることもできる病変であり,小葉中心性の肝細胞肥大は代謝酵素を誘導する物質の多くに認められる2)ことから,1例のみの発現ではあるが,3-メチルフェノール投与に関連した変化と考えられた.また,雌で腎臓の相対重量に有意な高値がみられたが,3-メチルフェノール投与に起因すると考えられる病理組織学的異常は認められなかった.回復期間終了時の検査では雌雄とも肝臓重量は逆に低値であったが,病理組織学的異常は認められなかった.その他に,投与期間終了時に雄の脳の相対重量の高値,雌の脾臓の絶対重量の低値,回復期間終了時に雄の脾臓,肺,下垂体および雌の肺,下垂体の絶対重量の低値がみられたが,体重の低値に伴った変化と考えられた.また,投与期間終了時および回復期間終了時にみられたその他の病理組織学的所見については,低頻度であること,対照群でもみられる種類の所見であること,あるいは血液または尿の検査結果との関連性のないことから,3-メチルフェノール投与に起因する変化とは考えられなかった.
300 mg/kg群では,投与期間終了時の雌の肝臓の相対重量に有意な高値が認められ,1000 mg/kg群でもみられている変化であることから,3-メチルフェノール投与に起因するものと考えられた.その他の検査項目には異常はみられなかった.
100 mg/kg群では,いずれの検査項目にも変化はみられなかった.
以上のことから,本試験条件下における無影響量(NOEL)は,雄で300 mg/kg/day,雌で100 mg/kg/dayであると結論される.
文献
| 1) | “13398の化学商品,”化学工業日報社,東京,1998, pp. 628-629. |
| 2) | 伊東信行編,“最新毒性病理学,”中山書店,東京,1994, pp. 157-171. |
| 連絡先 |
| 試験責任者: | 藤井咲子 |
| 試験担当者: | 堀川裕尚,咲間正志,平田真理子,古川正敏,山本美代子 |
| (株)化合物安全性研究所 |
| 〒004-0839 札幌市清田区真栄363番24 |
| Tel 011-885-5031 | Fax 011-885-5313 | |
| Correspondence |
| Authors: | Sakiko Fujii(Study director)
Hironao Horikawa, Masashi Sakuma, Mariko Hirata, Masatoshi Furukawa, Miyoko Yamamoto |
| Safety Research Institute for Chemical Compounds Co., Ltd. |
| 363-24 Shin-ei, Kiyota-ku, Sapporo, Hokkaido, 004-0839, Japan |
| Tel +81-11-885-5031 | Fax +81-11-885-5313 | |

 nwald-Giemsa染色)を測定した.また,3.8 %クエン酸ナトリウムで処理した後,3000 回転/分で10分間遠心分離して得られた血漿を用いて,プロトロンビン時間(トロンボプラスチン法)および活性化部分トロンボプラスチン時間(エラジン酸法)(以上,血液凝固自動測定装置アメルングKC-10A,バクスター)を測定した.
nwald-Giemsa染色)を測定した.また,3.8 %クエン酸ナトリウムで処理した後,3000 回転/分で10分間遠心分離して得られた血漿を用いて,プロトロンビン時間(トロンボプラスチン法)および活性化部分トロンボプラスチン時間(エラジン酸法)(以上,血液凝固自動測定装置アメルングKC-10A,バクスター)を測定した.
 blewski & La Due法)およびグルコース(ヘキソキナーゼ法)を測定し,無処理血液を3000回転/分で10分間遠心分離して得られた血清を用いてGPT(IFCC法),アルカリホスファターゼ(Bessey-Lowry法),γ-GTP(包接L-γ-グルタミル-ρ-ニトロアニリド基質法),総コレステロール(酵素法),トリグリセリド(遊離グリセロール消去法),総ビリルビン(アゾビリルビン法),尿素窒素(ウレアーゼ・インドフェノール法),クレアチニン(Jaff
blewski & La Due法)およびグルコース(ヘキソキナーゼ法)を測定し,無処理血液を3000回転/分で10分間遠心分離して得られた血清を用いてGPT(IFCC法),アルカリホスファターゼ(Bessey-Lowry法),γ-GTP(包接L-γ-グルタミル-ρ-ニトロアニリド基質法),総コレステロール(酵素法),トリグリセリド(遊離グリセロール消去法),総ビリルビン(アゾビリルビン法),尿素窒素(ウレアーゼ・インドフェノール法),クレアチニン(Jaff 法),カルシウム(OCPC法),無機リン(Fiske-SubbaRow法),総蛋白(ビウレット法)(以上,自動分析装置7150形,日立製作所),ナトリウム,カリウム(以上,炎光光度法,自動炎光光度計480型,コーニング),クロール(電量滴定法,クロライドカウンターCL-6M,平沼産業),蛋白分画およびA/G比(以上,セルロースアセテート膜電気泳動法,全自動電気泳動装置CTE-150,常光)を測定した.
法),カルシウム(OCPC法),無機リン(Fiske-SubbaRow法),総蛋白(ビウレット法)(以上,自動分析装置7150形,日立製作所),ナトリウム,カリウム(以上,炎光光度法,自動炎光光度計480型,コーニング),クロール(電量滴定法,クロライドカウンターCL-6M,平沼産業),蛋白分画およびA/G比(以上,セルロースアセテート膜電気泳動法,全自動電気泳動装置CTE-150,常光)を測定した.









