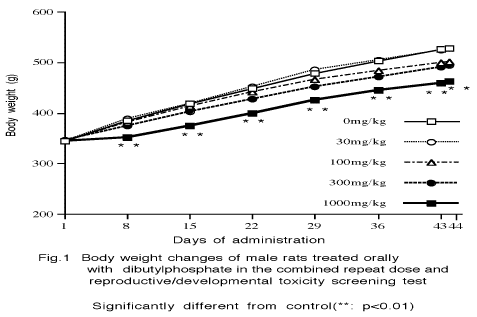
一方,雌親についても,100あるいは300mg/kg以上の群で,雄親と同様に膀胱および胃の粘膜に障害が認められ,1000mg/kg群では死亡も認められた.さらに,肝細胞の脂肪化および副腎皮質細胞における空胞の増加が100mg/kg以上の群に,肝細胞の腫大および肝臓重量の増加が1000mg/kg群に認められた.
以上の結果から,親動物に対する主な反復投与毒性は,その投与経路および排泄経路にあたる消化管,特に胃粘膜ならびに膀胱粘膜に対する障害であり,肝臓に対する影響も認められ,一般毒性学的影響に関する無影響量は,雌雄とも30mg/kg/dayと推定された.親動物の生殖に対しては,雌雄とも1000mg/kg/dayでも明らかな影響は認められなかった.児動物の発生に対しては,哺育4日生児数および生存率の減少が認められ,無影響量は,300mg/kg/dayと推定された.
投与方法は,投与液量を体重100g当たり0.5mlとし,胃ゾンデを装着した注射筒を用いて,1日1回(午前中),交配開始14日前から雄は44日間,雌は分娩後哺育3日(40〜51日間)まで,経口投与した.
投与期間中毎日,動物の生死,外観,行動等について観察した.
(2) 体重および摂餌量測定
体重の測定は,個体ごとに投与開始日(投与開始直前)およびその後は7日間隔で行い,さらに最終投与日および屠殺日あるいは死亡発見日に測定した.ただし,雌の妊娠後は,妊娠0,7,14および20日,ならびに哺育0および4日に測定した.摂餌量は,体重測定日に合わせて,ケージごとに翌日までの24時間の飼料消費量を測定した.雌の哺育4日の摂餌量は,前日からの24時間消費量を測定した.
(3) 交配および分娩状態観察
投与14日の午後に,雄のケージに同一群内の雌を入れて1対1の対を作り,交尾が確認されるまで(11日間で全例の交尾を確認),連続同居させた.交尾の確認は毎朝一定時刻(9:30分頃)に行い,膣栓形成あるいは膣垢中に精子が確認された日を妊娠0日とした.分娩状態の観察も同じ時刻に行い,1腹ごとに全例の出産が確認された日を哺育0日とした.交配および分娩の観察結果から,各群について交尾率[(交尾成立動物数/同居動物数)×100],受胎率[(受胎雌数/交尾成立雌数)×100]および出産率[(生児出産雌数/生存妊娠雌数)×100]ならびに分娩の確認された全例について妊娠期間(妊娠0日から分娩が確認された朝の前日までの期間)を算定した.
(4) 臨床病理学的検査
雄について,以下の検査を実施した.
尿検査:投与開始42日に,腰背部を刺激して強制排尿させ,pH,潜血,タンパク,糖,ケトン体,ビリルビンおよびウロビリノーゲン[以上,マイルス・三共(株),マルティスティックス]ならびに外観を検査した.
血液学的検査:供試血液の採取は,投与期間終了翌日における屠殺剖検時に行った.動物は採血前日の午後5時より除餌し,水のみを給与した.採血はエーテル麻酔下で開腹して腹大動脈より行った.採取した血液の一部をEDTA-2Kで凝固防止処理し,多項目自動血球計数装置[東亜医用電子(株),E-4000]により,赤血球数(電気抵抗検出方式),血色素量(ラウリル硫酸ナトリウム-ヘモグロビン法),ヘマトクリット値(パルス検出方式),平均赤血球容積,平均赤血球血色素量,平均赤血球血色素濃度(以上,計算値),白血球数および血小板数(以上,電気抵抗検出方式)を測定した.
血液生化学的検査:採取した血液の一部から血清を分離し,生化学自動分析装置[日本電子(株),JCA-VX-1000型クリナライザー]により,総タンパク(Biuret法),アルブミン(BCG法),A/G比(計算値),グルコース,トリグリセライド,総コレステロール(以上,酵素法),総ビリルビン(Jendrassik法),尿素窒素(Urease-UV法),クレアチニン(Jaffe法),GOT,GPT,γ-GTP(以上,SSCC法),アルカリフォスファターゼ(GSCC法),コリンエステラーゼ(BTC-DTNB法),カルシウム(OCPC法)および無機リン(酵素法)を,また電解質自動分析装置[東亜電波工業(株),NAKL-1]により,ナトリウム,カリウムおよび塩素を測定した.
(5) 病理学的検査
死亡動物および瀕死動物は発見後速やかに,雄の計画屠殺動物は採血に続いて,また雌の計画屠殺動物は哺育4日の観察終了後にエーテル麻酔下で,いずれも放血屠殺して剖検し,肝臓,腎臓,胸腺ならびに雄についてはさらに精巣,精巣上体を秤量した.分娩時あるいは分娩後に出産児の全例が死亡した雌は死亡が確認された日に,分娩予定日を過ぎても分娩が認められない雌については分娩予定の4日後(妊娠25日)にそれぞれ屠殺剖検し,同様に器官重量を測定した.雌については,卵巣の黄体数および子宮の着床数を調べ,着床率[(着床数/黄体数)×100]を算定した.
病理組織学的検査は,採取した器官を10%中性リン酸緩衝ホルマリン液(精巣,精巣上体のみブアン液)で固定後,対照群および1000mg/kg群では脳,心臓,肺,胸腺,肝臓,胃,腸,腎臓,脾臓,副腎,膀胱,精巣,卵巣について,30,100および300mg/kg群では1000mg/kg群で異常の認められた雌雄の胃,膀胱,雄の盲腸,雌の肝臓,胸腺,脾臓,副腎について,さらに不妊の対や全児が死亡した雌では対照群および1000mg/kg群で検査した器官に加えて下垂体,精巣上体,精のう,前立腺,子宮,膣について,常法に従いパラフィン切片を作製し,ヘマトキシリン・エオジン染色を施して鏡検した.
分娩完了の確認後各腹の産児数(生存児と死亡児の合計)を調べ,分娩率[(総出産児数/着床数)×100]を算定した.性別は肛門と生殖突起の距離の長短により判定し,群ごとの性比を算出した.
(2) 外表異常および一般状態の観察
分娩完了後,口腔内を含む外表の異常を観察した.また,毎日一般状態および生死を確認し,出生率[(出産確認時生児数/総出産児数)×100]および新生児生存率[(哺育4日生児数/出産確認時生児数)×100]を求めた.
(3) 体重測定
哺育0日および4日に,雌雄別に各腹ごとの総体重を測定し,1匹当たりの平均体重を算出した.
(4) 病理学的検査
死亡例はその都度,生存例は雌親の解剖時(哺育4日)にエーテル・クロロホルムで麻酔死させ,胸腹部における主要器官を肉眼的に観察した.
 法(群の大きさが異なる場合)により対照群に対する各群の比較検定を行った.カテゴリカルデータは,χ^2検定を行った.
法(群の大きさが異なる場合)により対照群に対する各群の比較検定を行った.カテゴリカルデータは,χ^2検定を行った.
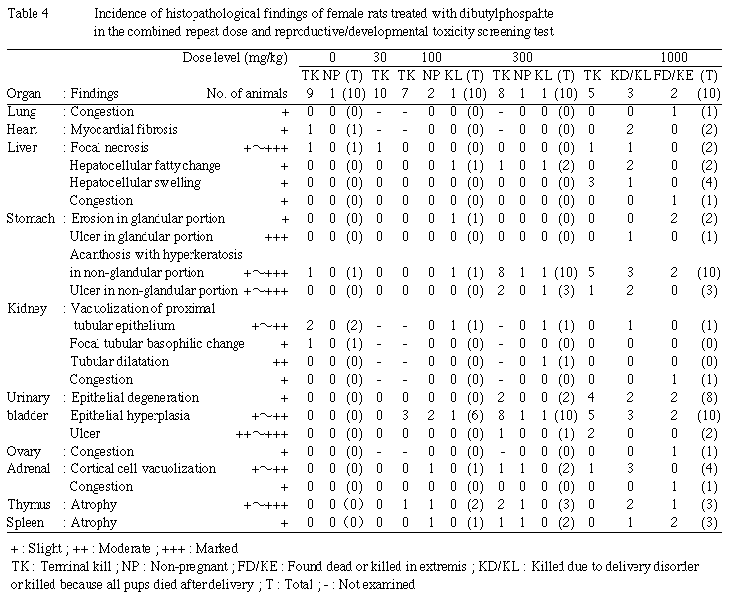
雌においても,流涎が100および300mg/kg群で各1匹,1000mg/kg群で全例に,下腹部被毛の尿による汚染が100mg/kg群で1匹,300mg/kg群で3匹,1000mg/kg群で5匹に認められた.赤色尿の排泄は100mg/kg群の1匹および300mg/kg群の2匹のみであった.
死亡については,1000mg/kg群で投与13日に雄の2匹および雌の1匹が死亡し,さらに雌の1匹は14日に,雄の1匹は28日に瀕死状態となったので切迫屠殺した.死亡率は,雄で30%,雌で20%であった.さらに,分娩時あるいは分娩後に全児が死亡した雌が100および300mg/kg群に各1匹,1000mg/kg群に3匹認められたが,これら死亡あるいは全児死亡の雌では,削痩,自発運動低下,深大呼吸,紅涙,軟便あるいは毛並み不良などの変化も認められた.

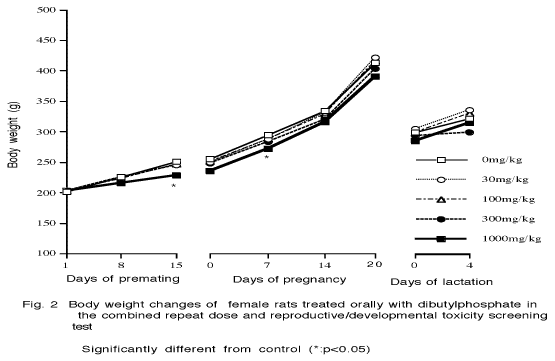
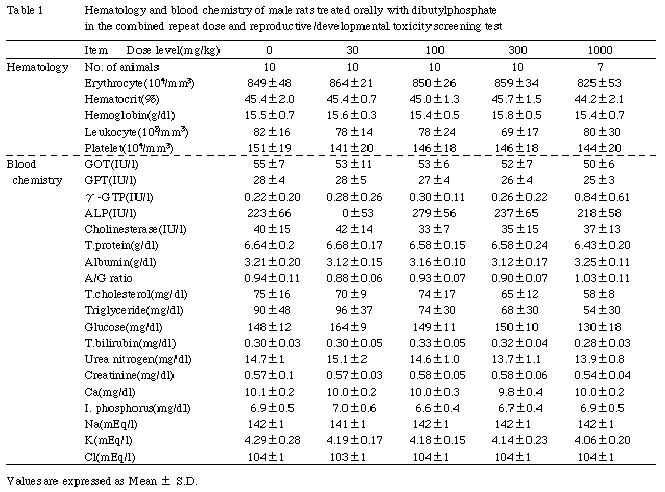

肝臓:小葉中心性の肝細胞腫大が,1000mg/kg群の雌で認められた.小葉中心ないし中間帯における肝細胞の脂肪化が,100mg/kg以上の群の主に全児死亡の雌に認められた.死亡動物ではうっ血が認められた.
胃:前胃部に重層扁平上皮の過形成および角化亢進による粘膜の肥厚が,300mg/kg以上の群の雌雄に認められた.このような変化は,100mg/kg以下の群では雌で対照群と100mg/kg群の各1匹に認められたのみであった.さらに,死亡動物や全児死亡の雌に共通して,腺胃部粘膜や前胃部粘膜にびらんや潰瘍の形成が認められ,雌では計画屠殺動物においても前胃部粘膜に潰瘍を認める例があった.
腸:盲腸において,表層上皮の軽度な変性を示す例が300mg/kg以上の群の雄で認められた.腸のその他の部位および雌では特に異常は認められなかった.
膀胱:多くは表層上皮の変性を伴う膀胱上皮の過形成が100mg/kg以上の群の雌雄に認められ,雌では300および1000mg/kg群で上皮が壊死し,潰瘍が形成されている例も認められた.
副腎:副腎皮質の特に束状帯細胞において,脂質含量の増加と考えられる空胞の増加が100mg/kg以上の群で認められた.この変化の発現例は,ほとんどが全児死亡の雌であった.死亡動物にはうっ血が認められた.
脾臓・胸腺:主に死亡動物および全児死亡の雌において,脾臓および胸腺の萎縮が認められた.
肺:1000mg/kg群における雌雄の死亡動物に共通して,うっ血あるいはうっ血水腫が認められた.
脳・心臓・腎臓・精巣/卵巣:いずれの器官にも,被験物質投与の影響と考えられる異常は認められなかった.
下垂体,精巣上体・精のう・前立腺/子宮・膣:不妊の対および全児死亡の雌において,これらの器官に異常は認められなかった.
以上の所見のほかにも,検査した各器官に異常が認められたが,いずれも被験物質の投与とは無関係な自然発生病変と考えられる変化であった.
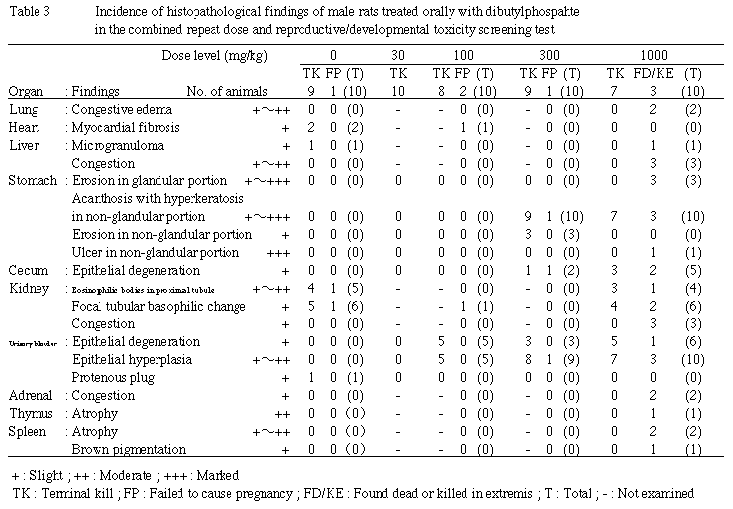
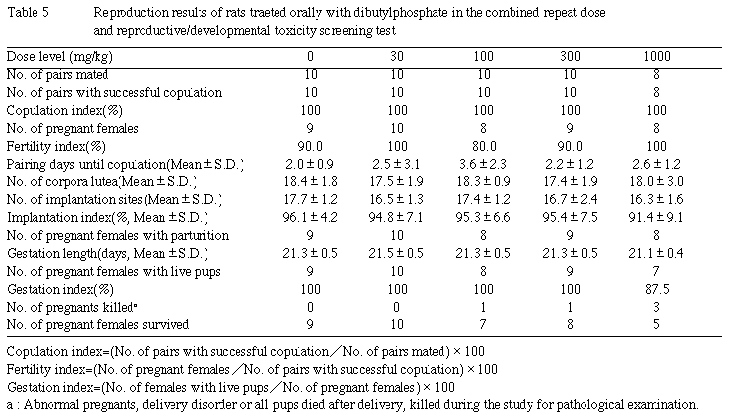
交尾は各群の全例に成立し,受胎率も対照群と被験物質投与群間に有意な差は認められなかった.また,同居開始から交尾成立までの日数にも有意な変化は認められなかった.
(2) 分娩および哺育状態
1000mg/kg群の1匹は,分娩予定日の夕方に最初の児が娩出されつつあったが難産で,翌朝の観察では分娩は終了していたものの全児が死亡していた.哺育については,100,300および1000mg/kg群の各1匹は,分娩後にほとんど哺育行動をとらず,哺育1〜3日に全児が死亡した.1000mg/kg群の別の1匹は,分娩後外部刺激に対して過敏な傾向にあり,哺育1日の投与後突然食殺行動を起こし,哺育2日には全児が食殺されていた.
(3) 黄体数,着床数および着床率
被験物質投与各群の黄体数,着床数および着床率は,いずれも対照群に比べて有意な差は認められなかった.
(4)出産率および妊娠期間
出産率は,1000mg/kg群で分娩確認時に全児死亡の1匹が認められたため減少傾向を示したが,有意な変化ではなく,また,妊娠期間にも対照群と被験物質投与群間に有意な差は認められなかった.
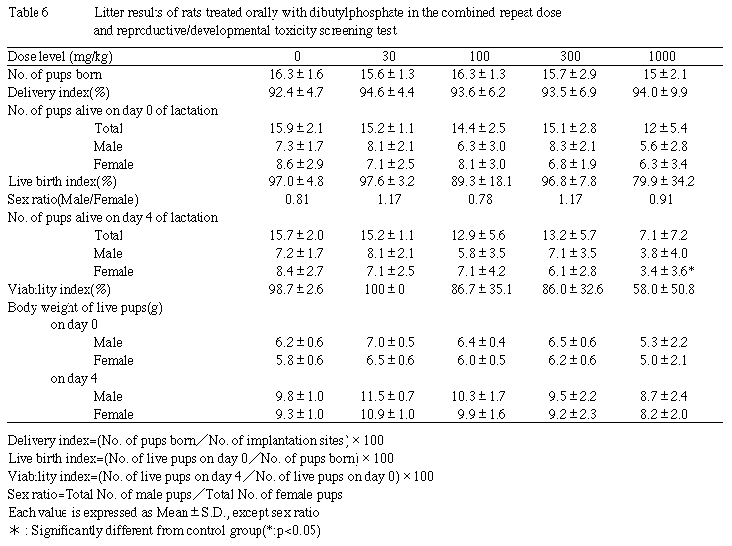
1000mg/kg群で,出産した8匹の雌親中3匹が分娩時や分娩後に全児が死亡したため,新生児数,哺育4日生児数および生存率は減少傾向を示し,4日生児雌数には対照群との間に有意差が認められた.総出産児数,分娩率および性比には有意な変化は認められなかった.
(2) 体重
新生児の体重は,哺育0日および4日のいずれにおいても,雌雄ともに対照群と被験物質投与群間に有意な差は認められなかった.
(3) 形態
外表異常は,痕跡尾を呈する新生児が対照群および300mg/kg群に各1例みられた以外,いずれの群にも異常例は観察されなかった.内臓異常は,全ての群の新生児に認められなかった.また,内臓変異についても,胸腺の頚部残留および左臍動脈遺残が被験物質投与各群の新生児に散発的に認められたが,発現傾向に用量依存性は認められなかった.
30mg/kg群で,毒性影響と考えられる変化は認められなかった.
100mg/kg以上の群では膀胱上皮の過形成が,300mg/kg以上の群では胃の前胃部粘膜の肥厚,下腹部被毛の尿による汚染および投与液に対する忌避性によると考えられる流涎が,いずれも雌雄に認められた.また,下腹部被毛の尿による汚染および流涎は100mg/kg群の雌でもみられたほか,赤色尿の排泄が100mg/kg以上の群の雄と100および300mg/kg群の雌に認められた.さらに,100mg/kg以上の群では投与初期に摂餌量の減少が雄に,1000mg/kg群では粘膜上皮の変性を伴う盲腸の拡張が雄に,体重増加の抑制および死亡が雌雄に認められた.
胃の前胃部粘膜の肥厚は,角化亢進を伴う重層扁平上皮の過形成によるもので,潰瘍形成を認める例があり,胃障害に対する上皮の反応性増殖と判断される変化であった.また,胃の腺胃部粘膜にもびらんや潰瘍を認める例があり,これらは経口投与したリン酸ジブチルの胃粘膜に対する局所障害性を示唆する変化と解せられる.なお,腸については,盲腸粘膜に軽度な上皮の変性が認められたが,その他の部位には明らかな変化は認められなかった.
一方,膀胱粘膜における変性や潰瘍の形成を伴った上皮の過形成についても,排泄臓器である腎臓を経て濃縮された尿中のリン酸ジブチルあるいはその代謝物の,膀胱粘膜に対する直接的な影響による変化と考えられる.これらの動物に認められた赤色尿の排泄は,障害された膀胱粘膜からの出血によるものと推察されるが,大部分の例は投与開始翌日にのみ認められ,投与終了時における雄の尿検査では,潜血反応の明らかな陽性例は認められなかった.腎臓に対しては,特に影響は認められなかった.
以上の消化管や膀胱における変化に加えて,1000mg/kg群の雌で,肝臓に肝細胞の腫大が認められ,肝臓重量は増加した.さらに,一般毒性学的影響が強く発現したためと考えられる全児死亡の雌においては,肝細胞の脂肪化も認められ,雌では肝臓に対する影響がうかがわれた.このような肝臓における病理学的変化は雄では明らかでなく,雄の臨床検査においても肝障害を示唆する変化は認められなかった.
死亡は投与13日から28日の間に発現し,病理学的検査では胃の前胃部粘膜や腺胃部粘膜に,びらんや潰瘍が共通して認められた.また,胃および腸はガスにより拡張し,脾臓および胸腺は萎縮していた.
100mg/kg以上の群で,分娩時あるいは分娩後に出産児の全例が死亡した雌親がみられたが,これらの動物においても死亡動物と類似した病理学的変化が認められた.さらに,このような雌親の副腎は肥大・退色し,病理組織学的には皮質細胞,特に束状帯細胞に空胞の増加も認められ,分娩あるいは授乳期にある動物では,リン酸ジブチルの毒性が強く現われる傾向がうかがわれた.
なお,リン酸ジブチルは有機リン化合物ではあるが,雄の血液生化学的検査においては血清コリンエステラーゼ活性に影響は認められなかった.
以上の結果から,リン酸ジブチルの反復投与毒性として,主に消化管,特に胃,および膀胱の粘膜に障害が発現することが明らかとなり,雌では肝臓に対する影響も認められた.また,無影響量については,雌雄とも30mg/kg/dayと推定された.
児動物の発生に対しては,出産児の全例が死亡した雌親が100mg/kg以上の群で発現し,1000mg/kg群では3匹と発現率が高かったため,1000mg/kg群の新生児数,哺育4日生児数および生存率は減少傾向を示し,統計学的有意差は哺育4日生児雌数のみに認められたが,雄を含めて哺育4日生児数の減少および生存率の低下は明らかであった.
全児死亡の雌親においては,胃にびらんや潰瘍が共通して認められ,重度な病理学的変化が確認されたが,下垂体や生殖器系器官には異常は認められなかった.したがって,発生毒性におけるこれらの指標の変化は,雌親に対する一般毒性学的影響により二次的に発現したものと判断された.
なお,交尾が確認されたにもかかわらず妊娠しなかった対が,投与量とは無関係に各群に散発したが,病理学的にはこれらの個体に生殖能の異常を示唆する変化は認められず,偶発的なものと考えられた.
以上の結果から,親動物の生殖に対しては,雌雄とも,1000mg/kg群においても対照群に比べて有意な変化は認められなかった.児動物の発生に対しては,1000mg/kg群で哺育4日生児数および生存率の減少が認められ,無影響量は300mg/kg/dayと推定された.
| 連絡先 | |||
| 試験責任者: | 伊藤義彦 | ||
| 試験担当者: | 山本 譲,野田 篤, 伊藤雅也,赤木 博,長谷川伸治 | ||
| (財)畜産生物科学安全研究所 | |||
| 〒 229 神奈川県相模原市橋本台 3-7-11 | |||
| Tel 0427-62-2775 | Fax 0427-62-7979 | ||
| Correspondence | |||
| Authors: | Yoshihiko Ito( Study director ) Yuzuru Yamamoto,Atsushi Noda,Masaya Ito,Hiroshi Akagi, Shinji Hasegawa | ||
| Research Institute for Animal Science in Biochemistry and Toxicology, Japan | |||
| 3-7-11 Hashimotodai, Sagamihara-shi, Kanagawa, 229, Japan | |||
| Tel 81-427-62-2775 | Fax 81-427-62-7979 | ||