4-�������ե��Ρݥ�Υ�åȤ��Ѥ���ñ����Ϳ�����
Single Dose Oral Toxicity Test of 4-Chlorophenol in Rats
����
OECD��¸����ʪ�������������˷��������Ĵ���ΰ�ĤȤ��ơ�4-�������ե��Ρݥ��1��5ɤ��Crj:CD(SD)IGS��åȤˡ�0(�о�)��690��980��1400�����2000 mg/kg�����̤�ñ��и���Ϳ�������ε�������������������ӳ�ά�����̤ˤĤ��Ƹ�Ƥ������
��˴�ϡ�2000 mg/kg����ͺ�����1400 mg/kg�ʾ�η�����Ϳ��30ʬ������Ϳ������ǧ���줿����ά�����̤ϡ�ͺ��2000 mg/kg�����1400 mg/kg�ȿ��ꤵ�줿�����̾��֤Ǥϡ����٤Ƥ��︳ʪ����Ϳ���λ�ͺ�ǡ���Ϳ���˸Ƶ�¥������ȯ��ư���㲼�����ʢ��̤���Ӵ˽��Ƶۤ�ǧ���졤980 mg/kg���λ�ͺ�Ǥ�ή��1400 mg/kg���λ�Ǥϲ���̤�ǧ���줿�����ˡ���˴��Ǥϴ�������ڻ�ޤ��ϥ����Ρݥ���ǧ���줿����¸��Ǥϡ��Ƶ�¥������Ϳ��15ʬ��ή����Ϳ��1���֡�ʢ��̤���Ӳ���̤ʤ�Ӥ˿������Ϳ��3���֡���ȯ��ư���㲼����Ӵ˽��Ƶۤ���Ϳ�����ޤǤ˾ü��������νŤǤϡ�1400 mg/kg�ʾ�η���ͺ����Ϳ����������������ǧ���줿������Ϳ��3������Ͻ�Ĵ�����ä�ǧ���줿�������ظ����ˤ����ơ���˴��Ǥϡ��٤�����Ū�˰��ֿ��á��ȿ���Ū�˿��ǧ���졤����������Ū�˰��ֿ������ȿ���Ū�˽з줬ǧ���줿����¸��Ǥ�����Ū�Ѳ���ǧ����ʤ��ä���
��ˡ
1.���︳ʪ���������Ϳ�դ�Ĵ��
4-�������ե��Ρݥ�(����99.29 %��Lot No. PJF-3�����̥�(��)�����)�ϡ���ø�쿧�η뾽�Ǥ��롥�������︳ʪ���ϡ������������ݴɤ�����Ϳ��λ������ˤ�ʬ�Ϥ�Ԥ�����������Ǥ��ä����Ȥ��ǧ���������Τˤϥ��ݥ���(Lot No. V8M6177���ʥ��饤�ƥ���(��))����Ѥ���������︳ʪ����6.9��9.8��14.0�����20.0 w/v%��ǻ�٤ˤʤ�褦�˳���Ϳ�դ���Ϳ����Ĵ���������ʤ���Ĵ����������Ϳ�դ�ǻ�٤�¬�ꤷ�������ͤΡ� 5 %����ˤ��뤳�Ȥ��ǧ�������ޤ�����Ĵ��ˡ�ˤ��0.2�����40 w/v%�Υ��������ϱդϡ�������������8���ְ���Ǥ��뤳�Ȥ��ǧ������
2.������ưʪ����ӻ�����
5�����Crj:CD(SD)IGS��å�(���ܥ��㡼�륹����С�(��))���ͺ��31ɤ��������7���֤θ����벽��Ԥä��Τ�����ͺ��25ɤ�������6����ǻ�˻��Ѥ�������Ϳ���ϻ����νŤϡ�ͺ��169.1��189.1 g����125.0��147.5 g�Ǥ��ä���ưʪ�ϡ�����24 �� 2 �����55 �� 10 %������12����(����7�������7��)����Ӵ������13��15��/�������ꤷ���Хꥢ�������ƥ���鼼�Ǿ���(�ۥ磻�ȥե졼�������ܥ��㡼�륹����С�(��))�����줿�ݥꥫ���ܥͥ�������������1������������2��3ɤ���ļ��Ƥ������餷���������ϡ��ⰵ�����Ƕݽ��������Ƿ�����(MF�����ꥨ����칩��(��))����ϼ������ǻ��ʥȥꥦ���ź��(��2 ppm)������줾�켫ͳ���ݼ褵������
3.����Ϳ�̡���Ϳ��ˡ�������������ӷ�ʬ��
��Ϳ�̤ϡ�ͽ����η�̤������ꤷ�������ʤ�������︳ʪ����250��500��1000�����2000 mg/kg���åȤ�ñ����Ϳ������̡���˴��2000 mg/kg���λ�ͺ��1/3��ˤߤ�줿���������äơ��ܻ�Ǥϻ�˴��ȯ����ͽ�ۤ����2000 mg/kg������̤Ȥ����ʲ�������1.43�ǽ�����1400��980�ڤ�690 mg/kg�η�4���̤줾�������2�������1����������̤Ȥ���������ϡ��嵭4���̤����ΤΤߤ���Ϳ�����оȤ�ä���5���Ȥ�����1���������ưʪ���ϻ�ͺ��5ɤ�Ȥ�����ʬ���ϡ���Ϳ�������νŤ�������Ϣ³̵��ٲ�ˡ�ǹԤä���
��Ϳ��ϩ�Ϸи��Ȥ���18��20�����俩������ưʪ�˰ߴɤ��Ѥ���1������Ϳ��������Ϳ���̤�10 mL/kg�Ȥ�����ưʪ����Ϳ���̤���Ϳ�����νŤ��˻��Ф�����
4.���ѻ�����
1)�����̾��ִѻ�
�ѻ����֤���Ϳ��14���֤Ȥ������δ֤˰��̾��֤���ӻ�˴��̵ͭ����Ϳ��(0��)����Ϳ��6���֤ޤǷл�Ū�ˡ���Ϳ��1������13����������������Ӹ���1��2����Ϳ��14���ϸ������1��ѻ�������
2)������
0���ܤ���Ϳ�����ʤ�Ӥ���Ϳ��1��3��5��7��10�����14���ܤ�¬�ꤷ����
3)�������ظ���
�ѻ�������˻�˴����ưʪ��ȯ����®�䤫�ˡ��ޤ����ѻ����ֽ�λ�����¸ưʪ�ϥ����ƥ���첼�������व�����Τ�˶������������Ū�˰۾郎ǧ���줿�ﴱ��Ŧ�Ф���10 %�����˾ץۥ�ޥ���ϱդ˸�����¸����ȤȤ�ˡ���ɽ��ˤĤ��������ȿ��ظ�����Ԥä���
5.�����ײ���
�νŤϡ��Ʒ����Ȥ�ʿ���ͤ�ɸ���к�������ʤ���ͭ�պ�����ϹԤ�ʤ��ä���
���
1.����˴��ȯ����������ӳ�ά������
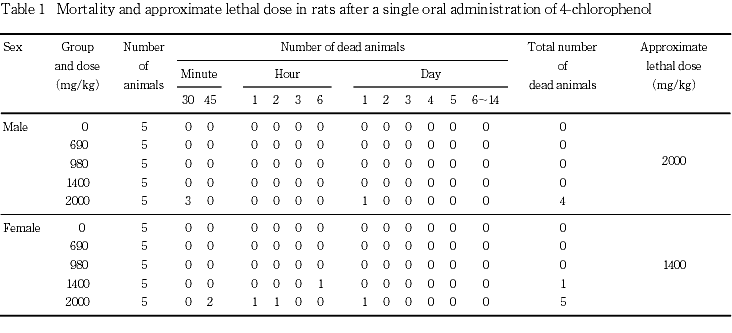
��˴��ȯ����������ӳ�ά�����̤�Table 1�˼�������
1400 mg/kg���λ�1�㡤2000 mg/kg����ͺ4�㤪��ӻ�5�㤬��Ϳ��30ʬ������Ϳ�����˻�˴��������ά�����̤ϡ�ͺ��2000 mg/kg�����1400 mg/kg�ȿ��ꤵ�줿��
2.�����̾���
���٤Ƥ��︳ʪ����Ϳ���λ�ͺ�ǡ���Ϳ��5ʬ����Ƶ�¥������ȯ��ư���㲼�����浪���ʢ��̡���Ϳ��15ʬ����˽��Ƶۤ�ǧ���줿���ޤ���980 mg/kg���λ�ͺ�Ǥ���Ϳ��30����45ʬ��ή���������졤1400 mg/kg���λ�Ǥ���Ϳ��15ʬ����2���֤˲���̤�ǧ���줿���ʤ�����˴��ǤϾ�Ҥν긫�˲ä��ơ���˴ľ���˴�������ڻ�ޤ��ϥ����Ρݥ���ǧ���줿����¸��Ǥϡ��Ƶ�¥������Ϳ��15ʬ��ή����Ϳ��1���֡�ʢ��̤���Ӳ���̤ʤ�Ӥ˿������Ϳ��3���֡���ȯ��ư���㲼����Ӵ˽��Ƶۤ���Ϳ�����ޤǤ˾ü�������
3.���ν�
1400 mg/kg�ʾ�η���ͺ����Ϳ����������������ǧ���줿����3������Ͻ�Ĵ�����ä�ǧ���줿�����Τۤ����︳ʪ����Ϳ���λ�ͺ�Ǥϡ��۾��ǧ����ʤ��ä���
4.��˶��
��˴��Ǥϡ��٤ΰ��ֿ��ä�2000 mg/kg���λ�ͺ��1���ǧ���졤Ʊ�����̤�ͺ1��˶����ΰ��ֿ�����ǧ���줿����¸��Ǥϡ��Ѳ���ǧ����ʤ��ä���
5.�������ȿ��ظ���
����Ū���٤ΰ��ֿ��ä���Ӷ����ΰ��ֿ������б����ơ��ȿ���Ū���٤ǿ�𡤶����ǽз줬ǧ���줿��
�ͻ�
OECD��¸����ʪ�������������˷�������Ĵ���ΰ�ĤȤ��ơ�Crj:CD(SD)IGS��åȤ��Ѥ���4-�������ե��Ρݥ�ηи���Ϳ�ˤ��ñ����Ϳ�������»ܤ�������Ϳ�̤�0(�о�)��690��980��1400�����2000 mg/kg�Ȥ�����
��˴�ϡ���Ϳ��30ʬ������Ϳ�����ޤǤ�2000 mg/kg����ͺ�����1400 mg/kg�ʾ�η��λ��ǧ���졤�ܻ��ﲼ�ˤ����복ά�����̤ϡ�ͺ��2000 mg/kg�����1400 mg/kg�ȿ��ꤵ�줿��
��˴��Ǥϡ��ɾ��Ȥ��ƸƵ�¥������ȯ��ư���㲼������˽��Ƶۡ���������ڻ�ޤ��ϥ����Ρݥ��ʤɤ�ǧ���줿���ޤ�����������Ǥϡ������ظ����ˤ���������Ū���٤ΰ��ֿ��á��ȿ���Ū���٤ο��ǧ����Ƥ��ꡤ����ϸƵ������ȿ仡���줿���ʤ���2000 mg/kg����ͺ1��Ǥϡ�����������Ū�˰��ֿ������ȿ���Ū�˽з줬ǧ���줿����Ʊ�ͤ��Ѳ��ϻ�˴��ǤϤ��Ф���ǧ����뤳�Ȥ��顤���������������Τȹͤ���줿��
��¸��Ǥϡ����٤Ƥ��︳ʪ����Ϳ������Ϳ��5ʬ����Ƶ�¥������ȯ��ư���㲼������ޤ��ϴ˽��Ƶۤʤɤξɾ���ǧ���졤�����ξɾ����ᤤ��Τ���Ϳ��30ʬ���٤��Ȥ���Ϳ�����˲����������ޤ����νŤǤ�1400 mg/kg�ʾ�η���ͺ����Ϳ����������������ǧ���줿����3���ʹߤϽ�Ĵ�����ä��Ƥ��ꡤ�ᤤ������������
| Ϣ���� |
| ���Ǥ�ԡ� | �������� |
| �ô���ԡ� | ��¼�ɲ���¼���ס����ܷ���������������������� |
| (��)�ѥʥե��ݥࡦ��ܥ�ȥ�ݥ������������ |
| ��869-0425�����ܸ����ڻԷ���Į1285 |
| Tel 0964-23-5111 | Fax 0964-23-2282 | |
| Correspondence |
| Authors: | Hidehiro Ogata(Study Director)
Eisuke Kimura, Masao Hamamura, Kenji Sugimoto, Hiroyuki Izumi, Emiko Kuwasaki |
| Safety Assessment Laboratory, Panapharm Laboratories Co., Ltd. |
| 1285 Kurisaki-machi, Uto-shi, Kumamoto, 869-0425, Japan |
| Tel +81-964-23-5111 | Fax +81-964-23-2282 | |

