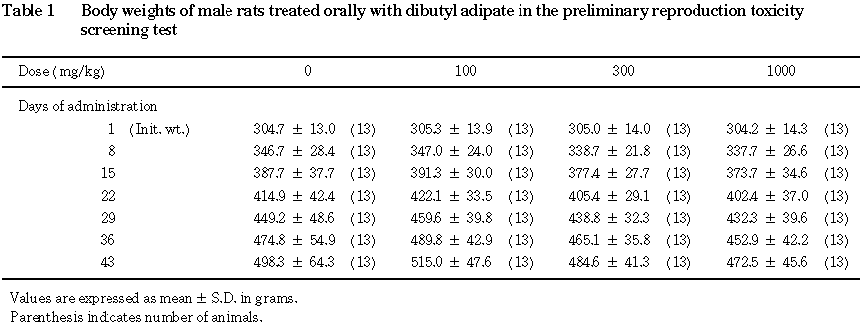
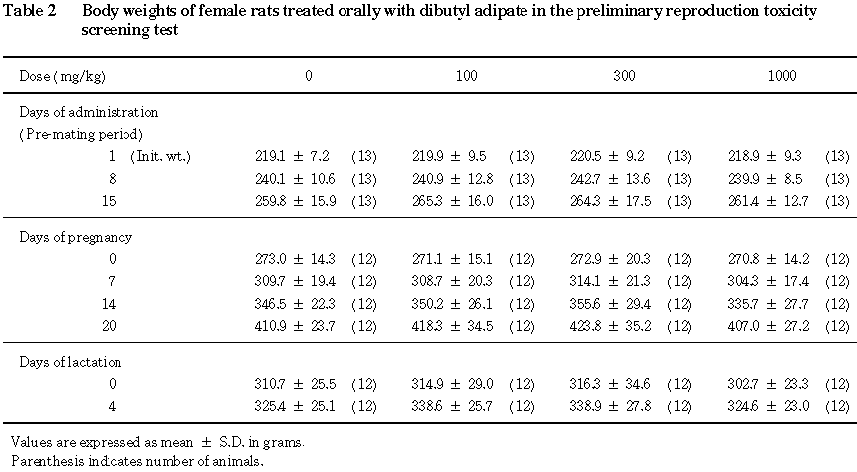
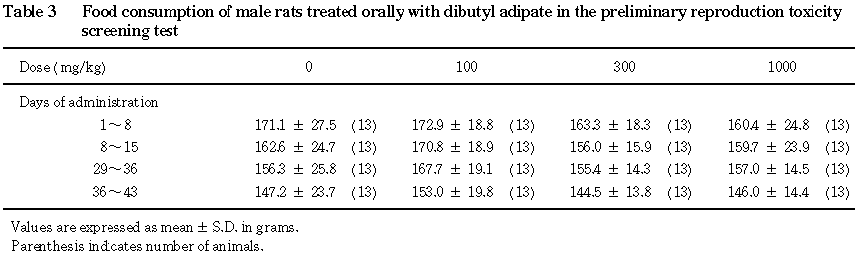
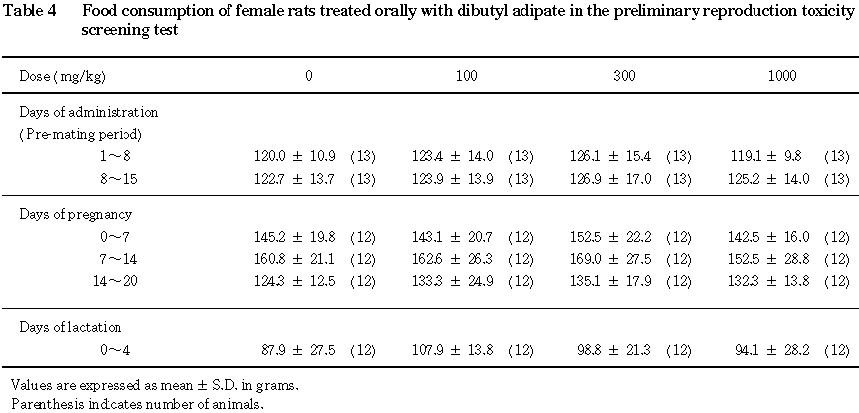
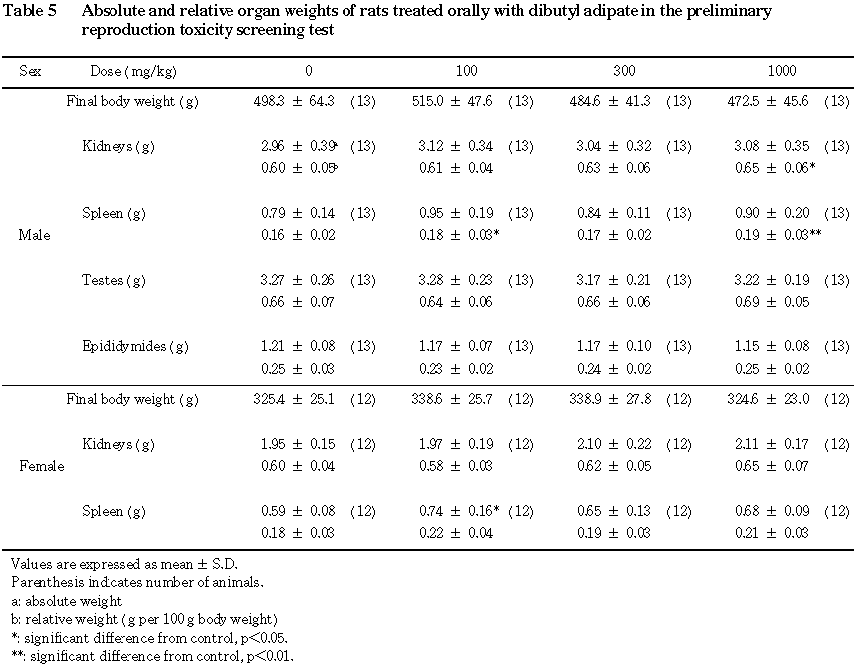
その結果,いずれの投与群においても死亡は認められず,また,毒性と考えられる一般状態の変化も観察されなかった.体重は, 1000 mg/kg投与群の雄においてやや低値を示したが,雌の体重および雌雄の摂餌量については,対照群とアジピン酸ジブチル各投与群との間に差はみられなかった.剖検および内部生殖器の組織検査では,アジピン酸ジブチル投与に起因したと考えられる異常は認められなかった.剖検時に測定した腎臓の重量は,1000 mg/kg投与群において雌雄とも高値を示した.
雌雄動物の交尾率,受胎率,さらには雌動物の妊娠維持,分娩および哺育に関して,アジピン酸ジブチル投与に起因したと考えられる異常は認められなかった.
1000 mg/kg投与群において,哺育4日の新生児生存率が低下し,哺育0日および4日の体重がやや低値を示したが,被験物質の影響を示唆する奇形はいずれのアジピン酸ジブチル投与群においても認められなかった.
これらのことから本試験の条件下では,アジビン酸ジブチルの親動物に対する無影響量は 300 mg/kg,生殖能力に対する無影響量は1000 mg/kg,次世代児に対する無影響量は300 mg/kgと推定される.
動物は,温度 24±1℃,相対湿度55±5%,換気回数約15回/時間,照明12時間(午前7時〜午後7時)に条件設定されたバリアーシステムの飼育室で,金属製ケージ(日本ケージ)に個別に収容して飼育し,固型飼料(CA-1,日本クレア)および水道水を自由に摂取させた.妊娠18日以後の母動物には,飼育ケージの床に金属製床板を敷き,床敷として木製チップ(ホワイトフレーク(R),日本チャールス・リバー)を適宜供給した.供給した飼料,水および床敷には試験に支障を来す可能性の考えられる混入物はなかった.
各用量の投与液は,雄に対しては交配前 14日間,交配期間14日間および交配期間終了後14日間の連続42日間,また,雌に対しては交配前14日間と最長14日間の交配期間中(交尾成立まで)ならびに妊娠期間を通して分娩後の哺育3日まで毎日1回,ラット用胃管を用いて強制的に経口投与した.毎日の投与は,原則として13時から15時の間に行い,各動物の投与液量は,雄ならびに交配前および交配期間中の雌については週1回の測定体重をもとに,また,交尾後の雌については,妊娠0日(腟栓または精子観察日)の体重をもとにそれぞれ算出した.
その結果,いずれの投与群においても,死亡は認められず,一般状態についても,アジピン酸ジブチル各投与群において,投与後に一過性の流涎が散見された以外に,投与の影響を示唆する変化はみられなかった.体重および摂餌量にも投与の影響は認められず,投与終了翌日に実施した剖検でも,異常は観察されなかった.腎臓および脾臓の重量は,アジピン酸ジブチル各投与群で若干増加したが,対照群との間に有意差は認められなかった.以上のことからアジピン酸ジブチルの 1000 mg/kgまでの投与量には,明らかな毒性徴候が認められなかったことから,OECD化学物質ガイドラインで定められた限度試験の用量を考慮して,本試験における高用量には 1000 mg/kg/dayを選び,以下を公比約3で除して中用量を300 mg/kg/day,低用量を100 mg/kg/dayに設定した.
雌雄とも,全例について試験期間中毎日観察した.
B. 体重
雌雄とも,全例について体重を試験期間中週 1回〔雄:投与1,8,15,22,29,36,43日,雌:投与1,8,15日〕に測定した.交尾が成立した雌では妊娠0,7,14,20日,分娩した雌では分娩後0および4日(哺育0および4日)の体重を測定した.
C. 摂餌量
雌雄とも,全例について体重測定日と同日に餌重量を測定し, 1週間の飼料消費量を算出した.2週間の交配期間中の摂餌量は測定しなかった.交尾成立雌では,妊娠0〜7,7〜14,14〜20日の,さらに分娩した雌では,哺育0〜4日の摂餌量を測定した.
D. 交配
交配は,投与 15日(投与開始日=投与1日)の夕方から最長2週間,同群内の雌雄動物を1対1で終日同居させて行った.交尾成立の確認は,毎朝,腟栓あるいは腟垢中の精子の存在を調べることにより行い,交尾が確認された雌は,その日を妊娠0日と起算して雄から分離し,個別に飼育した.交配結果から,各群について交尾率〔(交尾動物数/交配動物数)×100〕,受胎率〔(受胎動物数/交尾動物数)×100〕,同居開始日から交尾成立日までの日数およびその間に回帰した発情数を求めた.
E. 分娩状態
各群とも交尾成立雌は,全例を自然分娩させた.分娩観察の可能な動物については,異常の有無を観察し,分娩が直接観察できなかった動物についても,分娩後の徴候から分娩障害の有無を判断した.
F. 分娩日の算定
分娩の確認は,午前 9時〜11時に限定し,この時間帯に分娩が完了していることを確認した動物について,その日を分娩日(哺育0日)として妊娠期間(妊娠0日〜分娩日の日数)を計算し,各群の平均妊娠期間および出産率〔(生児出産雌数/受胎雌数)×100〕を求めた.分娩後は哺育状態を毎日観察した.
G. 剖検・病理組織検査
雄動物については,投与 42日の翌日に,ペントバルビタール麻酔下で放血・致死させ,剖検した.その際,腎臓,脾臓,精巣および精巣上体を摘出し,重量を測定した.また,精巣および精巣上体はブアン液に固定し,高用量投与群および対照群については,病理組織検査を実施した.
雌動物のうち,分娩した動物は哺育 4日に,交尾は確認されたが分娩しなかった動物は妊娠25日相当日に,それぞれペントバルビタール麻酔下で放血致死させ,剖検した.その際,腎臓および脾臓を摘出し,重量を測定した.また,卵巣および子宮も摘出して,卵巣については実体顕微鏡下で妊娠黄体数を数え,子宮については Salewski法4)を応用して着床数を確認して,着床率〔(着床数/黄体数)×100〕を算出した.不妊動物の卵巣については,さらにブアン液に固定後,病理組織検査を実施した.
A. 産児数および死亡児数の算定
哺育 0日に産児数(生存児+死亡児)を調べて,児の分娩率〔(産児数/着床痕数)×100〕および出生率〔(出産生児数/着床痕数)×100〕を求めた.また,新生児の外表異常の有無および性別を調べた.
哺育 0日以降は哺育4日まで毎日,死亡児数を調べ,哺育0日の生存率〔(生児数/産児数)×100〕および哺育4日の新生児生存率〔(哺育4日の生児数/哺育0日の生児数)×100〕を求めた.死亡児は剖検し,外表および内部器官の異常の有無を調べた.
B. 体重
哺育 0日および4日に一腹単位で雌雄別に体重(litter 重量)を測定し,産児平均体重(litter重量/測定児数)を各腹について求めた.
C. 剖検
産児は,哺育 4日にエーテル吸入により致死させ,剖検し,外表および内部器官の異常の有無を調べた.
 法を用いて対照群と各群との平均値の差の検定を行った.分散が均一でない場合および分散が0となる群が存在した場合は,Kruskal-Wallisの順位検定を行い,群間に有意性が認められた場合は,Dunnett型あるいはScheff
法を用いて対照群と各群との平均値の差の検定を行った.分散が均一でない場合および分散が0となる群が存在した場合は,Kruskal-Wallisの順位検定を行い,群間に有意性が認められた場合は,Dunnett型あるいはScheff 型の検定を行った.検定はいずれも対照群に対して5および1%の危険率で行った.
型の検定を行った.検定はいずれも対照群に対して5および1%の危険率で行った.
アジピン酸ジブチル各投与群において,投与 2日より,投与後に一過性の流涎を示す動物が観察された.流涎を示す動物の数は用量に依存して増加し,雄動物では, 100 mg/kg投与群で3匹,300 mg/kg投与群で11匹,1000 mg/kg投与群で13匹に認められ,雌動物では,100 mg/kg投与群で2匹,300 mg/kg投与群で9匹,1000 mg/kg投与群で13匹に認められた.その他に,一般状態の変化は観察されなかった.

肺では, 300 mg/kg投与群の2匹,1000 mg/kg投与群の1匹に暗赤色あるいは暗赤色点,100 mg/kg投与群の1匹,300および1000 mg/kg投与群の各2匹に暗赤色あるいは赤色域,100 および 1000 mg/kg 投与群の各1匹には退色あるいは灰白色点がみられた.腎臓については,対照群および300 mg/kg投与群の各1匹,100および 1000 mg/kg投与群の各2匹に腎盂の拡張,100および 300 mg/kg 投与群の各1匹に陥凹部が認められた.また,肝臓については100 mg/kg投与群に横隔膜ヘルニア,1000 mg/kg投与群に暗色化,脾臓については100 mg/kg投与群に腫大,1000 mg/kg投与群に白色点が各1匹にみられ,300 mg/kg投与群で空腸に憩室,対照群で精巣上体に黄白色の結節が各1匹に認められた.しかし,いずれの所見もその発現に用量依存の関係は認められなかった.
(2) 雌動物
対照群において肺の暗赤色域が 2匹,300 mg/kg投与群において肺の暗赤色化および暗赤色点と前胃の潰瘍が各1匹にみられたが,100および1000 mg/kg投与群には,異常は認められなかった.
対照群およびアジピン酸ジブチル各投与群に各 1匹みられた不妊雌の卵巣には,異常所見は認められなかった.
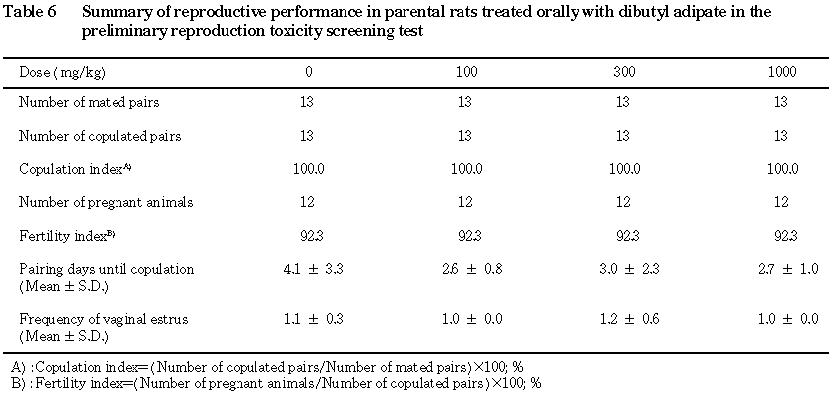

哺育状態については, 300 mg/kg投与群の1匹に哺育0日から哺育不良がみられ,哺育2日までに全出生児が死亡したが,その他の動物には,哺育状態の異常はみられなかった.
雌雄動物の交尾および受胎能力,さらには雌動物の妊娠維持,分娩ならびに哺育について,アジピン酸ジブチル投与の影響を示唆する変化はみられなかった.また,雄の精巣および精巣上体,不妊雌の卵巣の組織検査でも,アジピン酸ジブチル投与に起因した変化は認められなかった.
出生児については,哺育 4日の新生児生存率が1000 mg/kg投与群において若干低下し,同群の哺育0および4日の体重もやや低値を示したことから,アジピン酸ジブチルの1000 mg/kgは,出生児に軽度な影響を及ぼす可能性が示唆された.しかし,出生児の形態観察では,アジピン酸ジブチル投与の影響を示唆する奇形はみられなかった.
これらのことから,本試験条件下では,アジピン酸ジブチルの親動物に対する無毒性量は 300 mg/kg,生殖に対する無毒性量は1000 mg/kg,出生児に対する無毒性量は300 mg/kgであると推察される.
| 1) | H. F. Smyth, C. P. Carpenter, C. S. Weil: Range-finding toxicity data: List IV. Arch. Ind. Hyg., 4, 119(1951). |
| 2) | I. F. Gaunt, P. Grasso, A. B. G. Lansdown, S. D. Gangolli: Acute (rat and mouse) and short-term (rat) toxicity studies on dialkyl 79 adipate. Fd. Cosmet. Toxicol., 7, 35(1969). |
| 3) | A. R. Singh, W. H. Lawrence, J. Autian: Embryonic-fetal toxicity and teratogenic effects of adipic acid esters in rats. J. Pharm. Sci., 62, 1596(1973). |
| 4) | E. Salewski:F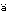 rbemethode zum makroskopischen Nachweis von Implantationsstellen am Uterus der Ratte. Naunyn-Schmiedeberg's Arch. Exp. Pathol. Pharmakol., 247, 367(1964). rbemethode zum makroskopischen Nachweis von Implantationsstellen am Uterus der Ratte. Naunyn-Schmiedeberg's Arch. Exp. Pathol. Pharmakol., 247, 367(1964). |
| 5) | 山崎実,野口雄次,丹田勝,新谷茂:ラット一般毒性試験における統計的手法の検討,対照群との多重比較のためのアルゴリズム,武田研究所報40,163 (1981). |
| 6) | 平塚秀明ほか:アジピン酸ジブチルのラットを用いた28日間反復経口投与毒性試験,Toxicity Testing Reports of Environmental Chemicals Vol. 3 化学物質毒性試験報告,245(1996). |
| 連絡先 | |||
| 試験責任者: | 長尾哲二 | ||
| 試験担当者: | 太田 亮,関 剛幸,佐藤昌子 | ||
| (財)食品薬品安全センター秦野研究所 | |||
| 〒257 神奈川県秦野市落合729-5 | |||
| Tel 0463-82-4751 | Fax 0463-82-9627 | ||
| Correspondence | |||
| Authors: | Tetsuji Nagao (Study director), Ryo Ohta, Takayuki Seki, Masako Sato | ||
| Hatano Research Institute, Food and Drug Safety Center | |||
| 729-5 Ochiai, Hadano, Kanagawa, 257, Japan | |||
| Tel +81-463-82-4751 | Fax +81-463-82-9627 | ||