1,3,5-トリス(2-プロペニル)イソシアヌル酸のラットを用いる
28日間反復経口投与毒性試験
Twenty-eight-day Repeat Dose Oral Toxicity Test of
1,3,5-Tris(2-propenyl)isocyanuric acid in Rats
要約
1,3,5-トリス(2-プロペニル)イソシアヌル酸を0(対照群),5,15及び50 mg/kgの用量でCrj:CD(SD)IGS系雌雄ラットに28日間強制経口投与し,その毒性を検討した.対照群,15及び50 mg/kg群については,別に14日間の回復群を設けた.
一般状態,尿検査及び血液学検査では,被験物質投与の影響は認められなかった.体重では,増加の抑制が50 mg/kg投与群の雌雄に認められた.摂餌量では,低値が50 mg/kg投与群の雄で投与21〜28日に認められた.血液化学検査では,ASAT,ALAT及びLDHの高値,並びに無機リンの低値が50 mg/kg投与群の雄,AlPの高値が50 mg/kg投与群の雌,総コレステロール及びリン脂質の高値が50 mg/kg投与群の雌雄に認められた.病理学検査では,肝臓重量の高値が50 mg/kg投与群の雌雄,暗赤色化が50 mg/kg投与群の雄に認められ,組織学的に肝細胞の小葉中心性肥大が5及び15 mg/kg投与群の雄及び50 mg/kg投与群の雌雄に観察された.また,肝細胞の単細胞壊死が50 mg/kg投与群の雄に,肝細胞の小葉中心性空胞化が5及び50 mg/kg投与群の雄,胆汁栓及び胆管周囲炎が50 mg/kg投与群の雌雄,胆管細胞の肥大が50 mg/kg投与群の雄に認められた.
回復性観察では,体重,摂餌量,尿検査,血液化学検査,剖検,肝細胞の単細胞壊死と小葉中心性空胞化の各所見は消失した.また,器官重量,肝細胞の小葉中心性肥大,胆汁栓,胆管周囲炎及び胆管細胞の肥大の出現頻度及びその程度は軽減し,傷害の修復像と考えられる肝細胞内好酸性封入体及び微小肉芽腫が小葉中心性に観察されたことから,回復性が示唆された.
これらの結果から,本試験における1,3,5-トリス(2-プロペニル)イソシアヌル酸の無影響量は雄で5 mg/kg/ day未満,雌で15 mg/kg/dayと判定された.
方法
1. 被験物質及び被験液の調製
1,3,5-トリス(2-プロペニル)イソシアヌル酸(日本化成,東京,ロット番号10011003,純度99.12 %)は淡黄色液体(室温)又は白色固体(冷所)である.なお,投与終了後の残余被験物質を供給元で分析した結果,使用期間中は安定であったことが確認された.
被験物質は,投与容量が10 mL/kg体重となるように乳鉢を用いて,オリブ油に懸濁して0.5,1.5及び5.0 mg/mL溶液を調製した.調製は最大7日分を一括して行い,1日分ずつ褐色ガラス瓶(遮光瓶)に入れて室温(実測値:16〜26℃)で保存した.なお,被験液は上記条件下で安定であることを確認した.また,投与1及び投与4週の2回,投与に使用した被験液について濃度及び均一性を測定した結果,適正な濃度,均一性であった.
2. 使用動物及び飼育条件
Sprague-Dawley系SPFラット〔Crj:CD(SD)IGS,日本チャールス・リバー,厚木飼育センター〕の雌雄各57匹を5週齢で入手し,9日間検疫・馴化飼育した後,体重増加が順調で一般状態に異常のみられない健康な雌雄各42匹を選び,6週齢で試験に供した.投与開始日の体重範囲は,雄で213〜234 g(平均値:223 g),雌で149〜174 g(平均値:162 g)であり,いずれの動物の体重も平均値±20 %以内であった.
動物は,群分け当日の体重に基づいて層別化し,各群平均体重がほぼ均等となるよう,コンピュータを用いて各群に割り付けた.
動物は,温度23 ± 3℃,相対湿度50 ± 20 %,換気回数1時間当たり10〜15回,照明1日12時間の飼育室で,金属製網ケージに1匹ずつ収容し,固形飼料(CRF-1,オリエンタル酵母工業)及び飲料水(水道水)を自由に摂取させ飼育した.
3. 投与量,群構成及び動物数
2週間投与による予備試験(投与量:17,50,150及び450 mg/kg)の結果,150 mg/kg投与群で雄2/5例,450 mg/kg投与群で雌雄全例が死亡した.50 mg/kg投与群の雌雄では肝臓重量の高値,更に雄でASAT,ALAT及び総コレステロールの高値,雌でヘマトクリット値の低値,ALAT及び総コレステロールの高値が認められた.これらの結果から,本試験では50,15及び5 mg/kgの3用量を設定し,これに対照群を加えた計4群を使用した.さらに,対照群,15及び50 mg/kg群では回復群を設けた.動物数はいずれの群も雌雄各6匹とした.
被験液の投与容量は10 mL/kg体重とし,胃管を用いて1日1回28日間強制経口投与した.対照群には溶媒(オリブ油)を同様に投与した.投与液量は最新の体重を基準に算出した.回復期間は14日間とした.
4. 検査項目
1) 一般状態の観察
投与期間中は毎日2回以上,回復期間中は毎日1回観察した.
(1) 詳細な一般状態の観察
投与開始前に1回,投与期間中及び回復期間中は毎週1回観察した.なお,観察及び検査は投与の情報を制限し,動物をランダムに配置した状態(ブラインド)で行った.
 ホームケージ内観察
ホームケージ内観察
姿勢,痙攣,異常行動
 手に持っての観察
手に持っての観察
ホームケージからの取り出し易さ,ハンドリングに対する反応(ハンドリング時の発声を含む),被毛・皮膚の状態(被毛の汚れ,粗毛,外傷,皮膚の色など),眼球(眼球突出,眼瞼の開き具合),眼・鼻の分泌物,可視粘膜,自律神経機能(流涙,流涎,立毛,瞳孔径,呼吸)
 オープンフィールド内観察
オープンフィールド内観察
歩行,姿勢,覚醒状態,振戦,痙攣,立ち上がり回数,排泄物(排糞数,排尿),常同行動(身繕い,旋回など),異常行動(自咬,後方突進など)
(2) 機能検査
投与第4週及び回復第2週に以下の検査をブラインドで行った.
[聴覚反応,接近反応,接触反応,痛覚反応,瞳孔反射,空中正向反射,着地開脚幅]
(3) 握力測定
上記機能検査に引き続き,前肢及び後肢の握力測定(CPUゲージMODEL-9502 A,アイコーエンジニアリング)の測定をブラインドで行った.
(4) 自発運動量の測定
上記握力測定に引き続き,投与第4週及び回復第2週に自発運動量の測定(実験動物用自発運動センサーNS-AS01,ニューロサイエンス)の測定をブラインドで行った.測定は1時間行い,10分間隔及び60分間の運動量を集計した.
2) 体重
投与期間及び回復期間を通じ,週2回(投与第1週と回復第1週は3回)の頻度で体重を測定した.
3) 摂餌量測定
投与期間及び回復期間を通じ,週2回(投与第1週は3回)の頻度で摂餌量を測定した.
4) 血液学検査
投与期間及び回復期間終了の翌日の剖検時に検査を行った.前日から一夜(約16時間)絶食させた動物をエーテル麻酔下で開腹し,腹大動脈から抗凝固剤(EDTA-2 K)を加えた採血ビンに血液を採取し,赤血球数(電気抵抗変化検出法),ヘモグロビン量(シアンメトヘモグロビン法),ヘマトクリット値(平均赤血球容積及び赤血球数から算出),平均赤血球容積(電気抵抗変化検出法),平均赤血球血色素量(ヘモグロビン量及び赤血球数から算出),平均赤血球血色素濃度(ヘモグロビン量及びヘマトクリット値から算出),血小板数(電気抵抗変化検出法),白血球数(電気抵抗変化検出法)(以上コールター全自動8項目血球アナライザーT890,ベックマン・コールター),網赤血球率(Brecher法)及び白血球百分率(May-Giemsa鏡検法)を測定した.また,3.8 %クエン酸ナトリウムを加えた容器に採取した血液を遠心分離(3000回転/分,10分間)し,得られた血漿を用いてプロトロンビン時間(クロット法),活性化部分トロンボプラスチン時間(クロット法)及びフィブリノーゲン量(トロンボプラスチン法)(以上,血液凝固自動測定装置,ACL 100,Instrumentation Laboratory)を測定した.
5) 血液生化学検査
血液学検査のための採血と同時に腹大動脈から採血し,遠心分離(3000回転/分,10分間)により得られた血清を用いてAlP(Bessey-Lowry法),総コレステロール(CEH-COD-POD法),トリグリセライド(LPL-GK-GPO-POD法),リン脂質(PLD-ChOD-POD法),総ビリルビン(ビリルビンオキシダーゼ法),グルコース(グルコースデヒドロゲナーゼ法),尿素窒素(Urease-LEDH法),クレアチニン(Creatininase-creatinase-sarcosine oxidase-POD法),ナトリウム,カリウム及び塩素(イオン選択電極法),カルシウム(OCPC法),無機リン(モリブデン酸法),総たん白質(Biuret法),アルブミン(BCG法)及びA/G比(総たん白質及びアルブミンから算出)を測定した.また,ヘパリンを加えた容器に採血し,遠心分離(3000回転/分,10分間)により得られた血漿を用いてASAT,ALAT,LDH(UV-rate法)及びγ-GTP(γ-グルタミル-3-カルボキシ-4-ニトロアニリド法)(以上,臨床化学自動分析装置TBA-120FR,東芝)を測定した.
6) 尿検査
投与第4週(検査当日の投与後)と回復第2週に動物を代謝ケージに個別に収容し,絶食・自由摂水下で4時間尿を,次いで自由摂食・自由摂水下でその後の20時間尿を採取した.採取した最初の4時間尿を用いてpH,たん白質,ケトン体,グルコース,潜血,ビリルビン,ウロビリノーゲン(以上オーションスティックス-7EA試験紙,アークレイ),色調(肉眼観察)及び沈渣(鏡検)を検査した.また,その後に得られた20時間尿を用いて浸透圧(氷点降下法,自動浸透圧測定装置 オートアンドスタット OM-6030,アークレイ)を測定し,4時間尿量及び20時間尿量から1日の尿量を算出した.更に,代謝ケージに収容した状態で,前日からの1日の摂水量を給水瓶を用いて測定した.
7) 剖検及び器官重量
上記血液学検査及び血液生化学検査のための採血後に放血致死させ,外表異常の有無を観察した後,頭部,胸部及び腹部を含む全身の器官・組織について肉眼的に異常の有無を観察した.続いて,脳,下垂体,甲状腺(上皮小体を含む),胸腺,心臓,肺(気管支を含む),肝臓,脾臓,腎臓,副腎,精巣,精巣上体,精嚢,卵巣及び子宮を摘出後,器官重量(絶対重量)を測定した.また,絶食後の体重及び絶対重量から体重100 g当たりの相対重量を算出した.
8) 病理組織学検査
全動物について以下に示す全器官・組織を採取し,リン酸緩衝10 %ホルマリン液(但し,眼球はリン酸緩衝液で調製した3 %グルタルアルデヒド・2.5 %ホルマリン液で,精巣及び精巣上体はブアン液で固定した後リン酸緩衝10 %ホルマリン液で保存)で固定した後パラフィンに包埋した.投与期間終了時剖検動物では,このうち対照群と高用量群は包埋した全ての器官・組織について切片とし,ヘマトキシリン・エオジン(H.E.)染色を施して鏡検した.その結果,被験物質投与による影響が疑われた雌雄の肝臓及び副腎については主群の中及び低用量群についても検索した.回復群は対照群及び高用量群で主群において被験物質投与による影響が疑われた雌雄の肝臓及び副腎を,中用量群で雄の肝臓を検査した.また,肉眼所見の認められた器官・組織については用量に関係なく検索した.更に,正常及び異常所見の代表例について写真を撮影した.
[脳,脊髄,坐骨神経,眼球,下垂体,甲状腺(上皮小体を含む),副腎,胸腺,脾臓,顎下リンパ節,腸間膜リンパ節,心臓,気管,肺(気管支を含む),胃,十二指腸,空腸,回腸,盲腸,結腸,直腸,肝臓,腎臓,膀胱,精巣,精巣上体,前立腺,精嚢,卵巣,子宮,骨及び骨髄(胸骨・大腿骨),大腿部骨格筋]
5. 統計解析
各検査項目のうち,数値化した成績についてまずBartlett法により各群の分散の均一性の検定(有意水準:両側1 %)を行った.その結果,分散が均一の場合にはDunnett法を用いて対照群と各投与群との平均値の差の検定を,分散が均一でない場合には,Dunnett型の方法(mean rank test法)を用いて対照群と各投与群との平均順位の差の検定を行った(有意水準:いずれも両側5及び1 %).また,尿の定性的項目及び病理組織学検査の成績についてはMann-WhitenyのU検定(有意水準:片側5及び1 %)を行った.
結果
1. 一般状態
いずれの動物においても,投与期間及び回復期間を通じ異常はみられなかった.
詳細な一般状態の観察,機能検査,握力測定及び自発運動量の測定においては,5 mg/kg投与群の雄で投与第2及び4週のオープンフィールド内における立ち上り回数に有意な高値,15 mg/kg投与群の雄で投与第4週の0から10分における自発運動量に有意な高値,15 mg/kg投与群の雌で回復第2週の後肢の握力に有意な低値が認められたが,いずれの変化も用量との関連性はなかった.その他の検査項目では,いずれの動物にも異常はみられなかった.
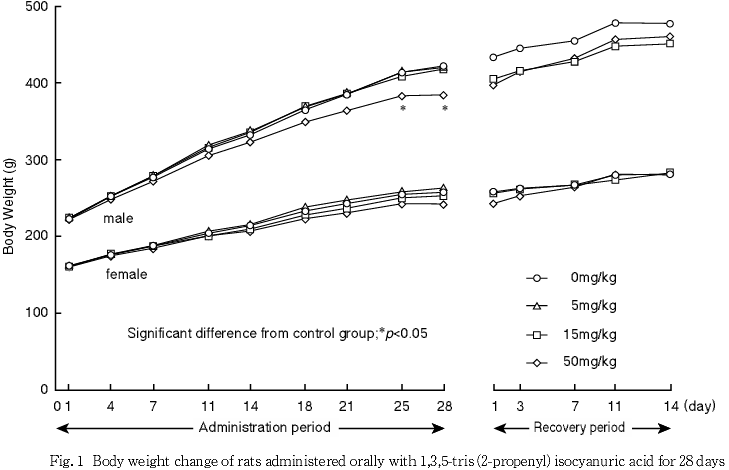
2. 体重(Fig.1)
1) 投与期間
50 mg/kg投与群では,雄で体重増加の抑制が投与4日以降みられ,投与25及び28日に有意差が認められた.同群の雌でも体重増加の抑制が投与14日以降みられたが,対照群との間に有意差は認められなかった.
15 mg/kg以下の投与群では,雌雄ともに対照群との間に有意差は認められなかった.
2) 回復期間
50 mg/kg投与群では,雌雄ともに対照群を上回る体重増加がみられ,回復期間中の体重増加量に有意な高値が認められた.
15 mg/kg投与群では,雌雄ともに対照群との間に有意差は認められなかった.
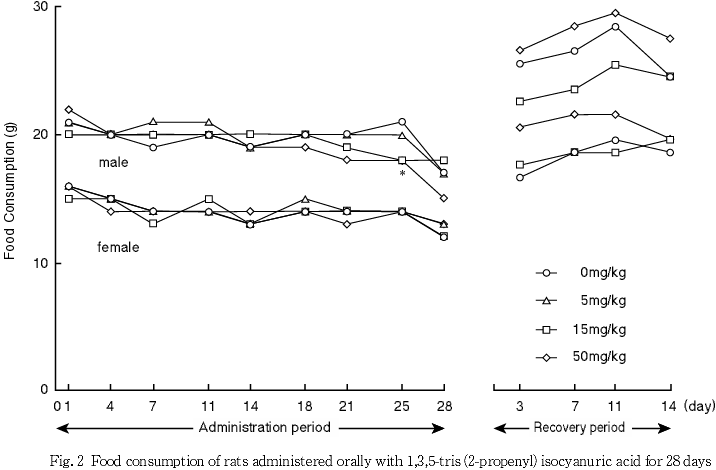
3. 摂餌量(Fig.2)
1) 投与期間
50 mg/kg投与群では,雄で投与21,25及び28日に低値が認められ,投与25日に有意差が認められた.雌に上記変化は認められなかった.
15 mg/kg投与群では,雄で投与25日に有意な低値が認められたが,一時的な変化であり,雌に上記変化は認められないことから,被験物質投与との関連はないと考えられた.
5 mg/kg投与群では,雌雄ともに対照群との間に有意差は認められなかった.
2) 回復期間
各被験物質投与群の雌雄ともに対照群との間に有意差は認められなかった.
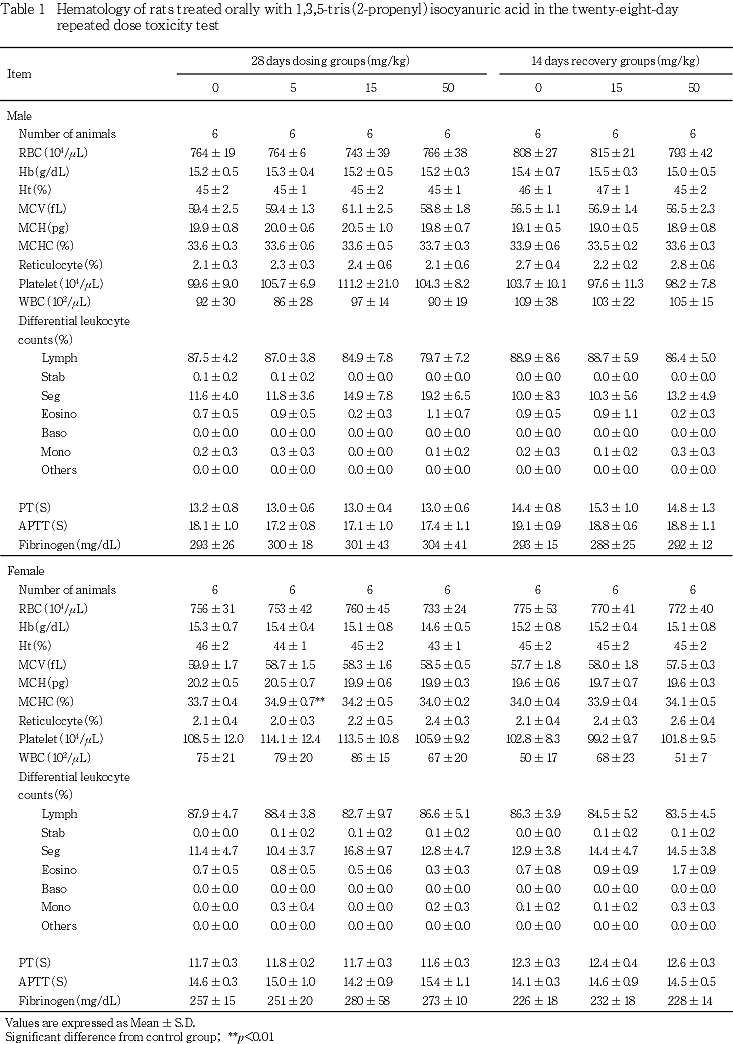
4. 血液学検査(Table 1)
1) 投与期間終了時検査
MCHCの有意な高値が5 mg/kg投与群の雌に認められたが,用量との関連性はなかった.その他の検査項目では,各被験物質投与群の雌雄ともに対照群との間に有意差は認められなかった.
2) 回復期間終了時検査
各被験物質投与群の雌雄ともに対照群との間に有意差は認められなかった.
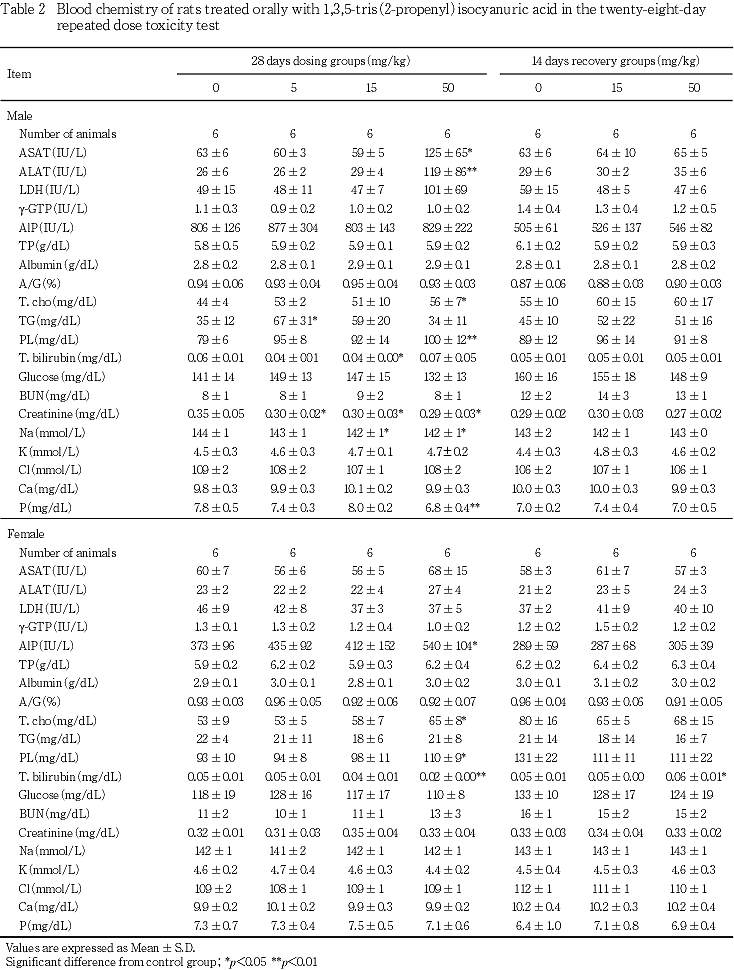
5. 血液生化学検査(Table 2)
1) 投与期間終了時検査
ASAT,ALAT,LDH,総コレステロール及びリン脂質の高値又は有意な高値,無機リンの有意な低値が50 mg/kg投与群の雄,AlP,総コレステロール及びリン脂質の有意な高値が50 mg/kg投与群の雌に認められた.また,ナトリウムの有意な低値が15 mg/kg以上の投与群の雄に認められた.その他,トリグリセライドの有意な高値が5 mg/kg投与群の雄に認められたが,用量との関連性はなかった.また,クレアチニンの有意な低値が5 mg/kg以上の投与群の雄に,総ビリルビンの有意な低値が15 mg/kg投与群の雄及び50 mg/kg投与群の雌に認められたが,毒性を示す増加性の変化でないことから毒性学的な意義はないと考えられた
2) 回復期間終了時検査
総ビリルビンの有意な高値が50 mg/kg投与群の雌に認められたが,投与期間終了時とは逆の変化であり,その程度は軽微であることから,生理的変動範囲内の変化と考えられた.
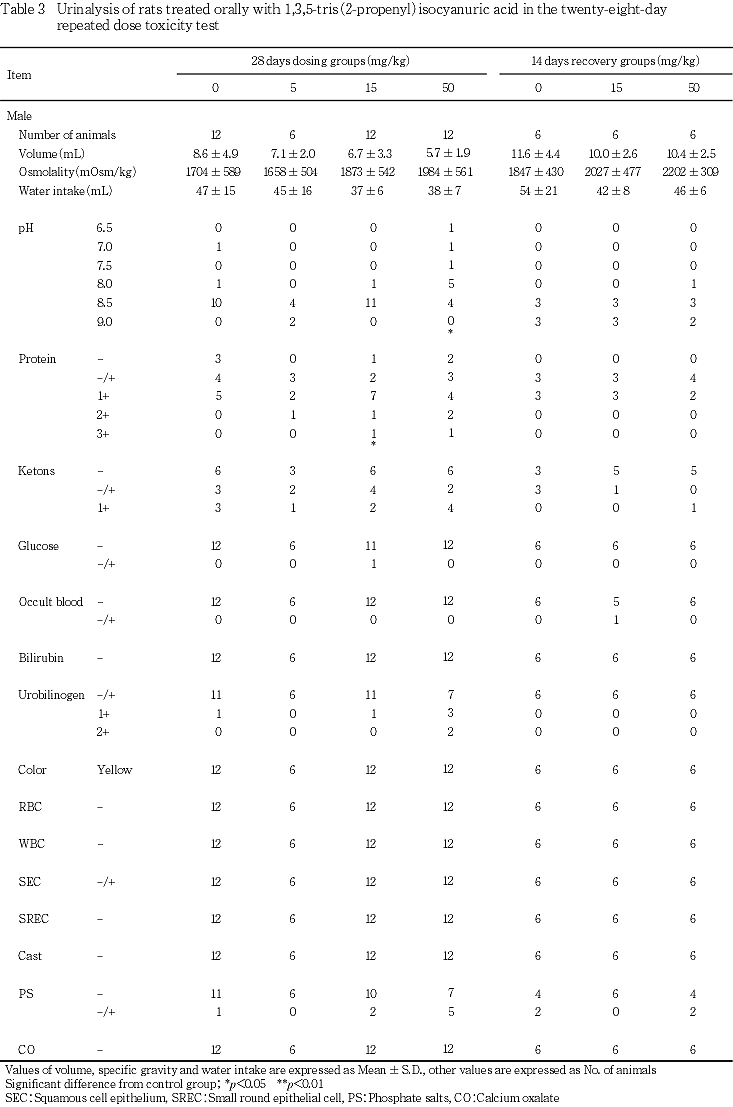
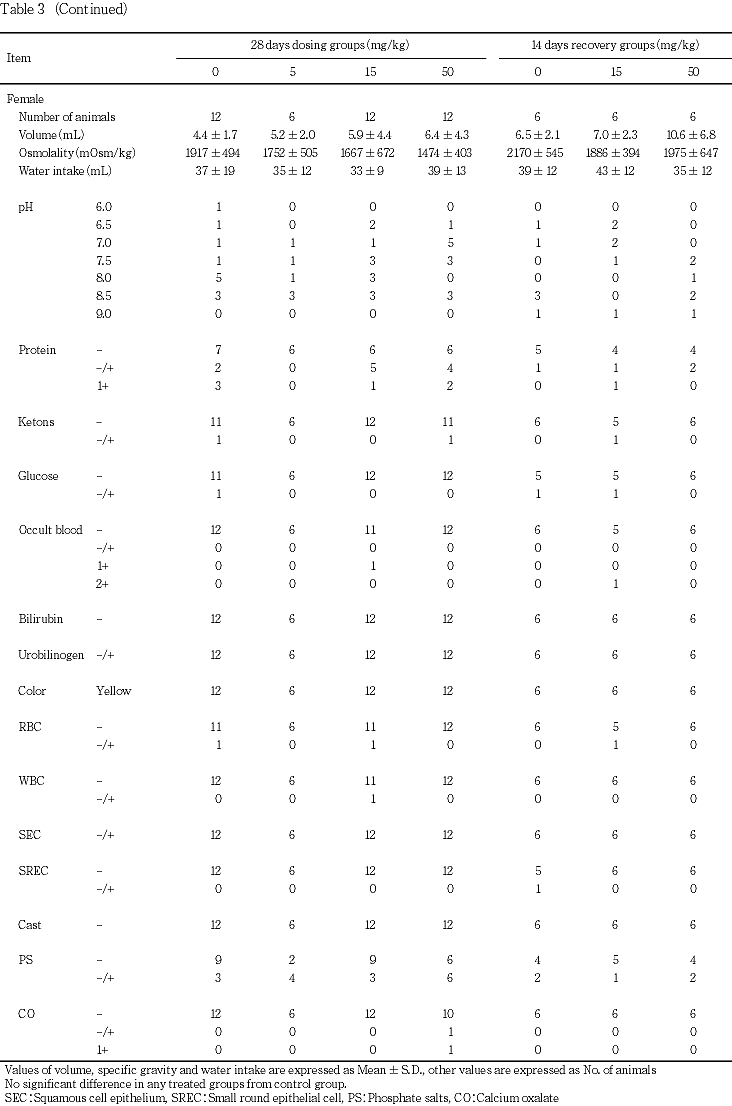
6. 尿検査(Table 3)
1) 投与第4週検査
尿pHの酸性化が50 mg/kg投与群の雄に認められた.たん白質陽性例の有意な増加が15 mg/kg投与群の雄に認められたが,雌に同変化はみられず,用量との関連性もなかった.その他の検査項目では,各被験物質投与群の雌雄ともに対照群との間に有意差は認められなかった.
2) 回復第2週検査
各被験物質投与群の雌雄ともに対照群との間に有意差は認められなかった.
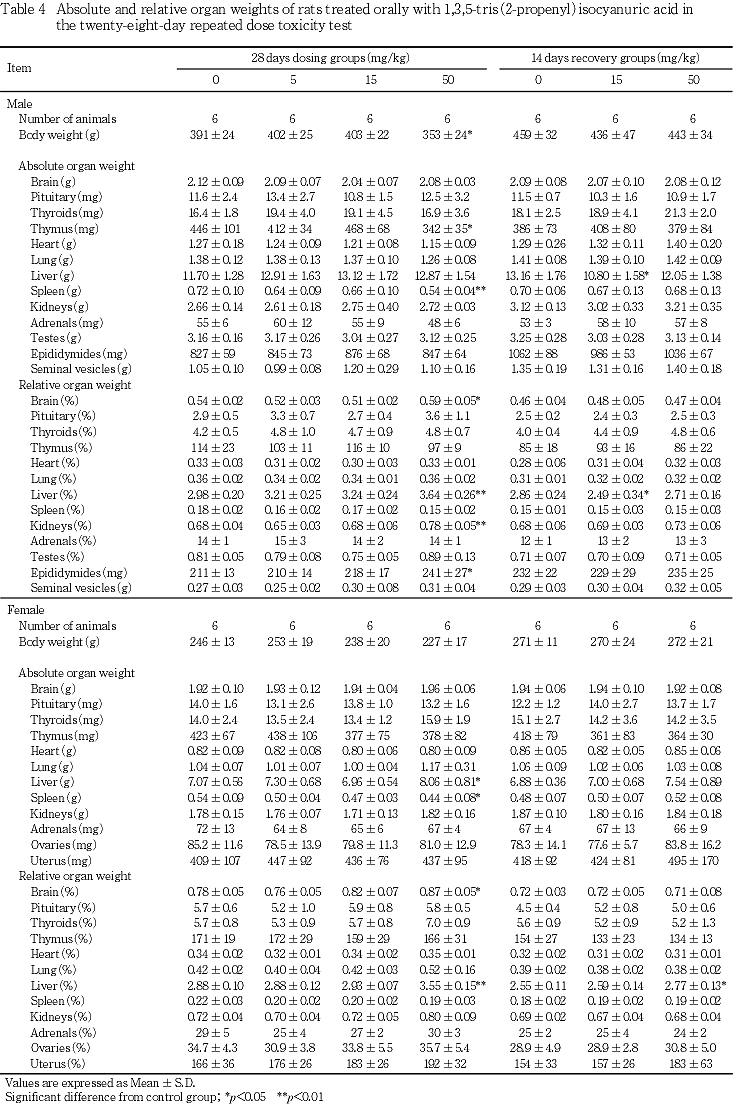
7. 器官重量(Table 4)
1) 投与期間終了時剖検例
被験物質投与の影響が肝臓にみられた.すなわち,50 mg/kg投与群おいて,肝臓の相対重量の有意な増加が雄,絶対及び相対重量の有意な増加が雌に認められた.
その他,50 mg/kg投与群で以下の変化が認められたが,剖検時の低体重による変化と考えられた.脳の相対重量の有意な増加が雌雄に,胸腺の絶対重量の有意な減少が雄に,脾臓の絶対重量の有意な減少が雌雄に,腎臓及び精巣上体の相対重量の有意な増加が雄に認められた.
2) 回復期間終了時剖検例
肝臓の絶対及び相対重量の高値又は有意な高値が50 mg/kg投与群の雌に認められた.他に,絶対及び相対重量の有意な低値が15 mg/kg投与群の雄に認められたが,用量との関連性はなかった.
8. 剖検所見
1) 投与期間終了時剖検例
肝臓の暗赤色化が50 mg/kg投与群の雄1例に認められた.他に,精巣及び精巣上体の小型化(片側性)が5 mg/kg投与群の雄1例,肝臓の大型化が15 mg/kg投与群の雄1例,腎臓のう胞(片側性)が50 mg/kg投与群の雌1例,甲状腺(上皮小体)の無形成(片側性)が対照群の雌1例にみられたが出現状況からいずれも偶発所見と判断した.
2) 回復期間終了時剖検例
いずれの器官・組織においても,異常はみられなかった.
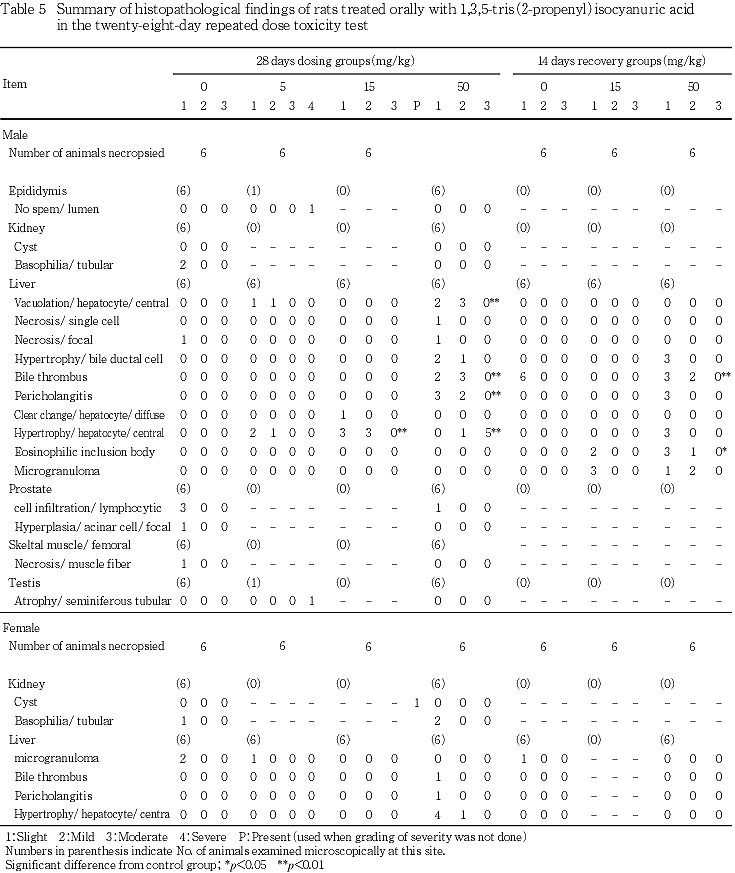
9. 病理組織学検査(Table 5)
被験物質投与の影響が5 mg/kg以上の投与群の肝臓に認められた.
1) 投与期間終了時剖検例
軽微から中等度な肝細胞の小葉中心性肥大が5 mg/kg投与群の雄3例,15 mg/kg投与群の雄6例及び50 mg/kg投与群の雄6例と雌5例にみられた.なお,肝細胞の肥大は高用量になるに従い,その領域が小葉中心から小葉中間帯まで拡大した.また,肥大した肝細胞の細胞質は空胞の領域を除けばスリガラス様であった.軽微又は軽度な肝細胞の小葉中心性空胞化が5 mg/kg投与群の雄2例及び50 mg/kg投与群の雄5例,肝細胞の軽微な単細胞壊死が50 mg/kg投与群の雄1例,軽微又は軽度な胆汁栓及び単核細胞浸潤を主体とする胆管周囲炎が50 mg/kg投与群の雄5例と雌1例,軽微又は軽度な胆管細胞の肥大が50 mg/kg投与群の雄3例にみられた.上記変化のうち,発現率の有意な増加が15 mg/kg投与群の雄及び50 mg/kg投与群の雌雄で肝細胞の小葉中心性肥大,50 mg/kg投与群の雄で肝細胞の小葉中心性空胞化,胆汁栓及び胆管周囲炎に認められた.
上記以外の所見は正常ラットでもしばしば認められる変化であること,あるいはその出現状況からいずれも偶発所見と判断した.
2) 回復期間終了時剖検例
軽微な肝細胞の小葉中心性肥大,小葉間胆管における軽微な胆管細胞の肥大及び胆管周囲炎が50 mg/kg投与群の雄3例,軽微又は軽度な胆汁栓が50 mg/kg投与群の雄5例にみられた.また,軽微又は軽度な肝細胞内好酸性封入体が15 mg/kg投与群の雄2例及び50 mg/kg投与群の雄4例,軽微又は軽度な微小肉芽腫が15及び50 mg/kg投与群の雄3例にいずれも小葉中心性にみられた.なお,肝細胞内好酸性封入体には核残渣物様の好塩基性顆粒を含むものも散見された.その他に,軽微な微小肉芽腫が対照群の雌1例にもみられたが,発現部位に特異性がないことから,被験物質投与群の小葉中心性に限局している微小肉芽腫とは異なる偶発的変化と考えられた.上記変化のうち,発現率の有意な増加が50 mg/kg投与群の雄で肝細胞内好酸性封入体及び胆汁栓に認められた.
考察
一般状態では,被験物質投与の影響は認められなかった.体重では,増加の抑制が50 mg/kg投与群の雌雄に認められたが,回復期間中は対照群を上回る体重増加がみられ,回復性のある変化であった.摂餌量では,低値が50 mg/kg投与群の雄で投与21〜28日に認められたが,回復期間中は対照群とほぼ同等の摂餌量がみられ,回復性のある変化であった.尿検査では,pHの酸性化が50 mg/kg投与群の雄に認められたが,ごく軽微な変化であり変動範囲内の変化と考えられた.回復第2週検査には同変化はみられなかった.血液学検査では,被験物質投与の影響は認められなかった.血液化学検査では,投与期間終了時でASAT,ALAT及びLDHの高値が50 mg/kg投与群の雄に認められ,組織学的にも肝細胞の単細胞壊死が観察され,被験物質の肝細胞への影響が示唆された.回復期間終了時では,細胞内小器官の変性に基づく自己貧食像と考えられる肝細胞内好酸性封入体,及び肝細胞の障害・壊死の修復像と考えられる微小肉芽腫が15及び50 mg/kg投与群の雄に小葉中心性にみられ,肝障害を示唆する逸脱酵素の変化も消失したことから,上記の肝障害性の変化には回復性が認められた.また,AlPの高値が50 mg/kg投与群の雌,総コレステロール及びリン脂質の高値が50 mg/kg投与群の雌雄に認められ,肝細胞の小葉中心性空胞化が5及び50 mg/kg投与群の雄,胆汁うっ滞に基づく一連の変化と考えられる胆汁栓及び胆管周囲炎が50 mg/kg投与群の雌雄,胆管細胞の肥大が50 mg/kg投与群の雄に観察された.これらのことから,被験物質の脂質代謝及び肝胆道系への影響が示唆された.回復期間終了時では,肝細胞の小葉中心性空胞化は消失し,胆汁栓,胆管周囲炎及び胆管細胞の肥大が50 mg/kg投与群の雄に認められたが,所見の発現頻度及び程度が投与期間終了時より軽減する傾向がみられ,かつ血液化学検査値の変化が消失したことから,可逆性の変化であった.その他,無機リンの有意な低値が50 mg/kg投与群の雄に認められたが,摂餌量の低値によるものと考えられた.回復期間終了時では,この変化は消失した.また,ナトリウムの有意な低値が15 mg/kg以上の投与群の雄に認められたが,その程度は軽微であり,かつ用量との関連はなく,背景データ内(141〜144 mmol/L)であることから,偶発的変化と考えられた.病理学検査では,上記の肝細胞の単細胞壊死,胆汁栓,胆管周囲炎,胆管細胞の肥大及び肝細胞の小葉中心性空胞化に加えて,肝臓重量の高値が50 mg/kg投与群の雌雄,肝臓の暗赤色化が50 mg/kg投与群の雄に認められ,組織学的に肝細胞の小葉中心性肥大が5及び15 mg/kg投与群の雄及び50 mg/kg投与群の雌雄に観察された.肥大した肝細胞の細胞質は空胞の領域を除けばスリガラス様であり,かつ肥大の領域が小葉中心性であること,また,同変化が雄に強くみられていることから,薬物代謝の亢進時にみられる滑面小胞体の増生による機能的適応と考えられた.回復期間終了時では,上記の肝臓における剖検所見は消失し,器官重量及び肝細胞の小葉中心性肥大の発現頻度または程度が軽減したことから,肝細胞肥大には回復性が認められた.
これらの結果から,本試験における1,3,5-トリス(2-プロペニル)イソシアヌル酸の無影響量は雄で5 mg/kg/ day未満,雌で15 mg/kg/dayと判定された.
| 連絡先 |
| 試験責任者: | 石田 茂 |
| 試験担当者: | 下山泰史,畠山和久,枝元 洋,
津田敏治,勝亦倶慶 |
| (株)ボゾリサーチセンター御殿場研究所 |
| 〒412-0039 静岡県御殿場市かまど1284 |
| Tel. 0550-82-2000 | Fax. 0550-82-2379 | |
| Correspondence |
| Authors: | Shigeru Ishida(Study director)
Yasushi Shimoyama,
Kazuhisa Hatayama
Hiroshi Edamoto, Toshiharu Tsuda
Toyohisa Katsumata |
| Gotemba Laboratory, Bozo Research Center Inc. |
| 1284, Kamado, Gotemba-shi, Shizuoka, 412-0039, Japan |
| Tel +81-550-82-2000 | Fax +81-550-82-2379 | |
 ホームケージ内観察
ホームケージ内観察 ホームケージ内観察
ホームケージ内観察 手に持っての観察
手に持っての観察 オープンフィールド内観察
オープンフィールド内観察






