1,3-ジフェニルグアニジンはゴム製品製造過程で使用されている化合物である.今回,既存化学物質の安全点検に関わる毒性調査事業の一環として,1,3-ジフェニルグアニジンについてSD系[Crj:CD(SD)IGS]ラットを用い,0,10,30および90 mg/kgの用量で28日間反復経口投与毒性試験を実施した.なお,対照群および90 mg/kg群にはそれぞれ雌雄各5匹の14日間回復群を設けた.
雌雄とも,90 mg/kg群で投与期間中に切迫解剖あるいは死亡例が認められた.雄では4週に1例が死亡し,雌では2〜4週に7例が切迫解剖あるいは死亡し,死亡率は雄で10 %,雌で70 %であった.病理学検査の結果,死因に結びつく変化は認められなかった.
一般状態の観察では,雌雄の30 mg/kg群で流涎,90 mg/kg群で流涎,腹臥位,側臥位,よろめき歩行,自発運動低下および驚愕反射が認められた.さらに,雌の90 mg/kg群の切迫解剖例あるいは死亡例では削痩,後肢の脱毛および被毛の汚れなども観察された.投与期間中に観察された症状は回復期間では観察されず,回復性を示した.
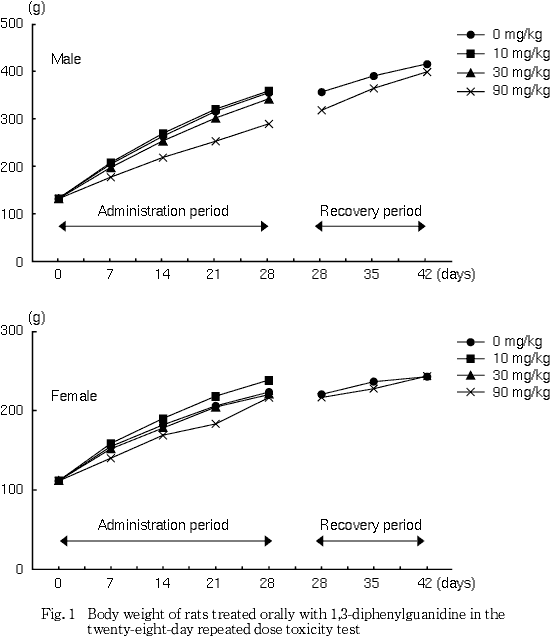
体重および摂餌量は,雌雄とも90 mg/kg群で投与期間中に有意な低値または低値傾向が認められ,投与4週間の体重増加量および総摂餌量にも有意な低値または低値傾向が認められた.いずれの変化も回復期間中には回復性が認められた.
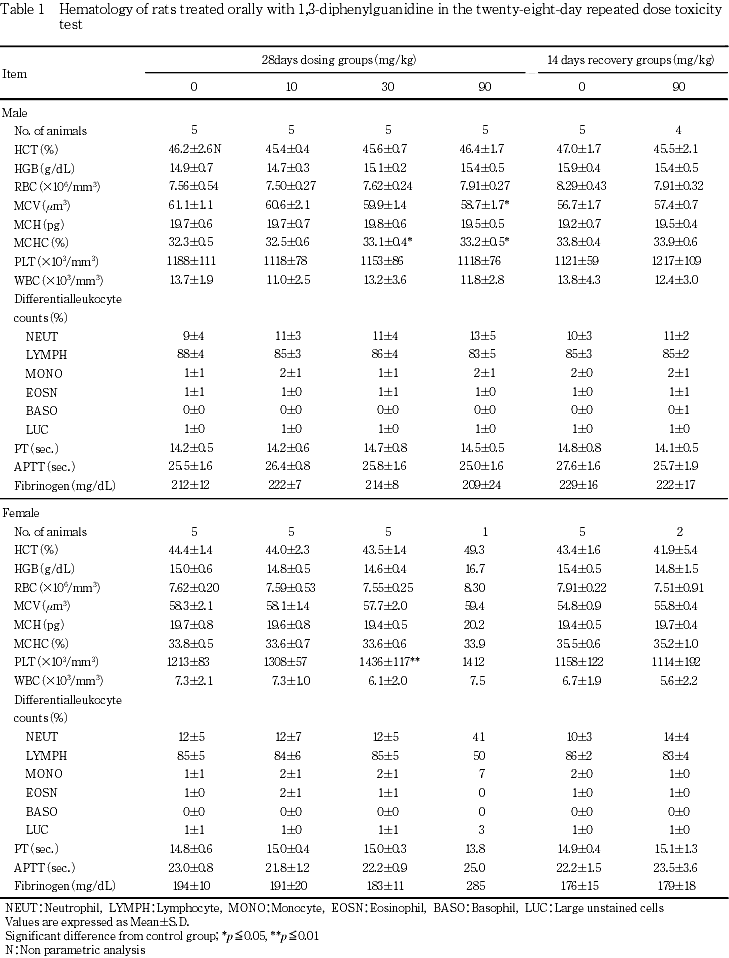
血液学検査の結果,雄では被験物質投与の影響は認められなかった.雌では30 mg/kg群で血小板数の有意な高値が認められ,90 mg/kg群の生存した1例でヘマトクリット値,ヘモグロビン量,赤血球数,血小板数,好中球比率,単球比率および大型非染色細胞比率の高値傾向,リンパ球比率の低値傾向が認められた.回復期間終了時では,雌雄とも対照群と被験物質投与群との間で有意な差は認められなかった.
血液凝固能検査の結果,雌の90 mg/kg群で投与終了時まで生存した1例でフィブリノーゲン量の高値傾向が認められたが,これを除き雌雄とも対照群と被験物質投与群との間で差は認められなかった.
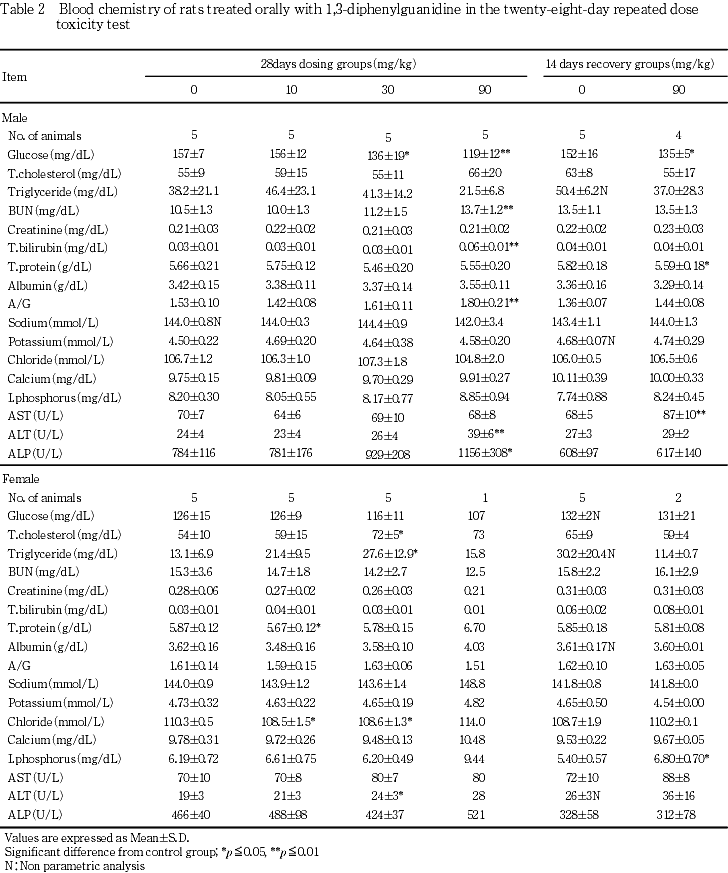
血液生化学検査の結果,雄では30および90 mg/kg群で血糖の有意な低値,90 mg/kg群で尿素窒素,総ビリルビン,A/G比,ALTおよびアルカリホスファターゼの有意な高値が認められた.雌の90 mg/kg群で投与終了時まで生存した1例で総コレステロール,総蛋白,アルブミン,ナトリウム,塩素,カルシウム,無機リンおよびALTの高値傾向が認められた.回復期間終了時には,雄の90 mg/kg群で血糖の僅かな低値が認められた.
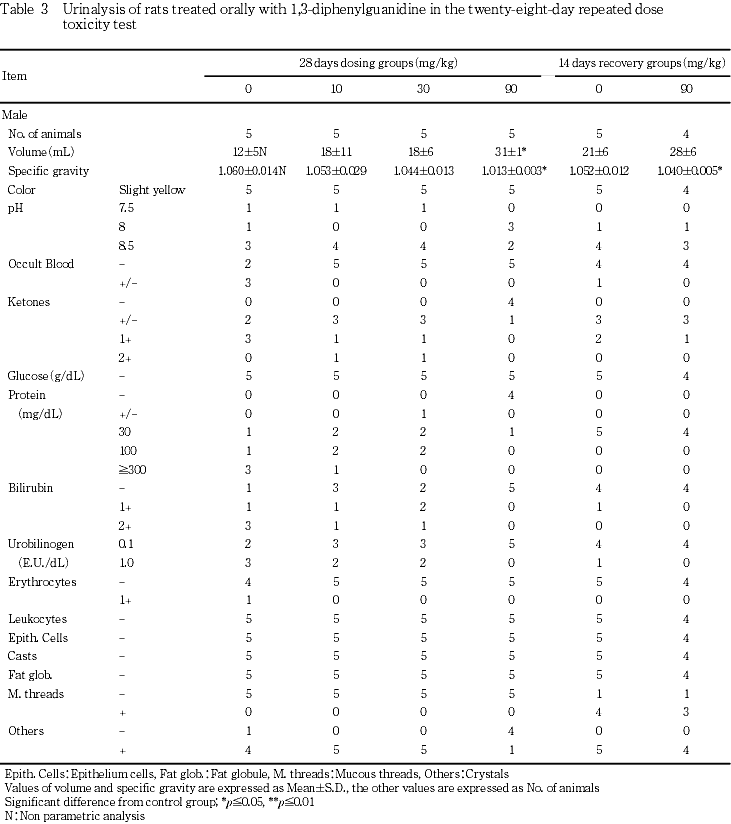
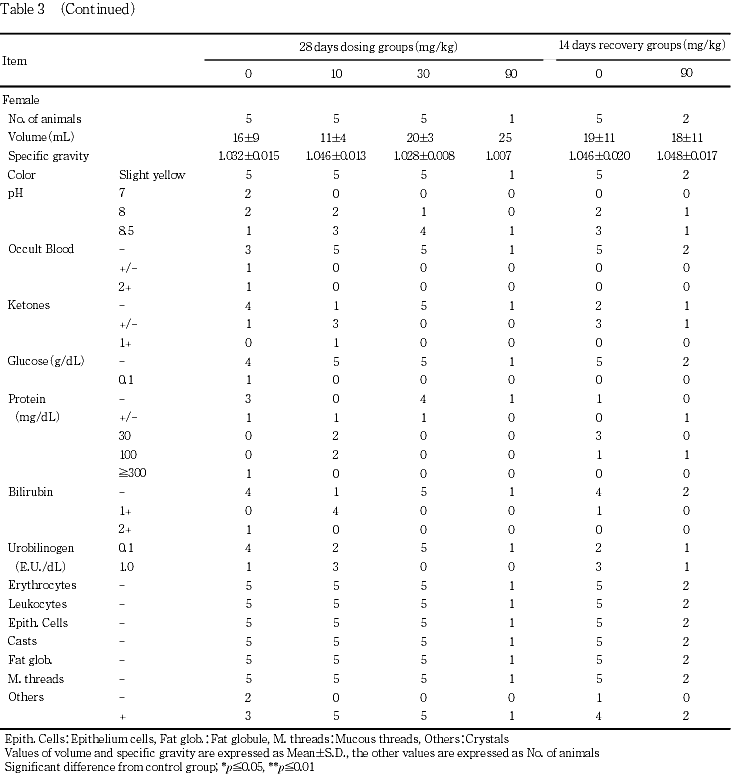
尿検査の結果,雌雄の90 mg/kg群で尿量の増加と比重の低下が認められ,さらに雄ではケトン体と蛋白の陰性例が増加した.回復期間終了時には,雄の90 mg/kg群で比重の有意な低値が認められた.
器官重量測定の結果,被験物質投与の明確な影響を示唆する変化は認められなかった.
病理学検査の結果,剖検所見では,切迫および死亡動物で削痩が観察された.また,毒性学的意義は不明であるが雄の30および雌雄の90 mg/kg群で肝臓の褐色化,雌雄の90 mg/kg群で鼓室胞の赤色化が観察された.組織学検査では,雌雄の90 mg/kg群で腎臓の集合管の水腫様変化が認められた.切迫および死亡動物では,子宮に未成熟の所見が高率に発生し,一方,発生数は少なかったが胸腺の萎縮あるいは核崩壊,肺の水腫あるいは出血,肝臓の鬱血あるいは壊死および腎臓の管腔拡張も認められた.また,毒性学的意義は明らかでないが,雄の30および90 mg/kg群で肝臓の脂肪化の減少が認められた.
以上の結果,本試験条件下における1,3-ジフェニルグアニジンの無影響量(NOEL)は雌雄とも10 mg/kg/dayと考えられた.
[用量設定理由]
用量設定のための2週間反復投与試験を0,3,10,30および90 mg/kgの5用量で実施した結果,高用量の90 mg/kg群では雌雄とも体重および摂餌量の低下,流涎および側臥位などの変化が認められ,雌の1例が最終投与後に死亡した.したがって,28日間反復投与毒性試験の高用量は本試験の高用量である90 mg/kgとし,以下公比3で除し,中用量を30 mg/kg,低用量を10 mg/kgと設定した.
病理組織学検査は固定した器官・組織のうち,全動物の脳,脊髄,胸腺,心臓,肺(気管支を含む),気管,肝臓,脾臓,腎臓,副腎,胃,精巣,精巣上体,子宮,卵巣,骨髄(大腿骨),坐骨神経および肉眼観察で変化の認められた鼓室胞について実施した.検査は,常法に従って薄切標本を作製し,ヘマトキシリン・エオジンで染色した後,鏡検した.
回復期間中には,雌雄とも対照群および90 mg/kg群で死亡例は認められなかった.
雌では,30 mg/kg群で流涎が投与8日より5例全例に単発的あるいは断続的に認められ,下顎部の外傷が投与15日より投与終了時まで5例中1例に連続的に観察された.90 mg/kg群では流涎が投与5日から10例全例に散発的あるいは断続的に発現した.さらに,腹臥位が投与8日より10例中5例,側臥位が投与3日より10例中9例,よろめき歩行が投与3日より10例全例,自発運動低下が投与4日より10例中5例,驚愕反射が投与9日より10例中7例に単発的あるいは断続的に認められた.さらに,削痩が投与12日に死亡した1例の死亡前2日間および投与12日に切迫解剖した1例の解剖前3日間,後肢の脱毛が投与25日に死亡した1例の死亡前17日間,被毛の汚れが投与13日に死亡した1例の死亡前日および投与16日に切迫解剖した1例の解剖当日,歯の欠損が投与13日に死亡した1例の死亡前日に認められた.
回復期間では,雌雄いずれの群にも異常を示す動物は観察されなかった.
雌では,90 mg/kg群で投与1週に有意な低値を示し,その後も低値傾向であった.回復期間は2例であったが,順調な体重増加が認められ,回復期間中の体重増加量は対照群を上回った.

雌では,90 mg/kg群で投与1〜3週に有意な低値,さらに投与期間中の総摂餌量が低値傾向を示したが,回復期間においては有意な高値を示した.
雄では,30および90 mg/kg群でMCHCが有意な高値を示し,90 mg/kg群ではMCVが有意な低値を示したが,ヘマトクリット値,ヘモグロビン量および赤血球数に有意な変化はなく,毒性学的意義はないと考えられた.
雌では,30 mg/kg群で血小板数が有意な高値を示し,90 mg/kg群では測定が1例であるもののヘマトクリット値,ヘモグロビン量,赤血球数,血小板数,好中球比率,単球比率および大型非染色細胞比率が高値傾向を示し,リンパ球比率が低値傾向を示した.
[回復期間終了時の検査結果]
雌雄とも対照群と被験物質投与群で差が認められなかった.
雄では対照群と被験物質投与群で差が認められなかった.
雌では,90 mg/kg群で測定が1例であるものの対照群に比較してフィブリノーゲン量が高値傾向を示した.
[回復期間終了時の検査結果]
雌雄とも対照群と被験物質投与群で差が認められなかった.
[投与期間終了時の検査結果]
雄では30および90 mg/kg群で血糖が有意な低値を示し,さらに90 mg/kg群では尿素窒素,総ビリルビン,A/G比,ALTおよびアルカリホスファターゼが有意な高値を示した.
雌では,30 mg/kg群で総コレステロール,中性脂肪およびALTが有意な高値を示した.その他,10 mg/kg群の総蛋白,10および30 mg/kg群で塩素が有意な低値を示したが用量に対応しない変化であった.90 mg/kg群では,測定が1例であるものの対照群に比較して総コレステロール,総蛋白,アルブミン,ナトリウム,塩素,カルシウム,無機リンおよびALTが高値傾向を示した.
[回復期間終了時の検査結果]
雄では,90 mg/kg群で血糖および総蛋白が有意な低値を示し,ASTが有意な高値を示した.
雌では,90 mg/kg群で無機リンが有意な高値を示した.
雄では,90 mg/kg群で尿量が有意に増加し,比重が有意な低値を示した.さらに,同群ではケトン体および蛋白の陰性例が増加した.
雌では,90 mg/kg群では測定が1例であるものの対照群に比較して尿量が増加し,比重が低値傾向を示した.
[回復期間終了時の検査結果]
雄では,90 mg/kg群で比重が有意な低値を示した.
雌では,対照群と被験物質投与群で差が認められなかった.
雄では,90 mg/kg群で脳,心臓,肝臓,腎臓および脾臓重量が有意な低値,胸腺重量が低値傾向を示した.その他,10および30 mg/kg群で副腎重量が有意な低値を示したが用量に対応しない変化であった.
雌では,90 mg/kg群で測定が1例であるものの対照群に比較して胸腺重量が低値傾向を示した.
[回復期間終了時の検査結果]
雄では,90 mg/kg群で脳重量が有意な低値を示した.
雌では,90 mg/kg群で副腎重量が有意な高値を示した.
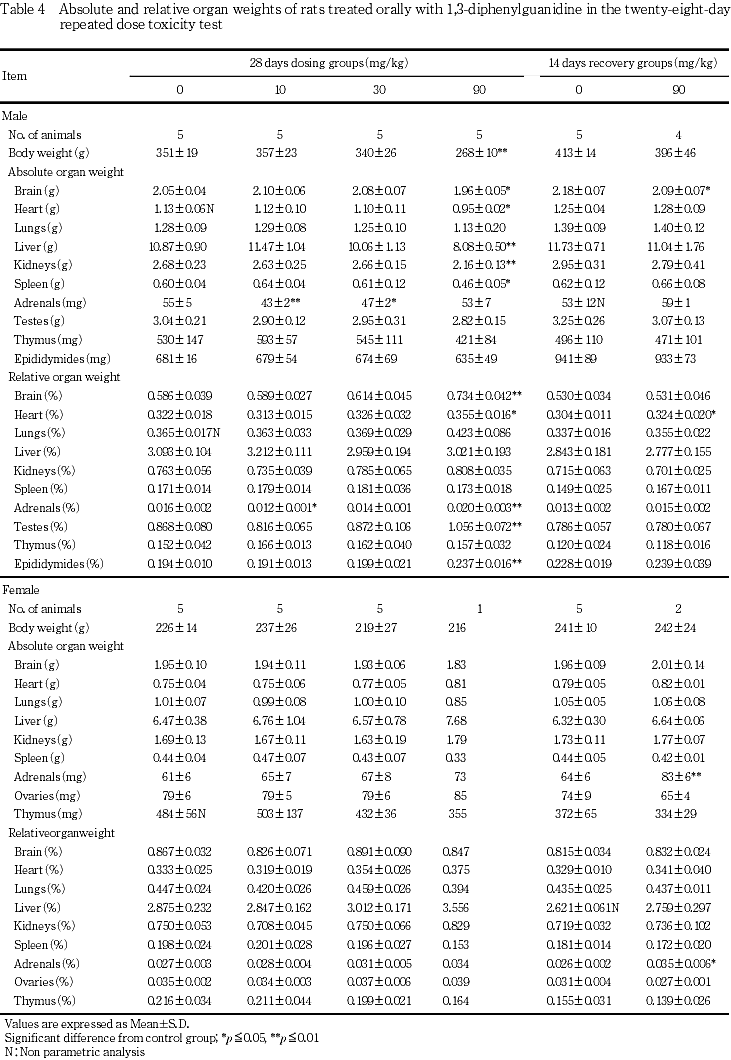
雄では,90 mg/kg群で脳,心臓,副腎,精巣および精巣上体の相対重量が有意な高値を示した.その他,10 mg/kg群で副腎の相対重量が有意な低値を示したが用量に対応しない変化であった.
雌では,90 mg/kg群で測定が1例であるものの対照群に比較して胸腺の相対重量が低値傾向を示した.
[回復期間終了時の検査結果]
雄では,90 mg/kg群で心臓の相対重量が有意な高値を示した.
雌では,90 mg/kg群で副腎の相対重量が有意な高値を示した.
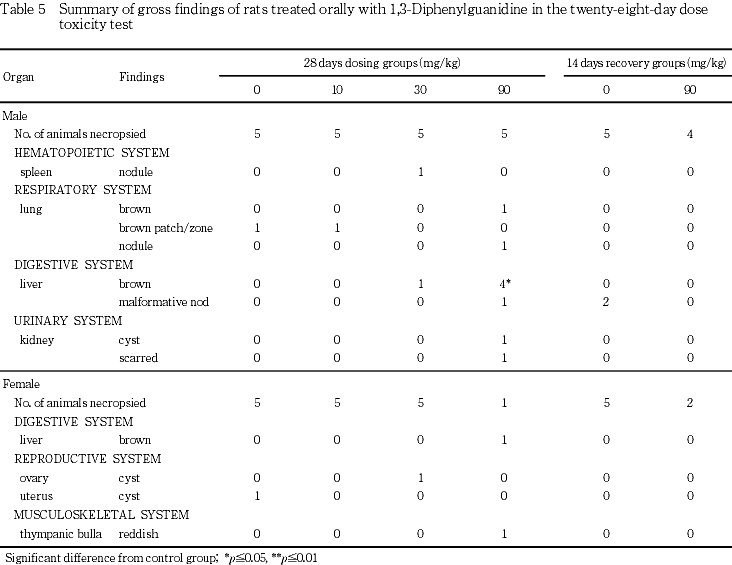
対照群と比較して,90 mg/kg群の雄で肝臓の褐色化の発生数が有意に増加した.つまり,肝臓の褐色化は90 mg/kg群で雄の4例(p≦0.05)および雌の1例,30 mg/kg群で雄の1例に観察された.また,鼓室胞の赤色化が90 mg/kg群で雌の1例に観察された.その他の変化はいずれも単発性あるいは少数例の発生であった.
[回復期間終了時計画解剖動物]
肝臓の奇形結節が対照群で雄の2例に観察されたのみであった.
[切迫および死亡動物]
鼓室胞の赤色化が雌雄各1例,肺の赤色斑/区域および全身の削痩が雌の2例に観察された.その他,心臓の白色斑点/区域,胸腺の萎縮,肺の黒色斑点/区域あるいは赤色化,小腸の白色化,歯の欠落,眼球の白色化および脱毛が雌で観察されたが,いずれも単発性の発生であった.
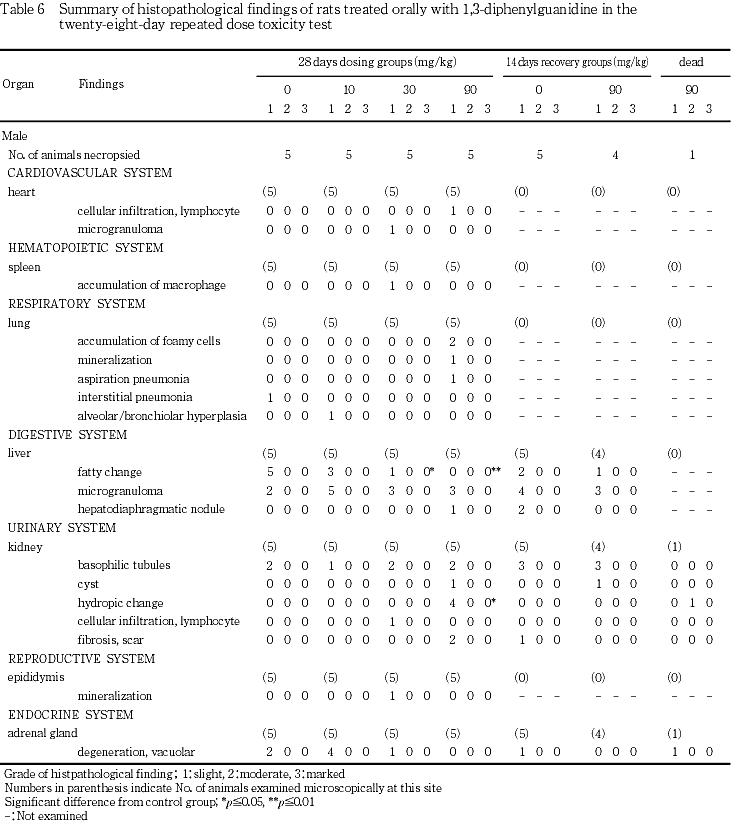
対照群と比較して,90 mg/kg群の雄で腎臓の集合管の水腫様変化の発生数が有意に増加(p≦0.05)し,30および90 mg/kg群の雄で肝臓の脂肪化の発生数が有意に減少(それぞれp≦0.05およびp≦0.01)した.つまり,腎臓の集合管の水腫様変化は90 mg/kg群で雄の4例および雌の1例,肝臓の脂肪化は対照群,10,30および90 mg/kg群で雄ではそれぞれ5,3,1および0例,雌では4,5,3および1例に認められた.また,肝臓の小肉芽腫が対照群で雄の2例および雌の5例,10 mg/kg群で雌雄各5例,30 mg/kg群で雌雄各3例,90 mg/kg群で雄の3例および雌の1例,副腎の空胞変性が対照群で雄の2例,10 mg/kg群で雄の4例,30 mg/kg群で雄の1例に認められた.その他の変化はいずれも単発性あるいは少数例の発生であった.
[回復期間終了時計画解剖動物]
肝臓の小肉芽腫が対照群で雄の4例および雌の5例,90 mg/kg群で雄の3例および雌の1例,腎臓の尿細管好塩基化が対照群で雄の3例および雌の2例,90 mg/kg群で雄の3例に認められた.その他の変化はいずれも単発性あるいは少数例の発生であった.
[切迫および死亡動物]
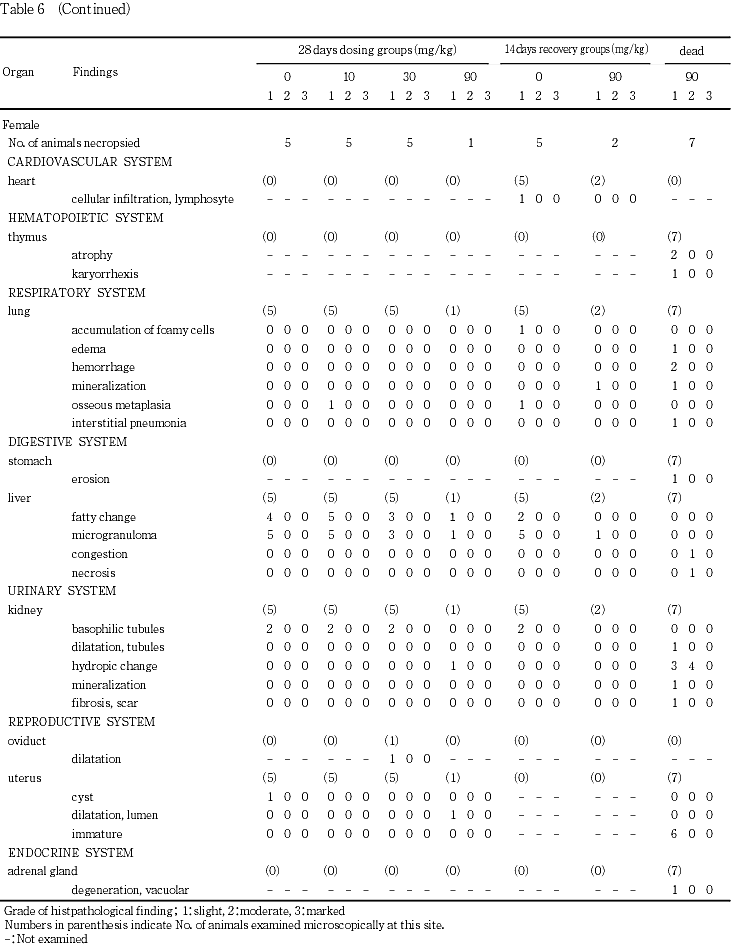
腎臓の集合管の水腫様変化が雄の1例および雌の7例に認められ,そのうち中等度であった雄の1例および雌の4例については,遠位尿細管にも同様な変化が認められた.また,子宮の未成熟が雌の6例に認められた.その他,胸腺の萎縮あるいは核崩壊,肺の水腫,出血,鉱質沈着あるいは間質性肺炎,胃の糜爛,中等度な肝臓の鬱血および壊死,腎臓の管腔拡張,鉱物沈着あるいは瘢痕性線維化および副腎の空胞変性が認められたが,いずれも単発性あるいは少数例の発生であった.
一般状態の観察では,30および90 mg/kg群の全例に流涎が認められたが,1,3-ジフェニルグアニジンには粘膜刺激性のあることが報告されている4)ので,この流涎は被験物質投与による変化と考えられた.90 mg/kg群の生存例では流涎の他に腹臥位,側臥位,よろめき歩行,自発運動低下,驚愕反射および鼻端の汚れが認められた.これらの症状はいずれも回復期間には認められず,被験物質投与の影響と考えられた.雌の30 mg/kg群の1例に発生した下顎部の外傷は自傷,90 mg/kg群の1例に発生した
歯の欠損は事故によるものと考えられた. 体重および摂餌量は,雌雄とも90 mg/kg群で投与期間中に低値または低値傾向が認められ,投与4週間の体重増加量および総摂餌量にも低値または低値傾向が認められた.いずれの変化も回復期間中には回復が認められた.
血液学検査および血液凝固能検査の結果,雄では被験物質投与の影響は認められなかった.雌の90 mg/kg群の生存した1例でヘマトクリット値,ヘモグロビン量,赤血球数,血小板数,好中球比率,単球比率および大型非染色細胞比率の高値傾向,リンパ球比率の低値傾向,さらに,血液凝固能検査ではフィブリノーゲン量の高値傾向が認められた.これらの変化からこの動物における軽度の血液濃縮と炎症の可能性が示唆された.また,雌の30 mg/kg群で認められた血小板数の有意な高値は,上記の90 mg/kg群の動物1例でも高値傾向であり,機序は不明であるが,被験物質による変化であると考えられた.
血液生化学検査の結果,雄の30および90 mg/kg群で血糖の低値が認められ,機序は不明であるが,被験物質投与による影響が示唆された.さらに,雄の90 mg/kg群で認められた尿素窒素の高値も被験物質投与による影響と考えられたが,クレアチニンの高値を伴わなかったことから腎臓への影響による変化とは考えられず,その機序は不明であった.雄の90 mg/kg群で認められた総ビリルビンおよびアルカリホスファターゼの高値,雄の90 mg/kg群と雌の30および90 mg/kg群で認められたALTの高値あるいは高値傾向は,被験物質投与による影響と考えられたが,病理学検査では胆道系の変化を含めてこれらを示唆する変化は認められなかった.雄の90 mg/kg群で認められたA/G比の高値は総蛋白やアルブミンの変化を伴わなかったことから毒性学的意義はないと考えられた.雌の90 mg/kg群の生存した1例で総コレステロール,総蛋白,アルブミン,ナトリウム,塩素,カルシウムおよび無機リンの高値傾向が認められたが,この動物の全身状態の悪化を反映した変化であると考えられた.また,雌の30 mg/kg群で認められた総コレステロールおよび中性脂肪の高値は僅かな変化であったが被験物質投与による影響と考えられた.回復期間終了時には,雄の90 mg/kg群で血糖の低値が認められたが,投与終了時の値と比較すると低下の程度は僅かであった.90 mg/kg群で認められた雄のASTの高値および総蛋白の低値,雌の無機リンの高値はいずれも軽微な変化であり,さらにASTの高値および総蛋白の低値は投与終了時には認められなかった変化でもあることから,被験物質投与との関連は示唆されなかった. 尿検査の結果,雌雄の90 mg/kg群で尿量の増加傾向と比重の低下が認められ,腎集合管の水腫様変化によって水分の再吸収が阻害されたことによる変化とも考えられたが,その機序は不明であった.さらに,雄の90 mg/kg群におけるケトン体と蛋白の陰性例の増加は尿量の増加に起因すると考えられた.回復期間終了時には,雄の90 mg/kg群で比重の低下が認められたが尿量の僅かな増加によるもので,投与終了時の値と比較すると低下の程度は僅かであった.
器官重量測定の結果,雄の90 mg/kg群で脳,心臓,肝臓,腎臓および脾臓重量が低値,胸腺重量が低値傾向を示したが,脳および心臓については相対重量はむしろ高値を示し,肝臓,腎臓,脾臓および胸腺については相対重量に変化は認められなかった.また,雄の90 mg/kg群では,副腎,精巣および精巣上体の相対重量が高値を示し,雌の90 mg/kg群では胸腺の実重量および相対重量が低値傾向を示したがいずれも軽微な変化であり,病理学検査でも対応する変化は認められず,被験物質投与による影響とは考えられなかった.
回復期間終了時の結果では,雄の90 mg/kg群で脳重量が低値,心臓の相対重量が高値を示したが軽微な変化であった.また,90 mg/kg群の雌では,副腎の実重量ならびに相対重量が高値を示したが,投与終了時には認められなかった変化であり,被験物質投与による影響とは考えられなかった.
病理学検査の結果,剖検所見で被験物質投与による影響と考えられる変化は,雌の切迫および死亡動物で観察された全身の削痩であった.また,肝臓の褐色化が雄の30および雌雄の90 mg/kg群で,鼓室胞の赤色化が雌雄の90 mg/kg群で観察されたが,組織学検査では対応する変化が認められず,毒性学的意義は不明であった.
組織学検査で被験物質投与によると考えられる変化は,腎臓の水腫様変化,肝臓の脂肪化の減少および子宮の未成熟であった.加えて,単発性あるいは少数例の発生であったが,切迫あるいは死亡動物で認められた胸腺の萎縮あるいは核崩壊,肺の水腫あるいは出血,肝臓の鬱血あるいは壊死および腎臓の管腔拡張などの変化も被験物質投与による変化と考えられた.このうち腎臓の水腫様変化については雌雄ともに90 mg/kg群で主に集合管で認められたが,切迫および死亡動物では程度が増強し遠位尿細管でも認められた.集合管あるいは遠位尿細管などのネフロンの末梢部では他の部位に比べ化学物質やその代謝物の濃度が高くなることから,被験物質あるいはその代謝物の直接的な影響も考えられるが,同部位では腎血流の末梢であることやプロスタグランジンあるいはアルドステロンなどの副腎皮質ホルモンの影響も受け易い部位でもあるため,それらを介した二次的な影響も否定できなかった.肝臓の脂肪化の減少については雄の30および90 mg/kg群で認められ,剖検所見における肝臓の変化として褐色化が同群で認められたが,脂肪化以外に肝細胞あるいは胆管系に器質的変化は認められないことから,何らかの機能的な変化の可能性については否定できず,毒性学的意義についても不明であった.子宮の未成熟については,切迫および死亡動物にのみ高率に認められた.切迫および死亡動物では剖検時の体重が計画解剖動物に比べて明らかに少ないことから,被験物質投与による全身状態の悪化が発育途上の子宮に対し成熟抑制をもたらしたと考えられた.また,切迫あるいは死亡動物で認められた変化のうち胸腺については全身状態の悪化,肺および肝臓については循環障害,腎臓については集合管病変にそれぞれ起因した病変と考えられた.
その他,対照群を含め観察された変化は明らかな用量相関性がないか発生数も少ないことから自然発生病変と考えられた.
回復期間終了時には,投与終了時に認められた被験物質投与に関連すると考えられる変化は認められず,観察された変化はいずれも自然発生病変と考えられた.
また,一般状態の観察において驚愕反射などの神経症状が発現したことから,脳(脳幹を含む割面),脊髄および坐骨神経について組織学検査を行ったが,被験物質投与によると考えられる変化は認められなかった.
以上の結果,30 mg/kg群の雌雄で流涎,雌で血小板数の有意な高値,雄で血糖の有意な低値が認められたことから,無影響量(NOEL)は雌雄とも10 mg/kg/dayと判断された.
| 1) | 佐野正樹,岡山佳弘,医薬安全性研究会会報,32,21(1990). |
| 2) | M. Yoshida, J. Japanese. Soc. Comp. Stat., 1, 111(1988). |
| 3) | 倍味繁,稲葉太一,医薬安全性研究会会報,40, 33(1994). |
| 4) | R. E. Lenga, “The Sigma-Aldrich Library of Chemical Safety Data,” 3, Vol.1, ed. by E. L. Robert, Sigma-Aldrich Corporation, Milwaukee, Wisconsin, 1988, p.1457. |
| 連絡先 | |||
| 試験責任者: | 村田共治 | ||
| 試験担当者: | 各務 進,伊賀達也,向井大輔,長谷川和成,大橋信之 | ||
| (財)食品農医薬品安全性評価センター | |||
| 〒437-1213 静岡県磐田郡福田町塩新田字荒浜582-2 | |||
| Tel 0538-58-1266 | Fax 0538-58-1393 | ||
| Correspondence | ||||
| Authors: | Kyoji Murata(Study director) Susumu Kakamu, Tatsuya Iga, Daisuke Mukai, Kazushige hasegawa, Nobuyuki Oohashi | |||
| Biosafety Research Center, Foods, Drugs and Pesticides(An-pyo Center) | ||||
| 582-2 Arahama, Shioshinden, Fukude-cho, Iwata-gun, Shizuoka, 437-1213, Japan | ||||
| Tel +81-538-58-1266 | Fax +81-538-58-1393 | |||