ジシクロヘキシルアミンのラットを用いる経口投与簡易生殖毒性試験
Preliminary Reproduction Toxicity Screening Test of Dicyclohexylamine
by Oral Administration in Rats
要約
ジシクロヘキシルアミンは,シクロヘキサノールやアニリンを原料として合成され,染料,ゴム製品等の合成過程での触媒並びにボイラーの錆防止剤や軟鋼の腐食防止を目的とする気相抑制剤として用いられる鎖式アミンである.ジシクロヘキシルアミンは,ラット精細管を用いた試験において,アドレナリンa受容体遮断作用に対する保護作用1),ノルアドレナリンの反応に対する増強作用2, 3)を有することが知られている.また,ジシクロヘキシルアミンは,眼,咽喉,鼻の粘膜に対する刺激性を有し,ラットにおける急性経口投与によるLD50値は,373 mg/kg,ラットにおける28日間反復経口投与試験の無影響量は,20 mg/kg/dayであることが明らかになっている4).
そこで今回,ジシクロヘキシルアミンのラットにおける経口投与簡易生殖毒性試験を行ない,雌雄動物の性腺機能,交尾行動,受胎及び分娩などの生殖発生に及ぼす影響について検索した.投与量は,80 mg/kgを高用量とし,以下40及び20 mg/kgとした.対照として媒体(コーンオイル)投与群を設けた.
1. 反復投与毒性
雄では,80 mg/kg群において体重増加が抑制されたが、一般状態,摂餌量,剖検所見,精巣及び精巣上体重量並びにこれら器官の病理組織学検査所見に被験物質投与の影響は認められなかった.40 mg/kg以下の投与群には一般状態,体重,摂餌量,剖検所見,精巣及び精巣上体重量に被験物質投与の影響は認められなかった.
雌では,80 mg/kg群において妊娠21日及び22日に各1例が死亡した.同群では一般状態の変化として,哺育期間に粗毛,児集め不良が認められた.交配前投与期間,妊娠期間及び哺育期間の各期間における体重は増加が抑制され,摂餌量は低値を示した.しかし,剖検所見及び卵巣の病理組織学検査所見に被験物質投与の影響は認められなかった.40 mg/kg以下の投与群には一般状態,体重,摂餌量及び剖検所見に被験物質投与の影響は認められなかった.
2. 生殖発生毒性
親動物に関して,雌の性周期,雌雄の交尾及び受胎,妊娠期間及び分娩に及ぼす被験物質投与の影響は認められなかった.哺育異常として,80 mg/kg群では児集め不良の母動物が多く認められ,哺育4日までに生存児を有していた母動物は4例のみであった.しかし,哺育の異常は,40 mg/kg以下の投与群には認められなかった.生児出産雌数,出産率,黄体数,着床痕数及び着床率に被験物質投与の影響は認められなかった.
新生児では,80 mg/kg群では死産児数が多く,生存児数が少ないため出生率は有意に低下したが,40 mg/kg以下の投与群には生存児数,死産児数及び出生率に及ぼす被験物質投与の影響は認められなかった.分娩率に被験物質投与の影響は認められなかった.新生児の性比に及ぼす被験物質投与の影響は認められず,被験物質投与に起因する外表異常も認められなかった.80 mg/kg群では,哺育期間中の児の死亡が多く,同群の新生児の4日の生存率は,著しい低値を示した.同群における新生児の体重は,雌雄とも哺育0日及び4日に低値を示した.しかし,40 mg/kg以下の投与群には新生児の生存率及び体重に及ぼす被験物質投与の影響は認められなかった.
以上の成績から,ジシクロヘキシルアミンの一般毒性学的な無影響量は,雌雄ともに40 mg/kg/dayであると判断される.また,生殖発生毒性学的な無影響量は,雄に関しては80 mg/kg/day,雌に関しては40 mg/kg/day,新生児に関しては40 mg/kg/dayであると判断される.
方法
1. 被験物質
被験物質は,本州化学工業(株)(和歌山)より提供されたジシクロヘキシルアミン(ロット番号:970924,純度:99.89 %,無色透明の液体)を用い,開封後は窒素置換し冷蔵保存した.なお,動物試験終了後の被験物質については製造元で分析した結果,動物試験期間中安定であったことが確認された.
被験物質は,コーンオイル(ナカライテスク(株))に溶解して4,8及び16 mg/mL濃度になるように投与液を調製した.なお,本被験物質の4及び40 mg/mL濃度のコーンオイル溶液は,冷蔵(約4℃)・遮光下8日間保存後,更に室温・遮光下24時間保存条件下で安定であることが確認されていることから,調製は週1回の頻度で行い,調製後の被験液は使用までの間,冷蔵(約4℃),遮光下で保存した.
被験液の濃度確認は,投与開始前及び雄の投与最終週の2回,投与に使用する各濃度の被験液について実施した結果,表示値に対する割合は,いずれも97〜101 %の範囲内であり,ほぼ設定濃度のジシクロヘキシルアミンが含有されていたことを確認した.
2. 使用動物及び飼育条件
試験には,雌雄とも日本チャールス・リバー(株)より購入したSprague-Dawley系ラット(Crj:CD, SPF)を使用した.動物は,購入後7日間検疫・馴化飼育した後,一般状態に異常がなく体重増加が良好で,さらに雌では性周期に異常が認められないものを試験に供した.群分け時の体重範囲は,雄で306〜335 g,雌で201〜224 gであった.
動物は,温度23±3℃,相対湿度50±20 %,換気回数1時間10〜15回,照明1日12時間(午前7時〜午後7時)の飼育室で飼育した.動物は,交配期間及び妊娠17日から哺育4日までの期間を除きブラケット式金属製網ケージ(リードエンジニアリング(株))に個別に収容し、飼育した.妊娠17日以降の母動物は,哺育4日まで床敷(ホワイトフレーク,日本チャールス・リバー(株))を入れたプラスチック製エコンケージ(日本クレア(株))に母児共に収容した.飼料は固形飼料NMF(オリエンタル酵母工業(株)),飲料水は水道水(御殿場市営水道水)を自由に摂取させた.
3. 投与量,群構成、投与期間及び投与方法
ジシクロヘキシルアミンの投与量は,先に実施した予備試験の結果を参考にして決定した.すなわち,0,20,40,80及び160 mg/kgを雄及び雌に2週間反復経口投与したところ,160 mg/kg群では雄5例中2例,雌5例中4例が死亡した.80 mg/kg群では死亡例は認められなかったが,一般状態観察において雌雄とも流涎が認められた.同群の体重及び摂餌量は,雄には明らかな変化は認められなかったが,雌では体重増加抑制,摂餌量の低値傾向が認められた.しかし,雌の性周期,剖検所見及び器官重量に被験物質投与の影響は認められなかった.20及び40 mg/kg群では,40 mg/kg群において流涎が認められた以外に明らかな被験物質投与の影響は認められなかった.したがって,本試験における高用量は,雌の体重及び摂餌量に被験物質投与の影響が認められたが,死亡例のなかった80 mg/kgとし,以下,公比2で除して中及び低用量には40及び20 mg/kgを設定した.対照群を加え4群とし,1群当たりの動物数は,雌雄各12匹とした.
投与経路は,経口投与を選択した.また,投与回数は1日1回とし,雄は交配前14日間,その後剖検前日までの49日間,雌は交配前14日間,交配期間及び妊娠期間を通して哺育3日までとした.投与容量は,5 mL/kg体重とし,1日1回,金属製胃ゾンテを用いて,強制経口投与した.対照群には媒体(コーンオイル)を同様に投与した.なお,投与時に分娩中の動物は分娩終了後に投与した.個体毎の投与液量は,雄は各測定日の体重,雌の交配前及び交配期間中は各測定日の体重,妊娠期間中は妊娠0日,7日,14日及び21日の体重,哺育期間中は哺育0日の体重を基準に算出した.
4. 反復投与毒性に関する観察・検査
1) 一般状態の観察
一般状態の観察は,雌雄とも全例について試験期間中毎日行った.
2) 体重
雄の体重は,投与第1,4,8,11,15,22,29,36,43日及び剖検日に測定した.雌の体重は,交配前投与期間については投与第1,4,8,11及び15日,妊娠期間中については妊娠0,7,14及び21日,哺育期間中は哺育0及び4日に測定した.
3) 摂餌量
摂餌量は、雄では体重測定日と同じ日に,雌では交配前投与期間については体重測定日と同じ日,妊娠期間中については妊娠1,7,14及び21日,哺育期間中については哺育1及び4日に残餌量を測定し,前日の給餌量との差から1日摂取量を算出した.なお,交配期間中の摂餌量は測定しなかった.
4) 病理学検査
雄は全例を最終投与の翌日に,雌は生存動物については哺育4日にエーテル麻酔下で腹大動静脈より放血致死させて剖検し,内部器官及び組織を肉眼的に観察した.さらに,雄では精巣及び精巣上体を採取し,重量測定後,ブアン液に固定した.雌では黄体数及び着床痕数を調べ,卵巣及び子宮をリン酸緩衝10 %ホルマリン液に固定し,保存した.また,剖検で異常が認められた器官・組織は,リン酸緩衝10 %ホルマリン液に固定し,保存した.妊娠期間中に死亡した80 mg/kg群の2例,全児が死産であったり,哺育期間中に全児が死亡した同群の6例については,発見後,同様に剖検した.
病理組織学検査として,全例の精巣及び精巣上体,卵巣をパラフィン包埋し,対照群及び高用量群について切片を作製して精巣及び精巣上体についてはヘマトキシリン・エオジン染色及びPAS染色を,卵巣についてはヘマトキシリン・エオジン染色を行い,鏡検した.
5. 生殖発生毒性に関する観察・検査
1) 性周期観察及び交配
性周期観察は,全例の雌について投与第1日から交尾が確認されるまで毎日行い、発情期から次の発情期までの日数を調べ,平均性周期を算出した.
交配は,被験物質を交配前14日間にわたって投与した後,同一群の雌雄を1対1の組み合わせで終夜同居させて行った.同居期間は,最長14日間とし,交尾が確認されるまでとした.交尾の確認は,毎朝,腟栓形成あるいは腟スメア中の精子の有無により行い、これらが確認された日を妊娠0日とした.交配結果から、交尾率[(交尾動物数/交配動物数)×100],受胎率[(受胎動物数/交尾動物数)×100]及び交尾までの日数を算出した.
2) 分娩及び哺育観察
交尾が確認された雌は,自然分娩させ,分娩状態を観察した.午前10時30分の時点で分娩が終了していた動物を当該日分娩とし,その日を哺育0日とした.午前10時30分をすぎて分娩が終了した場合は翌日を哺育0日とした.
分娩終了が確認された母動物については出生児を哺育させ,哺育4日まで巣作り,児集め及び授乳の有無を指標にして哺育状態を観察した.これらの結果から,妊娠期間[哺育0日(分娩確認日)-妊娠0日],出産率[(生児出産雌数/受胎動物数)×100],着床率[(着床痕数/黄体数)×100]及び分娩率[(総出産児数/着床痕数)×100]を算出した.
6. 新生児の観察・検査
1) 新生児の観察
哺育0日に生存児数,死産児数を数え,性別及び外表異常の有無を検査した.生存児は全例を母動物に哺育させ,死亡の有無の観察を毎日1回行った.これらの結果から,性比[雄/雌],出生率[(哺育0日の生存児数/総出産児数)×100]及び新生児の4日の生存率[(哺育4日の生存児数/哺育0日の生児数)×100]を算出した.
2) 体重
体重は,哺育0及び4日に測定し,1腹ごとに雌雄の平均値を算出した.
3) 剖検
全例の新生児を哺育4日にエーテル麻酔下で放血致死させて剖検し,内部器官及び組織を肉眼的に観察した.
7. 統計解析
体重,摂餌量,性周期,同居日数,妊娠期間,器官重量,黄体数,着床痕数,出生児数,死産児数、性比,着床率,分娩率,出生率及び新生児の4日の生存率は,Bartlett法により各群の分散の均一性についての検定を行い,分散が均一の場合は一元配置法による分散分析を行い,群間に有意差が認められた場合,Dunnett法を用いて対照群と各投与群との一対比較検定を行った.分散が均一でない場合はKruskal-Wallisの順位検定を行い,有意であれば対照群と各投与群との平均順位の差についてDunnett型の検定を行った.また,交尾率,受胎率及び出産率はχ^2検定を,病理組織学検査における所見の発現頻度及び程度の増強についてはMann-WhitneyのU検定を行った.
有意水準は両側5及び1 %とし,新生児に関するデータは,1腹の平均を標本の単位とした.また,誤投与と考えられた20 mg/kg群の雌1例のデータは交尾率及び受胎率のデータを除いて統計解析から除外した.
結果
1. 反復投与毒性
1) 一般状態
40 mg/kg以下の群では雌雄ともに一般状態の変化は認められなかった.80 mg/kg群では妊娠21及び22日に各1例が死亡した.同群の一般状態の変化として妊娠22日の分娩終了後の投与2時間後に腹臥姿勢,呼吸数減少,体温低下,出生児の児集め不良が1例に認められ,哺育期間中に粗毛が2例,児集め不良が7例に認められた.なお,同群の雌雄ともに投与直後に流涎が多数例において投与第7あるいは8日以降,一時的あるいは継続して観察されたが,同群では他の神経症状が認められていないため,流涎は被験物質投与の影響とは判断しなかった.
2) 体重及び摂餌量(Fig. 1〜4)
40 mg/kg以下の群における体重及び摂餌量には,雌雄ともに被験物質投与の影響は認められなかった.80 mg/kg群では雌雄ともに体重増加が抑制され,摂餌量は雌において交配前投与期間,妊娠期間及び哺育期間の各期間において低値を示す日があり,哺育期に顕著に認められた.しかし,同群の雄における摂餌量には,被験物質投与の影響は認められなかった.
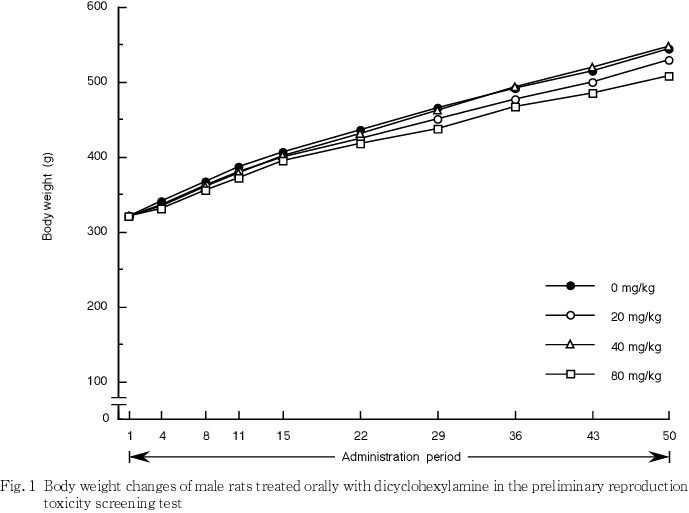
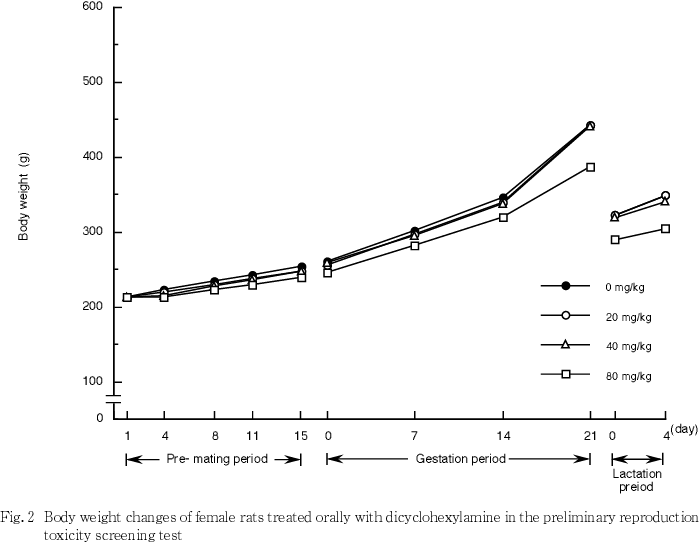
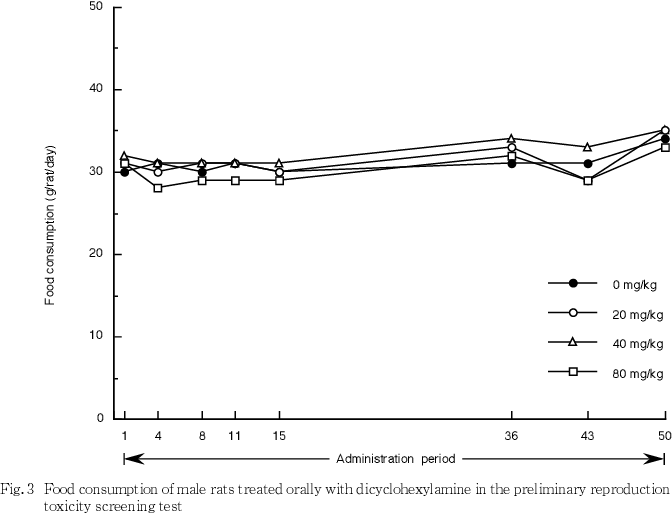
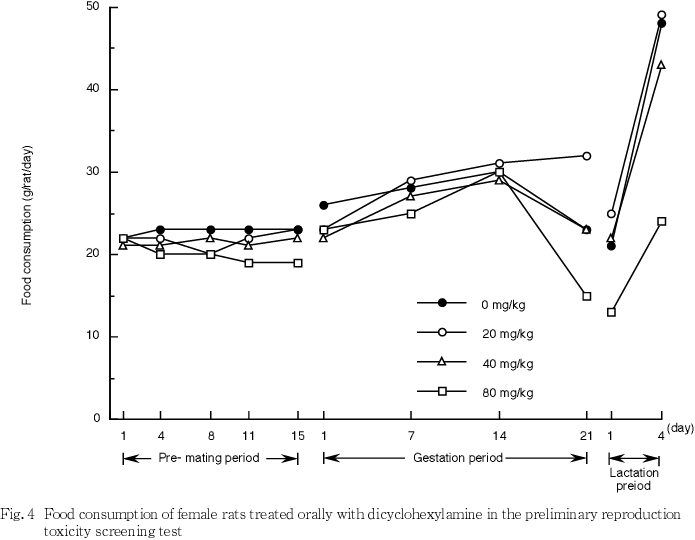
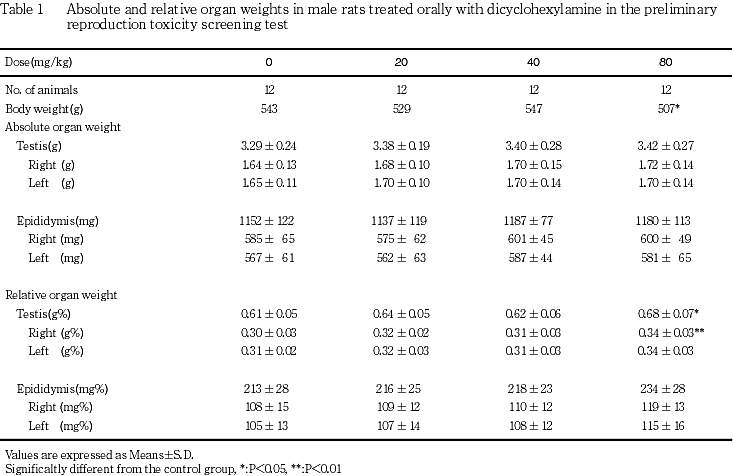
3) 器官重量(Table 1)
精巣及び精巣上体の絶対重量には対照群と被験物質群との間に有意な差は認められなかった.相対重量では80 mg/kg群の精巣重量が高値を示し,右側及び両側の重量に有意な差が認められたが,最終体重の低値に起因した変化であると考えられ,被験物質投与の影響とは考えられなかった.
4) 剖検所見
80 mg/kg群の雄1例に肺の暗赤色点,妊娠22日に死亡した同群の雌1例において横隔膜ヘルニア,腺胃に暗赤色点が認められ,同例の外部所見では粗毛が認められた.しかし,これらの所見は,同群の他の例では認められていないこと,あるいは先天的な異常であることから偶発所見と判断した.その他のいずれの例においても内部器官及び組織の肉眼的な異常は観察されなかった.
5) 病理組織学検査
対照群及び80 mg/kg群について実施した精巣,精巣上体及び卵巣の検索では,精巣に軽微な精子停滞,精巣上体管腔内の精子減少及び崩壊細胞が対照群及び80 mg/kg群に各1例,精巣上体に軽度な精子肉芽腫が80 mg/kg群に1例認められたが,組織学的性状から偶発性変化と考えられた.
卵巣には,いずれの例においても異常所見は認められなかった.
2. 生殖発生毒性
1) 生殖機能(Table 2)
被験物質投与群における性周期(発情期から次の発情期までの日数)は対照群と同等であり,有意な差は認められなかった.交尾は,対照群及び被験物質投与群のいずれの例においても同居開始後4日以内に成立し,各群の交尾率は100 %であった.また,交尾までに要した平均日数には対照群と被験物質投与群との間に有意な差は認められなかった.非妊娠動物は,対照群及び被験物質投与群のいずれにも認められず,各群の受胎率は100 %であった.

2) 分娩及び哺育状況(Table 3)
被験物質投与群における妊娠期間は,対照群とほぼ同等であり,有意な差は認められなかった.分娩異常は,対照群及び被験物質投与群のいずれにも認められなかった.哺育状況では,40 mg/kg以下の投与群に異常は認められなかった.しかし,80 mg/kg群では前述の如く児集め不良の母体が7例認められた.
黄体数,着床痕数,着床率,出産率及び分娩率に対照群と被験物質投与群との間には有意な差は認められなかった.
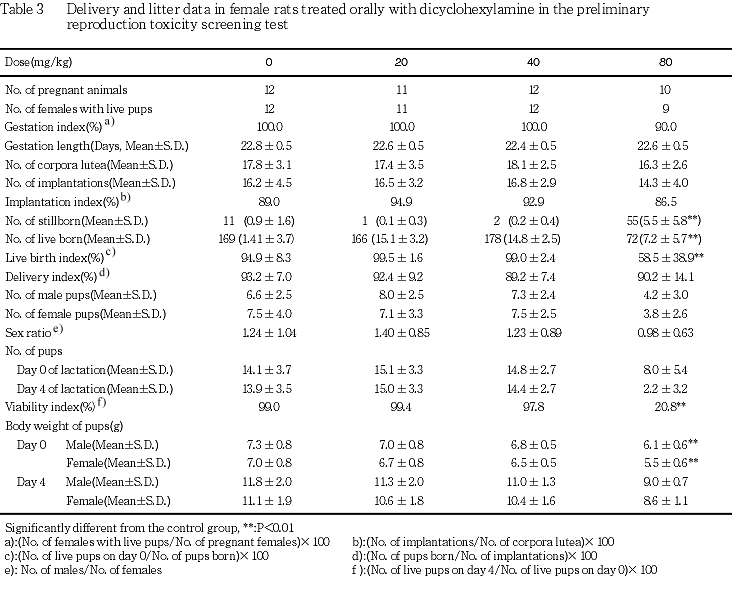
3) 新生児(F1)に及ぼす影響(Table 3)
40 mg/kg以下の投与群における出生児数,死産児数及び出生率には対照群との間に有意な差は認められなかった.一方,80 mg/kg群では死産児数の有意な高値,出生児数の有意な低値,出生率の有意な低値が認められた.
性比には対照群と被験物質投与群との間に有意な差は認められず,新生児の外表異常として,40 mg/kg群の1母体に痕跡尾及び鎖肛が1例観察されたのみであった.
40 mg/kg以下の投与群における新生児の4日の生存率には対照群との間に有意な差は認められなかった.一方,80 mg/kg群では哺育期の死亡が多く,哺育4日までに生存児を有していた母動物は9例中4例のみであった.したがって,同群における新生児の4日の生存率は,著しく低く,対照群との間に有意な差が認められた.
40 mg/kg以下の投与群における哺育0及び4日の体重は,雌雄ともに対照群とほぼ同等の値を示し,有意な差は認められなかったが,80 mg/kg群における生後0及び4日の体重は,雌雄ともに低値を示し,生後0日に対照群との間に有意な差が認められた.
哺育4日に実施した剖検では,胸腺の頸部遺残,脾臓の位置異常,大動脈弓から分岐する動脈の分岐異常あるいは膀胱に結節の所見が対照群,20及び40 mg/kg群の少数例に認められたが,80 mg/kg群にはこれらの所見は観察されず,偶発的変化と判断した.
考察
1. 反復投与毒性
雄では,80 mg/kg群において体重増加が抑制されたが,同群の一般状態,摂餌量,剖検所見,精巣及び精巣上体重量並びにこれら器官の病理組織学検査所見に被験物質投与の影響は認められなかった.一方,40 mg/kg以下の投与群には一般状態,体重,摂餌量,剖検所見,精巣及び精巣上体重量に被験物質投与の影響は認められなかった.
雌では,80 mg/kg群において妊娠21及び22日に各1例が死亡した.また,被験物質投与による一般状態の変化として,死亡例1例に粗毛が,生存例1例では妊娠22日の分娩終了後に腹臥姿勢,呼吸数減少,体温低下,出生児の児集め不良が認められ,哺育期間中における変化として,粗毛,児集め不良が認められた.さらに,同群では,体重増加が抑制され,摂餌量が低値を示したが,剖検所見及び卵巣の病理組織学検査所見に被験物質投与の影響は認められなかった.一方,40 mg/kg以下の投与群には一般状態,体重,摂餌量及び剖検所見に被験物質投与の影響は認められなかった.
以上のことから,ジシクロヘキシルアミンの反復投与により80 mg/kg群では雌2匹が死亡し,雌雄に体重増加抑制,雌に摂餌量の低下が認められた.したがって,ジシクロヘキシルアミンの一般毒性学的な無影響量は,雌雄ともに40 mg/kg/dayであると判断される.
2. 生殖発生毒性
雌の性周期,雌雄の交尾及び受胎,妊娠期間及び分娩に及ぼす被験物質投与の影響は認められなかった.哺育状況では,80 mg/kg群において児集め不良の母動物が多く認められ,哺育4日までに生存児を有していた母動物は4例のみであった.しかし,40 mg/kg以下の投与群に哺育異常は認められなかった.一方,出産率,黄体数,着床痕数及び着床率に被験物質投与の影響は認められなかった.
新生児に関して,80 mg/kg群では死産児数が有意な高値を示したことから,出生児数が有意な低値を示し、出生率の有意な低値が認められた.しかし,40 mg/kg以下の投与群には死産児数及び出生率に及ぼす被験物質投与の影響は認められなかった.また,分娩率にはいずれの投与群においても被験物質投与の影響は認められなかった.性比に被験物質投与の影響は認められず,被験物質投与に起因する外表異常は認められなかった.哺育期間中の児の死亡は,80 mg/kg群において多く,同群の新生児の4日の生存率は,著しい低値を示した.しかし,40 mg/kg以下の投与群における新生児の4日の生存率には被験物質投与の影響は認められなかった.新生児の体重は,80 mg/kg群において雌雄とも哺育0及び4日に低値を示したが,40 mg/kg以下の投与群における体重には被験物質投与の影響は認められなかった.哺育児の哺育4日の剖検では被験物質投与に起因すると考えられる異常は認められなかった.
以上のことから,ジシクロヘキシルアミンの反復投与により80 mg/kg群では哺育期の児集め不良の母動物が多く認められ,新生児の生存及び発育に及ぼす被験物質投与の影響が認められた.したがって,ジシクロヘキシルアミンの生殖発生学的な無影響量は,雄に関しては80 mg/kg/day,雌に関しては40 mg/kg/day,新生児に関しては40 mg/kg/dayであると判断される.
文献
| 1) | J. A. Hickman, D. R. Mottram and C. Kidman, Arch. Int. Pharmacodyn., 228, 191(1979). |
| 2) | D. R. Mottram and J. A. Hickman, Arch. Int. Pharmacodyn., 242, 50(1979). |
| 3) | C. Kidman, D. R. Mottram and J. A. Hickman, Arch. Int. Pharmacodyn., 228, 180(1979). |
| 4) | 厚生省生活衛生局企画課生活化学安全対策室監修,"化学物質毒性試験報告,"Vol. 6,化学物質点検推進連絡協議会,東京,1998, p. 105. |
| 連絡先 |
| 試験責任者: | 梅村建夫 |
| 試験担当者: | 片平勝也,田村一利,勝亦慶倶 |
| (株)ボゾリサーチセンター 御殿場研究所 |
| 〒412-0039 静岡県御殿場市かまど1284 |
| Tel 0550-82-9912 | Fax 0550-82-9913 | |
| Correspondence |
| Authors: | Tatsuo Umemura (Study director)
Katsuya Katahira, Kazutoshi Tamura, Tomoyoshi Katsumata |
| Gotemba Laboratory, Bozo Research Center Inc. |
| 1284 Kamado, Gotemba-shi, Shizuoka-ken, 412-0039, Japan. |
| Tel +81-550-82-9912 | Fax +81-550-82-9913 | |







