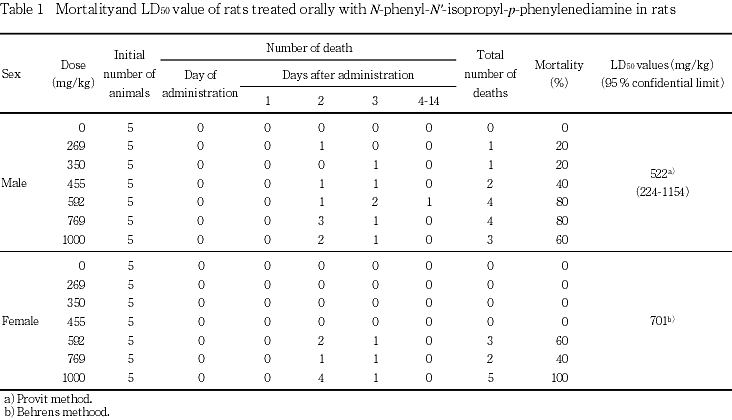
観察第3日から第5日にかけて,雄では269,350,455,592,769および1000 mg/kg投与群でそれぞれ1,1,2,4,4および3例が死亡し,雌では592,769および1000 mg/kg投与群でそれぞれ3,2および5例が死亡した.被験物質投与群では,投与日から淡赤色ないし淡褐色尿,うずくまりおよび閉眼が,加えて,観察第2日以降は,排便量の減少および皮膚色蒼白が観察され,一部の例で強い黄色調を示す尿および腹部膨満が認められたが,生存例ではいずれの所見も観察第11日までに回復した.死亡例では腹臥位姿勢,よろめき,呼吸数の減少,流涙,体表温の低下も散見された.また,観察第4日までは,体重減少ないし増加抑制が認められたが,観察第8日以降は順調に増加した.
剖検時には,死亡例で肝臓の腫大,腎臓の腫大ないし淡色化が観察され,胸水,腹水,肺の水腫様変化,脾臓の小型化および淡色化,前胃粘膜の剥離,赤色領域,腺胃粘膜の白濁,肥厚,皮下組織の黄色化などが認められた.生存例では,前胃粘膜の白濁および肥厚が観察された.
組織学検査では,死亡例で小葉中心性の肝細胞壊死ないし変性ならびに肝細胞の肥大が観察され,近位尿細管上皮の変性あるいは壊死,肺胞水腫,前胃粘膜下織の出血および浮腫,腺胃粘膜の出血およびびらんが認められた.生存例では,小葉中心性の肝細胞肥大および肝細胞の分裂像ならびに再生尿細管が散見され,一部の例で肺の好中球および泡沫細胞浸潤,前胃の褐色色素沈着ならびに腺胃の再生上皮が認められた.また,雄で脾臓の髄外造血が増加した.
以上のことから,N-フェニル-N'-イソプロピル-p-フェニレンジアミンのLD50は,雄で522 mg/kg(95 %信頼限界は224〜1154 mg/kg),雌では701 mg/kgと算出された.また,被験物質投与により肝臓および腎臓が障害され,肺胞水腫,胃粘膜の浮腫および前胃粘膜下織の出血,胸水および腹水の貯留,皮下組織の黄色化などが観察されることが明らかとなった.また,皮膚色蒼白および生存例の脾臓における髄外造血の増加から溶血性貧血が生じた可能性が示唆された.
検体調製では,被験物質を粉砕後,乳鉢で磨砕し,媒体を加えて練り上げて高用量群の懸濁液を調製してから,段階希釈して他群の投与検体を調製した.媒体には,日局注射用水(ロット番号9912ST,光製薬(株))を溶媒として0.5 %に調製した日局カルメロースナトリウム(ロット番号6Z09,丸石製薬(株))水溶液を使用した.
投与検体は8日間の安定性が確認されているため,投与前日に調製し,使用時まで冷蔵庫にて保管した.また,含量測定および均一性試験の結果から,各濃度の投与検体中には所定濃度の被験物質が含有され,均一性も良好であることが確認された.
群分けは,雌雄とも各群5匹とし,投与開始日前日の体重に基づいて体重別層化無作為抽出法により行った.
動物は,温度21.0〜25.0 ℃,湿度40.0〜75.0 %,換気回数約15回/時および照明12時間(7時〜19時点灯)に設定された飼育室内で,金属製金網床ケージに1匹ずつ収容し,固型飼料(CE-2,日本クレア(株))と水道水(秦野市水道局給水)を自由に摂取させて飼育した.
投与経路は経口とし,動物をあらかじめ約18時間絶食させた後,ラット用胃管を用いて強制的に単回投与した.投与容量は10 mL/kgとし,投与液量は投与日の投与前に測定した体重を基に個体別に算出した.

観察第2日には,269 mg/kg投与群の雄4例雌2例,350 mg/kg投与群の雄5例雌4例,455 mg/kg以上を投与した群の雌雄全例で排便量が減少し,個体によっては観察第7日まで継続した.また,観察第2日から第5日にかけて,雄の269 mg/kg投与群および雌雄の350 mg/kg以上を投与した群の多数例で皮膚色が蒼白となった.さらに,観察第3日から第10日の間に,強い黄色調を示す尿が,雄の各被験物質投与群ならびに雌の769および1000 mg/kg投与群の一部の動物で認められ,観察第4日から第10日までの間に,雄の769 mg/kg投与群の1例および1000 mg/kg投与群の雄2例雌1例では,腹部膨満が観察された.その他,観察第2日から第4日にかけて,雄の350 mg/kg投与群ならびに雌の269 mg/kg投与群および592 mg/kg以上を投与した群で被毛の汚れが散見された.生存例では,雌雄とも観察第11日以降,一般状態の変化は観察されなかった.
死亡例では,死期が迫るに従って,上記の所見に加えて腹臥位姿勢,よろめき,呼吸数の減少,流涙,体表温の低下などが散見された.なお,死亡例の所見に群間の差はなかった.
肝臓は,雄12例雌3例で腫大していた.また,腎臓では,雄8例雌3例で腫大が,雌1例で淡色化が認められた.
肺では,雄10例雌全例で水腫様変化が観察され,雄10例で暗赤色点ないし暗赤色領域が,雌5例で暗色化が認められた.
胸腔には胸水が貯留し,雄1例および雌4例で無色透明,雄6例で赤色調を呈した.また,腹腔には腹水が観察され,雌2例で無色透明,雄3例および雌3例で赤色調を呈した.
脾臓では,観察第3日の一般状態観察後に死亡した(16時に死亡発見)雄1例および観察第4日および第5日に死亡した雌雄全例(雄7例雌3例)で小型化および淡色化が認められた.
前胃粘膜は,雄12例雌6例で剥離し,雄10例雌9例で暗色から赤色調を呈する点または領域が観察されたほか,白濁および陥凹部がそれぞれ雄1例で認められた.腺胃粘膜は,雄8例雌5例で肥厚し,雄11例雌9例で白濁が,雌雄各5例で陥凹部が観察され,雄5例雌3例で暗色から暗赤色調を呈する点または領域が認められた.
この他,観察第3日の一般状態観察後に死亡した雄1例および観察第4日に死亡した雄2例雌3例では,皮下組織の黄色化が認められた.
観察期間終了時屠殺例(生存例)では,前胃粘膜に,455および592 mg/kg投与群でそれぞれ雌5例中1例および雌2例中1例,769 mg/kg投与群で雄1例中1例および雌3例中2例,1000 mg/kg投与群で雄2例全例に白濁および肥厚が観察された.この他には,いずれの例の器官・組織にも異常所見は認められなかった.
肝臓では,592および769 mg/kg投与群の雌各1例を除く雌雄全例で,軽微から中等度の小葉中心性肝細胞の壊死ないし変性が観察された.また,雄9例雌9例で肝細胞の肥大が認められた.
腎臓では,雄12例雌6例で近位尿細管上皮の変性あるいは壊死がみられ,雄は雌に比較して変化の程度が強い傾向にあった.また,雄10例雌8例で近位尿細管管腔に細胞片と考えられる顆粒円柱が観察され,1000 mg/kg投与群の雌4例で遠位尿細管管腔の拡張が認められた.
肺では,269および455 mg/kg投与群の雄各1例を除く雌雄全例で,軽度から強度の肺胞水腫が観察された.この他,雄8例雌6例で肺胞の出血が,雄6例雌8例で泡沫細胞浸潤が観察され,雌3例では好中球浸潤が認められた.
脾臓では,雌雄全例で萎縮が観察され,1000 mg/kg投与群の雌2例で髄外造血の増加が認められた.
前胃では,雄12例雌9例で粘膜下織の出血が,雄10例雌8例で粘膜下織の浮腫が観察され,雄4例雌7例でびらんが,雄10例雌2例で粘膜上皮の空胞変性が,雄12例雌10例で好中球浸潤が認められた.腺胃では,雄7例雌5例でびらんが,雄5例雌4例で粘膜の出血が,粘膜下織の浮腫ないし好中球浸潤がそれぞれ雄1例に認められた.
観察期間終了時まで生存した各群それぞれ1例について行った組織学検査では,剖検時に変化があった胃のほか,肝臓,腎臓,肺および脾臓で次に示すような所見があった.
肝臓では,455 mg/kg以上を投与した雄の各群および769 mg/kg投与群の雌で,小葉中心性の肝細胞肥大が観察され,769および1000 mg/kg投与群の雄で肝細胞の分裂像の増加が認められた.また,455 mg/kg以上を投与した雄の各群ならびに雌の対照群,350 mg/kg投与群および592 mg/kg以上を投与した各群で髄外造血が認められた.
腎臓では,455および769 mg/kg投与群の雌雄で髄質に再生尿細管が,455 mg/kg投与群の雄および769 mg/kg投与群の雌でリンパ球浸潤が観察されたほか,対照群の雌で皮髄境界部に鉱質沈着が認められた.
肺では,592 mg/kg投与群の雄で軽微な好中球浸潤および軽度の泡沫細胞浸潤が認められ,対照群の雌で軽微な肺胞の出血が観察された.
脾臓では,対照群の雌を除く雌雄全群で髄外造血の増加が認められ,雄では対照群と比較して被験物質投与群で程度が強く,455および592 mg/kg投与群では強度の増加となった.
胃では,769 mg/kg投与群の雄で前胃の褐色色素沈着および腺胃の再生上皮が観察され,455 mg/kg投与群の雌で腺胃の粘膜下織に好酸球浸潤が認められた.
観察第3日から5日にかけて,雄では,269,350,455,592,769および1000 mg/kg投与群でそれぞれ5例中1,1,2,4,4および3例が死亡し,雌では,592,769および1000 mg/kg投与群でそれぞれ5例中3,2および5例が死亡した.
肝臓では,死亡例で肝細胞肥大および小葉中心性の肝細胞壊死ないし変性が観察され,生存例では,肝細胞の分裂像増加および小葉中心性の肝細胞肥大が認められた.肝臓,特に小葉中心部は化学物質による毒性が発現しやすい部位8)であるが,肝臓の高い再生能より,損傷後は肝細胞が盛んに分裂して速やかに修復されることが知られている.以上のことから,被験物質を投与することにより肝障害が生じ,その後,生存例では回復に転じることが考えられた.この他,腎臓において,死亡例で,近位尿細管上皮の変性あるいは壊死がみられ,細胞片と考えられる顆粒状の円柱が観察されたほか,尿細管管腔の拡張が散見された.また,生存例では,数例で再生尿細管およびリンパ球浸潤が認められた.これら死亡例および生存例の尿細管における所見は,被験物質投与による腎障害を示唆するものであると考えられた.さらに,死亡例では肺の水腫および出血,前胃粘膜下織の浮腫および出血が認められ,腹水および胸水の貯留も散見された.肝障害および腎障害時には,組織の浮腫および腹水などが生じるほか,肺の出血および粘膜下織の出血が認められることが知られている9).本試験は肝臓および腎臓の障害が示唆されたことから,浮腫および出血は,肝臓および腎臓の変化に起因する可能性が考えられた.
一般状態観察時に強い黄色調を示す尿が観察され,剖検では,死亡例で皮下組織の黄色化が散見されたことから,黄疸であることが推測され,黄疸の原因として,肝臓の障害像との関連が示唆された.また,一般状態観察時に多数例で皮膚色蒼白が観察され,死亡例では剖検時に脾臓の小型化および淡色化が認められたことから貧血が示唆されたが,死亡例の雌2例で脾臓の髄外造血が軽度に増加し,生存例では皮膚色蒼白が数日で回復して雄で脾臓の髄外造血が増加したことから,黄疸の発現には溶血が関与した可能性も考えられた.なお,被験物質投与群で淡赤色ないし淡褐色尿が観察されたが,予備試験および被験物質の反復投与毒性試験(未公刊)で認められた本試験と同様の赤色ないし暗赤色尿は潜血反応が陰性であったこと,ならびに,ウサギおよびヒトでN-フェニル-N'-イソプロピル-p-フェニレンジアミンが尿中に排泄されるという報告がある10-12)ことから,溶血に由来したものではなく,尿中に排泄された被験物質の色調に由来する可能性が示唆された.
死亡例で,前胃のびらんならびに腺胃のびらんおよび粘膜出血などが観察され,生存例でも,前胃の褐色色素沈着および腺胃の再生上皮などが認められた.胃粘膜上皮,特に前胃粘膜の損傷は,刺激性物質を投与することにより生じることが知られており13),N-フェニル-N'-イソプロピル-p-フェニレンジアミンは,局所刺激性を有することが報告されていることから14),今回観察された胃粘膜上皮の損傷の一因として,被験物質の刺激性が考えられた.
この他,雌雄とも各被験物質投与群で,体重減少ないし増加が抑制され,排便量が減少した.また,一般状態の変化として,うずくまり,閉眼および排便量の減少などが観察され,死亡例では,さらに,よろめき,流涙,腹臥位姿勢,呼吸数の減少,体表温低下などが観察されたが,本試験結果からは,これらが一般状態の悪化に伴うものであるのか,被験物質の直接作用によるものであるのかは判断できなかった.
以上の結果から,N-フェニル-N'-イソプロピル-p-フェニレンジアミンのLD50は,雄で522 mg/kg(95 %信頼限界は224〜1154 mg/kg),雌では701 mg/kgとなった.また,被験物質投与により肝臓および腎臓が障害され,肺胞水腫,胃粘膜の浮腫および前胃粘膜下織の出血,胸水および腹水の貯留,皮下組織の黄色化などが観察されることが明らかとなった.また,皮膚色蒼白および生存例の脾臓における髄外造血の増加から溶血性貧血が生じた可能性が示唆された.
| 1) | 櫻本裕助,高分子加工,438(1977). |
| 2) | 鹿庭正昭ら,衛生化学,28(3), 137(1982). |
| 3) | S. E. Feinman, J. Toxicol. -Cut. & Ocular Toxicol. 6(2), 117(1987). |
| 4) | Y. Ikarashi, et al., Contact Dermatitis, 28, 77(1993). |
| 5) | J. Momma, et al., Toxicol. 126, 75(1998). |
| 6) | A. Takahashi, Intern. Polymer Sci. & Technol., 3(1), T/93(1976). |
| 7) | W. E. McCormick, Rubber Chem. & Technol., 45, 627(1972). |
| 8) | M. T. Moslen, "Toxic responses of the liver in" Casarett and Doull's Toxicology:the basic science of poisons" 5th ed." eds. by C. D. Klassen, McGraw-Hill Companies Inc., New York, 1996, pp. 403-416. |
| 9) | 松澤佑次編,Molecular Med., 35(1998). |
| 10) | 斉藤浩司ら,薬学雑誌,100(2), 126(1980). |
| 11) | G. Scansetti, et al., Int. Arch. Occup. Environ. Health, 59, 537(1987). |
| 12) | G. Scansetti, et al., Med. Lav., 74, 464(1983). |
| 13) | 高橋道人監訳"毒性病理学の基礎,"ソフトサイエンス社,東京,1992, |
| 14) | NIOSH:RTECS®, 2000-4:RTECS No. ST2650000(2000). |
| 連絡先 | |||
| 試験責任者: | 森村智美 | ||
| 試験担当者: | 一原佐知子,永田伴子,稲田浩子,三枝克彦,安生孝子 | ||
| (財)食品薬品安全センター秦野研究所 | |||
| 〒257-8523 神奈川県秦野市落合729-5 | |||
| Tel 0463-76-8033 | Fax 0463-82-9627 | ||
| Correspondence | ||||
| Authors: | Tomomi Morimura(Study Director) Sachiko Ichihara, Tomoko Nagata, Hiroko Inada,Katsuhiko Saegusa, Takako Anjo | |||
| Hatano Research Institute, Food and Drug Safety Center | ||||
| 729-5 Ochiai, Hadano-shi, Kanagawa, 257-8523, Japan | ||||
| Tel +81-463-82-4751 | Fax +81-463-82-9627 | |||