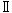 D,(株)ニコン)を用いて測定した.
D,(株)ニコン)を用いて測定した.
雌においては,死亡例が50 mg/kg群で妊娠末期にみられた.一般状態では,50 mg/kg群で自発運動の低下,体温下降および口の周囲の汚れがみられた.体重は,交配開始前および交配期間中に50 mg/kg群で低値,妊娠および哺育期間中に15 mg/kg以上の群で低値がみられた.摂餌量は,交配開始前,妊娠および哺育期間中とも15 mg/kg以上の群で低値あるいは低値傾向がみられた.剖検では,5 mg/kg群で胸腺萎縮および肝臓の白色斑,15 mg/kg群で胸腺萎縮および前胃粘膜の肥厚,50 mg/kg群で胸腺萎縮,肝臓の白色斑および前胃粘膜潰瘍がみられた.器官重量は,1.5 mg/kg以上の群で胸腺の絶対および相対重量の低値あるいは低値傾向,15 mg/kg以上の群で副腎の絶対および相対重量の高値あるいは高値傾向,脾臓の絶対重量の低値あるいは低値傾向,肝臓,腎臓および卵巣の相対重量の高値あるいは高値傾向がみられた.病理組織学検査では,肺において1.5 mg/kg群で泡沫細胞集簇,5 mg/kg群で限局性の炎症性細胞浸潤,15および50 mg/kg群で泡沫細胞集簇および限局性の炎症性細胞浸潤,肝臓において5 mg/kg群で限局性の肝細胞壊死,50 mg/kg群で限局性の肝細胞壊死および肝細胞空胞化,胃において1.5 mg/kg群で前胃粘膜下織細胞浸潤,5 mg/kg群で前胃粘膜下織細胞浸潤,15 mg/kg群で前胃粘膜下織細胞浸潤,前胃の扁平上皮過形成および前胃粘膜下織水腫,50 mg/kg群で粘膜下織炎症性細胞浸潤,前胃潰瘍,前胃糜爛および前胃上皮下浮腫,胸腺において1.5 mg/kg以上の群で萎縮,腎臓において15 mg/kg群で尿細管上皮変性,50 mg/kg群で尿細管上皮空胞変性および尿細管上皮変性,副腎において1.5 mg/kg以上の群で束状帯肥大がみられた.
受胎率,妊娠黄体数,着床数,着床率では,投与による変化はみられなかった.出産率は,15 mg/kg以上の群で低値傾向がみられた.
児動物では,15 mg/kg以上の群で哺育0日の新生児数および児の産出率の低値傾向,出生率の低値,死産児数の高値がみられた.一般状態では,15 mg/kg以上の群で体温下降がみられた.15 mg/kg以上の群で哺育4日の生存児数および哺育4日の生存率の低値傾向あるいは低値がみられた.投与による外表異常はみられなかった.体重は,1.5 mg/kg以上の群で哺育0および4日に雌雄体重の低値あるいは低値傾向がみられた.剖検では,投与による変化はみられなかった.
以上のように,硝酸カドミウム四水和物の一般毒性学的無影響量は,雄では1.5 mg/kg投与によりフィブリノーゲンの低値が認められたことから1.5 mg/kg/day未満,雌では1.5 mg/kg投与により胸腺の絶対および相対重量の低値,肺,胃,胸腺および副腎の組織学変化が認められたことから1.5 mg/kg/day未満と考えられる.また,生殖発生毒性学的な無影響量は,雄では50 mg/kg投与しても交尾能および授胎能に影響が認められなかったことから50 mg/kg/day,雌では5 mg/kg投与により哺育行動異常が認められたことから1.5 mg/kg/dayと考えられる.児動物では,1.5 mg/kg投与により体重の低値が認められたことから,1.5 mg/kg/day未満と考えられる.
被験物質は,注射用水で溶解して調製した.なお,被験物質の調製に際して,水和物および純度による換算を実施した.0.3〜100 mg/mLの調製液は,室温・遮光条件下で7日間保存しても安定性に問題のないことが確認されているため,各濃度の調製液は調製後,室温・遮光条件下で保存し,調製後7日以内に使用した.投与開始日および雄投与終了日に使用した各投与検体中の被験物質濃度を測定した結果,被験物質濃度に問題はなかった.
動物は,室温20〜26 ℃,湿度40〜70 %,明暗各12時間(照明:午前6時〜午後6時),換気回数12回/時に維持されている飼育室で飼育した.検疫・馴化期間中はステンレス製ケージを用いて1ケージ当たり5匹までの群飼育とし,群分け後はステンレス製ケージを用いて個別飼育した.母動物は,妊娠18日以降オートクレーブ処理した床敷(サンフレーク,日本チャールス・リバー(株))を入れたプラスチック製ケージで個別飼育し,自然分娩および哺育させた.飼料は,固型飼料(CRF-1,オリエンタル酵母工業(株))を自由に摂取させた.ただし,雄は,投与終了日の夕刻から絶食した.飲料水は,水道水を自由に摂取させた.
投与量は,雄ラットを用いた2週間経口投与による予備試験(投与段階:0,12.5,25,50および100 mg/kg)の結果により決定した.すなわち,死亡例が,100 mg/kg群で2/5例認められた.また,12.5 mg/kg以上の群で摂餌量の低値,25 mg/kg以上の群で流涎,体重の増加抑制,50 mg/kg以上の群で前胃粘膜の潰瘍がみられた.そこで,当試験では,50 mg/kgを最高用量とし,以下公比約3により15,5および1.5 mg/kgとした(投与量は硝酸カドミウム無水和物で表示).また,対照として媒体(注射用水)のみを同容量投与する群を設けた.各群の使用動物数は雌雄各12例とした.
投与期間は,雄では交配前14日間とその後35日間の合計49日間とし,雌では交配前14日間,交配期間中(最長12日間),妊娠期間中および哺育3日までの合計40〜51日間とした.なお,投与開始日を投与1日とした.
一般状態および死亡の有無は,投与前・後の1日2回観察した.
(2) 体重測定
体重は,1週間に2回測定した.
(3) 摂餌量測定
摂餌量は,交配開始前14日間および交配期間終了後から1週間に2回測定した.
(4) 尿検査
投与期間終了前に採尿ケージを用いて絶食・給水下で3時間で採取した尿(3時間尿)と引き続いて給餌・給水下で21時間で採取した尿(21時間尿)ならびにそれらを合計した尿(24時間尿)について,以下の検査を実施した.
3時間尿:色調は,外観判定とした.pH,蛋白質,ブドウ糖,ケトン体,ビリルビン,潜血,ウロビリノーゲンは,尿検査試験紙(栄研化学(株))と尿自動分析装置(US-2100,栄研化学(株))を用いて検査した.尿沈渣は,沈渣を尿沈渣染色液(Sternheimer変法,和光純薬工業(株))で染色後に顕微鏡下で観察した.なお,当日の検体投与後に行った.
21時間尿:比重を屈折率により屈折型尿比重計(ユリペット-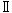 D,(株)ニコン)を用いて測定した.
D,(株)ニコン)を用いて測定した.
24時間尿:尿量を比重と重量から算出した.
(5) 血液学検査
最終投与の翌日にペントバルビタールナトリウムの腹腔内投与による麻酔下で腹大動脈から血液を採取し,以下の血液学検査を実施した.
赤血球数(RBC),ヘモグロビン,ヘマトクリット,血小板数および白血球数(WBC)は,EDTA-2K処置した血液について,多項目自動血球計数装置(Sysmex K-4500,シスメックス(株))を用いて測定した.さらに,平均赤血球容積(MCV),平均赤血球血色素量(MCH)および平均赤血球血色素濃度(MCHC)を算出した.
網状赤血球比率は,EDTA-2K処理した血液をBrecher法により超生体染色後,Giemsa染色標本を作製して顕微鏡下で赤血球1000個中の網状赤血球数を計数した.
白血球百分率は,EDTA-2K処理した血液のMay-Giemsa染色標本を作製して顕微鏡下で白血球100個を分類計数した.
プロトロンビン時間(PT),活性化部分トロンボプラスチン時間(APTT)およびフィブリノーゲンは,3.13 %クエン酸ナトリウムで処理後,遠心分離(約4 ℃,3000 rpm,15分間)して得た血漿について,散乱光検出方式により血液凝固分析装置(コアグマスター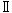 ,三共(株))を用いて測定した.
,三共(株))を用いて測定した.
(6) 血液生化学検査
血液学検査用の血液と同時期に腹大動脈から採取した血液から遠心分離(約4 ℃,3000 rpm,15分間)して得た血清について,以下の血液生化学検査を実施した.
ASTはMDH-UV法,ALTはLDH-UV法,ALPはρ-ニトロフェニルリン酸基質法,γ-GTPはL-γ-グルタミル-3-カルボキシ-4-ニトロアニリド基質法,総蛋白はBiuret法,総ビリルビンは安定化ジアゾニウム塩法,尿素窒素はウレアーゼ・GrDH法,クレアチニンはクレアチニナーゼ・F-DAOS法,ブドウ糖はヘキソキナーゼ・G-6-PDH法,総コレステロールはCOD・HDAOS法,トリグリセライドはGPO・HDAOS法,Caはο-CPC法,無機リンはPNP・XDH法,Na,KおよびClはイオン選択電極法により,いずれも生化学自動分析装置(AU 400,オリンパス光学工業(株))を用いて測定した.
アルブミンは総蛋白および蛋白分画[電気泳動法,自動電気泳動装置(AES 310,オリンパス光学工業(株))]から,A/G(アルブミン/グロブリン)は蛋白分画から算出した.
(7) 剖検および器官重量測定
採血した動物をさらに放血致死させた後に剖検した.脳(大脳,小脳,延髄),下垂体,甲状腺,胸腺,心臓,肝臓,脾臓,腎臓,副腎,精巣および精巣上体は重量を測定した(ただし,下垂体および甲状腺重量は20 %中性緩衝ホルマリンで1晩固定後測定した).これらの器官は,肺,気管,膵臓,唾液腺(舌下腺・顎下腺),食道,胃,十二指腸,空腸,回腸,盲腸,結腸,直腸,リンパ節(下顎・腸間膜),膀胱,精嚢,前立腺,上皮小体,脊髄,坐骨神経,眼球,ハーダー腺および骨髄(胸骨・大腿骨)とともに20 %中性緩衝ホルマリンで固定した.ただし,精巣および精巣上体はブアン液で2〜3時間固定後90 %アルコールに再固定し,眼球はグルタールアルデヒド・ホルマリンで1晩固定後20 %中性緩衝ホルマリンに再固定した.
(8) 病理組織学検査
対照群および50 mg/kg群について,各器官・組織のHE染色組織標本を作製し,病理組織学検査を実施した.50 mg/kg群の検査で対照群と比べて異常を示す動物数に差があると考えられた肺,肝臓,膵臓,腎臓,副腎および骨髄については,1.5,5および15 mg/kg群についても同様に検査した.
一般状態および死亡の有無は,投与前・後の1日2回観察した.
死亡例は,発見後速やかに剖検した.
(2) 性周期
性周期は,投与開始日から交尾確認日まで毎日1回観察した.なお,発情期が連続2日間にわたって観察された場合は1回と計数した.
(3) 体重測定
体重は,交配開始前14日間および交配期間中は1週間に2回,妊娠期間中は妊娠0,7,14および21日に,哺育期間中は哺育0および4日にそれぞれ測定した.
(4) 摂餌量測定
摂餌量は,交配開始前14日間までは1週間に2回測定した.また,妊娠期間中は妊娠2,9,16および21日に,哺育期間中は哺育4日に測定した.
(5) 分娩状態の観察
交尾雌は自然分娩させ,分娩状態の異常の有無,分娩終了の確認を妊娠21日から妊娠25日の午前10時まで毎日行った.午前10時に分娩が終了していた場合,その日を哺育0日とした.
(6) 哺育状態の観察
母動物は,哺育状態を哺育4日まで毎日観察した.
新生児が全例死亡した母動物は,エーテル麻酔下で腹大動脈から放血致死させた後に剖検し,妊娠黄体数および着床数を数えた.
(7) 剖検および器官重量測定
母動物は,哺育4日にエーテル麻酔下で腹大動脈から放血致死させた後に剖検し,妊娠黄体数および着床数を数えた.脳(大脳,小脳,延髄),下垂体,甲状腺,胸腺,心臓,肝臓,脾臓,腎臓,副腎および卵巣は重量を測定した(ただし,下垂体および甲状腺重量は20 %中性緩衝ホルマリンで1晩固定後測定した).これらの器官は,肺,気管,膵臓,唾液腺(舌下腺・顎下腺),食道,胃,十二指腸,空腸,回腸,盲腸,結腸,直腸,リンパ節(下顎・腸間膜),膀胱,子宮,腟,上皮小体,脊髄,坐骨神経,眼球,ハーダー腺,骨髄(胸骨・大腿骨)および乳腺とともに20 %中性緩衝ホルマリンで固定した.ただし,眼球はグルタールアルデヒド・ホルマリンで1晩固定後20 %中性緩衝ホルマリンに再固定した.
(8) 病理組織学検査
対照群および50 mg/kg群について,各器官・組織のHE染色組織標本を作製し,病理組織学検査を実施した.50 mg/kg群の検査で対照群と比べて異常を示す動物数に差があると考えられた肺,肝臓,胃,胸腺,腎臓および副腎については,1.5,5および15 mg/kg群についても同様に検査した.
交尾確認は毎朝ほぼ一定時刻に行い,腟垢内に精子または腟栓を確認した雌を交尾成立動物として,その日を妊娠0日として起算した.
出産時に総出産児数と性,死産児数,新生児数および外表異常の有無を観察した.
(2) 児動物の観察
児動物は,一般状態および死亡の有無を毎日1回観察した.
(3) 体重測定
体重は,哺育0日(出生日)および4日に測定した.
(4) 剖検
生存児は,哺育4日にエーテル麻酔下で腹大動脈から放血致死させた後に剖検した.
体重,摂餌量,尿量,尿比重,血液学検査,血液生化学検査,器官の絶対重量および相対重量,発情回数,交尾所要日数,妊娠期間,妊娠黄体数,着床数,着床率,総出産児数,新生児数,死産児数,分娩率,児の産出率,出生率,哺育4日の生存児数,哺育4日の生存率,外表異常の出現率および性比は,各群で平均値および標準偏差を算出した.その後,Bartlett法による等分散性の検定を行い,等分散の場合には一元配置法による分散分析を行い,有意ならばDunnett法により行った.一方,等分散と認められなかった場合は,順位を利用した一元配置法による分析(Kruskal-Wallisの検定)を行い,有意ならば順位を利用したDunnett型の検定法により行った.
交尾率,受胎率および出産率は,χ2検定により行った.
病理組織学検査において,50 mg/kg群の雌雄で毒性学的影響が示唆され他の用量群についても検査を実施した雄の肺,肝臓,膵臓,腎臓,副腎および骨髄,雌の肺,肝臓,胃,胸腺,腎臓および副腎の所見については,対照群との群間比較を上記の順位を利用したDunnett型の検定法を用いて行った.
死亡および瀕死例は,いずれの群でも認められなかった.
一般状態観察において,対照群および1.5 mg/kg群では異常はみられなかった.5 mg/kg以上の群では,一過性の流涎がみられた.
(2) 体重推移(Fig. 1)
1.5および5 mg/kg群では,対照群と比べていずれの測定日の体重にも有意差はみられなかった.15 mg/kg群では,対照群と比べて投与15〜49日に体重の有意な低値がみられた.50 mg/kg群では,対照群と比べて投与4〜49日に体重の有意な低値がみられた.
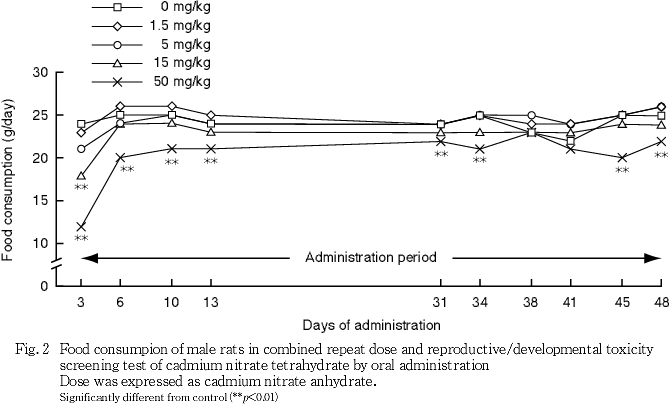
(3) 摂餌量(Fig. 2)
1.5および5 mg/kg群では,対照群と比べていずれの測定日の摂餌量にも有意差はみられなかった.15 mg/kg群では,対照群と比べて投与3日に摂餌量の有意な低値がみられた.50 mg/kg群では,対照群と比べて投与3〜34,45および48日に摂餌量の有意な低値がみられた.
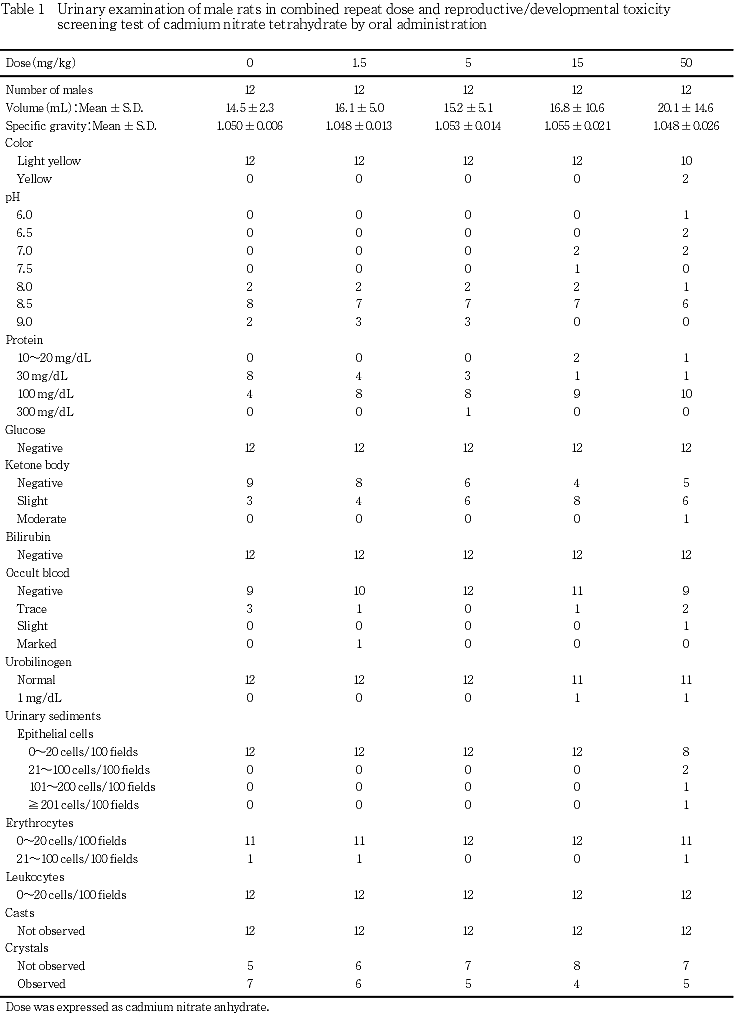
(4) 尿検査(Table 1)
1.5,5および15 mg/kg群では,対照群と比べて尿量および比重に有意差はみられなかった.50 mg/kg群では,対照群と比べて尿量の高値傾向がみられた.
色調,pH,蛋白質,ブドウ糖,ケトン体,ビリルビン,潜血,ウロビリノーゲンおよび沈渣は,1.5,5および15 mg/kg群では対照群とほぼ同程度であった.50 mg/kg群では,対照群と比べてpHの低値傾向がみられた.
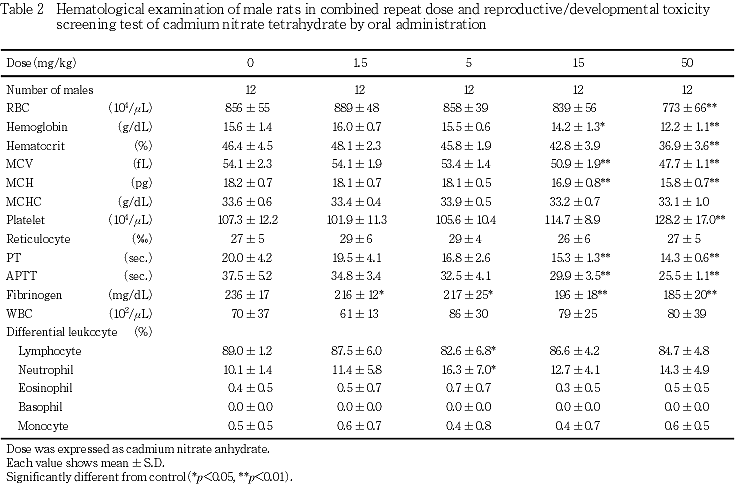
(5) 血液学検査(Table 2)
1.5および5 mg/kg群では,対照群と比べてフィブリノーゲン濃度の有意な低値がみられた.15 mg/kg群では,対照群と比べてヘモグロビン量,MCV,MCH,PT,APTTおよびフィブリノーゲン濃度の有意な低値がみられた.50 mg/kg群では,対照群と比べて赤血球数,ヘモグロビン量,ヘマトクリット値,MCV,MCH,PT,APTTおよびフィブリノーゲン濃度の有意な低値,血小板数の有意な高値がみられた.
その他,5 mg/kg群では,対照群と比べてリンパ球率の有意な低値および好中球率の有意な高値がみられたが,高用量群で有意差は認められないことから,投与に基づく変化ではないと判断される.
(6) 血液生化学検査(Table 3)
1.5 mg/kg群では,対照群と比べていずれの測定項目にも有意差はみられなかった.5 mg/kg群では,対照群と比べて総蛋白の有意な低値および無機リンの有意な高値がみられた.15 mg/kg群では,対照群と比べてALPおよび総蛋白の有意な低値,ALTおよび無機リンの有意な高値がみられた.50 mg/kg群では,対照群と比べてALP,総蛋白,アルブミンおよびNaの有意な低値,AST,ALT,γ-GTP,総コレステロールおよび無機リンの有意な高値がみられた.
その他,5および15 mg/kg群では,対照群と比べてA/Gの有意な高値がみられたが,高用量群で有意差は認められないことから,投与に基づく変化ではないと判断される.

(7) 剖検
対照群では,腎臓に白色斑が1例みられた.1.5,5および15 mg/kg群では,異常はみられなかった.50 mg/kg群では,精巣上体に黄白色結節が1例みられたが,通常認められるものであり,偶発例と判断される.
(8) 器官重量(Table 4)
剖検日の体重において,1.5および5 mg/kg群では対照群と比べて有意差はみられなかった.15および50 mg/kg群では,対照群と比べて体重の有意な低値がみられた.
器官重量において,1.5 mg/kg群では対照群と比べていずれの絶対および相対重量にも有意差はみられなかった.50 mg/kg群では,対照群と比べて胸腺の絶対重量の有意な低値,副腎の絶対重量の有意な高値,肝臓,脾臓,腎臓および副腎の相対重量の有意な高値がみられた.
その他,5 mg/kg群では,対照群と比べて下垂体の絶対重量の有意な低値がみられたが,高用量群で有意差は認められないことから,投与に基づく変化ではないと判断される.15 mg/kg群では,対照群と比べて心臓および腎臓の絶対重量の有意な低値および脳および精巣の相対重量の有意な高値がみられたが,それらは体重差に基づく変化と考えられることから,投与によるものではないと判断される.また,50 mg/kg群では,対照群と比べて下垂体および心臓の絶対重量の有意な低値,脳,精巣および精巣上体の相対重量の有意な高値がみられたが,それらは体重差に基づく変化と考えられることから,投与によるものではないと判断される.

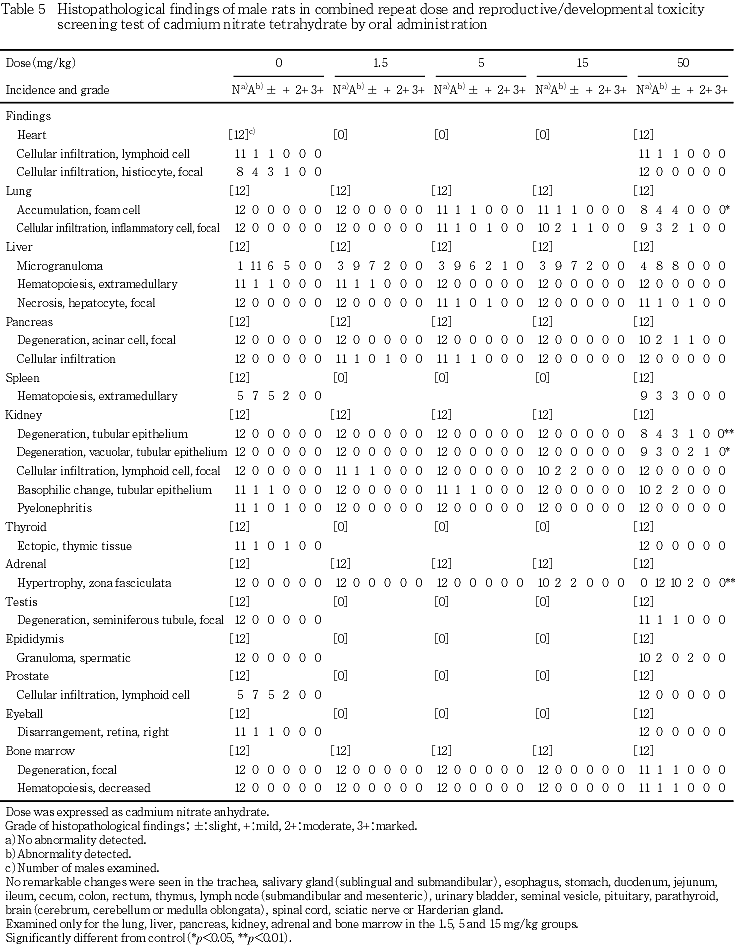
(9) 病理組織学検査(Table 5)
肺:5 mg/kg群では,泡沫細胞集簇が1例および限局性の炎症性細胞浸潤が1例みられた.15 mg/kg群では,泡沫細胞集簇が1例および限局性の炎症性細胞浸潤が2例みられた.50 mg/kg群では,泡沫細胞集簇が4例および限局性の炎症性細胞浸潤が3例みられた.なお,泡沫細胞集簇は,50 mg/kg群で対照群と比べて有意差が認められた.
肝臓:5 mg/kg群では,限局性の肝細胞壊死が1例みられた.50 mg/kg群では,限局性の肝細胞壊死が1例みられた.
膵臓:50 mg/kg群では,限局性の腺細胞変性が2例みられた.
腎臓:50 mg/kg群では,尿細管上皮変性が4例および尿細管上皮空胞変性が3例みられた.尿細管上皮変性および尿細管上皮空胞変性は,50 mg/kg群で対照群と比べて有意差が認められた.
副腎:15 mg/kg群では,束状帯肥大が2例みられた.50 mg/kg群では,束状帯肥大が12例みられた.束状帯肥大は,50 mg/kg群で対照群と比べて有意差が認められた.
精巣:限局性の精細管変性が50 mg/kg群で1例みられた.
骨髄:50 mg/kg群では,限局性の変性が1例および造血減少が1例みられた.
その他に認められた変化は,対照群でも通常観察される変化であること,投与群の変化は対照群の出現頻度と比べて差がないことから,偶発的変化と判断される.
死亡例は,50 mg/kg群で妊娠19〜21日に5例認められた.
一般状態において,交配開始前および交配期間中には対照群,1.5および5 mg/kg群では異常はみられなかった.15 mg/kg以上の群では,一過性の流涎がみられた.
妊娠期間中には,対照群,1.5および5 mg/kg群では一般状態に異常はみられなかった.15 mg/kg群では,一過性の流涎がみられた.50 mg/kg群では,死亡例において一過性の流涎,自発運動の低下,体温下降および口の周囲の汚れがみられた.50 mg/kg群の生存例では,一過性の流涎がみられた.
哺育期間中には,対照群,1.5および5 mg/kg群では一般状態に異常はみられなかった.15 mg/kg以上の群では,一過性の流涎がみられた.50 mg/kg群では,自発運動の低下がみられた.
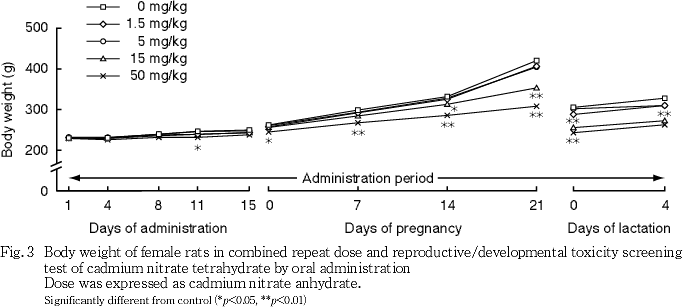
(2) 体重推移(Fig. 3)
交配開始前および交配期間中には,1.5,5および15 mg/kg群では対照群と比べていずれの測定日の体重にも有意差はみられなかった.50 mg/kg群では,対照群と比べて投与11および18日に体重の有意な低値がみられた.
妊娠期間中には,1.5および5 mg/kg群では対照群と比べていずれの測定日の体重にも有意差はみられなかった.15 mg/kg群では,対照群と比べて妊娠14および21日に体重の有意な低値がみられた.50 mg/kg群では,対照群と比べて妊娠0〜21日に体重の有意な低値がみられた.
哺育期間中には,1.5および5 mg/kg群では対照群と比べていずれの測定日の体重にも有意差はみられなかった.15 mg/kg群では,対照群と比べて哺育0および4日に体重の有意な低値がみられた.50 mg/kg群では,対照群と比べて哺育0日に体重の有意な低値,哺育4日に低値傾向がみられた.
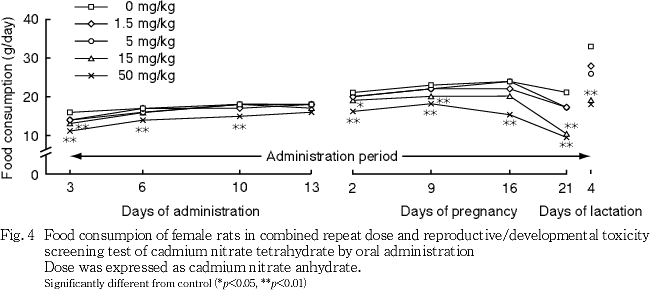
(3) 摂餌量(Fig. 4)
交配開始前には,1.5および5 mg/kg群では対照群と比べていずれの測定日の摂餌量にも有意差はみられなかった.15 mg/kg群では,対照群と比べて投与3日に摂餌量の有意な低値がみられた.50 mg/kg群では,対照群と比べて投与3〜10日に摂餌量の有意な低値がみられた.
妊娠期間中には,1.5および5 mg/kg群では対照群と比べていずれの測定日の摂餌量にも有意差はみられなかった.15 mg/kg群では,対照群と比べて妊娠2,9および21日に摂餌量の有意な低値がみられた.50 mg/kg群では,対照群と比べて妊娠2〜21日に摂餌量の有意な低値がみられた.
哺育期間中には,1.5および5 mg/kg群では対照群と比べて摂餌量に有意差はみられなかった.15 mg/kg群では,対照群と比べて哺育4日に摂餌量の有意な低値がみられた.50 mg/kg群では,対照群と比べて哺育4日に摂餌量の低値傾向がみられた.
(4) 剖検
生存例においては,対照群では脾臓と脂肪組織の癒着が1例みられた.1.5 mg/kg群では,異常はみられなかった.5 mg/kg群では,胸腺萎縮が2例および肝臓の白色斑が1例みられた.15 mg/kg群では,胸腺萎縮が10例および前胃粘膜の肥厚が1例みられた.50 mg/kg群では,胸腺萎縮が7例,肝臓の白色斑が2例および前胃粘膜潰瘍が2例みられた.
50 mg/kg群の死亡例においては,胸腺萎縮が3例,腺胃粘膜暗赤色化が2例,副腎腫大が4例および前胃粘膜潰瘍が1例みられた.
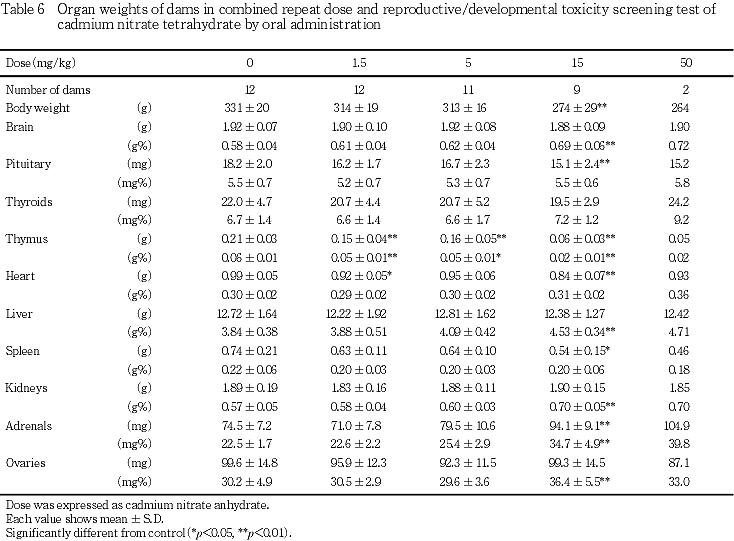
(5) 器官重量(Table 6)
剖検日の体重において,1.5および5 mg/kg群では対照群と比べて有意差はみられなかった.15 mg/kg群では,対照群と比べて体重の有意な低値がみられた.50 mg/kg群では,対照群と比べて体重の低値傾向がみられた.
器官重量において,1.5および5 mg/kg群では対照群と比べて胸腺の絶対および相対重量の有意な低値がみられた.15 mg/kg群では,対照群と比べて胸腺の絶対および相対重量の有意な低値,副腎の絶対および相対重量の有意な高値,脾臓の絶対重量の有意な低値,肝臓,腎臓および卵巣の相対重量の有意な高値がみられた.50 mg/kg群では,対照群と比べて胸腺の絶対および相対重量の低値傾向,副腎の絶対および相対重量の高値傾向,脾臓の絶対重量の低値傾向,肝臓,腎臓および卵巣の相対重量の高値傾向がみられた.
その他,1.5 mg/kg群では,対照群と比べて心臓の絶対重量の有意な低値がみられたが,高用量群で有意差は認められないことから,投与に基づく変化ではないと判断される.また,15 mg/kg群では,対照群と比べて下垂体および心臓の絶対重量の有意な低値,脳の相対重量の有意な高値がみられたが,それらは体重差に基づく変化と考えられることから,投与によるものではないと判断される.
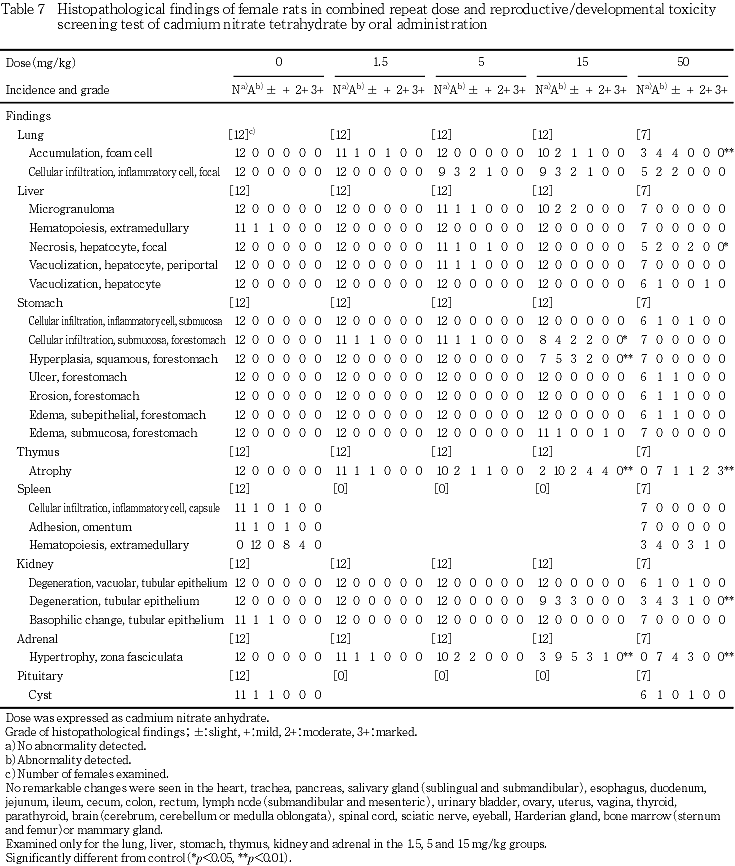
(6) 病理組織学検査(Table 7)
肺:1.5 mg/kg群では,泡沫細胞集簇が1例みられた.5 mg/kg群では,限局性の炎症性細胞浸潤が3例みられた.15 mg/kg群では,泡沫細胞集簇が2例および限局性の炎症性細胞浸潤が3例みられた.50 mg/kg群では,泡沫細胞集簇が4例および限局性の炎症性細胞浸潤が2例みられた.なお,泡沫細胞集簇は,50 mg/kg群で対照群と比べて有意差が認められた.
肝臓:5 mg/kg群では,限局性の肝細胞壊死が1例みられた.50 mg/kg群では,限局性の肝細胞壊死が2例および肝細胞空胞化が1例みられた.なお,限局性の肝細胞壊死は,50 mg/kg群で対照群と比べて有意差が認められた.
胃:1.5 mg/kg群では,前胃粘膜下織細胞浸潤が1例みられた.5 mg/kg群では,前胃粘膜下織細胞浸潤が1例みられた.15 mg/kg群では,前胃粘膜下織細胞浸潤が4例,前胃の扁平上皮過形成が5例および前胃粘膜下織水腫が1例みられた.50 mg/kg群では,粘膜下織炎症性細胞浸潤が1例,前胃潰瘍が1例,前胃糜爛が1例および前胃上皮下浮腫が1例みられた.前胃粘膜下織細胞浸潤および前胃の扁平上皮過形成は,15 mg/kg群で対照群と比べて有意差が認められた.
胸腺:1.5 mg/kg群では,萎縮が1例みられた.5 mg/kg群では,萎縮が2例みられた.15 mg/kg群では,萎縮が10例みられた.50 mg/kg群では,萎縮が7例みられた.萎縮は,15および50 mg/kg群で対照群と比べて有意差が認められた.
腎臓:15 mg/kg群では,尿細管上皮変性が3例みられた.50 mg/kg群では,尿細管上皮空胞変性が1例および尿細管上皮変性が4例みられた.尿細管上皮変性は,50 mg/kg群で対照群と比べて有意差が認められた.
副腎:1.5 mg/kg群では,束状帯肥大が1例みられた.5 mg/kg群では,束状帯肥大が2例みられた.15 mg/kg群では,束状帯肥大が9例みられた.50 mg/kg群では,束状帯肥大が7例みられた.束状帯肥大は,15および50 mg/kg群で対照群と比べて有意差が認められた.
その他に認められた変化は,対照群でも通常観察される変化であること,投与群の変化は対照群の出現頻度と比べて差がないことから,偶発的変化と判断される.
50 mg/kg群の死亡例においては,肺に鬱血が2例および限局性の線維化が1例,肝臓に限局性の肝細胞壊死が4例および微小肉芽腫が1例,胃に粘膜の黄褐色色素沈着が1例,前胃の限局性潰瘍が1例および腺胃鬱血が1例,胸腺に萎縮が1例,副腎に束状帯肥大が4例,鬱血が1例みられた.
交配開始前の投与期間(14日間)の発情回数は,各投与群とも対照群と比べて有意差はみられなかった.
交尾率はいずれの群とも100 %であった.交尾所要日数は,各投与群とも対照群との間に有意差はみられなかった.受胎率はいずれの群とも100 %であった.

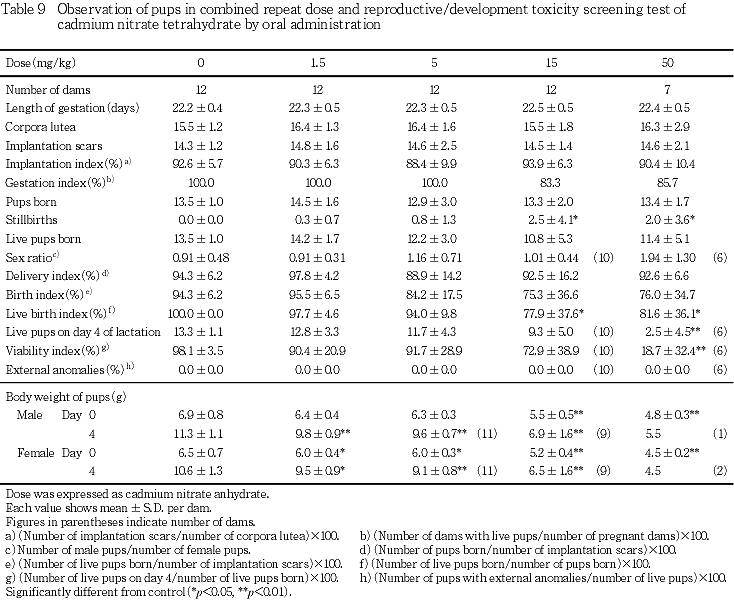
(2) 妊娠期間,分娩状態,妊娠黄体数,着床率および出産率(Table 9)
妊娠期間は,各投与群とも対照群と比べて有意差はみられなかった.
分娩状態において,対照群,1.5および5 mg/kg群では異常はみられなかった.15 mg/kg群の2母動物および50 mg/kg群の1母動物では,出産児が全例死亡したため,新生児は得られなかった.
各投与群とも,対照群と比べて妊娠黄体数,着床数および着床率に有意差はみられなかった.
出産率は,対照群,1.5および5 mg/kg群では100 %であった.15 mg/kg群では,2母動物で新生児が得られなかったため,出産率は83.3 %であった.50 mg/kg群では,1母動物で新生児が得られなかったため,出産率は85.7 %であった.なお,50 mg/kg群の5母動物は,妊娠後期に死亡したため出産率の集計から除外した.
哺育状態において,対照群および1.5 mg/kg群では異常はみられなかった.5 mg/kg群では,1母動物で巣作り不良および乳頭発育不良がみられ,全新生児が死亡した.15 mg/kg群では,3母動物で巣作り不良および乳頭発育不良がみられ,1母動物の全新生児は死亡した.50 mg/kg群では,3母動物で巣作り不良および乳頭発育不良,1母動物で巣作り不良がみられ,4母動物の全新生児が死亡した.
1.5および5 mg/kg群では,対照群と比べて総出産児数,死産児数,哺育0日の新生児数,性比,分娩率,児の産出率および出生率に有意差はみられなかった.15 mg/kg群では,対照群と比べて哺育0日の新生児数および児の産出率の低値傾向,出生率の有意な低値,死産児数の有意な高値がみられた.50 mg/kg群では,対照群と比べて出生率の有意な低値,死産児数の有意な高値,哺育0日の新生児数および児の産出率の低値傾向がみられた.
(2) 児動物の一般状態および生存率(Table 9)
1.5および5 mg/kg群では,対照群と比べて哺育4日の生存児数および哺育4日の生存率に有意差はみられなかった.15 mg/kg群では,対照群と比べて哺育4日の生存児数および哺育4日の生存率の低値傾向がみられた.50 mg/kg群では,対照群と比べて哺育4日の生存児数および哺育4日の生存率の有意な低値がみられた.
新生児の外表観察においては,対照群,各投与群とも異常はみられなかった.
新生児の一般状態において,対照群,1.5および5 mg/kg群では異常はみられなかった.15 mg/kg群では,2母動物の新生児で体温下降がみられた.50 mg/kg群では,4母動物の新生児で体温下降がみられた.
(3) 児動物の体重推移(Table 9)
1.5 mg/kg群では,対照群と比べて哺育4日に雄体重,哺育0および4日に雌体重の有意な低値,哺育0日に雄体重の低値傾向がみられた.5 mg/kg群では,対照群と比べて哺育4日に雄体重,哺育0および4日に雌体重の有意な低値,哺育0日に雄体重の低値傾向がみられた.15 mg/kg群では,対照群と比べて哺育0および4日に雌雄体重の有意な低値がみられた.50 mg/kg群では,対照群と比べて哺育0日に雌雄体重の有意な低値,哺育4日に雌雄体重の低値傾向がみられた.
(4) 児動物の剖検
対照群,1.5,15および50 mg/kg群では,異常はみられなかった.5 mg/kg群では,腎盂拡張が雄1例みられたが,偶発例と考えられる.
雄に関しては,死亡および瀕死例はいずれの群にも認められなかった.一般状態では,5 mg/kg以上の群で一過性の流涎がみられたが,被験物質の刺激性に基づくものと判断され,毒性症状とはみなさなかった.体重において,15 mg/kg以上の群でほぼ投与期間を通して低値がみられた.摂餌量においては,15 mg/kg群で一過性の低値,50 mg/kg群でほぼ投与期間を通して低値がみられた.尿検査において,50 mg/kg群で尿量の高値傾向およびpHの低値傾向がみられた.血液学検査において,1.5 mg/kg以上の群でフィブリノーゲンの低値,15 mg/kg以上の群でヘモグロビン,MCV,MCH,PTおよびAPTTの低値,50 mg/kg群で赤血球数,ヘマトクリットの低値ならびに血小板数の高値がみられた.血液生化学検査において,5 mg/kg以上の群で総蛋白の低値ならびに無機リンの高値,15 mg/kg以上の群でALPの低値ならびにALTの高値,50 mg/kg群でアルブミンおよびNaの低値,AST,γ-GTPおよび総コレステロールの高値がみられた.剖検では,投与に起因する変化はみられなかった.器官重量では,50 mg/kg群で胸腺の絶対重量の低値,副腎の絶対重量の高値,肝臓,脾臓,腎臓および副腎の相対重量の高値がみられた.病理組織学検査では,肺において5 mg/kg以上の群で泡沫細胞集簇および限局性の炎症性細胞浸潤がみられた.肝臓において,5および50 mg/kg群で限局性の肝細胞壊死がみられた.膵臓において,50 mg/kg群で限局性の腺細胞変性がみられた.腎臓において50 mg/kg群で尿細管上皮変性および尿細管上皮空胞変性がみられた.副腎において,15 mg/kg以上の群で束状帯肥大がみられた.精巣において,50 mg/kg群で限局性の精細管変性がみられた.骨髄において,50 mg/kg群で限局性の変性および造血減少がみられた.以上のように,硝酸カドミウム四水和物の一般毒性学的影響としては肺,肝臓,膵臓,腎臓,副腎,精巣および骨髄への影響が顕著であった.器官重量で認められた50 mg/kg群の胸腺の絶対重量の低値ならびに脾臓の相対重量の高値は,それらの器官・組織に病理組織学的影響はみられなかったことから,軽微な変化と考えられる.
雌に関しては,50 mg/kg群で5例が妊娠末期に死亡した.50 mg/kg群の死亡例では,一般状態観察において自発運動の低下,体温下降および口の周囲の汚れ,剖検において胸腺萎縮,腺胃粘膜暗赤色化,前胃粘膜潰瘍および副腎腫大,病理組織学的には肺に鬱血および限局性の線維化,肝臓に限局性の肝細胞壊死,胃粘膜の黄褐色色素沈着,前胃の限局性潰瘍,腺胃鬱血,胸腺に萎縮,副腎に束状帯肥大および鬱血が認められた.したがって,呼吸器障害,消化管障害あるいは全身状態の悪化による衰弱が死因と考えられる.一般状態観察において,雄の場合と同様に15および50 mg/kg群で認められた流涎は毒性症状とはみなさなかった.体重において,交配開始前および交配期間中に50 mg/kg群で低値,妊娠および哺育期間中に15 mg/kg以上の群で低値がみられた.摂餌量において,交配開始前,妊娠および哺育期間中とも,15 mg/kg以上の群で低値あるいは低値傾向がみられた.剖検において,5 mg/kg群で胸腺萎縮および肝臓の白色斑,15 mg/kg群で胸腺萎縮および前胃粘膜の肥厚,50 mg/kg群で胸腺萎縮,肝臓の白色斑および前胃粘膜潰瘍がみられた.器官重量では,1.5 mg/kg以上の群で胸腺の絶対および相対重量の低値あるいは低値傾向,15 mg/kg以上の群で副腎の絶対および相対重量の高値あるいは高値傾向,脾臓の絶対重量の低値あるいは低値傾向,肝臓,腎臓および卵巣の相対重量の高値あるいは高値傾向がみられた.病理組織学検査では,肺において1.5 mg/kg群で泡沫細胞集簇,5 mg/kg群で限局性の炎症性細胞浸潤,15 mg/kg群で泡沫細胞集簇および限局性の炎症性細胞浸潤,50 mg/kg群で泡沫細胞集簇および限局性の炎症性細胞浸潤,肝臓において5 mg/kg群で限局性の肝細胞壊死,50 mg/kg群で限局性の肝細胞壊死および肝細胞空胞化,胃において1.5 mg/kg群で前胃粘膜下織細胞浸潤,5 mg/kg群で前胃粘膜下織細胞浸潤,15 mg/kg群で前胃粘膜下織細胞浸潤,前胃の扁平上皮過形成および前胃粘膜下織水腫,50 mg/kg群で粘膜下織炎症性細胞浸潤,前胃潰瘍,前胃糜爛および前胃上皮下浮腫,胸腺において1.5 mg/kg以上の群で萎縮,腎臓において15 mg/kg群で尿細管上皮変性,50 mg/kg群で尿細管上皮空胞変性および尿細管上皮変性,副腎において1.5 mg/kg以上の群で束状帯肥大がみられた.以上のように,硝酸カドミウム四水和物の一般毒性学的影響としては雄の場合と同様に肺,肝臓,腎臓および副腎への影響が顕著であった.また,病理組織学検査において雄では影響は認められなかった胃および胸腺にも異常がみられた.しかし,病理組織学検査において雄で影響の認められた膵臓および骨髄に異常はみられなかった.器官重量で認められた15 mg/kg以上の群の脾臓の絶対重量の低値あるいは低値傾向,卵巣の相対重量の高値あるいは高値傾向は,それらの器官・組織に病理組織学的影響はみられなかったことから,軽微な変化と考えられる.なお,ヒトにおいて低レベルのカドミウムに長期間暴露したときの主症状は,慢性の閉塞性肺疾患,肺気腫および慢性腎尿細管障害であり,心血管および骨格系にも影響が生じるとされている1, 2).したがって,当試験において肺に認められた組織学的変化は,ヒトにおいてカドミウムに長期間暴露したときに肺に生じる変化と類似したものと考えられる.
親動物の生殖発生に対しては,前述したように50 mg/kg群でも精巣,精巣上体,精嚢,前立腺,卵巣,子宮,腟および乳腺に病理組織学的変化は認められなかった.また,発情回数,交尾率,交尾所要日数,受胎率,妊娠黄体数,着床数,着床率および妊娠期間では,投与に起因する変化はみられなかった.分娩状態において,15 mg/kg群の2母動物および50 mg/kg群の1母動物では,出産児が全例死亡した.哺育状態において,5 mg/kg群の1母動物で哺育行動異常がみられ,全新生児が死亡した.15 mg/kg群では3母動物で哺育行動異常がみられ,1母動物の全新生児が死亡した.50 mg/kg群では4母動物で哺育行動異常がみられ,4母動物の全新生児が死亡した.すなわち,5 mg/kg以上の群で哺育状態に異常が認められ,15 mg/kg以上の群で哺育率が低値傾向にあると考えられる.したがって,当試験条件下における硝酸カドミウム四水和物の生殖発生毒性学的な無影響量は,雄親動物が50 mg/kg/day,雌親動物が1.5 mg/kg/dayと考えられる.
児動物に対しては,15 mg/kg以上の群で哺育0日の新生児数および児の産出率の低値傾向,出生率の低値,死産児数の高値,体温下降がみられた.また,15 mg/kg以上の群で哺育4日の生存児数および哺育4日の生存率の低値傾向あるいは低値がみられた.新生児の外表観察において,投与に起因する異常はみられなかった.児動物の体重では,1.5 mg/kg以上の群で哺育0および4日に雌雄体重の低値あるいは低値傾向がみられた.児動物の剖検では,投与に起因する変化はみられなかった.
以上のように,硝酸カドミウム四水和物の一般毒性学的無影響量は,雄では1.5 mg/kg投与によりフィブリノーゲンの低値が認められたことから1.5 mg/kg/day未満,雌では1.5 mg/kg投与により胸腺の絶対および相対重量の低値,肺,胃,胸腺および副腎の組織学変化が認められたことから1.5 mg/kg/day未満と考えられる.また,生殖発生毒性学的な無影響量は,雄では50 mg/kg投与しても交尾能および授胎能に影響が認められなかったことから50 mg/kg/day,雌では5 mg/kg投与により哺育行動異常が認められたことから1.5 mg/kg/dayと考えられる.児動物では,1.5 mg/kg投与により体重の低値が認められたことから,1.5 mg/kg/day未満と考えられる.
| 1) | K. Nomiyama, Sci. Total Environ., 14, 199(1980). |
| 2) | L. Friberg, T. Kjellstrom, "Disorders of Mineral Metabolism," Vol. 1, eds. by F. Bronner, J. W. Coburn, Academic Press, Inc., New York, 1981, pp. 318-334. |
| 連絡先 | |||
| 試験責任者: | 古橋忠和 | ||
| 試験担当者: | 長瀬孝彦,内藤一嘉,岡田雅昭,木村 均,吉島賢一 | ||
| (株)日本バイオリサーチセンター 羽島研究所 | |||
| 〒501-6251 岐阜県羽島市福寿町間島6-104 | |||
| Tel 058-392-6222 | Fax 058-392-1284 | ||
| Correspondence | ||||
| Authors: | Tadakazu Furuhashi(Study director) Takahiko Nagase, Kazuyoshi Naito, Masaaki Okada, Hitoshi Kimura, Ken-ichi Yoshijima | |||
| Nihon Bioresearch Inc. | ||||
| 6-104, Majima, Fukuju-cho, Hashima, Gifu, 501-6251, Japan | ||||
| Tel +81-58-392-6222 | Fax +81-58-392-1284 | |||