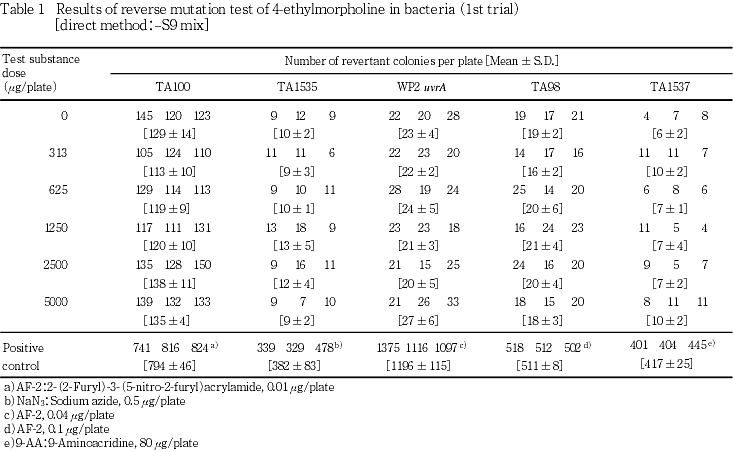
試験は,指標菌株としてSalmonella typhimurium TA100,TA1535,TA98,TA1537およびEscherichia coli WP2 uvrAを用い,S9 mix 非存在(直接法)および存在(代謝活性化法)下でプレインキュベーション法により行った.
用量は,用量設定試験の結果,5000 μg/plateまでの用量で直接法および代謝活性化法ともに全ての菌株において生育阻害が認められなかったため,313〜5000 μg/plateの範囲(公比2)で設定した.
試験を2回行った結果,代謝活性化の有無にかかわらず,全ての菌株において復帰変異コロニー数の増加は認められず,また,菌の生育阻害も認められなかった.
以上の成績から,4-エチルモルホリンの細菌に対する遺伝子突然変異誘発性は陰性と判定した.
試験に際して,各凍結菌株を解凍後,その25 μLをニュートリエントブロス(Bacto nutrient broth dehydrated,Difco Laboratories)液体培地 15 mL に接種し,37℃で12時間振盪培養した.培養後の懸濁菌液は濁度を測定し,濁度と生菌数の換算式より1 mLあたり1×109以上の生菌数が得られていることを確認し,試験菌液とした.
各菌株の遺伝的特性検査は,凍結保存菌の調製時並びに各実験ごとに行い,本試験に用いた菌株が規定の特性を保持していることを確認した.
実験終了後,残余被験物質を分析した結果,安定性に問題はなかった.
| AF-2 | : | 2-(2-フリル)-3-(5-ニトロ-2-フリル)アクリルアミド(和光純薬工業) |
| 2-AA | : | 2-アミノアントラセン(和光純薬工業) |
| NaN3 | : | アジ化ナトリウム(和光純薬工業) |
| 9-AA | : | 9-アミノアクリジン(Aldrich Chemical) |
| 硫酸マグネシウム・七水塩 | 0.2 g |
| クエン酸・一水塩 | 2 g |
| リン酸水素二カリウム | 10 g |
| リン酸一アンモニウム | 1.92 g |
| 水酸化ナトリウム | 0.66 g |
| グルコース | 20 g |
| 寒天(OXOID Agar No.1) | 15 g |
試験管に使用溶媒0.1 mL,被験物質供試液0.1 mLあるいは陽性対照物質溶液0.1 mLを入れ,次いで直接法では 0.1 Mリン酸ナトリウム緩衝液(pH 7.4)を0.5 mL,代謝活性化法では S9 mix を0.5 mL加え,続いて試験菌液0.1 mLを分注し,37℃で20分間振盪培養した.培養終了後,45℃に保温したトップアガー2 mLを加えた混合液をプレート上に重層した.37℃で48時間培養後,復帰変異コロニーを計数し,同時に指標菌株の生育阻害の有無を実体顕微鏡を用いて観察した.プレートは,用量設定試験では各用量とも1枚,本試験では3枚を使用した.本試験は,同一用量を用いて2回行った.
但し,明確な用量依存性が認められない場合においても,陽性値を示す試験結果に再現性が認められれば陽性と判定することとした.
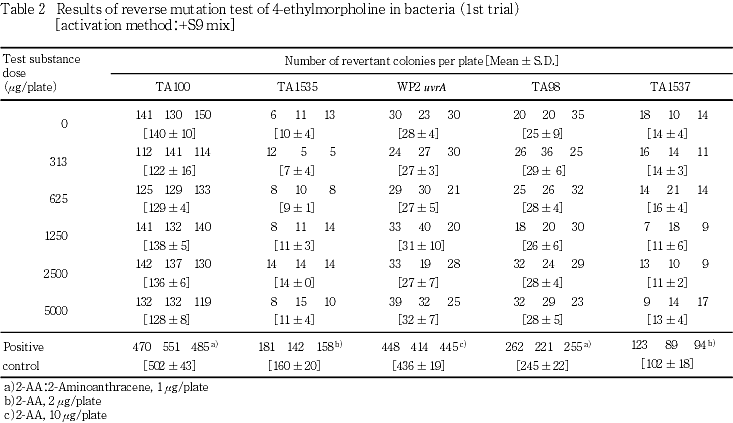
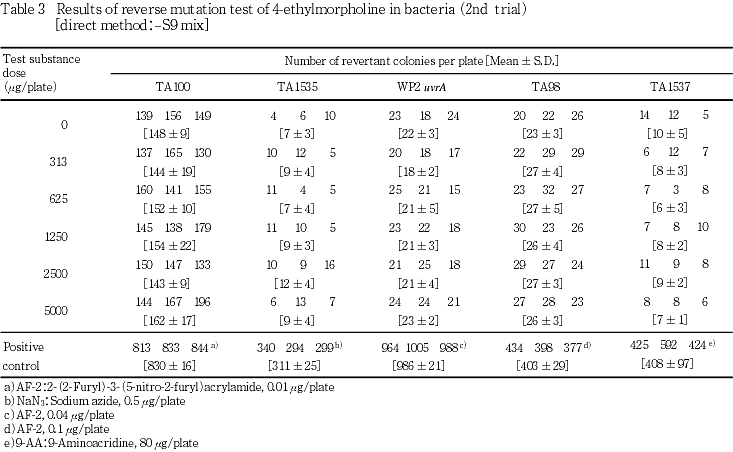
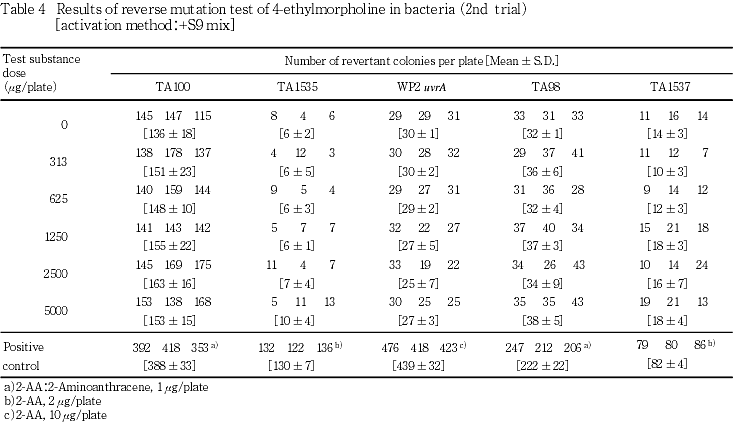
試験を2回行った結果(Tables 1〜4),直接法および代謝活性化法のいずれの場合も,供試した全ての菌株において復帰変異コロニー数は,溶媒対照値の2倍を越えることはなく,また,菌の生育阻害も認められなかった.
以上の成績から,本実験条件下では,4-エチルモルホリンの遺伝子突然変異誘発性は陰性と判定した.
4-エチルモルホリンの変異原性については,Salmonella typhimuriumを用いた復帰突然変異試験で,ラットおよびハムスターの肝臓から調製された3濃度のS9を用いた代謝活性化法によるTA1535で弱い陽性または疑陽性との結果3)が報告されている.それらは,いずれも6667または10000 μg/plateの高用量で認められた結果であり,3333 μg/plate以下の用量では復帰変異コロニー数の増加は認められていない.今回の試験で設定した5000 μg/plate以下の用量では,陽性または疑陽性の結果は得られなかった.また,L5178Y細胞を用いたマウスリンフォーマアッセイおよびBALB/3T3細胞を用いたトランスフォーメーションアッセイでいずれも陰性4)と報告されている.
4-エチルモルホリンの類縁化合物の変異原性について,モルホリンは,L5178Y細胞を用いたマウスリンフォーマアッセイおよびBALB/3T3細胞を用いたトランスフォーメーションアッセイでいずれも陽性4),また,N-メチルモルホリンオキシドは,同様の試験でいずれも陰性4)と報告されている.N-ニトロソモルホリンは,E. coli PQ37 strainを用いたSOS chromotest で陽性5),S. typhimuriumを用いた宿主経由試験および体細胞突然変異試験でいずれも陽性6),ショウジョウバエを用いた伴性劣性致死試験で陽性6),V79細胞およびシリアンハムスター由来の培養細胞を用いた体細胞突然変異試験でいずれも陽性6),ラット肝細胞を用いた不定期DNA試験で陽性6),シリアンハムスター由来の培養細胞を用いた細胞形質転換試験で陽性6),ラットリンパ球を用いた染色体異常試験で陽性6),マウスを用いた優性致死試験で陰性6)と報告されている.

| 1) | Maron DM, Ames BN:Revised methods for the Salmonella mutugenitiy test. Mutation Research, 113:173-215(1983). |
| 2) | Green MHL:“Handbook of Mutagenicity Test Procedures”, Vol.3, Kilbey BJ, Legator M, Nichols W, Ramel C(eds.), Elsevier, Amsterdam, New York, Oxford(1984)pp.161-187. |
| 3) | Zeiger E, Anderson B, Howorth S, Lawlor T, Mortelmans K, Speck W:Salmonella Mutagenicity Tests,  . Results from the testing of 255 chemicals. Environmental and Molecular Mutagenesis, 19:1-110(1987). . Results from the testing of 255 chemicals. Environmental and Molecular Mutagenesis, 19:1-110(1987). |
| 4) | Conaway CC, Myhr BC, Rundell JO, Brusick DJ:Evaluation of morpholine, piperazine and analogues in the L5178Y mouse lymphoma assay and BALB/3T3 transformation assay. Environmental Mutagenesis, 4:390(1982). |
| 5) | Quillardet P, Bellecombe C, Hofnung M:The SOS chromotest, a colorimetic bacterial assay for genotoxins, validation study with 83 compounds. Mutation Research, 147:79-95(1985). |
| 6) | 賀田恒夫,石館 基(監修):「環境変異原データ集1」サイエンティスト,東京(1980)p.317. |
| 連絡先 | |||
| 試験責任者: | 野田 篤 | ||
| 試験担当者: | 野田 篤,昆 尚美 | ||
| (財)畜産生物科学安全研究所 | |||
| 〒229-1132 神奈川県相模原市橋本台3-7-11 | |||
| Tel 042-762-2775 | Fax 042-762-7979 | ||
| Correspondence | ||||
| Authors: | Atsushi Noda(Study director) Naomi Kon | |||
| Research Institute for Animal Science in Biochemistry and Toxicology 3-7-11 | ||||
| Hashimotodai, Sagamihara-shi, kanagawa, 229-1132 Japan | ||||
| Tel +81-42-762-2775 | Fax +81-42-762-7979 | |||