4-エチルモルホリンの28日間反復経口投与毒性試験(回復14日間)を雌雄のSprague-Dawley系ラットを用いて実施した.雌雄とも50,200および800 mg/kgの用量で被験物質を投与する3群ならびに媒体である注射用水を投与する対照群の計4群を設定し,各群5匹(対照群および800 mg/kg投与群は回復試験用5匹を加えた10匹)の動物に28日間反復強制経口投与した.
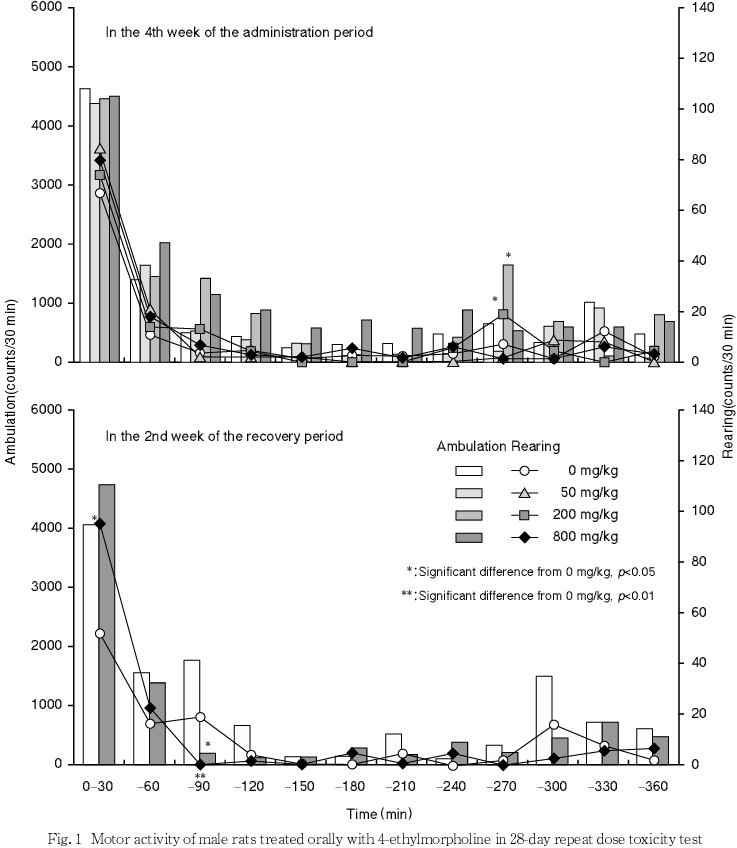
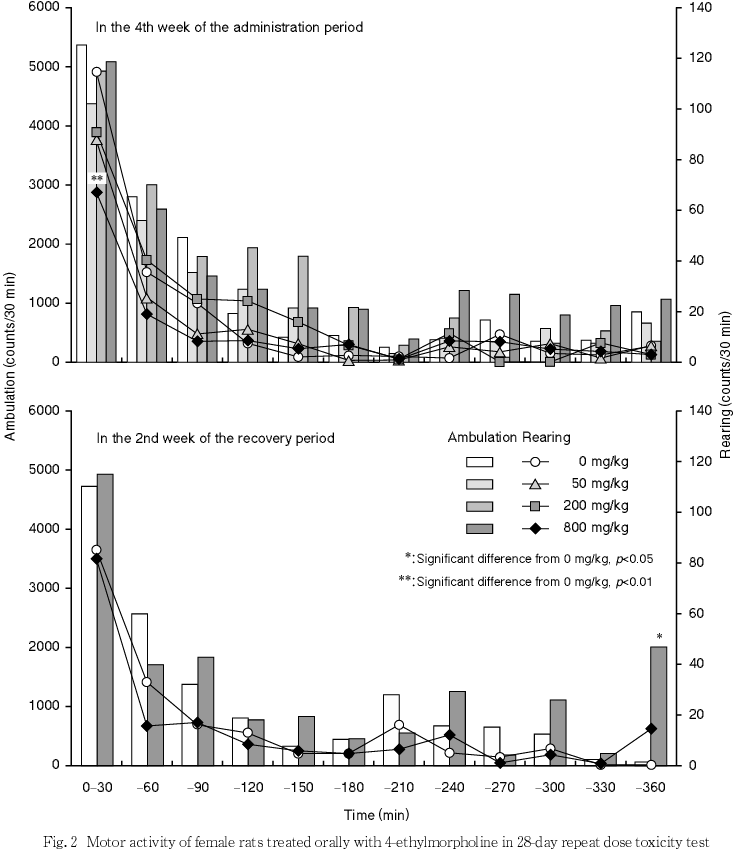
死亡例はなく,一般状態の変化として,200および800 mg/kg投与群では,ケージ内を舐める動作および咀嚼様動作が観察され,800 mg/kg投与群では,動作振戦,活動性低下,うずくまり,閉眼および流涎も散見された.詳細な臨床観察において,800 mg/kg投与群では,雌雄で動作振戦が観察され,回復期間を含めて接触に対する反応がやや過敏となり,ケージからの取り出し時およびハンドリング時に発声する個体が増加した.また,同群の雌では歩行時,断続的に停止し,腹臥位を呈する個体が散見された.自発運動量測定において,800 mg/kg投与群では,雌雄各個体で位置移動が認められない時間帯が少ない傾向にあり,雌で投与後30分間の立上がり回数が減少し,雄で回復期間中に測定開始後30分間の立ち上がり回数が増加した.
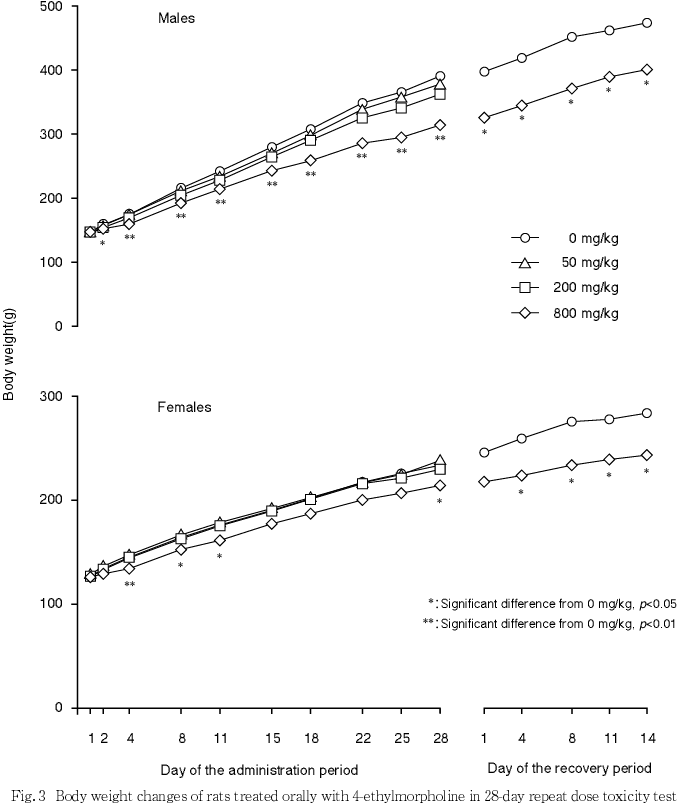
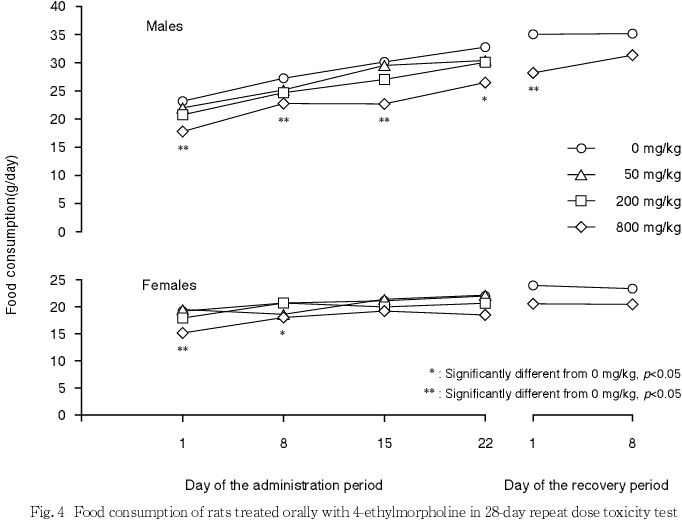
800 mg/kg投与群では,雌雄とも摂餌量が減少し,体重増加が抑制された.
尿検査では,800 mg/kg投与群の雄で尿蛋白が減少し,雌でケトン体およびウロビリノーゲンが増加して尿比重が低下した.
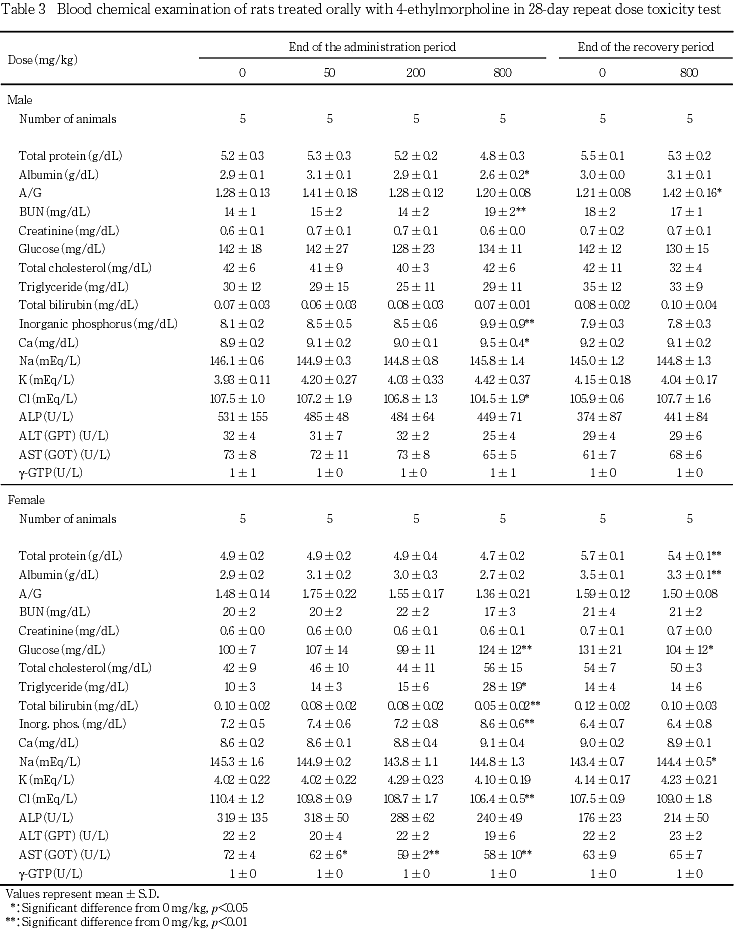
血液および血液生化学検査では,800 mg/kg投与群の雌雄で無機リン濃度が上昇し,塩素濃度が低下したほか,雄でカルシウム濃度が上昇した.また,同群の雄でプロトロンビン時間および活性部分トロンボプラスチン時間が短縮し,アルブミン濃度の低下および尿素窒素濃度の上昇が認められたほか,雌でブドウ糖濃度およびトリグリセライド濃度の上昇ならびに総ビリルビン濃度の低下が認められた.
病理学検査では,800 mg/kg投与群において,雌雄で肝臓と腎臓の重量が増加し,組織学的に小葉中心性の肝細胞肥大および遠位尿細管あるいは遠位からヘンレ係蹄にかけての上皮細胞の空胞化が観察された.この他,雄では副腎重量が増加した.
以上の結果から,本試験条件下における4-エチルモルホリンの無作用量は雌雄とも50 mg/kg/dayであると考えられた.また,毒性標的器官は中枢神経系,肝臓,腎臓であることが示唆され,肝臓および腎臓の変化は14日間の投与中止により回復したが,中枢神経系に対する作用の一部は回復しなかった.
投与検体は,溶媒である日局注射用水(製造番号A106AA,光製薬)に被験物質を溶解して高用量を調製してから,段階希釈して他の用量を調製した. 投与検体は,8日間の安定性が確認されているため1週間に1回の頻度で調製し,使用時まで冷蔵庫にて保管した.また,含量測定の結果,各濃度の投与検体中には所定濃度の被験物質が含有されていることが確認された.
群分けは,投与開始日前日の体重に基づいて体重別層化無作為抽出法により行った.各群の動物数は,雌雄とも対照群および高用量群を各10匹とし,低および中用量群を各5匹とした.
動物は,温度21.0〜25.0℃,湿度40.0〜75.0 %,換気回数約15回/時および照明12時間(7時〜19時点灯)に設定された飼育室内で,金属製金網床ケージに1匹ずつ収容し,固型飼料(CE-2,日本クレア)と水道水(秦野市水道局給水)を自由に摂取させて飼育した.
投与経路は経口とし,1日1回,28日間,ラット用胃管を用いて強制的に投与し,最終投与日翌日に剖検した.投与容量は5 mL/kgとし,雌雄とも最近時の体重をもとに個体別に投与液量(mL)を算出した.なお,回復期間は14日間とした.
体重は,投与第1週には3回,その後は毎週2回の頻度で測定したほか,投与期間終了日,回復期間終了日および剖検日にも測定した.
 法,Rate),ALP活性(GSCC法),AST(GOT)活性(IFCC法),ALT(GPT)活性(IFCC法),γ-GTP活性(IFCC法),トリグリセライド濃度(GPO・HDAOS法,グリセリン消去法),総ビリルビン濃度(アゾビリルビン変法),無機リン濃度(モリブデン 酸直接法)およびカルシウム 濃度(OCPC法)を測定し,A/G比を算出した.また,全自動電解質分析装置(EA05,エーアンドティ)により,ナトリウム濃度,カリウム濃度および塩素濃度(いずれもイオン電極法)を測定した.
法,Rate),ALP活性(GSCC法),AST(GOT)活性(IFCC法),ALT(GPT)活性(IFCC法),γ-GTP活性(IFCC法),トリグリセライド濃度(GPO・HDAOS法,グリセリン消去法),総ビリルビン濃度(アゾビリルビン変法),無機リン濃度(モリブデン 酸直接法)およびカルシウム 濃度(OCPC法)を測定し,A/G比を算出した.また,全自動電解質分析装置(EA05,エーアンドティ)により,ナトリウム濃度,カリウム濃度および塩素濃度(いずれもイオン電極法)を測定した.
回復試験第2週では,800 mg/kg投与群の雄で開始直後から30分にかけての立上がり回数の増加,ならびに開始後60から90分にかけての位置移動回数および立上がり回数の減少が有意な変化となった.800 mg/kg投与群の雄で測定開始後60分から90分に観察された立ち上がり回数および位置移動回数の低下は,測定開始直後から30分に立ち上がり回数(探索行動)が亢進したことによる反動であり,抑制性の作用によるものではないと考えられた.雌では,開始後330分から360分にかけての位置移動回数が有意に増加したが,投与期間中に認められなかった変化であること,環境変化による探索行動が沈静化した後に認められた増加であることから,被験物質の作用の継続ないし退薬症候ではないと判断した.

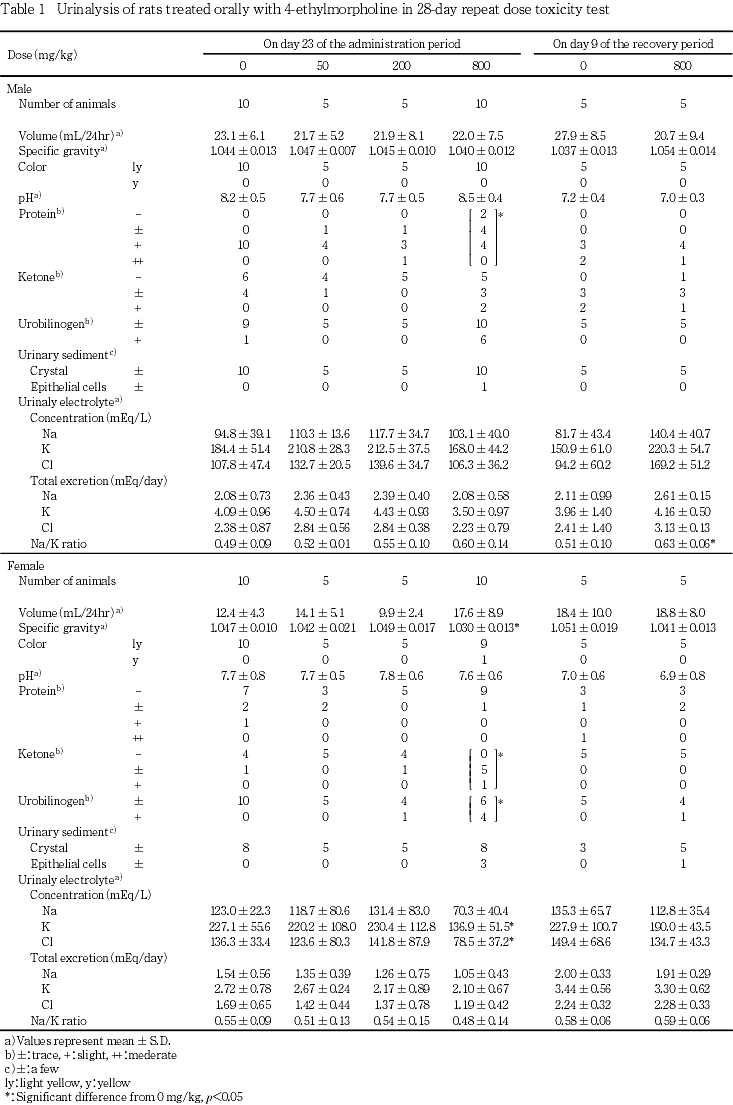
回復期間終了時剖検例では,800 mg/kg投与群の雌で,血小板数が有意に増加し,血色素量が有意に低下した.投与期間終了時に貧血を示唆するような所見は観察されていないことから,血色素量の低下は被験物質投与による影響ではないと判断した.
なお,投与期間終了時剖検例のうち,50および200 mg/kg投与群の雄各1例は,投与第4週の握力検査時に爪が剥がれてその後数日間出血が認められたが,本来の被験物質投与に起因した変化が不明瞭となることが懸念されたため,この2例の血液学検査データは統計解析から除外することとした.
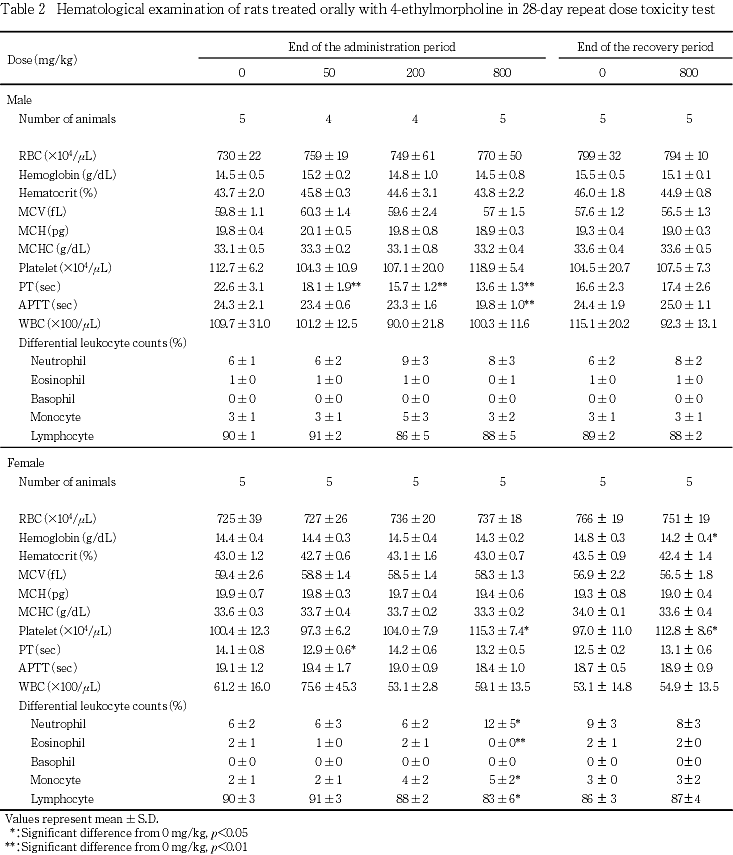
回復期間終了時剖検例では,800 mg/kg投与群において,雄でA/G比が有意に上昇し,雌で総蛋白濃度およびアルブミン濃度が有意に低下した.なお,同群の雌ではナトリウム濃度が有意に上昇したが,生体内における電解質濃度の調節は速やかに行われるため,投与期間終了時に認められた塩素濃度低下の影響である可能性は少ないこと,この他の電解質濃度は変化していないことから,投与中止による変化ではないと判断した.また,800 mg/kg投与群の雌では,ブドウ糖濃度が低下したが,投与期間中には認められていないことから,被験物質投与の影響によるものではないと判断した.
回復期間終了時剖検例では,800 mg/kg投与群の雌雄で,解剖時体重が有意に低下し,脳の相対重量が有意に増加したが,投与期間終了時の雄と同様,体重が低値であったために脳の相対重量増加が有意となったと判断した.また,800 mg/kg投与群の雄では,心臓および肝臓の実重量が有意に低下したが,投与期間中に認められた変化ではなく,また,相対重量も変化しなかったため,被験物質投与による影響ではないと判断した.
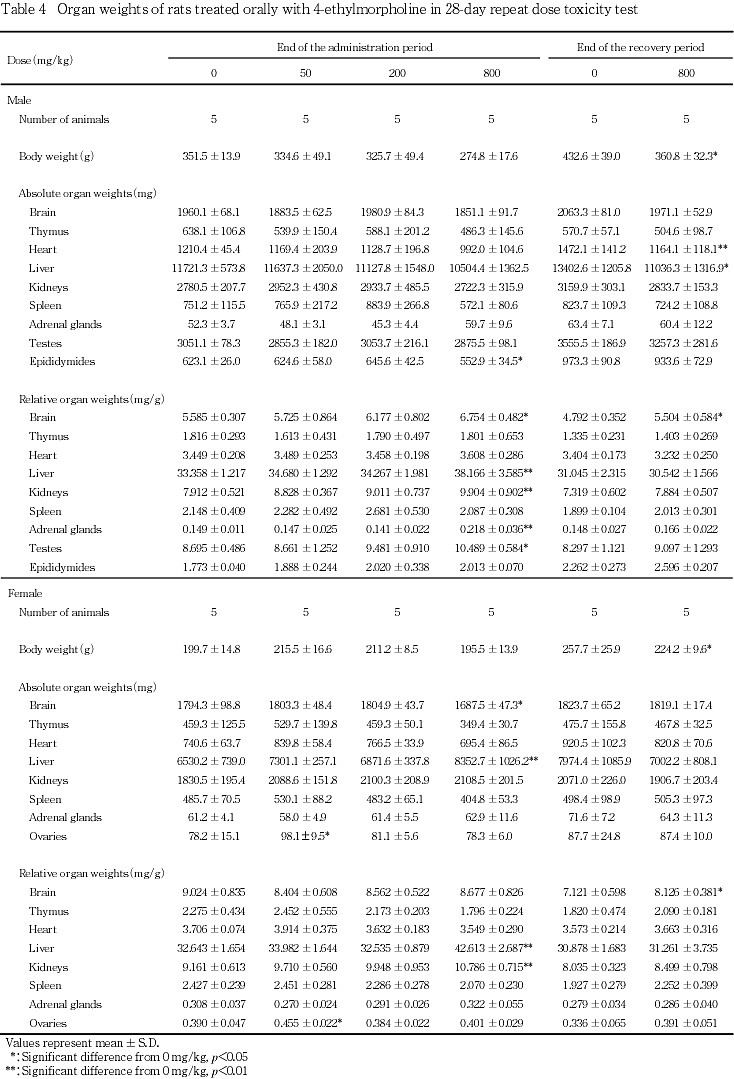
 投与期間終了時剖検例
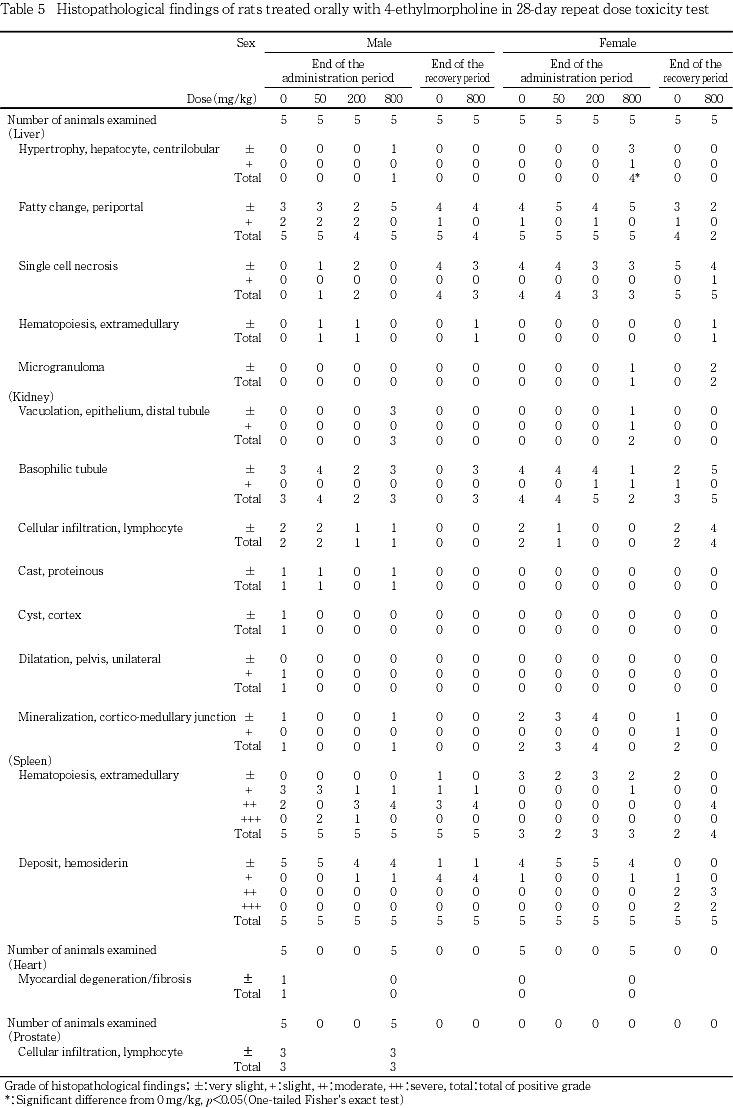
投与期間終了時剖検例腎臓では,800 mg/kg投与群の雄3例および雌2例で遠位尿細管あるいはヘンレ系蹄から遠位尿細管にかけての上皮細胞に空胞化が観察された.この他,対照群を含む雌雄各群で好塩基性尿細管が観察され,200および800 mg/kg投与群の雌を除く雌雄各群でリンパ球浸潤が,対照群の雌雄,50および200 mg/kg投与群の雌ならびに800 mg/kg投与群の雄で皮髄境界部の鉱質沈着が散見され,200 mg/kg投与群を除く雄の各群の各1例で蛋白円柱が,皮質の嚢胞あるいは腎盂拡張が雄の対照群の1例に認められたが,いずれも被験物質投与群で増強していないことから,被験物質投与に起因した変化ではないと判断した.
脾臓では,対照群を含む雌雄各群で,髄外造血およびヘモジデリン沈着が観察されたが,対照群と各被験物質投与群との間に発生頻度および程度とも差はなく,被験物質投与に起因した変化ではないと考えられた.
この他,心臓では,対照群の雄1例で,軽微な心筋の変性および線維化が観察され,前立腺では,雄の対照群および800 mg/kg投与群の各3例で軽微なリンパ球浸潤が認められたが,いずれも対照群に限り,あるいは対照群を含む被験物質投与群で認められた変化であったため,被験物質投与に起因した変化ではないと判断した.なお,対照群の雌1例で肉眼的に赤色化が認められた空腸および回腸には,変化が認められなかった.
 回復期間終了時剖検例
回復期間終了時剖検例腎臓では,対照群の雌および800 mg/kg投与群の雌雄で好塩基性尿細管が観察され,雌の各群でリンパ球浸潤が,対照群の雌で皮髄境界部の鉱質沈着が散見された.脾臓では,対照群を含む雌雄各群で髄外造血およびヘモジデリン沈着が観察された.しかし,いずれの変化も対照群のみあるいは対照群を含む各群で認められた変化であったため,被験物質投与に起因した変化ではないと判断した.
800 mg/kg投与群で動作振戦が観察された.4-エチルモルホリンの単回経口投与毒性試験(未公刊)および本試験予備試験で振戦および痙攣が認められていることから,4-エチルモルホリンの中枢神経系に対する興奮作用が示唆された.200および800 mg/kg投与群で観察されたケージ内を舐める動作および咀嚼様動作は,常同行動の一種であると考えられていることから,被験物質の中枢神経系への影響の一つであると判断した.また,800 mg/kg投与群の雌で投与後30分間に立ち上がり回数が減少したことから探索行動の抑制が,雌雄で静止することが少ない傾向にあったことから自発運動の亢進が示唆された.常同行動の発現時には,自発運動が亢進し,探索行動が抑制されることから,これら自発運動量の変化は,常同行動の発現と関連した変化であると考えられた.一方,800 mg/kg投与群の雄では,回復期間中に,開始直後から30分にかけての立ち上がり回数が増加した.投与期間中に立ち上がり回数は増加せず,雄1例で詳細な臨床観察における探索行動の亢進が認められたのみであったが,計測値として相反する常同行動が発現していたことにより抑制されていた可能性もあり,回復期間中に認められた立ち上がり回数の増加は被験物質投与による影響であると判断した.さらに,800 mg/kg投与群では,回復期間中を含めて接触に対する反応がやや過敏となり,ケージからの取り出し時ないしハンドリング時に発声する個体が増加したことから,易刺激性が示唆された.驚愕反応が1例でわずかに亢進したことも易刺激性によるものと考えられた.今回,易刺激性および探索行動の亢進といった4-エチルモルホリンの中枢神経系に対する作用の一部は投与を中止しても回復性を示さなかったが,本試験と同用量の4-エチルモルホリンを単回経口投与し,24時間後に尿中濃度を測定した試験では,投与量の約20〜70 %(平均約40 %)の4-エチルモルホリンが未変化体として尿中に検出されていること(未公刊),類似化合物であるモルホリンは,ラットではほとんど血漿蛋白質と結合せず,投与後24時間で70〜90 %が尿中に,残りが糞中と呼気中にいずれも未変化体として排泄されること(半減期115分)から6),被験物質の蓄積性によるものではなく,非可逆的あるいは,回復に時間を要する変化が中枢神経系に生じたためであると推測された.この他,800 mg/kg投与群では,うずくまり,活動性の低下,閉眼が観察されたが,同様の所見は,4-エチルモルホリンの単回投与毒性試験で痙攣ないし振戦が表れた後に認められていることから(未公刊),4-エチルモルホリンの中枢神経系に対する作用の一つであると考えられた.また,詳細な臨床観察時,800 mg/kg投与群の雌数例で断続的に歩行を停止して腹臥位を呈したが,脱力および歩行障害は観察されなかったことから,中枢神経系に対する作用と関連する可能性が示唆された.さらに,800 mg/kg投与群の雄2例雌1例では,投与後約2時間の観察時に流涎が,雌1例で流涎の痕跡が観察された.このうち雄1例を除く3例で動作振戦を伴っていたこと,4-エチルモルホリンの単回投与毒性試験でも振戦および流涎が観察されていること(未公刊),モルホリンのラット単回投与では振戦,自発運動の抑制の他,流涎および流涙が報告されていること7)から,投与後約2時間で観察された流涎は,4-エチルモルホリンの作用の一つであると考えられた.この他,800 mg/kg投与群の雌で血漿中ブドウ糖濃度が上昇したが,本試験では易刺激性が認められているもののストレス状態を示唆する所見はなく,ブドウ糖濃度の上昇が,4-エチルモルホリン投与によるものであるか否か判断出来なかった.また,800 mg/kg投与群の雄1例で回復期間中に探索行動の抑制が観察され,この例では,回復第1週に易刺激性も観察されたが,回復第2週では探索行動の抑制のみが観察されたため,被験物質投与の影響によるものであるか否か判断できなかった.また,投与第4週に800 mg/kg投与群の雌1例で身繕いが観察されたが,1例のみの変化であり,被験物質投与による影響であるか否か判断できなかった.
800 mg/kg投与群では,摂餌量が減少し,体重増加が抑制された.しかし,摂餌に影響を及ぼすような一般状態の変化は観察されていないこと,体重減少を示した800 mg/kg投与群の雄1例でも,摂餌量減少および排便量減少が観察された前日には常同行動以外の変化が認められなかったことから,摂餌量の減少および体重増加の抑制は,一般状態の悪化による二次的な変化ではないと考えられた.また,800 mg/kg投与群の雄で血中アルブミン濃度の低下および尿蛋白の減少が認められた.この週齢の雄ラットでは尿蛋白の大半がα2uグロブリンであることから8),尿蛋白の減少が,血中アルブミン濃度の低下を反映している可能性は低いが,尿蛋白が陰性だった個体で体重が低かったことから摂餌量減少と関連した変化である可能性が考えられた.雌の尿中ケトン体の増加は被験物質投与による変化である可能性はあるが,原因は不明であった.なお,回復期間に観察された血漿蛋白の変化は,被験物質投与による影響であるか否か判断できなかった.
800 mg/kg投与群の雌雄において,肝重量の増加および小葉中心性の肝細胞肥大が観察され,雌では,個体別にみて所見の一致があったことから,肝重量増加の一因として肝細胞肥大が示唆された.病理組織学的および血液生化学的に肝臓の損傷を示唆する所見はなく,肝細胞肥大が肝障害を意味するものではないと考えられたが,薬物代謝酵素の誘導を示す変化であるか否かは判断できなかった.この他,800 mg/kg投与群では,雄で血液凝固時間の短縮が認められ,雌でトリグリセライド濃度の上昇およびビリルビン濃度の低下が認められた.これらは,個体別にみて必ずしも肝臓の変化と一致しなかったが,肝重量がより増加した雄の1例では凝固時間が短縮し,雌の1例ではビリルビン濃度が低下してトリグリセライド濃度が上昇したことから,肝臓への影響と関連した変化である可能性が示唆された.また,800 mg/kg投与群の雌でみられた尿中ウロビリノーゲンの増加は,血漿中のビリルビン濃度の変化と関連する可能性もあるが,明らかではなかった.なお,肝細胞肥大を含め,いずれの変化も回復期間終了時には認められず,肝臓に関する所見は投与中止により回復すると考えられた.
800 mg/kg投与群では腎重量が増加し,組織学的にはヘンレ係蹄あるいは遠位の尿細管上皮に空胞化が観察された.雄で尿素窒素濃度がわずかに上昇した以外に,尿細管壊死や再生尿細管のような損傷を示唆する所見の増強はなく,個体別の比較では,尿素窒素濃度が高値となった1例で尿細管の空胞化が観察されたほかは,腎重量の増加と尿細管の空胞化あるいは尿素窒素濃度の増加を示す個体が必ずしも一致していなかった.また,雌では,尿比重低下を伴う尿量増加が示唆された.尿細管の空胞化が観察されたヘンレ係蹄および遠位尿細管は,主として水および電解質の再吸収を行っていることから,尿比重に影響が表れる可能性もあるが,個体別に比較して腎重量の増加および尿細管の空胞化が著しかった1例では比重および尿量は変化していなかった.類似化合物であるモルホリンは,マウスに経口投与することにより,腎機能低下が起こることおよびラット吸入暴露により肝臓および腎臓の重量が増加し,尿細管壊死が観察されることが確認されている9).また,モルホリンオレイン酸塩では,マウスに経口投与することにより腎重量の増加,血中尿素窒素濃度の上昇,尿比重増加および遠位尿細管の混濁腫脹が報告されている10).これらのことから,4-エチルモルホリンも同様に腎臓に作用する可能性が示唆されたが,組織所見は異なっており,遠位尿細管上皮の空胞化が何を示すのか本試験結果からは明らかとはならなかった.しかし,尿中に被験物質の未変化体が検出されていること(未公刊),被験物質は化学反応の触媒として利用されていることから,予備試験において,試験紙(クリニティック200+)が異常発色したこと,本試験の尿蛋白測定時のpH調整で800 mg/kg投与群の雄でより多くの酢酸を必要としたことは,尿中に被験物質が存在することを示唆するものであると考えられた.
800 mg/kg投与群で血漿中塩素濃度が低下した.今回,重炭酸濃度は測定していないため,カリウム濃度およびナトリウム濃度の和から塩素濃度を減ずることによりアニオンギャップを推測すると,塩素濃度がより低下した個体で増加する傾向にあり,塩素濃度低下の一因として,塩素以外の陰イオンの血中濃度が増加した可能性が示唆された.また,800 mg/kg投与群の雌雄で血中無機リン濃度が,雄でカルシウム濃度が上昇し,この変化は,塩素イオン濃度がより低値であった個体と一致する傾向にあった.血漿中電解質濃度の変化が,血液中に存在する被験物質の物理化学的影響によるものなのか,被験物質の生体に対する作用の結果であるのかは,本試験結果からは判断できなかったが,いずれも,14日間投与中止により回復することが確認された.また,800 mg/kg投与群では,雄で副腎重量が増加し,雌の1例でも高値を示したが,血漿電解質あるいは易刺激性といった変化に関連した所見であるのか判断できなかった.
以上の肝臓,腎臓,副腎および電解質の変化は,影響が強く表れた個体が一致する傾向にあり,被験物質投与による影響が相互に関連する,あるいは被験物質に対する感受性に個体差がある可能性が考えられた.また,28日間反復投与後に尿中の被験物質濃度を測定した試験では,尿中の被験物質濃度にばらつきがあったことから被験物質の影響の個体差が示唆されたが,雌雄全体として比較すると有意差があった項目に差異はあるものの,標的器官への影響は類似していることから性差は少ないと考えられた.
800 mg/kg投与群の雌雄において,投与保定時ないし投与直後から投与後約20分にかけて流涎が観察された.この流涎は投与第3週になってから認められ,この他の一般状態の変化と比較して発現時間が短く,投与前の保定段階でも観察された.刺激性物質の経口投与に際しては,しばしば反射性の流涎が観察されるが,本被験物質は刺激性を有するという情報があること,本被験物質の単回投与毒性試験において,被験物質の刺激性が示唆される腺胃粘膜の変化が観察されていることから,被験物質の物理的刺激による反射性の流涎であると考えられた.
この他,800 mg/kg投与群の雌では,好中球比率が上昇し,リンパ球比率が低下した.白血球百分比に白血球数を乗じることにより算出した白血球数で比較すると1例を除き,リンパ球数は対照群の範囲内にあり,好中球数は増加していたことから,好中球の増加による百分比の変動であることが示唆された.また,同様に計算して好酸球数の減少および単球数の増加が示唆されたが,この他の検査項目で関連する所見に変化は認められず,今回の試験結果のみでは,これら白血球数の変化と被験物質投与との関連は不明であった.この他,800 mg/kg投与群の雌で血小板数の増加が認められたが,同群の雄で観察された血液凝固系の変化と関連の有無,さらには被験物質投与による変化であるのか否かは本試験結果からは判断できなかった.
以上の結果から,本試験条件下における4-エチルモルホリンの無作用量は雌雄とも50 mg/kg/dayであると考えられた.また,4-エチルモルホリンの標的器官は中枢神経,肝臓,腎臓であることが示唆された.常同行動,易刺激性および振戦などの中枢神経興奮作用,肝重量および腎重量の増加ならびに肝細胞肥大および腎臓のヘンレ系蹄から遠位尿細管にかけての尿細管上皮細胞の空胞化が認められ,摂餌量低下を伴う体重増加抑制,塩素イオン濃度低下を主とした血液中の電解質濃度の変化が生じることが明らかとなった.これらの変化のうち,中枢神経に対する影響は14日間の投与中止によっても認められたが,その他は回復した.
| 1) | National toxicology program study overviews and general protocols. NTP home page. Last updated 11th Feb 2002. |
| 2) | Hazardous substances data bank national library of medicin's toxicology data network (TOXNETR). Last updated 10th May 2002. |
| 3) | Occupational safety & health administration U.S. department of labor. OSHA technical links, health guidelines, n-ethylmorpholine. Revision date 27th Apr 1999. |
| 4) | Smyth HF, Carpenter CP et al.:Range-finding toxicity data list V. Arch Ind Hyg Occupational Med, 10:61-68 (1954). |
| 5) | Maeda H, Omori M et al.:Comparison of historical control data between Crj:CD(SD)IGS and Crj:CD(SD) rats. In “Biological Reference Data on CD(SD)IGS Rats-1999” Matsuzawa T, Inoue H (eds.), CD(SD)IGS Study Group, Yokohama (1999) pp.106-118. |
| 6) | Sohn SO, Fiala SE et al.:Metabolism and disposition of morpholine in the rat, hamster, and guinea pig. Toxicol Appli Pharmacol, 64:486-491 (1982). |
| 7) | Patty's Industrial Hygiene and Toxicology, Vol. 2A, Clayton DG, Clayton EF (eds.), John Wiley & Sons, New York (1981) pp.2693-2697. |
| 8) | 堀内茂友,輿水 馨(編):B.動物別の尿性状B-1ラット.In「実験動物の生物学的特性データ」田嶋嘉雄(監修)ソフトサイエンス社,東京(1989) pp.205-208. |
| 9) | IARC Monographs on the evaluation of carcinogenic risks to humans. Vol.47, IARC working group, Lyon (1989) pp.199-213. |
| 10) | Shibata M, Kurata Y et al.:13-week subchronic toxicity study with morpholine oleic acid salt administered to B6C3F1 mice. J Toxicol Env Health, 22:187-194 (1987). |
| 連絡先 | |||
| 試験責任者: | 森村智美 | ||
| 試験担当者: | 加藤博康,関剛幸,古谷真美, 永田伴子 | ||
| (財)食品薬品安全センター秦野研究所 | |||
| 〒257-8523 神奈川県秦野市落合729-5 | |||
| Tel 0463-82-4751 | Fax 0463-82-9627 | ||
| Correspondence | ||||
| Authors: | Tomomi Morimura(Study Director) Hiroyasu Kato, Takayuki Seki, Mami Furuya, Tomoko Nagata | |||
| Hatano Research Institute, Food and Drug Safety Center | ||||
| 729-5 Ochiai, Hadano-shi, Kanagawa, 257-8523, Japan | ||||
| Tel +81-463-82-4751 | Fax +81-463-82-9627 | |||