2-�ӥ˥�ԥꥸ���
Ӯ�������ܺ�˦���Ѥ��������ΰ۾�
In Vitro Chromosomal Aberration Test
of 2-Vinylpyridine on Cultured Chinese Hamster Cells
����
2-�ӥ˥�ԥꥸ�����ܺ�˦�˵ڤܤ���˦������Ū�ƶ��ˤĤ��ơ����㥤�ˡ������ϥॹ�������ܺ�˦(CHL)���Ѥ��������ΰ۾���»ܤ�����
��˦�����������̤��Ȥˡ�Ϣ³����ˡ��24���ֽ�����30.0 ��g/ml��48���ֽ�����15.0 ��g/ml��û���ֽ�����S9 mix��¸�߲���120 ��g/ml��S9 mix¸�߲��Ǥ�300 ��g/ml��ǹ����ǻ�٤Ȥ�������1/2��1/4�����1/8���줾���ǻ�١���ǻ�٤������ǻ�٤Ȥ������ꤷ����Ϣ³�����Ǥϡ�S9 mix��¸�߲��ˤ�����24���֤����48����Ϣ³�����塤û���ֽ����Ǥ�S9 mix¸�߲��������¸�߲���6���ֽ���(18���֤β�������)�塤ɸ�ܤ���������������뤳�Ȥˤ�������ΰ۾�Ͷȯ����Ƥ������
���η�̡�Ϣ³�����ʤ�Ӥ�û���ֽ����Τ��٤Ƥν������ˤ����ơ������ι�¤�۾�����Τ�Ͷȯ���Ѥ�ǧ���줿���ʤ���������ν������ˤ����Ƥ⡤�ܿ�����˦��Ͷȯ���Ѥ�ǧ����ʤ��ä���
�ʾ�η�̤�ꡤ�ܻ��ﲼ�Ǥ�2-�ӥ˥�ԥꥸ��ϡ������ΰ۾��Ͷȯ����(����)�ȷ���������
��ˡ
1.�����˦��
Ӯ�������ܺ�˦���Ѥ��������ΰ۾��˹������Ѥ���Ƥ��뤳�Ȥ��顤���˦���Ȥ��ƥ��㥤�ˡ������ϥॹ��������ͳ������ݲ��˦��(CHL)������������59ǯ11��15���˹�Ω������꤫��ʬͿ������������ϥ�����륹��ۥ�����(DMSO:MERCK��)��10%ź�ä����塤�������������¸�����Ĥ��3��5�����Ȥ˷��夷�����ʤ����������ΰ۾��Ǥϲ��������5�κ�˦���Ѥ�����
2.�����ܱդ�Ĵ��
Eagle-MEM��������(LIFE TECHNOLOGIES��)�ˡ����֥��ե��륿��(0.45 ��m:CORNING��)���Ѥ��Ʋð��ɲ���ݤ�����Ư��(56�30ʬ)�ѤƵ�����(LIFE TECHNOLOGIES��)��ǽ�ǻ�٤�10%�ˤʤ�褦�ä����塤��˻��Ѥ�����Ĵ��������ܱդ���Ž�(4��)����¸������
3.�����ܾ��
CO2����١�����(FORMA�Ҥ��뤤�ϻ����ŵ��õ�(��))���Ѥ���CO2ǻ��5%��37��ξ��Ǻ�˦�����ܤ�����
4.��S9 mix
��¤��6�������Υ��å����ޥ�(��)��S9 mix���˻��Ѥ�����S9 mix���S9��ͶƳ�ޤȤ��ƥե��ΥХ�ӥ����뤪���5,6-�٥ե�ܥ����Ϳ����Sprague-Dawley��ͺ��åȤδ�¡����Ĵ�����줿��ΤǤ��롥S9 mix�������Ͼ��������ˡ�˽��ä�1)��
5.���︳ʪ��
�︳ʪ����2-�ӥ˥�ԥꥸ��(���å��ֹ�:95-022��CAS No.:100-69-6)��ʬ�Ҽ�C7H7N��ʬ����105.15������98.3%(�Խ�ʪ�Ȥ���2-�ԥ����0.9%��2-������ԥꥸ��0.4%�����2-�����ԥꥸ��0.4%��ޤ�)�α��ΤǤ��롥ͭ���������ʹ���(��)�������줿�︳ʪ������Ѥ��������λ�塤�︳ʪ�����ˤ����ƻ�;�︳ʪ����ʬ�Ϥ�����̡�������������Ϥʤ��ä���
6.���︳ʪ���ϱդ�Ĵ��
DMSO���︳ʪ�����ϲ�Ĵ�����դȤ�����Ĵ�����դ�������ޤ��Ѥ��ƽ缡����ǻ�٤˴��ᤷ���塤ľ���˽�����Ԥä�(�ѻ�Ĵ��)��
7.��ͽ���(��˦���������)
��˦�����ѥե饹��(��������25cm2)�˺�˦���ż路������3������︳ʪ���ϱդ����������Ϣ³�����ξ�硤24���뤤��48����Ϣ³���ƽ�����»ܤ���û���ֽ����Ǥ�S9 mix��¸�߲�(-S9 mix)���뤤��¸�߲�(+S9 mix)��6���ֽ��������塤���������ܱդ˸��Ƥ����18�������ܤ�³������
��˦��10%�����˾ץۥ�ޥ���(�¸���������(��))�Ǹ��ꤷ���塤0.1%���ꥹ���롦�Х�����å�(���첽��(��))���ϱդ�10ʬ�����������������Ͻб�(30%�����Ρ��롤1%�ݻ����ϱ�)��Ŭ�̲ä���5ʬ���������֤��ƿ��Ǥ��ϽФ����塤580 nm�Ǥε۸��٤�¬�ꤷ���������̷��ˤĤ��������оȷ��Ǥε۸��٤��Ф����桤���ʤ����˦��¸Ψ�Ф�����
���η�̡�������ν���ˡ�ˤ����Ƥ⸲���ʺ�˦�����������ѻ����줿(Fig��1)���ץ��ӥå�ˡ���Ѥ��ƻ��Ф���50%��˦��������ǻ�٤�Ϣ³24���ֽ�����33.4 ��g/ml��Ʊ48���ֽ�����7.90��mg/ml��û���ֽ�����S9 mix��¸�߲���109 ��g/ml��S9 mix¸�߲���147 ��g/ml�Ǥ��ä���
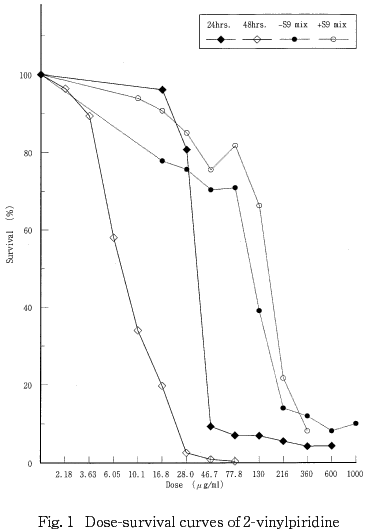
8.������̤���ӻ��������
��˦�����������̤��Ȥˡ������ΰ۾��Ǥ�Ϣ³24���ֽ�����30.0 ��g/ml��Ʊ48���ֽ�����15.0 ��g/ml��û���ֽ�����S9 mix��¸�߲���120 ��g/ml��S9 mix¸�߲���300 ��g/ml��ǹ����ǻ�٤Ȥ����ʲ�����2�Ǹ�������4���̤ʤ�Ӥ������оȷ������ꤷ����
�����оȤȤ��ơ�Ϣ³�����ξ�硤�ޥ��ȥޥ�����C(MMC:����Ȱ�ڹ���(��))��24���ֽ�����0.05 ��g/ml��48���ֽ�����0.025 ��g/ml�����̤ǡ�û���ֽ����ξ�硤�������ۥ��ե��ߥ�(CP:���������(��))��12.5 ��g/ml�����̤ǻ������
9.��������ɸ�ܤκ���
��˦�����ѥե饹�����Ѥ���ͽ�����Ʊ�ͤ��︳ʪ�����ν�����Ԥä������ܽ�λ2�������ˡ��ǽ�ǻ�٤�0.2 ��g/ml�Ȥʤ�褦���륻�ߥ�(LIFE TECHNOLOGIES��)��ź�ä������ȥ�ץ�������Ǻ�˦����Υ��������ʬΥ�ˤ���˦����������75 mM�������ꥦ����ϱդ���ĥ������Ԥä��塤�����(��Ρ���3��:�ݻ�1��)�Ǻ�˦����ꤷ������������ˡ��������ɸ�ܤ���������塤1.2%���ॶ�����դ�12ʬ������������
10.�������Τδѻ�
�ƥץ졼�Ȥ�����100�ġ����ʤ������������200�Ĥ�ʬ����������������Ǵѻ����������Τη���Ū�Ѳ��Ȥ��ƥ���å�(gap)������ʬ������(ctb)������������(csb)������ʬ�θ�(cte)�������θ�(cse)����Ӥ���¾(oth)�ι�¤�۾��ʬ�ष����Ʊ���ˡ��ܿ�����˦�νи�Ψ��Ͽ�����������Τ�ʬ�Ϥ����ܴĶ��Ѱ۸��ز�Ӯ��ưʪ�ʬ�ʲ�2)�ˤ��ʬ��ˡ�˽��äƼ»ܤ�����
���٤Ƥ�ɸ�ܤ��ɲ������塤�ѻ�������
11.��̤β���
����åפΤ���ͭ�����˦��ޤ���(+gap)�ȡ��ޤ�ʤ����(-gap)�Ȥ˶��̤��������ι�¤�۾�νи����٤�ɽ��������
�ƻ���ι�¤�۾��ͭ�����˦���뤤���ܿ�����˦�νи����٤��дۤ�3)�δ��˽��ä�Ƚ�ꤷ���������ΰ۾��ͭ�����˦�νи����٤�5%̤������(-)��5%�ʾ�10%̤��������(��)��10%�ʾ������(+)�Ȥ������ǽ�Ū�ˤϺƸ������뤤�����̤˰�¸����ǧ���줿����������Ƚ�ꤷ����
�ʤ������׳�Ū��ˡ���Ѥ�������ϼ»ܤ��ʤ��ä���
�ޤ���������̤�����ϤˤĤ��Ƥϡ��Ǿ����ˡ�ˤ��D20�ͤ��������̤ˤ���������ʬ�θνи�����(%)������(mg/ml)�ǽ������Ȥˤ��TR�ͤ��줾�컻�Ф�����
��̤���ӹͻ�
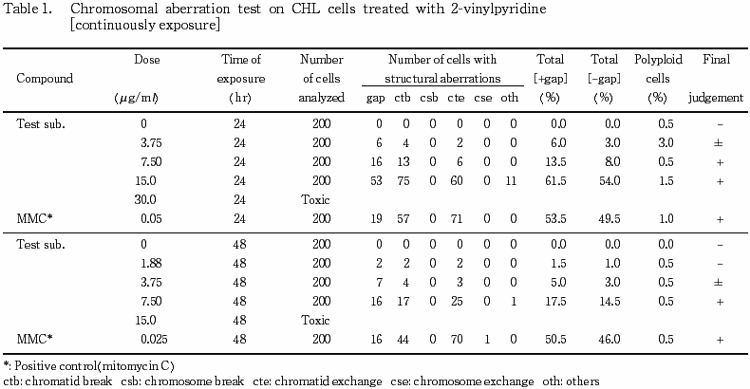
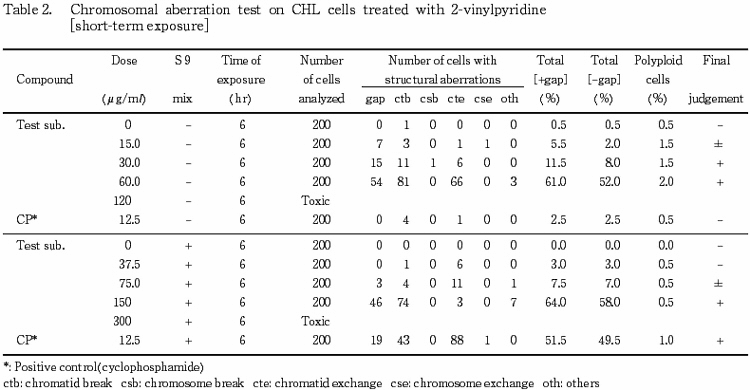
Ϣ³�����Ǥλ��̤�Table 1�ˡ�û���ֽ����Ǥη�̤�Table 2�˼�������2-�ӥ˥�ԥꥸ��������ξ�硤���٤Ƥλ�Ϥˤ����ơ����̤˰�¸���������ι�¤�۾�����Τ�Ͷȯ���ѻ����줿���ޤ����ܿ�����˦�ˤĤ��Ƥ�Ͷȯ�����ϴѻ�����ʤ��ä����Ѱ۸����ζ����˴ؤ�������Ū����ͤǤ���D20�ͤ����TR�ͤϤ��줾��0.00557(mg/ml)����� 2000�Ȼ��Ф��줿���ʤ����ƻ���κǹ����ǻ�٤Ǥϡ��︳ʪ���αƶ��ˤ��ʬ�����κ�ʴ���������뤫�����뤤����¸��˦���ۤȤ�ɸ����ʤ��ä����ᡤ�����δѻ���»ܤ��ʤ��ä��������������о�ʪ���ξ�硤Ϣ³����ˡ�Ǥ�MMC�ʤ�Ӥ�S9 mix¸�߲��Ǥ� CP�ǽ���������˦�Ǥ������Τι�¤�۾�θ�����Ͷȯ��ǧ���줿���ʤ�����������Ͻ�������ɮ���٤��Ѳ��ϴѻ�����ʤ��ä����ʾ�λ��̤��顤�ܻ��ﲼ�ˤ�����2-�ӥ˥�ԥꥸ���Ӯ�������ܺ�˦���Ф��������ΰ۾�Ͷȯ���˴ؤ���������Ƚ�ꤷ����
ʸ��
| 1) | A��Matsuoka��M��Hayashi and M��Ishidate Jr.��Mutat��Res.��66��277(1979). |
| 2) | ���ܴĶ��Ѱ۸��ز�Ӯ��ưʪ�ʬ�ʲ��ԡ��ɲ���ʪ���ˤ�������ΰ۾異�ȥ饹����ī�ҽ�Ź�������1988��pp��31-35�� |
| 3) | �д۴𡡴ƽ����ɡ�����������ΰ۾��ǡ��������ɥ��롦�����������ҡ������1987��pp��19-24�� |
| Ϣ���衧 |
| ���Ǥ�� | ���衡Ԥ |
| �ô���� | ����������ƣ����������ʿ�һʡ������� |
| (��)�����������ʰ�����ɾ������ |
| ��437-12 �Ų������ķ�ʡ��Į�����Ļ�����582-2 |
| Tel 0538-58-1266 | Fax 0538-58-1393 | |
| Correspondence |
| Authors: | Authors:Madoka Nakajima(Study director)
Michiyo Kitazawa��Masataka Fujiwara,Satoshi Kumadaira��Shoji Masumori |
| Biosafety Research Center/Foods��Drugs and Pesticides(An-pyo Center) |
| 582-2 Shioshinden Aza Arahama,Fukude-cho,
Iwata-gun,Shizuoka,437-12,Japan |
| Tel +81-538-58-1266 | Fax +81-538-58-1393 | |



