ラットは1群雌雄各5匹で対照群を含む4群,さらに対照群および高用量群には雌雄各5匹の回復群を設け,計60匹を使用した.
N-メチルアニリンは,コーン油に溶解し,0,5,25および125 mg/kgを毎日1回,4週間連続経口投与し,一般状態の観察,体重測定,摂餌量測定,血液学検査,血液凝固能検査,血液生化学検査,尿検査,器官重量測定および病理学検査を行った.なお,回復期間は2週間とし,投与終了時と同様な検査を実施した.
その結果は,次のとおりである.
投与期間および回復期間を通じて,雌雄いずれの群にも死亡例は認められなかったが,雌雄の125 mg/kg群でチアノーゼが観察され,回復期間に入っても継続して認められた例があった.
体重および摂餌量は,投与期間中,雌雄とも群間で明確な差が認められなかったが,回復期間では雄の125 mg/kg群で摂餌量の増加,体重の高値が認められた.
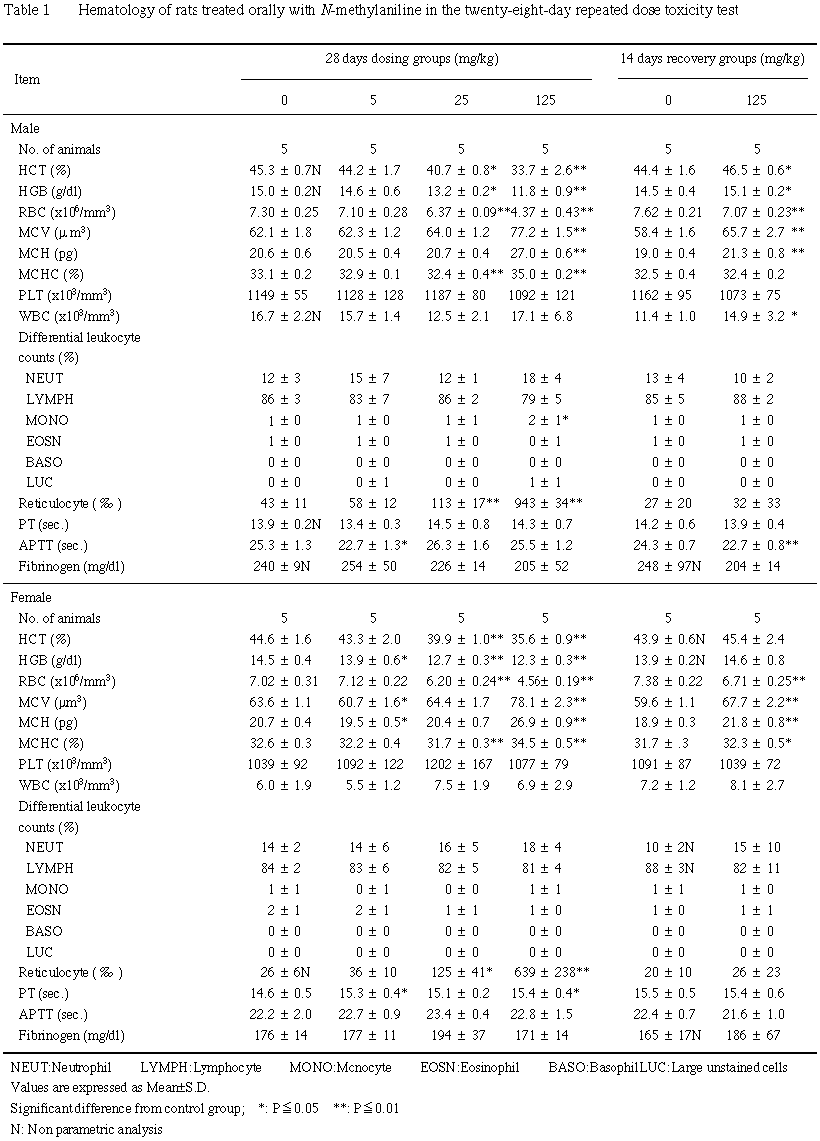
血液学検査の結果,雌雄とも25および125 mg/kg群でヘマトクリット値,ヘモグロビン量および赤血球数が低値,網赤血球率が高値を示し,さらに25 mg/kg群でMCHCの低値, 125 mg/kg群でMCV,MCH,MCHCおよび単球比率の高値が認められた.回復期間終了時の検査では,回復傾向は認められたものの雌雄とも赤血球数が僅かに低値であった.
血液凝固検査の結果,雌の125 mg/kg群でプロトロンビン時間に僅かな延長が認められた.
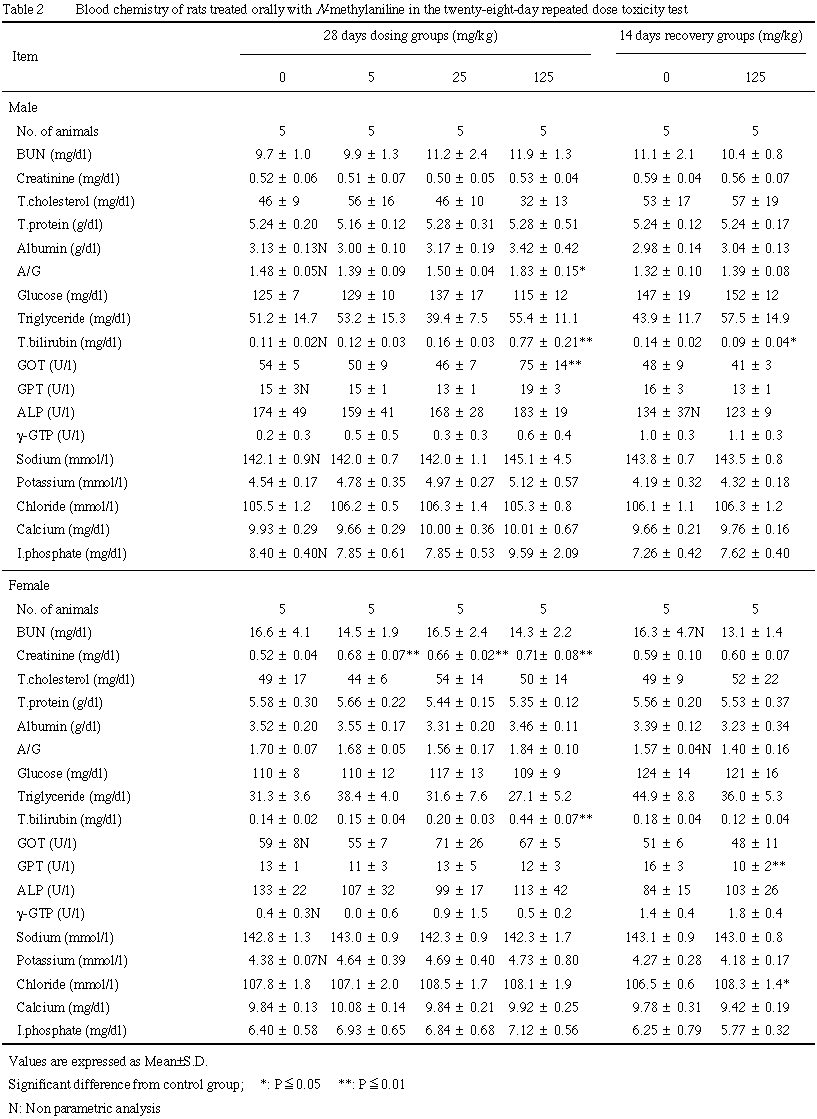
血液生化学検査の結果,雌雄の125 mg/kg群で総ビリルビンが高値を示し,さらに雄の同群でGOTの高値,雌の同群でクレアチニンの高値が認められた.これらの変化は回復期間終了時の検査ではすべて回復した.
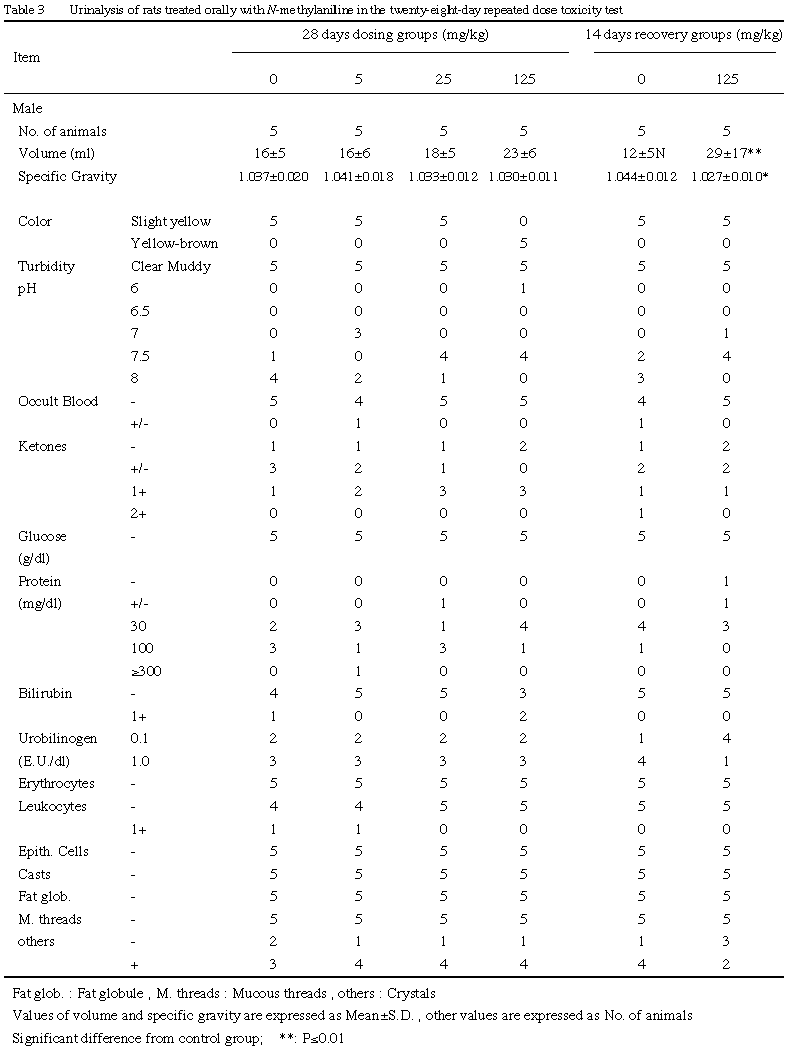
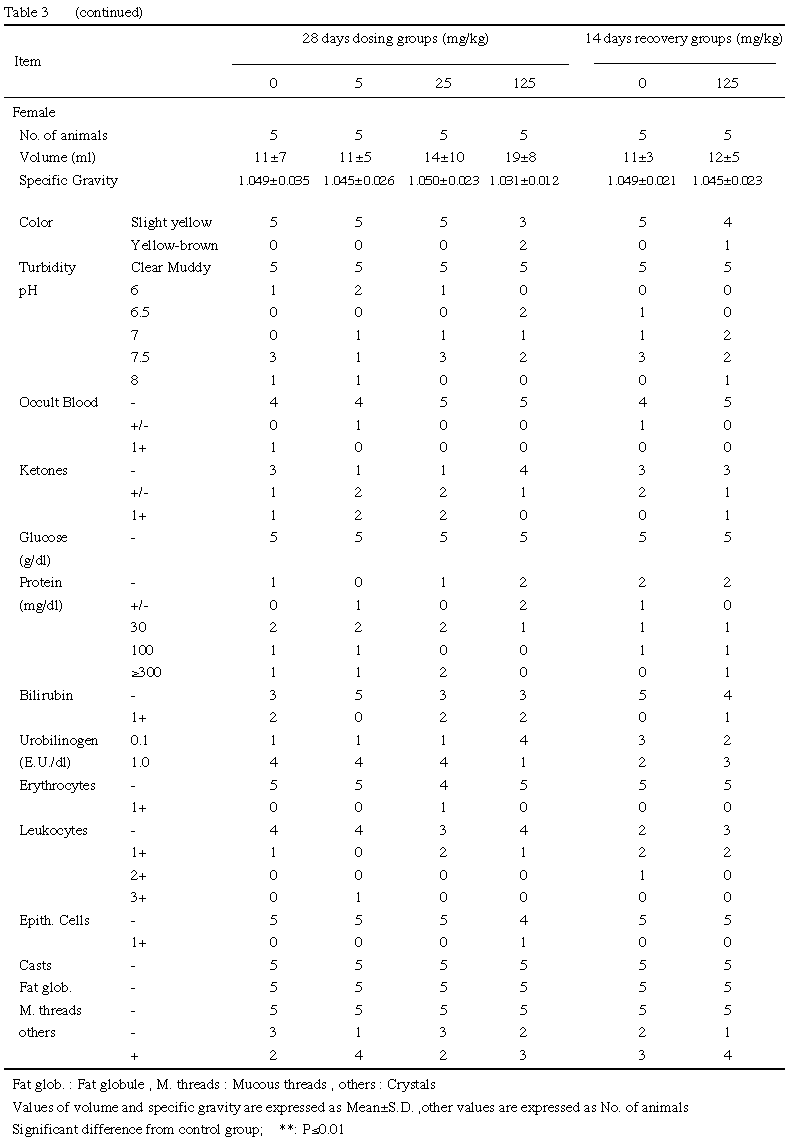
尿検査の結果,雌雄の125 mg/kg群で黄褐色尿動物が増加し,尿量が増加傾向を示し,雄の25および125 mg/kg群でケトン体 1+(15 mg/dl)動物が増加した.回復期間終了時の検査では,雄の125 mg/kg群で尿量の増加,比重の低値が認められ,雌の125 mg/kg群で黄褐色尿動物が1例認められた.
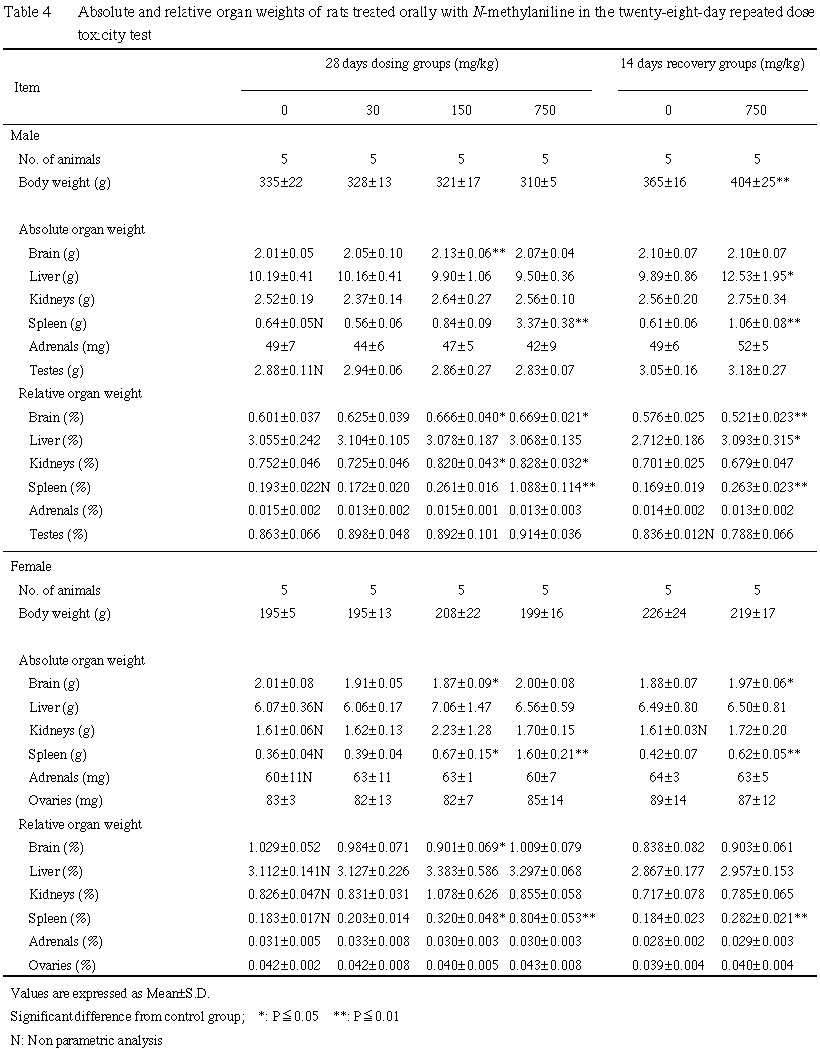
器官重量測定の結果,雄の125 mg/kg群,雌の25および125 mg/kg群で脾臓の実重量および相対重量が高値を示し,さらに雄の25および125 mg/kg群で脳および腎臓相対重量が高値を示した.回復期間終了時の検査では,雌雄の125 mg/kg群では,脾臓の実重量および相対重量が高値を示し,さらに雄の同群で肝臓の実重量および相対重量の高値,脳相対重量の低値が認められた.
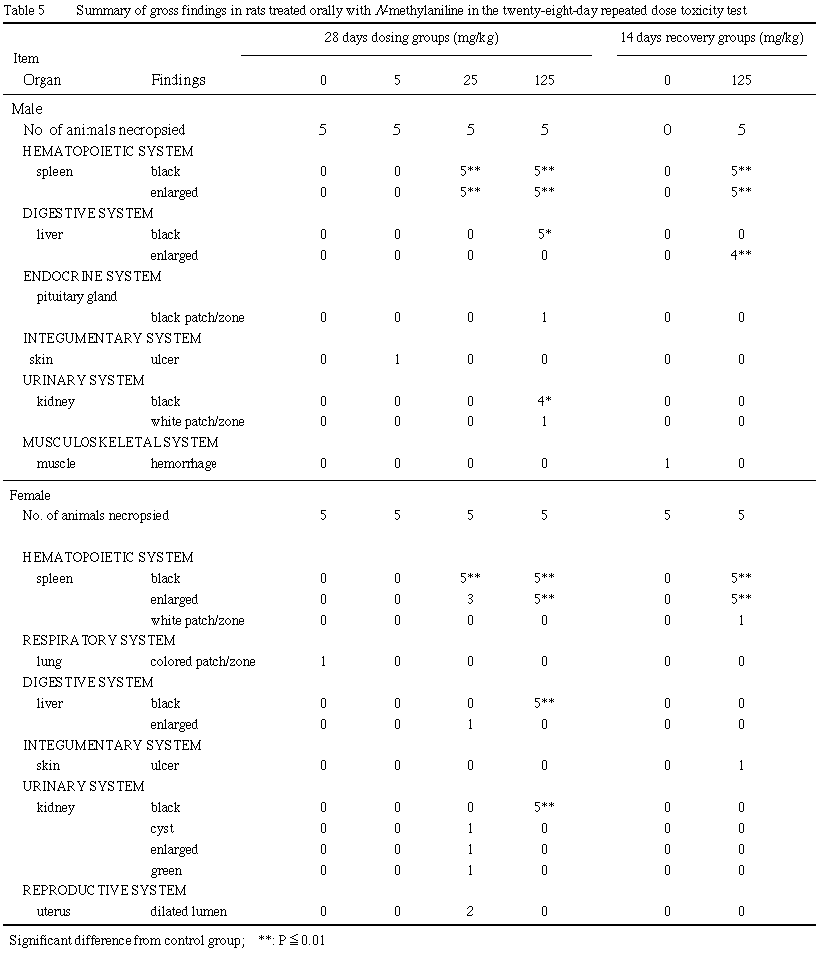
病理学検査の結果,投与終了時において対照群に比較して被験物質投与群で多く見られた剖検所見は,脾臓の黒色化および肥大,肝臓および腎臓の黒色化が雌雄で観察された.脾臓の黒色化および肥大は,回復試験終了時においても125 mg/kg群の雌雄で観察された.また,回復試験終了時の125 mg/kg群の雄で肝臓の肥大が観察された.
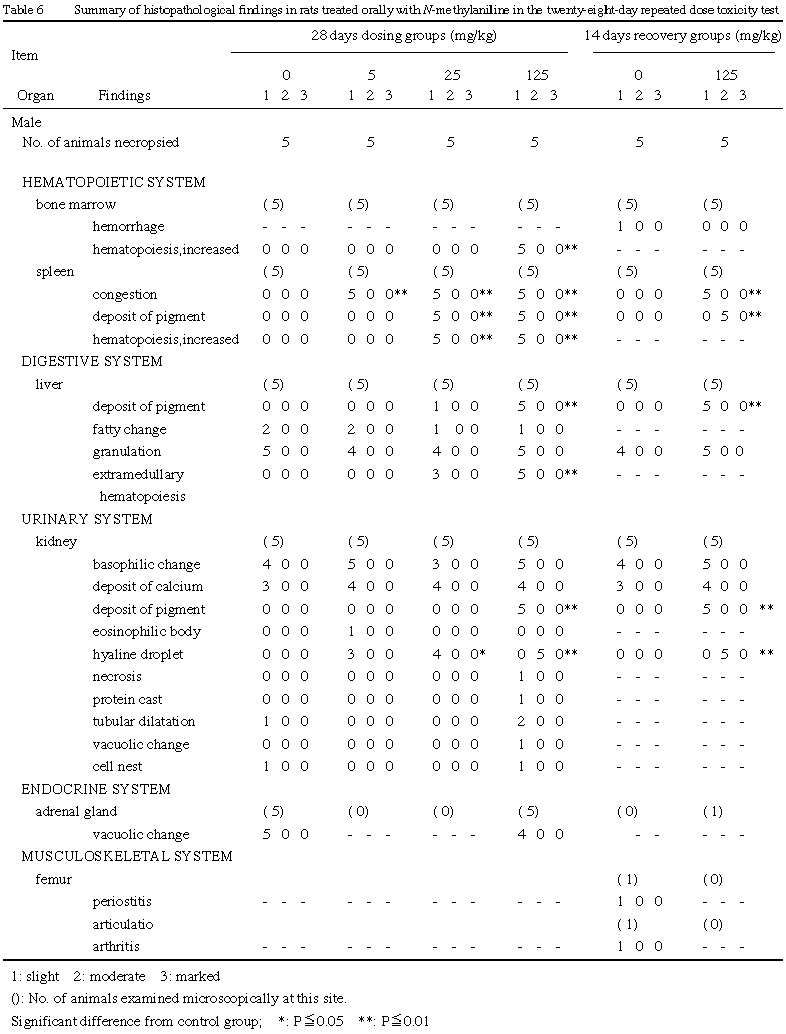
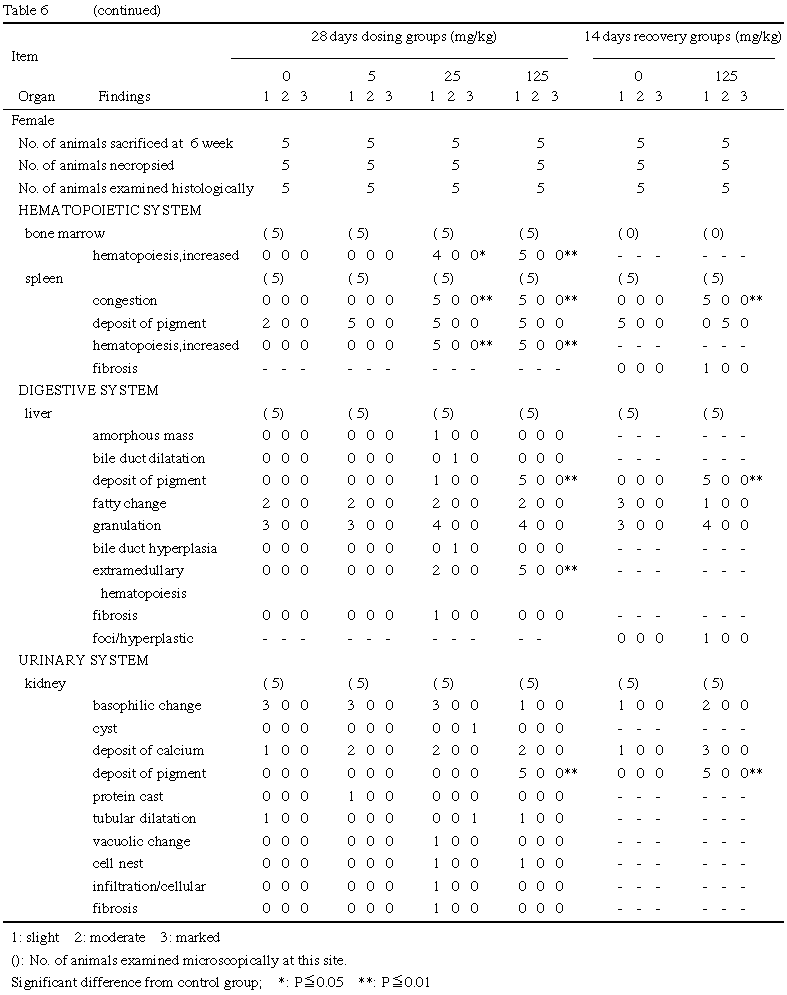
組織所見では,投与終了時において脾臓の充血,造血亢進および色素沈着,骨髄の造血亢進,肝臓の髄外造血および色素沈着,腎臓の近位尿細管の色素沈着が雌雄の被験物質投与群で対照群に比較して多く観察された.硝子滴変性は雄の被験物質投与群で観察され,125 mg/kg群では程度の増加が認められた.脾臓の充血,肝臓および腎臓の色素沈着は回復試験終了時においても125 mg/kg群の雌雄で観察され,腎臓の近位尿細管の硝子滴変性は投与終了時と同程度の変化が回復試験終了時に125 mg/kg群の雄で観察された.脾臓の色素沈着は回復試験終了時の125 mg/kg群の雌雄においても観察されたが,投与終了時に比べ程度の増加が認められた.また,剖検所見で回復試験終了時に雄の125 mg/kg群の4例にみられた肝臓の肥大に相当する組織学的所見は観察されなかった.
以上の結果,雌雄とも5 mg/kgでは障害作用は認められなかったものの,病理組織学的にメトヘモグロビン血症の代償作用と考えられる変化が認められ,無影響量は5 mg/kg以下と考えられた.
動物を検収後,試験環境に8日間馴化させた後,6週齢で投与を開始した.動物はあらかじめ体重によって層別化し,無作為抽出法により各試験群を構成するように群分けした.動物の識別は,個別飼育ケージに動物標識番号(Animal ID-No.)を付すことにより行った.投与開始時の体重は雄で129〜144 g,雌で111〜122 gであった.
(株)東京技研サービスの水洗式飼育機を使用し,金属製前面・床網目飼育ケージに動物を1匹ずつ収容し,オリエンタル酵母工業(株)製造の放射線滅菌改良NIH公開ラット・マウス飼料および水道水を自由に摂取させた.飼育ケージは隔週1回,給餌器は週1回取り換えた.
なお,動物の馴化期間を含め,投与および回復期間中,データの信頼性に影響を及ぼしたと思われる環境要因の変化はなかった.
a. 血液学検査
検査にはEDTA-3Kを添加した初血を用いた.
白血球数(WBC:暗視野板法),赤血球数(RBC:暗視野板法),ヘモグロビン量(HGB:シアンメトヘモグロビン法),ヘマトクリット値(HCT:全赤血球の容積より補正),平均赤血球容積(MCV:RBC, HCTより算出),平均赤血球血色素量(MCH:HGB, RBCより算出),平均赤血球血色素濃度(MCHC:HGB, HCTより算出),血小板数(PLT:暗視野板法)および白血球百分率(フローサイトケミストリー法)を血液自動分析装置THMS H6000(米国テクニコン社)を用いて測定した.
網赤血球(RC)率算定用に,全血をキャピロット(テルモ株式会社)で染色後,血液塗抹標本を作製し鏡検した.
また,クエン酸ソーダ添加血液の血漿について,プロトロンビン時間(Quick 1 段法),活性化部分トロンボプラスチン時間(クロット法)およびフィブリノーゲン量(トロンビン時間法)を血液凝固自動測定装置 KC-40(独国 Amelung社)を用いて測定した.
b. 血液生化学検査
血清を用いて,総蛋白(ビューレット法),アルブミン(B.C.G.法),A/G比(計算値),血糖(グルコースオキシダーゼ法),中性脂肪(酵素法),総コレステロール(酵素法),尿素窒素(BUN:ウレアーゼ改良法),総ビリルビン(ジアゾ色素法),カルシウム(アルセナゾIII色素法),無機リン(モリブデン酸アンモニウム法),ナトリウム(電極法),カリウム(電極法)および塩素(電極法)をEKTACHEM 700N(米国コダック社)で,クレアチニン(アルカリ性ピクリン酸比色法),グルタミン酸オキザロ酢酸トランスアミナーゼ(GOT:Karmen改良法),グルタミン酸ピルビン酸トランスアミナーゼ(GPT:Karmen改良法),γ-グルタミルトランスペプチダーゼ(γ-GTP:Szasz改法)およびアルカリホスファターゼ(ALP:Bessey-Lowry-Brock改良法)をCentrifiChem ENCOREII(米国ベーカー社)で測定した.
c. 尿検査
血液学検査に先立ち,採尿器を用いて24時間(午前10時から翌日午前10時まで)尿を採取し,尿量,色調および濁度を検査後,尿比重計UR-S((株)アタゴ)を用いて尿比重を測定した.また,尿を遠心分離後Sternheimer変法により沈渣を染色し,鏡検した.
pH,潜血,ケトン体,糖,蛋白,ビリルビンおよびウロビリノーゲンについて,N-マルティスティックス SG 試験紙(マイルス・三共(株))およびCLINITEK 200(米国マイルス社)を用いて測定した.
病理組織学検査は固定した器官・組織のうち,対照群と高用量群の心臓,肝臓,脾臓,腎臓,副腎および大腿骨について行った.常法に従って薄切標本を作製し,ヘマトキシリン・エオジン染色し鏡検した.
なお,用量相関性については,Jonckheereの傾向検定を用いて有意差を検定した.
有意水準は5および1%の片側検定で実施した.
雌では,125 mg/kg群でチアノーゼが投与4週に4例観察された.チアノーゼは回復期間に入っても引続き観察され,回復1週に3例に認められたが,回復2週には消失した.
回復期間では,雄の125 mg/kg群で回復2週に対照群に比較して高値が認められ,雌では対照群と125 mg/kg群で差がなかった.
回復期間では,雄の125 mg/kg群で回復1および2週に対照群に比較して増加が認められた.
雌では,対照群に比較してすべての被験物質投与群でヘモグロビン量が低値を示し,さらに,25および125 mg/kg群でヘマトクリット値および赤血球数の低値,網赤血球率の高値,25 mg/kg群でMCHCの低値,125 mg/kg群で MCV,MCHおよびMCHCの高値が認められた.その他,5 mg/kg群でMCVおよびMCHの低値がみられたが,軽微かつ用量相関性のない変化であった.
回復試験終了時において対照群に比較して被験物質投与群で多く見られた剖検所見は,脾臓の黒色化および肥大が125 mg/kg群の雌雄全例に観察された.また,肝臓の肥大が雄の 125 mg/kg群の4例に観察された.その他の剖検所見は,単発性の発生であった.
回復試験終了時においては,脾臓の充血,肝臓および腎臓の色素沈着が125 mg/kg群の雌雄全例に観察された.腎臓の近位尿細管の硝子滴変性は125 mg/kg群の雄の全例で投与終了時と同程度の変化が観察された.脾臓の色素沈着は雄の125 mg/kg群の全例,雌の対照群および125 mg/kg群の全例で観察されたが,125 mg/kg群の雌雄全例で投与終了時に比べて程度の増加が認められた.また,剖検所見で回復試験終了時に雄の125 mg/kg群の4例にみられた肝臓の肥大に相当する組織学的所見は観察されなかった.
その他,対照群を含め雌雄に観察された主な所見は,肝臓の脂肪化および肉芽巣,腎臓の好塩基化および石灰沈着であった.その他,観察された所見は単発性の発生に止まった.

死亡例は,雌雄いずれの群にも認められなかった.
体重および摂餌量は,投与期間中,雌雄とも群間で明確な差が認められなかったが,回復期間では,雄の125 mg/kg群で摂餌量が増加し,体重も回復2週に高値を示した.
血液学検査の結果,前述のとおり本被験物質はメトヘモグロビン血症をおこすため,雌雄とも25および125 mg/kg群で貧血が認められ,ヘマトクリット値,ヘモグロビン量および赤血球数は低値を示し,赤血球恒数にも変化が認められ,網赤血球率も著しい増加を 示した.ヘモグロビン量の低値は,雌の5 mg/kg群でも認められたが,同群の値は背景値(14.2±0.5 mg/dl,n=35)の範囲内の値であった.回復期間終了時の検査結果では,貧血に回復傾向が認められたが,125 mg/kg群の赤血球数は対照群に比較して僅かながら低値であり,完全回復には至らなかった.
血液凝固検査の結果,雌の125 mg/kg群でプロトロンビン時間の延長が認められたが,軽微な変化で毒性学的意義は乏しいと考えられた.
血液生化学検査の結果,雌雄の125 mg/kg群で認められた総ビリルビンの高値,雌の125 mg/kg群で認められたクレアチニンの高値は,メトヘモグロビン血症に溶血が伴ったためと考えられるが,尿中ウロビリノーゲンの高値が認められないことから,溶血は軽度と考えられる.雌におけるクレアチニンの高値は5および25 mg/kg群でも認められたが,対照群の値が低値傾向にあり,これら両群の値は背景値(0.63±0.06 mg/dl,n=35)の範囲内の値であった.その他,雄の125 mg/kg群でGOTおよびA/G比が高値を示したが,GOTは逸脱酵素であるが病理組織学的に対応すると考えられ臓器に障害は認められず,溶血が起因とも考えられる.また,A/G比の高値は,総蛋白およびアルブミンは対照群と差がないことから,特に意義はないと考えられる.回復期間終了時の検査では,投与終了時に認められた変化はいずれも回復した.
尿検査の結果,雌雄の125 mg/kg群で黄褐色尿動物の増加が認められた.血液および血液化学的検査結果などから,メトヘモグロビン尿も考えられるが,尿量が増加傾向にあり,潜血およびウロビリノーゲンの高値は認められず,色調変化も暗赤色ではなく黄褐色であることなどから明確ではなかった.回復期間終了時の検査では,雄の125 mg/kg群で尿量の増加(尿比重の低値),雌の同群で黄褐色尿を呈する動物が認められ,完全な回復までには至らなかった.
器官重量測定の結果,雄の125 mg/kg群,雌の25および125 mg/kg群で認められた脾臓の実重量および相対重量の高値が被験物質投与による血液毒性に随伴した変化と考えられた.回復期間終了時の検査では,雌雄の125 mg/kg群とも回復傾向が認められたものの完全には回復せず,雄の同群では肝臓の実重量および相対重量の増加が認められた.また,この群で認められた脳相対重量の低値は,体重高値による二次的変化と考えられた.
病理学検査の結果,投与終了時に観察された剖検所見のうち,脾臓の黒色化と肥大は25 mg/kg以上の群の雌雄のほぼ全例で観察され,肝臓と腎臓の黒色化は125 mg/kg群の雌雄のほぼ全例に観察されたことから被験物質による変化と考えられた.脾臓の黒色化および肥大は,回復試験終了時においても125 mg/kg群の雌雄全例に観察されたことから,2週間の回復期間においては不可逆性の変化と考えられた.また,回復試験終了時に観察された肝臓の肥大は雄の125 mg/kg群のみに4例発生したことから被験物質投与による変化であることが示唆された.
組織学的にも,投与終了時において脾臓,骨髄,肝臓,腎臓に被験物質投与によると示唆される変化を示した.すなわち,脾臓の充血が雄の5 mg/kg以上,雌の25 mg/kg以上の群の全例に,造血亢進が25 mg/kg以上の群の雌雄全例に認められた.また,色素沈着は雄の25 mg/kg以上の群の全例,雌の対照群の2例,5 mg/kg以上の群の全例と,雄では被験物質投与群のみに観察され,雌でも対照群に比べて被験物質投与群に多く観察された.骨髄の造血亢進は雄の125 mg/kg群の全例,雌の25および125 mg/kg群の4および全例に,肝臓の髄外造血は雄の25および125 mg/kg群の3および全例,雌の25および125 mg/kg群の2および全例に,色素沈着は25および125 mg/kg群の雌雄それぞれ1および全例と,被験物質投与群においてほぼ用量相関的な発生率の増加を示した.また,腎臓の近位尿細管の色素沈着が125 mg/kg群の雌雄全例と,被験物質投与群のみに観察され,硝子滴変性が雄の5,25および125 mg/kg群の3,4および全例と,被験物質投与群において用量相関的な発生率の増加を示し,125 mg/kg群の全例で程度の増加を示した.
脾臓の充血,肝臓および腎臓の色素沈着は回復試験終了時においても125 mg/kg群の雌雄全例に観察され,腎臓の近位尿細管の硝子滴変性は投与終了時と同程度の変化が回復試験終了時に125 mg/kg群の雄の全例で観察されたことから,これらは同群では2週間の回復期間においては不可逆性の変化と考えられた.脾臓の色素沈着は,回復試験終了時に雄の125 mg/kg群の全例,雌の対照群および125 mg/kg群の全例に観察されたが,125 mg/kg群の雌雄全例で投与終了時と比べて程度が増加した.また,剖検所見で回復試験終了時に雄の125 mg/kg群の4例に肝臓の肥大が観察されたが,相当する組織学的所見は観察されなかった.
以上の結果,雌雄とも25 mg/kg以上の群で血液毒性が認められ,5 mg/kg群でもその代償作用と考えられる変化が組織学的に認められた.無影響量は5 mg/kg以下と判断される.
| 1) | R.P. Smith, M.V. Olson :Drug-induced Methemoglobinemia, Seminars in Hematology, 10, pp. 253-268 (1973). |
| 2) | 林 昭, メトヘモグロビン:中毒研究, 1, 135-141 (1988). |
| 3) | T.M. Markosyan :Comparative toxicity of monomethylaniline and dimethylaniline in chronic test (Russ.), Gig. Sanit., 34, 7 (1969). |
| 連絡先 | |||
| 試験責任者 | :井上博之 | ||
| 試験担当者 | :各務 進,庄子明徳,渡 修明, 加藤睦美,小林和雄,榎本 眞 | ||
| (財)食品農医薬品安全性評価センター | |||
| 〒437-12静岡県磐田郡福田町塩新田字荒浜 582-2 | |||
| Tel 0538-58-1266 | Fax 0538-58-1393 | ||
| Correspondence | |||
| Authors: | Hiroyuki Inoue (Study director), Susumu Kakamu,Akinori Syouzi, Nobuaki Watari,Mutumi Katoh, Kazuo Kobayashi,Makoto Enomoto | ||
| Biosafety Research Center/Foods, Drugs and | |||
| Pesticides (An-pyo Center) | |||
| 582-2 Shioshinden Aza Arahama, Fukude-cho, | |||
| Iwata-gun, Shizuoka, 437-12, Japan | |||
| Tel +81-538-58-1266 | Fax +81-538-58-1393 | ||