一般状態の観察では,79 mg/kg群の雌雄で投与後 2 時間以降に流涎が,119 mg/kg群の雌で投与後2時間以降に流涎および自発運動の低下がみられた.178 mg/kg以上の群の雌雄では,投与後20分あるいは2時間以降に自発運動の低下,よろめき歩行,腹臥,流涎,表皮温下降,呼吸緩徐,鼻・口周囲の被毛汚染がみられ,投与後1日には前記症状に加えて流涙がみられた.投与後1〜2日には178 mg/kg群の雌雄各1例,267 mg/kg群の雄 4例と雌5例,400 mg/kg以上の群の雌雄各 5 例が死亡した.
LD50値は,雄で 218(166〜287)mg/kg,雌で208mg/kgであった.
体重は,267 mg/kg以上の群の雌雄で投与後1日には投与前に比して減少し,雄では各群ともに対照群に比して有意差が認められた.178 mg/kg以下の群の雌雄では投与後1〜7日頃までは増加抑制傾向であったが,剖検時には対照群とほぼ同程度の体重を示した.
剖検では,死亡例で胸腺の暗赤色斑散在,腺胃粘膜の暗赤色化,膀胱内に緑色液体貯留,膀胱粘膜の暗赤色化,赤褐色腹水貯留がみられた.
病理組織学的検査では,死亡例で胸腺(皮質および髄質)の出血,膀胱粘膜および粘膜下組織の出血がみられた.
投与検体液は,被験物質を0.5% CMC水溶液に用時懸濁して調製した.投与検体液中の被験物質濃度を,試験施設内で滴定法により測定した.その結果,被験物質濃度は適正範囲内の値を示した.
動物は,室温20〜24℃,湿度40〜70%,明暗各12時間,換気回数12回/時に設定した飼育室で飼育した.検疫・馴化期間中および絶食期間中はステンレス製懸垂式ケージを用いて1ケージあたり5匹までの群飼育とし,群分け後はステンレス製五連ケージを用いて個別飼育した.
飼料は,固型飼料(CRF-1,オリエンタル酵母工業(株))を給餌器に入れ,自由に摂取させた.ただし,投与前日の夕刻から投与までの約19時間と投与後約6時間まで絶食させ,その後に飼料を与えた.飲料水は,水道水を給水瓶を用いて自由に摂取させた.ただし,群分け時から投与後約6時間までは絶水させ,その後に飲料水を与えた.飼料および飲料水の分析の結果,いずれも検査成績は試験施設で定めた基準値の範囲内であった.
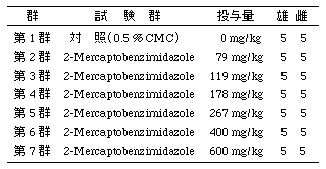
群構成は、以下の如くとした.1 群の動物数は,雌雄各5匹とした.

投与量設定の理由:雄ラットを用いた投与量設定のための予備試験(投与量:0,2,20,200,2000 mg/kg,1群3 匹)の結果,最高用量の2000 mg/kgでは投与後 2 日までに全例が死亡した.200 mg/kgでは投与後1日に有意な体重増加抑制が認められたものの,20 mg/kg以下の群と同様に死亡例はみられなかった.また,雌雄ラットを用いた予備試験(II)(投与量:0,191,305,488,781,1250,2000 mg/kg,1群5匹)では,雌は191 mg/kg以上の全例が死亡し,雄は191 mg/kg群および305 mg/kg群の各2例と488 mg/kg以上の全例が死亡した.
これらの結果を考慮して,今回の試験では600 mg/kgを最高用量とし,以下公比約1.5により400,267,178,119 および79 mg/kg群を設定した.対照として,同一液量の媒体投与群を設けた.
| 観察期間: | 観察期間は,投与後14 日間とした. |
| 一般状態: | 投与日は投与前および投与後6時間まで,投与翌日からの観察期間中は1日1回,一般状態および死亡の有無を観察した. |
| 体重測定: | 投与日および投与後1,3,7,10 ならびに14日の午前中に体重を測定した. |
| 剖検: | 死亡動物は発見後速やかに剖検した.生存動物は観察期間終了時にエーテル麻酔下で腹大動脈から放血致死させた後に器官・組織の肉眼的観察を行った.剖検で異常の認められた器官・組織,およびその比較対照となる同部位の器官・組織(対照群の代表例)は,10%中性緩衝ホルマリン液で固定し,保存した. |
| 病理組織学 的検査: | 投与後24時間以上生存した動物の内,剖検で異常が認められた器官・組織(胃,胸腺および膀胱)の代表例および対照群の同一部位の代表例につき,常法に従ってパラフィン包埋後にH-E染色組織標本を作製し,病理組織学的検査を行った. |
| LD50値: | 観察期間中の死亡率から,Probit法あるいはBehrens-Karber法によりLD50値を算出した. |
| 体 重: | 体重は,各群で平均値および標準偏差を算出した.有意差検定は対照群と被験物質各投与群の間で多重比較検定を用いて行い,危険率 5%未満を有意とした.すなわち,Bartlett法による等分散性の検定を行い,等分散の場合には一元配置法による分散分析を行い,有意ならば対照群との群間比較をDunnett法(例数が等しい場合)またはScheff 法(例数が等しくない場合)により行った.一方,等分散と認められなかった場合は順位を利用した一元配置法による分析(Kruskal-Wallisの検定)を行い,有意ならば対照群との群間比較は順位を利用したDunnett法またはScheff 法(例数が等しくない場合)により行った.一方,等分散と認められなかった場合は順位を利用した一元配置法による分析(Kruskal-Wallisの検定)を行い,有意ならば対照群との群間比較は順位を利用したDunnett法またはScheff 法を用いて行った. 法を用いて行った. |
267 mg/kg以下の群では,雌雄とも投与後30分以内には異常症状は観察されなかった.79 mg/kg群の雌雄では投与後2時間以降に流涎が各1例にみられたが,雄では投与後6時間には消失し,雌では投与後1日には消失していた.119 mg/kg群では,雌で投与後 2時間以降に流涎および自発運動の低下が2〜3例にみられ,自発運動の低下は投与後1日にも1例でみられたが,投与後 2 日以降には異常症状は観察されなかった.178 mg/kg群および267 mg/kg群の雌雄では,投与後2時間以降に自発運動の低下,腹臥,流涎,表皮温下降,呼吸緩徐などの症状が1〜5例にみられた.両群の雌雄では投与後1日には自発運動の低下,腹臥,表皮温下降,呼吸緩徐などの症状に加えて流涙が1〜5例に,さらに178 mg/kgおよび267 mg/kg群の雄では鼻・口周囲の被毛汚染が1〜2例にみられた.178 mg/kg群の雄1例は投与後 1日の午後に,雌の1例は投与後2日に死亡した.また, 267 mg/kg群の雄 1 例は投与後1日の午後に死亡し,投与後2日にも腹臥,表皮温下降,呼吸緩徐を示した1例を含む3例は同日の午後に死亡した.267 mg/kg群の雌では,投与後2日に5例が死亡した.
400 mg/kg以上の群の雌雄では,投与後20分以降に自発運動の低下,よろめき歩行,腹臥,流涎,表皮温下降,呼吸緩徐,鼻・口周囲の被毛汚染,流涙などの症状が1〜5例にみられ,投与後1日には600 mg/kg群の雌1例が死亡した.投与後1日には,両群の雌雄で腹臥,鼻・口周囲の被毛汚染,表皮温下降,呼吸緩徐,流涙などの症状が1〜5例にみられ,400 mg/kg群および600 mg/kg群の雌雄各1例が同日の午後に死亡した.投与後2日には,400 mg/kg以上の群の雌雄の残る全例が死亡した.
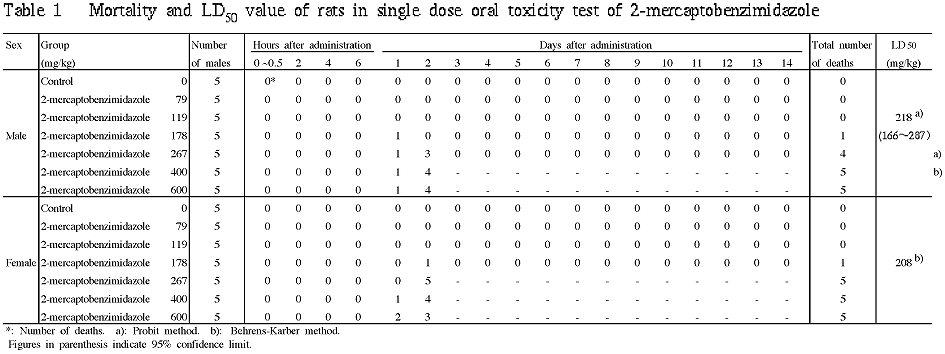
死亡経過およびLD50値を Table 1に示した.
178 mg/kg群では,雄は投与後1日に,雌は投与後2日に各1例が死亡した.267 mg/kg群では,雄は投与後1日に1例,投与後2日に3例が,雌は投与後2日に5例が死亡した.400 mg/kg以上の群では,雌雄とも投与後2日までに全例が死亡した.死亡例は,投与後1日よりも投与後2日に多くみられた.
LD50値は,雄で 218(95%信頼限界:166〜287)mg/kg,雌で 208 mg/kgであった.
死亡例では,投与後2日の雌雄のほぼ全例で膀胱内に緑色液体貯留が,投与後1および2日の雌雄の半数例以上で腺胃粘膜の暗赤色化および胸腺に散在性の暗赤色斑がみられた.その他に,投与後1および2日の死亡例の雌雄の少数例で膀胱粘膜の暗赤色化が,投与後1日の死亡例の雄1例で赤褐色の腹水貯留がみられた.
| 胸腺: | 剖検で散在性の暗赤色斑がみられた雌雄の死亡例では,皮質および髄質に中等度〜高度の出血が観察された. |
| 膀胱: | 剖検で粘膜の暗赤色化がみられた雌の死亡例では,粘膜および粘膜下組織に中等度の出血が観察された. |
胃では,いずれの例とも著変はみられなかった.
LD50値は,雄で218(166〜287)mg/kg,雌で208 mg/kgであり,雌雄差は認められなかった.
死亡例は,投与後6時間まではみられず,投与後1日よりも投与後2日に多くみられた.投与後3日以降の生存例では一般状態に異常は観察されず,投与後10日頃からの体重は対照群とほぼ同様の推移を示していることから,生存例では投与の影響からの回復は早いものと思われた.剖検では,投与後2日の死亡例の半数例以上で膀胱内に緑色液体貯留がみられた.これは,被験物質あるいはその代謝物の尿中排泄に関連した変化と思われたが,生存例の尿の色調および外部生殖器周囲の被毛の汚れなどの異常は観察されなかった.さらに,投与後1および2日の死亡例の少数例に膀胱粘膜の暗赤色化がみられ,病理組織学的検査で粘膜および粘膜下組織に出血が観察されたことから,尿中排泄物は膀胱粘膜刺激性を有する可能性が考えられた.また,投与後1および2日の死亡例のほとんどの例に腺胃の暗赤色化がみられたが,病理組織学的検査で著変は見られず,胃粘膜に対しては膀胱粘膜に及ぼす程の影響はないものと思われた.その他に,死亡例の胸腺の暗赤色斑(病理組織学的検査における出血)は死戦期の変化の一つと考えられた.
| 連絡先 | |||
| 試験責任者: | 和田 浩 | ||
| 試験担当者: | 藤村高志,内藤一嘉,小池 恒雄, 木村 均,牧野浩平 | ||
| (株)日本バイオリサーチセンター 羽島研究所 | |||
| 〒 501-62 岐阜県羽島市福寿町間島 6-104 | |||
| Tel 058-392-6222 | Fax 058-391-3171 | ||
| Correspondence | |||
| Authors: | Hiroshi Wada(Study director) Takashi Fujimura, Kazuyoshi Naitou, Tsuneo Koike, Hitoshi Kimura and Kohei Makino | ||
| Nihon Bioresearch Inc. Hashima Laboratory | |||
| 6-104, Majima, Fukuju-cho, Hashima, Gifu, 501-62, Japan | |||
| Tel +81-58-392-6222 | Fax +81-58-391-3171 | ||