エテニルトリメトキシシランについて,Salmonella typhimurium TA100,TA1535,TA98,TA1537およびEscherichia coli WP2 uvrAを用いる復帰変異試験を実施した.
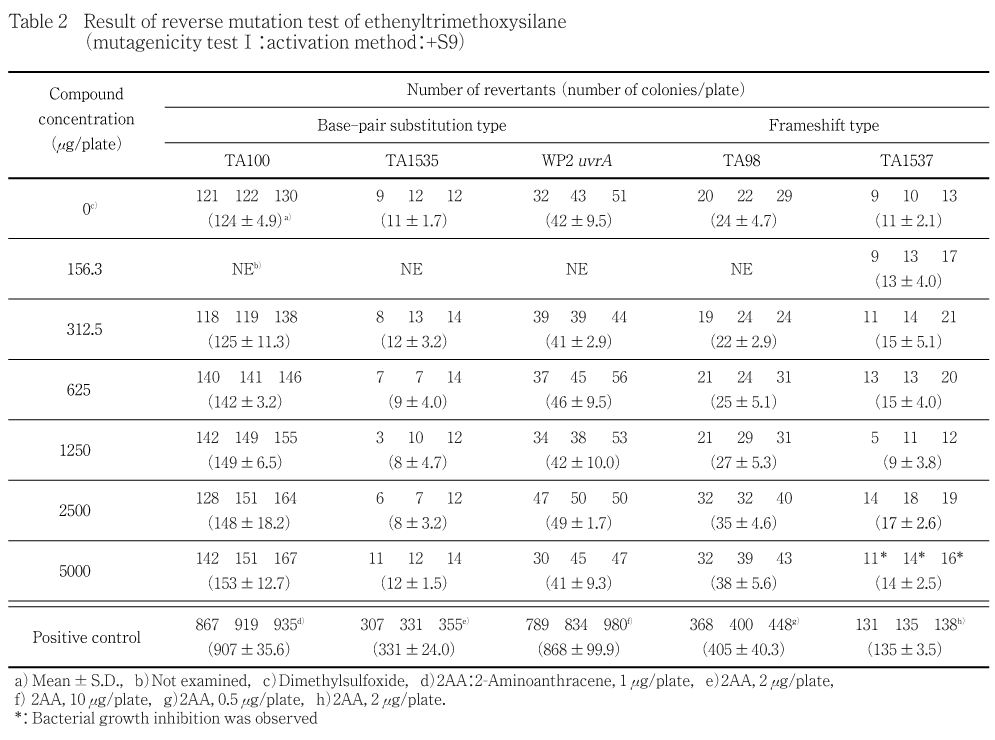
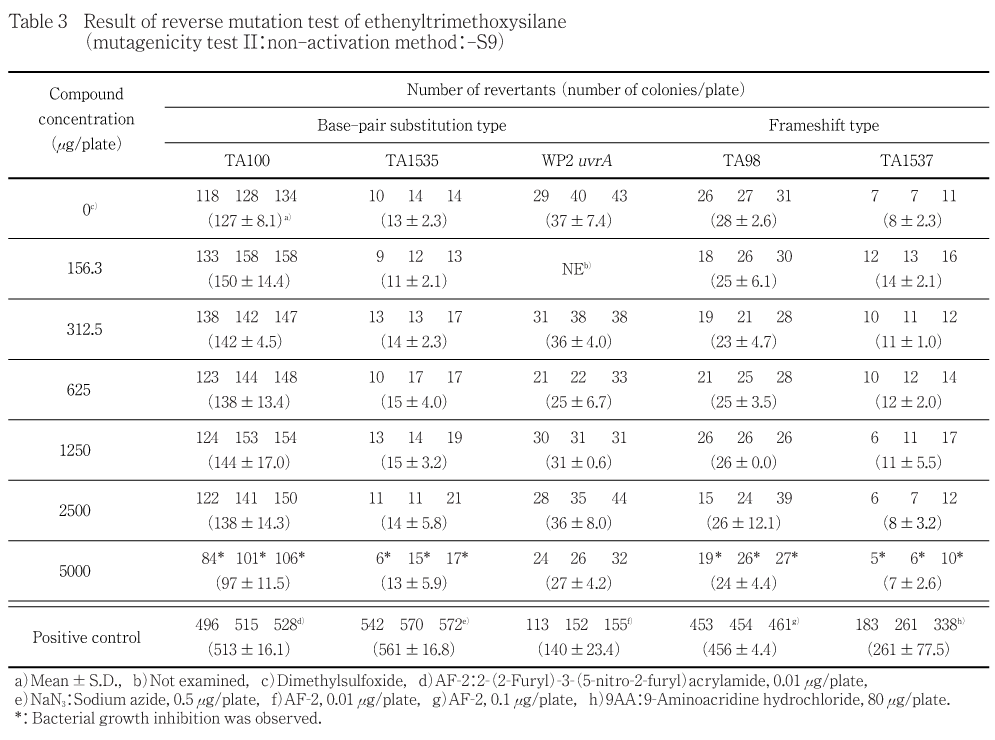
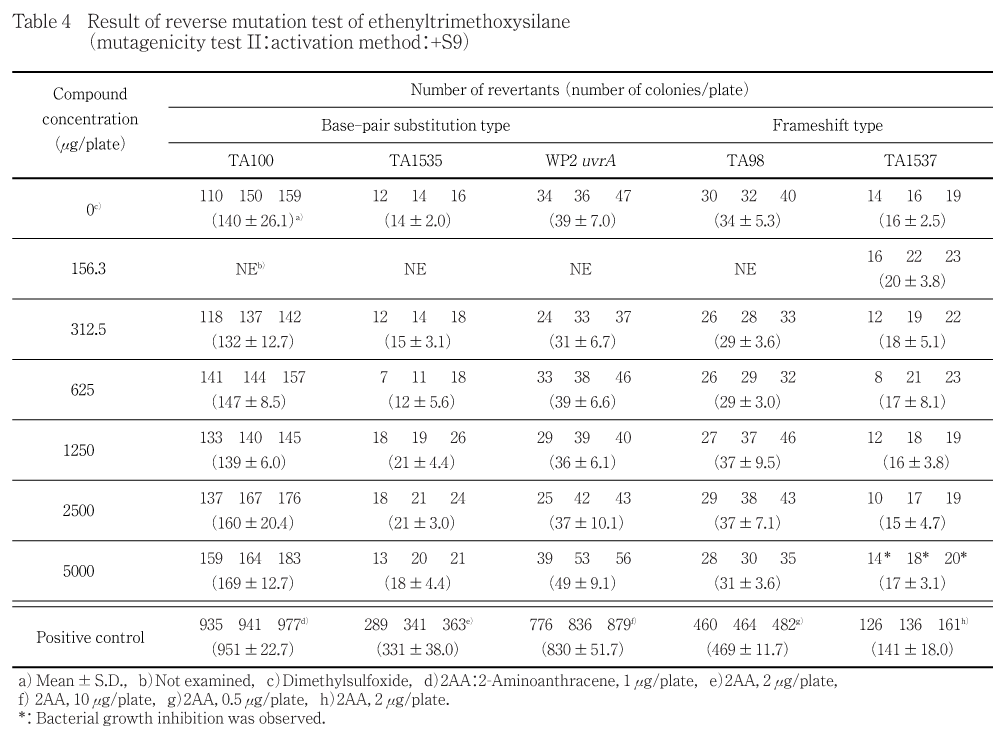
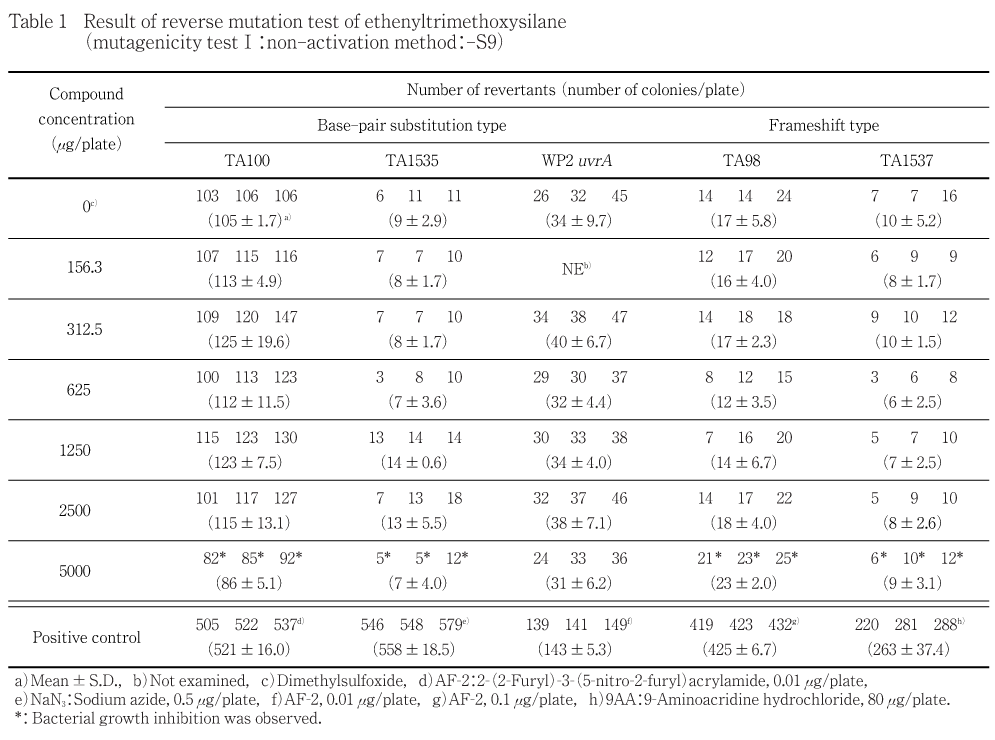
用量設定試験の結果をもとに,本試験ではS9 mix無添加および添加の場合とも,菌の生育阻害が認められた菌株については,菌の生育阻害を示さないと考えられる濃度が4濃度以上含まれるように公比2により6濃度を,菌の生育阻害が認められなかった菌株については,5000 μg/plateを最高濃度として,公比2により5濃度を設定した.すなわち,S9 mix無添加の場合,TA100,TA1535,TA98およびTA1537では156.3,312.5,625,1250,2500,5000 μg/plate,WP2 uvrAでは312.5,625,1250,2500,5000 μg/plate,S9 mix添加の場合,TA100,TA1535,WP2 uvrAおよびTA98では312.5,625,1250,2500,5000 μg/plate,TA1537では156.3,312.5,625,1250,2500,5000 μg/plateとした.
2回の本試験の結果,S9 mix無添加および添加のいずれの濃度においても,復帰変異コロニー数が陰性対照値の2倍以上に増加しなかった.
以上の結果から,本試験条件下では,エテニルトリメトキシシランは変異原性を有しない(陰性)と結論する.
エテニルトリメトキシシランは,無色透明の液体で微臭があり,水に難溶(加水分解性あり)である[Lot No. 308595,含量:100 %,沸点:123℃,蒸気圧:2.7 kPa以下/25℃,揮発性:なし,融点:0℃以下,比重又は嵩比重:0.97(25℃),信越化学工業(東京)].入手後は,冷蔵・遮光の条件下で保管した.実験終了後に被験物質を分析し,使用期間中安定であったことを確認した.
被験物質はジメチルスルホキシド(以下DMSO,同仁化学研究所)に用時溶解して最高濃度原液を調製し,その後,DMSOで順次希釈して所定の濃度の被験物質調製液を調製した.
陽性対照物質として下記のものを用いた.
| 2AA : | 2-アミノアントラセン | (Sigma-Aldrich) | |
| NaN3 : | アジ化ナトリウム | (ナカライテスク) | |
| 9AA : | 9-アミノアクリジン | (ナカライテスク) | |
| AF-2 : | 2-(2-フリル)-3-(5-ニトロ-2-フリル)アクリルアミド | (和光純薬工業) |
NaN3は注射用水(大塚製薬工場)に,その他はDMSOに溶解したものを使用した.
Salmonella typhimurium TA98,TA100,TA1535,TA1537 1)およびEscherichia coli WP2 uvrA 2)の5菌株を用いた.これら5菌株は,日本バイオアッセイ研究センターから分与された.試験菌株は,超低温フリーザー(-80℃)で凍結保存したものを使用した.これら菌株はアミノ酸要求性,紫外線感受性,膜変異,薬剤耐性などの遺伝的特徴を事前に調べ,特性を備えていることを確認した.
試験に際して,L字型試験管にニュートリエントブロス(Oxoid Nutrient Broth No.2)溶液を10 mL分注し,これに凍結保存した菌懸濁液を融解して20 μLを接種した.37℃で8時間振盪培養した後,濁度計を用いて濁度を測定し,濁度と生菌数の換算式から1 mLあたりの生菌数が1×10^9以上であることを確認した.
注射用水100 mLに対して,Bacto Agar (DIFCO) 0.6 g,塩化ナトリウム0.5 gの割合で加え,高圧蒸気滅菌し完全に溶解させた後,S. typhimuriumの場合には0.5 mmol/L L-ヒスチジンと0.5 mmol/L D-ビオチンを混合した水溶液を,E. coliの場合には0.5 mmol/L L-トリプトファン水溶液を10:1の割合で加えて調製した.
テスメディアAN培地(オリエンタル酵母工業)を購入し,使用した.なお,培地1 Lあたりの組成は下記のとおりである.
| 硫酸マグネシウム・七水塩 | 0.2 g | |
| クエン酸・一水塩 | 2 g | |
| リン酸水素二カリウム | 10 g | |
| リン酸一アンモニウム | 1.92 g | |
| 水酸化ナトリウム | 0.66 g | |
| グルコース | 20 g | |
| 寒天 | 15 g |
培地は,径90 mmのシャーレ1枚あたり30 mLを流して固めたものである.
S9(オリエンタル酵母工業)は,誘導剤としてフェノバルビタールおよび5,6-ベンゾフラボンを投与したSprague-Dawley系雄ラットの肝臓から調製され,製造後6ヵ月以内のものを用いた.S9 mixは,S9mix用のCofactor(Cofactor-I,オリエンタル酵母工業)を注射用水で溶解して,使用直前にS9 を加えて調製した.
S9 mix 1 mLあたりの組成は下記のとおりである.
| S9 | 0.1 mL | |
| 塩化カリウム | 33 μmol | |
| 塩化マグネシウム六水塩 | 8 μmol | |
| D-グルコース6-リン酸 | 5 μmol | |
| b-NADPH | 4 μmol | |
| b-NADH | 4 μmol | |
| Na-リン酸緩衝液(pH7.4) | 100 μmol | |
| 注射用水 | 残量 |
試験はプレインキュベーション法で実施した.
乾熱滅菌した試験管に(i)被験物質調製液,陰性対照(DMSO),陽性対照0.1 mL,(ii)0.1 mol/L Na-リン酸緩衝液(pH7.4)0.5 mL(S9 mix無添加)またはS9 mix 0.5 mL(S9 mix添加),(iii)菌懸濁液0.1 mLの順に加え,37℃で20分間振盪培養した.その後,45℃に保温したトップアガー2 mLを加え混和し,最少グルコース寒天平板培地上に播き広げ,トップアガーが凝固した後,プレートを転倒して37℃で48時間培養した.
培養終了後,被験物質による菌の生育阻害を調べるため,実体顕微鏡(×100)を用いて菌の生育状態を観察した.また,目視により被験物質の析出の有無を確認した.復帰変異コロニー数は,自動コロニーカウンターにより計測した.用量設定試験は各濃度につき1枚のプレートを使用した.本試験は各濃度につき3枚のプレートを使用し,再現性を確認するため2回実施した.
被験物質における復帰変異コロニー数が,陰性対照の2倍以上の値を示し,濃度に依存して増加し,さらにその増加に再現性が認められた場合に,変異原性を有する(陽性)と判定した.なお,結果の判定には統計学的手法は用いなかった.
用量設定試験を0.305,1.22,4.88,19.5,78.1,312.5,1250,5000 μg/plateの8濃度で実施した結果,S9 mix無添加の場合,TA100,TA1535,TA98およびTA1537の5000 μg/plateにおいて,S9 mix添加の場合,TA1537の5000 μg/plateにおいて菌の生育阻害が認められた.なお,S9 mix無添加および添加の場合とも,析出物は認められなかった.従って,本試験の試験濃度は,菌の生育阻害が認められた菌株については,菌の生育阻害を示さないと考えられる濃度が4濃度以上含まれるように公比2により6濃度を,菌の生育阻害が認められなかった菌株については,5000 μg/plateを最高濃度として,公比2により5濃度を設定した.すなわち,S9 mix無添加の場合,TA100,TA1535,TA98およびTA1537では156.3,312.5,625,1250,2500,5000 μg/plate,WP2 uvrAでは312.5,625,1250,2500,5000 μg/plate,S9 mix添加の場合,TA100,TA1535,WP2 uvrAおよびTA98では312.5,625,1250,2500,5000 μg/plate,TA1537では156.3,312.5,625,1250,2500,5000 μg/plateを設定した.
2回の本試験の結果,S9 mix無添加および添加の場合とも,いずれの菌株においても,陰性対照値の2倍以上を示す復帰変異コロニー数の増加は認められなかった
S9 mix無添加および添加の場合とも,すべての濃度において析出は認められなかった.
なお,S9 mix無添加および添加において陽性対照が各菌株に誘発した復帰変異コロニー数は,各菌株の溶媒対照の復帰変異コロニー数と比較して,明らかに2倍以上に増加し,陽性結果を示した.
以上の結果から,本試験条件下では,エテニルトリメトキシシランは変異原性を有しない(陰性)と結論する.
なお,エテニルトリメトキシシランは当試験施設で同時期に実施した哺乳類の培養細胞を用いる染色体異常試験で陽性の結果が得られている3).
| 1) | Maron DM, Ames BN:Revised methods for the Salmonella mutagenicity test. Mutation Res, 113: 173-215(1983). |
| 2) | Green MHL, Muriel WJ:Mutagen testing using Trp+ reversion in Escherichia coli. Mutation Res, 38: 3-32(1976). |
| 3) | 三輪芳久ら:エテニルトリメトキシシランの哺乳類の培養細胞を用いる染色体異常試験.化学物質毒性試験報告,13:182-186(2006). |
| 連絡先 | |||
| 試験責任者: | 三輪芳久 | ||
| 試験担当者: | 後藤幸二,小林梨沙 | ||
| (株)日本バイオリサーチセンター 羽島研究所 | |||
| 〒501-6251 岐阜県羽島市福寿町間島6-104 | |||
| Tel 058-392-6222 | Fax 058-392-1284 | ||
| Correspondence | |||
| Authors: | Yoshihisa Miwa(Study director) Kouji Goto, Risa Kobayashi |
||
| Hashima Laboratory, Nihon Bioresearch Inc. | |||
| 104, 6-chome, Majima, Fukuju-cho, Hashima, Gifu, 501-6251, Japan. | |||
| Tel +81-58-392-6222 | Fax +81-58-392-1284 | ||