ディスパーズレッド206のラットを用いる28日間反復経口投与毒性試験
Twenty-eight-day Repeat Dose Oral Toxicity Test of Disperse Red 206 in Rats
要約
ディスパーズレッド206の0,250,500および1000 mg/kgを1群につき雌雄各7匹のCrj:CD(SD)IGSラットに28日間反復経口投与してその毒性を検討した.また,投与終了の翌日から0および1000 mg/kg投与群の雌雄各7匹について14日間観察を継続し,投与期間中にみられた毒性の回復性についても検討し,以下の成績を得た.
500 mg/kg投与群の雄および1000 mg/kg投与群の雌雄に,ヘマトクリット値あるいは平均赤血球ヘモグロビン量の低値がみられ,回復期間終了時にも1000 mg/kg投与群の雌雄に平均赤血球容積および平均赤血球ヘモグロビン量の低値,雌にヘモグロビン量の低値が認められた.
また,250 mg/kg以上の投与群の雄にγ-グロブリン分画比の低値がみられ,回復期間終了時には1000 mg/kg投与群の雌に無機リン濃度の高値が認められた.
250 mg/kg以上の投与群の雄および1000 mg/kg投与群の雌で肝臓重量の高値,500 mg/kg以上の投与群の雌雄で胸腺重量の低値,1000 mg/kg投与群の雌で卵巣重量の低値が認められた.回復期間終了時にも1000 mg/kg投与群の雄で肝臓重量の高値,脾臓重量の低値,雌で下垂体重量の低値が認められた.
なお,被験物質の色調を反映して250 mg/kg以上の投与群の雌雄に消化管(空腸・回腸・盲腸)の内容物や器官および組織(空腸・回腸・腹腔内脂肪織・全身の皮下織)の赤色あるいは暗緑色の変色がみられ,回復期間終了時にも全身の皮下織および腹腔内脂肪織に同様の変化が認められた.
以上のことより,雄で250 mg/kg以上の投与群に肝臓重量の高値とγ-グロブリン分画比の低値,雌で500 mg/kg以上の投与群に胸腺重量の低値など被験物質投与による影響が認められていることから,本試験条件下におけるディスパーズレッド206の無影響量(NOEL)は,雄で250 mg/kg/day未満,雌で250 mg/kg/dayと考えられた.
方法
1. 被験物質および対照物質の調製
ディスパーズレッド206 [Lot No. 00132,提供者:三井BASF染料(株)(福岡)] を乾燥させて粉末としたものを被験物質(純度:97.65 %)として使用した.ディスパーズレッド206は,融点150 ℃以上,比重約0.5,分配係数log Pow 3.91の水に懸濁するが不溶で,DMSOおよびアセトンにも不溶の赤黒褐色で無臭の粉末である.ディスパーズレッド206は気密容器に入れ,冷所に保存した.試験期間中の被験物質の安定性を,残余被験物質を用いた純度の分析成績により確認した.
0.5 %メチルセルロース水溶液を用いて被験物質を懸濁した.遮光気密容器に入れ,冷暗所に調製後1週間を限度として保存し,室温に戻してから投与に使用した.
投与に先立って調製液中のディスパーズレッド206の均一性および安定性ならびに投与に用いる各濃度の調製液中のディスパーズレッド206濃度を分析して確認した.
2. 試験動物および飼育条件
日本チャールス・リバー(株)厚木飼育センター生産のSPF Crj:CD(SD)IGSラットを4週齢で購入し,6〜7日間馴化飼育を行い,雌雄各42匹を5週齢で試験に供した.投与前々日の体重に基づいて層化無作為抽出法により群分けを行った.
動物は温度21〜24 ℃,湿度45〜68 %,換気回数10〜15回/時間,照明時間8〜20時でブラケット式金属製金網床ケージに,群分け前は3匹,群分け後は1匹収容した.飼料はγ線照射固型飼料CRF-1(オリエンタル酵母工業(株))を金属製給餌器により,飲料水は札幌市水道水を自動給水装置により,それぞれ自由摂取させた.
3. 投与量および投与方法
雌雄のSD系ラットに0,250,500および1000 mg/kgを14日間投与した予備試験の結果,1000 mg/kg投与群の雄で肝臓および腎臓,雌で肝臓に重量増加または増加傾向が認められた.このことから,高用量群に1000 mg/kgを設定し,公比2で除して,500および250 mg/kgの中用量群および低用量群,ならびに溶媒対照群を加えた雌雄4群を設定した.
1日1回,28日間,9:30から12:00の間に胃ゾンデを用いて強制的に胃内に5 mL/kgの投与容量で経口投与した.なお,各個体の投与液量は投与日に最も近い測定日の体重に基づいて算出した.
4. 検査項目
1) 一般状態観察
投与開始日を投与1日,投与28日の翌日を回復1日としてそれぞれ起算し,投与終了時解剖例は投与28日の翌日の剖検日まで,回復終了時解剖例は回復14日の翌日の剖検日まで,個々の動物の生死,外観,行動等について,毎日の投与前および投与後に各1回観察した.回復期間中は毎日1回観察した.
2) 体重および摂餌量測定
個々の動物の体重および摂餌量を,投与1,2,7,14,21および28日の投与前,回復1,7および14日に,各期間終了の翌日の剖検日にも体重を電子式上皿天秤を用いて測定した.体重増加量および体重増加率を投与期間中は体重増加量=(投与28日体重)-(投与1日体重),体重増加率=[(体重増加量)/(投与1日体重)]× 100,回復期間中は体重増加量=(回復14日体重)-(回復1日体重),体重増加率=[(体重増加量)/(回復1日体重)]× 100により算出した.摂餌量は給与量から残量を減じた後,1日分の消費量を算出した.
3) 尿検査
投与4週および回復2週に,全例について非絶食下でラット用代謝ケージ((株)夏目製作所)を用いて採尿し,投与直後から3時間前後までに排泄した新鮮尿についてpH,蛋白,糖,ケトン体,ウロビリノーゲン,ビリルビン,潜血反応(以上,マルティスティックス,バイエルメディカル(株)),色調(肉眼観察),沈渣(鏡検)を,また約21時間の蓄尿で尿量(容量測定)および比重(屈折計法,アタゴ(株))を測定し,同時に採尿中の飲水量(重量測定)を測定した.
4) 血液学検査
全例について,約16〜21時間絶食させたラットをエーテル麻酔し,腹部大動脈より採血した.EDTA・2Kで処理した血液約1 mLを用い,赤血球数,ヘマトクリット値,血小板数,白血球数(以上,電気抵抗法),ヘモグロビン量(シアンメトヘモグロビン法),平均赤血球容積(赤血球数,ヘマトクリット値より算出),平均赤血球ヘモグロビン量(赤血球数,ヘモグロビン量より算出),平均赤血球ヘモグロビン濃度(ヘマトクリット値,ヘモグロビン量より算出)(以上,自動血球計数装置F-820,シスメックス),網赤血球数(Brecher法),白血球百分比(May-Gr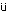 wald-Giemsa染色)を測定した.また,3.8 %クエン酸ナトリウムで処理し,3000回転/分10分間の遠心分離により得られた血漿を用いて,プロトロンビン時間(トロンボプラスチン法)および活性化部分トロンボプラスチン時間(エラジン酸法)(以上,血液凝固自動測定装置アメルングKC-10A,バクスター)を測定した.
wald-Giemsa染色)を測定した.また,3.8 %クエン酸ナトリウムで処理し,3000回転/分10分間の遠心分離により得られた血漿を用いて,プロトロンビン時間(トロンボプラスチン法)および活性化部分トロンボプラスチン時間(エラジン酸法)(以上,血液凝固自動測定装置アメルングKC-10A,バクスター)を測定した.
5) 血液生化学検査
全例について,血液学検査と同時に採血し,ヘパリンナトリウム処理後,3000 回転/分10分間の遠心分離により得られた血漿を用いて,GOT(IFCC法),乳酸脱水素酵素(Wr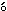 blewski & La Due法)およびグルコース(ヘキソキナーゼ法)を測定し,分離剤入り試験管に血液を採取し,3000 回転/分で10分間の遠心分離により得られた血清を用いて,GPT(IFCC法),アルカリホスファターゼ(GSCC法),γ-GTP(L-γ-グルタミル-3-カルボキシ-4-ニトロアニリド基質法),総コレステロール(酵素法),トリグリセリド(遊離グリセロール消去法),総ビリルビン(アゾビリルビン法),尿素窒素(ウレアーゼ・インド
フェノール法),クレアチニン(Jaff
blewski & La Due法)およびグルコース(ヘキソキナーゼ法)を測定し,分離剤入り試験管に血液を採取し,3000 回転/分で10分間の遠心分離により得られた血清を用いて,GPT(IFCC法),アルカリホスファターゼ(GSCC法),γ-GTP(L-γ-グルタミル-3-カルボキシ-4-ニトロアニリド基質法),総コレステロール(酵素法),トリグリセリド(遊離グリセロール消去法),総ビリルビン(アゾビリルビン法),尿素窒素(ウレアーゼ・インド
フェノール法),クレアチニン(Jaff 法),カルシウム(OCPC法),無機リン(Fiske-Subba Row法),総蛋白(ビウレット法)(以上,自動分析装置7150形,日立製作所),ナトリウムおよびカリウム(炎光光度法)(以上,自動炎光光度計480型,コーニング),クロール(電量滴定法,クロライドカウンターCL-6M,平沼産業),蛋白分画およびA/G比(セルロースアセテート膜電気泳動法,全自動電気泳動装置CTE-150,常光)を測定した.
法),カルシウム(OCPC法),無機リン(Fiske-Subba Row法),総蛋白(ビウレット法)(以上,自動分析装置7150形,日立製作所),ナトリウムおよびカリウム(炎光光度法)(以上,自動炎光光度計480型,コーニング),クロール(電量滴定法,クロライドカウンターCL-6M,平沼産業),蛋白分画およびA/G比(セルロースアセテート膜電気泳動法,全自動電気泳動装置CTE-150,常光)を測定した.
6) 剖検および器官重量測定
全例について,投与28日あるいは回復14日の翌日に剖検した.剖検時には,体外表を観察し,エーテル麻酔下で採血後,放血致死させ,全身の器官・組織を肉眼的に観察した.また,電子式上皿天秤を用いて脳,肺,心臓,肝臓,腎臓,脾臓,副腎,下垂体,胸腺,甲状腺(上皮小体含む),精巣,精巣上体,卵巣を固定する前に重量測定した.左右のある器官は左右併せて測定した.個々の器官の絶対重量を剖検当日に測定した体重で除し,100を乗じた相対重量を算出した.
7) 病理組織学検査
全例について剖検時に固定・保存した全器官・組織について,パラフィン包埋後薄切し,ヘマトキシリン・エオジン染色標本を作製して鏡検した.鏡検は対照群および1000 mg/kg投与群の全例について行った.
5. 統計解析
投与期間中は,0および1000 mg/kg投与群については回復群の動物も合わせて集計し,0 mg/kg投与群を対照として比較検定を行った.
体重,体重増加量および増加率,摂餌量,尿検査の定量的項目(尿比重を除く),血液学的検査(白血球百分比を除く),血液化学的検査,器官の絶対および相対重量の成績についてBartlettの検定法によって等分散性を解析し,等分散の場合は一元配置分散分析法,不等分散の場合はKruskal-Wallisの検定法で解析した.一元配置分散分析の結果,有意差がみられた場合は,Dunnettの検定法を用いて,Kruskal-Wallis法の解析の結果,有意差がみられた場合は,Mann-WhitneyのU-検定法を用いてそれぞれ対照群との比較を行った.
尿検査の定性的項目,尿比重および白血球百分比の成績については,群毎の傾向をKruskal-Wallisの検定法で解析し,有意差がみられた場合はMann-WhitneyのU-検定法を用いて対照との比較を行った.なお,白血球百分比については毎の平均値および標準偏差も算出した.対照群との比較検定については,危険率5 %未満を統計学的に有意とした.
成績
1. 一般状態
投与期間,回復期間いずれにおいても,各投与群の雌雄ともに異常は認められなかった.
2. 体重(Fig. 1)
250 mg/kg投与群の雄にのみ投与28日間の体重増加量および体重増加率に有意な高値がみられたが,用量依存的な変化ではなかった.

3. 摂餌量(Fig. 2)
250 mg/kg投与群の雄にのみ投与28日に対照群と比較して有意な増加がみられたが,用量依存的な変化ではなかった.

4. 尿検査(Table 1, 2)
投与期間,回復期間いずれにおいても,雌雄の各投与群に対照群と比較して有意な変化みられなかった.


5. 血液学検査(Table 3, 4)
500 mg/kg投与群の雄に赤血球数およびヘマトクリット値の有意な低値がみられ,1000 mg/kg投与群の雄にヘマトクリット値の有意な低値,雌に平均赤血球ヘモグロビン量の有意な低値がみられ,回復期間終了時にも1000 mg/kg投与群の雌雄ともに平均赤血球容積および平均赤血球ヘモグロビン量の有意な低値,雌にヘモグロビン量の有意な低値が認められた.回復期間終了時の1000 mg/kg投与群の雄に好酸球百分比の有意な高値がみられたが,生理学的変動範囲内の値であり毒性学的意義はないと判断した.


6. 血液生化学検査(Table 5, 6)
250 mg/kg以上の投与群の雄にγ-グロブリン分画比に対照群と比較して有意な低値がみられ,回復期間終了時に1000 mg/kg投与群の雌に無機リン濃度の有意な高値が認められた.
他に,250 mg/kgの投与群の雌にクレアチニン濃度の有意な高値,500 mg/kg投与群の雌にカリウム濃度の有意な高値,1000 mg/kg投与群の雄にα2-グロブリン分画比の有意な高値,雌にγ-GTP活性の有意な高値が認められたが,用量依存的な変化ではなかった.回復期間終了時にも1000 mg/kg投与群の雌にトリグリセリド濃度の有意な低値がみられたが,背景データの変動範囲内の変化であり,毒性学的意義はないと判断した.


7. 剖検
250 mg/kg以上の投与群の雄および500 mg/kg以上の投与群の雌に空腸・回腸内容物の赤紫色化,250 mg/kg以上の投与群の雌雄に盲腸内容物の暗緑色化,空腸・回腸および腹腔内脂肪織の淡赤色化がみられた.これらの変化は,用量の増加に伴う例数の増加がみられた.また,250 mg/kg投与群の雌1例,500 mg/kg以上の投与群の雌雄に全身の皮下織の淡赤色化がみられ,回復期間終了時にも1000 mg/kg投与群の雌雄に全身の皮下織および腹腔内脂肪織の淡赤色化が全例にみられた.この変化は消化管から吸収された被験物質そのものの色調を反映したものであり,色調の変化自体には毒性学的意義はないと判断した.
8. 器官の絶対および相対重量(Table 7, 8)
対照群と比較して250 mg/kg以上の投与群の雄に肝臓の絶対および相対重量の有意な高値,500 mg/kg以上の投与群の雌雄に胸腺の絶対および相対重量に有意な低値あるいは低値傾向,1000 mg/kg投与群の雌に肝臓の相対重量の有意な高値,絶対重量の高値傾向,卵巣の相対重量の有意な低値,絶対重量の低値傾向がみられ,回復期間終了時にも1000 mg/kg投与群の雄に肝臓の絶対重量の有意な高値,相対重量の高値傾向,脾臓の絶対重量の低値傾向,相対重量の有意な低値が認められた.
他に,250 mg/kg投与群の雄に副腎の絶対重量の有意な高値がみられたが,用量依存的な変化ではなく,回復期間終了時に1000 mg/kg投与群の雌に下垂体の絶対および相対重量の有意な低値がみられたが,投与終了時にはみられない変化であった.


9. 病理組織学検査
1000 mg/kg投与群の雄1例と雌2例に腎臓,肝臓,下垂体などの軽度な変化が散見されたのみであった.回復期間終了時でも1000 mg/kg投与群の雄3例の肺,肝臓,腎臓などに軽度な変化が散見されたのみであった.
考察
500 mg/kg投与群の雄に赤血球数およびヘマトクリット値の有意な低値がみられ,1000 mg/kg投与群でも雄にヘマトクリット値の有意な低値,雌に平均赤血球ヘモグロビン量の有意な低値が認められた.これらの変化はディスパーズレッド206と同様にアゾ基を持つPonceau 3R,Yellow ABなどのアゾ色素で肝障害,成長抑制あるいは貧血などが報告されている1)ことから,ディスパーズレッド206に起因して発現した貧血と考えられた.この貧血は,回復期間終了時にも回復することなく認められた。
投与期間終了時に250 mg/kg以上の投与群の雄にγ-グロブリン分画比の有意な低値がみられ,この分画が免疫グロブリンの存在する部分であること,500 mg/kg以上の投与群で胸腺の絶対重量が雌雄ともに低値傾向を示していることから,免疫機能の低下による可能性が考えられた.しかし,白血球数およびリンパ球百分比などに変化がなく,病理組織学検査においても免疫機能の低下を示唆する変化はみられないことから,この変化は極軽微なものと考えられた.回復期間終了時には1000 mg/kg投与群の雌で無機リン濃度の有意な高値がみられたが,ディスパーズレッド206投与の影響である可能性が示唆された.
250 mg/kg以上の投与群の雄および1000 mg/kg投与群の雌で,肝臓の絶対および相対重量に有意な高値あるいは高値傾向が認められた.雄で250あるいは500 mg/kg投与群にも有意差がみられていることについては,本試験における雄の対照群の体重が低値であることに起因する可能性も考えられたが,被験物質の影響も否定することはできなかった.1000 mg/kg投与群の雌に卵巣の絶対および相対重量に低値傾向または低値がみられたが,その発現機序を明らかにすることはできなかった.一方,回復期間終了時に1000 mg/kg投与群の雄で脾臓の相対重量に低値がみられ,投与期間終了時に胸腺重量の低値等により免疫機能の低下が示唆されていることから,ディスパーズレッド206による影響と考えられた.
以上のことより,雄で250 mg/kg以上の投与群に肝臓重量の高値,γ-グロブリン分画比の低値,雌で500 mg/kg以上の投与群に胸腺重量の低値など被験物質投与による影響が認められていることから,本試験条件下におけるディスパーズレッド206の無影響量(NOEL)は,雄で250 mg/kg/day未満,雌で250 mg/kg/dayと考えられた.
文献
| 1) | 浦口健二ら編,"トキシコロジー毒理学の基本的問題点とその実際,"地人書館,東京,1978, p. 978. |
| 連絡先 |
| 試験責任者: | 須永昌男 |
| 試験担当者: | 木口雅夫,咲間正志,笠原みゆき,平田真理子,古川正敏 |
| (株)化合物安全性研究所 |
| 〒004-0839 札幌市清田区真栄363-24 |
| Tel 011-885-5031 | Fax 011-885-5313 | |
| Correspondence |
| Authors: | Masao Sunaga(Study director)
Masao Kiguchi, Masashi Sakuma, Miyuki Kasahara, Mariko Hirata, Masatoshi Furukawa |
| Safety Research Institute for Chemical Compounds Co., Ltd. |
| 363-24 Shin-ei, Kiyota-ku, Sapporo-shi, Hokkaido, 004-0839, Japan |
| Tel +81-11-885-5031 | Fax +81-11-885-5313 | |
ディスパーズレッド206のラットを用いる28日間反復経口投与毒性試験(追加試験)
Twenty-eight-day Repeat Dose Oral Toxicity Additional Test of Disperse Red 206 in Rats
要約
ディスパーズレッド206のラットにおける28日間反復経口投与毒性試験において,250 mg/kg以上の投与群で肝重量の増加ならびにγ-グロブリンの低値が認められ,雄において無影響量を求めることができなかったため,250 mg/kg投与における変化の再現性を確認し,併せて雄における無影響量を求めることを目的とし,ディスパーズレッド206の0,80および250 mg/kgを1群につき7匹のCrj:CD(SD)IGS雄ラットに28日間反復経口投与し,以下の成績を得た.
剖検で250 mg/kg投与群に消化管(回腸および盲腸)の内容物や器官および組織(回腸および腹腔内脂肪織)の赤色あるいは暗緑色の被験物質の色調を反映した変色がみられたが,肝重量の増加ならびにγ-グロブリンの低値等の変化は認められなかった.
以上のことより,ディスパーズレッド206の80および250 mg/kg/dayを28日間連続経口投与し,250 mg/kg投与群において肝重量の増加ならびにγ-グロブリンの低値等の再現性は確認されず,いずれの投与群においても被験物質投与による変化は認められなかった.
方法
1. 被験物質および対照物質の調製
ディスパーズレッド206 [Lot No. 00132,提供者:三井BASF染料(株)(福岡)] を乾燥させて粉末としたものを被験物質(純度:96.97 %)として使用した.ディスパーズレッド206は,融点150 ℃以上,比重約0.5,分配係数log Pow 3.91の水に懸濁するが不溶で,DMSOおよびアセトンにも不溶の赤黒褐色で無臭の粉末である.ディスパーズレッド206は気密容器に入れ,冷所に保存した.試験期間中の被験物質の安定性を,残余被験物質を用いた純度の分析成績により確認した.
0.5 %メチルセルロース水溶液を用いて被験物質を懸濁した.遮光気密容器に入れ,冷暗所に調製後1週間を限度として保存し,室温に戻してから投与に使用した.
投与に先立って調製液中のディスパーズレッド206の均一性および安定性ならびに投与に用いる各濃度の調製液中のディスパーズレッド206濃度を分析して確認した.
2. 試験動物および飼育条件
日本チャールス・リバー(株)厚木飼育センター生産のSPF Crj:CD(SD)IGS雄ラットを4週齢で購入し,6日間馴化飼育を行い,21匹を5週齢で試験に供した.投与前々日の体重に基づいて層化無作為抽出法により群分けを行った.
動物は温度22〜24 ℃,湿度53〜71 %,換気回数10〜15回/時間,照明時間8〜20時で,ブラケット式金属製金網床ケージに,群分け前は3匹,群分け後は1匹収容した.飼料はg線照射固型飼料,CRF-1(オリエンタル酵母工業(株))を金属製給餌器により,飲料水は札幌市水道水を自動給水装置により,それぞれ自由摂取させた.
3. 投与量および投与方法
先に実施したディスパーズレッド206のラットにおける28日間反復経口投与毒性試験において雄の250 mg/kg投与群において,γ-グロブリンの高値および肝臓重量の増加が認められ,無影響量が求められなかったことから,高用量に250 mg/kgを,低用量にその約1/3量である80 mg/kgを,対照に0.5 %MC水溶液を投与する対照群を加えた3群を設定した.1日1回,28日間,9:00から11:30の間に胃ゾンデを用いて強制的に胃内に5 mL/kgの投与容量で経口投与した.なお,各個体の投与液量は投与日に最も近い測定日の体重に基づいて算出した.
4. 検査項目
1) 一般状態観察
投与開始日を投与1日として起算し,投与28日の翌日の剖検日まで,個々の動物の生死,外観,行動等について,毎日の投与前および投与後に各1回観察した.
2) 体重および摂餌量測定
個々の動物の体重および摂餌量を,投与1,2,7,14,21および28日の投与前ならびに投与28日の翌日の剖検日にも体重を電子式上皿天秤を用いて測定した.体重増加量および体重増加率を体重増加量=(投与28日体重)-(投与1日体重),体重増加率=[(体重増加量)/(投与1日体重)]× 100により算出した.摂餌量は給与量から残量を減じた後,1日分の消費量を算出した.
3) 血液生化学検査
全例について,約16〜19時間絶食させたラットをエーテル麻酔し,腹部大動脈より採血し,ヘパリンナトリウム処理後,3000 回転/分10分間の遠心分離により得られた血漿を用いて,GOT(IFCC法)を測定し,分離剤入り試験管に血液を採取し,3000 回転/分で10分間の遠心分離により得られた血清を用いて,GPT(IFCC法),総蛋白(ビウレット法)(以上,自動分析装置7150形,日立製作所),蛋白分画およびA/G比(セルロースアセテート膜電気泳動法,全自動電気泳動装置CTE-150,常光)を測定した.
4) 剖検および器官重量測定
全例について,投与28日の翌日に剖検した.剖検時には,体外表を観察し,エーテル麻酔下で採血後,放血致死させ,全身の器官・組織を肉眼的に観察した.また,電子式上皿天秤を用いて脳,肺,心臓,肝臓,腎臓,脾臓,副腎,下垂体,胸腺,甲状腺(上皮小体含む),精巣,精巣上体を固定する前に重量測定した.左右のある器官は左右併せて測定した.個々の器官の絶対重量を剖検当日に測定した体重で除し,100を乗じた相対重量を算出した.
5) 病理組織学検査
全例の肝臓について,パラフィン包埋後薄切し,ヘマトキシリン・エオジン染色標本を作製して鏡検した.
5. 統計解析
体重,体重増加量および増加率,摂餌量,血液生化学検査,器官の絶対および相対重量の成績についてBartlettの検定法によって等分散性を解析し,等分散の場合は一元配置分散分析法,不等分散の場合はKruskal-Wallisの検定法で解析した.一元配置分散分析の結果,有意差がみられた場合は,Dunnettの検定法を用いて,Kruskal-Wallis法の解析の結果,有意差がみられた場合は,Mann-WhitneyのU-検定法を用いてそれぞれ対照群との比較を行った.対照群との比較検定については,危険率5 %未満を統計学的に有意とした.
成績
1. 一般状態
80および250 mg/kg投与群ならびに対照群の全例ともに異常は認められなかった.
2. 体重(Fig. 1)
80および250 mg/kg投与群いずれにも,平均体重,投与期間中の体重増加量および体重増加率に対照群と比較して有意差は認められなかった.

3. 摂餌量(Fig. 2)
80および250 mg/kg投与群いずれにも,投与期間中に対照群と比較して有意差は認められなかった.

4. 血液生化学検査(Table 1)
80および250 mg/kg投与群いずれにも,対照群と比較して有意差は認められなかった.

5. 剖検
80 mg/kg投与群に異常は認められなかったが,250 mg/kg投与群の7例中の3例で回腸が淡赤色化し,内容物が赤紫色を呈した.また,全例で盲腸内容物の暗緑色化および腹腔内脂肪織の淡赤色化が認められた.
6. 器官重量(Table 2)
80および250 mg/kg投与群いずれにも対照群と比較して有意差は認められなかった.

7. 病理組織学的検査
肝臓に小肉芽腫が各投与群に散見されたが,被験物質投与による変化は認められなかった.
考察
先に実施したディスパーズレッド206のラットにおける28日間反復経口投与毒性試験において,250 mg/kg以上の投与群の雄および1000 mg/kg投与群の雌で,肝臓の絶対および相対重量に有意な高値あるいは高値傾向がみられた.この変化は,雄の対照群の体重が低値であること,また250 mg/kg投与群の体重増加量および増加率に有意差がみられ体重が対照群と比較して高値であったことに起因する可能性も考えられたが,被験物質の影響を否定することはできず,無影響量の推定根拠とした.しかし,追加試験においては,80および250 mg/kg投与群に肝臓の絶対および相対重量のいずれにも対照群と比較して有意差は認められなかった.
γ-グロブリンの低値については,先に実施した試験において雄の250 mg/kg以上の投与群に,γ-グロブリン分画比の有意な低値が認められ,この分画が免疫グロブリンの存在する部分であること,500 mg/kg以上の投与群で胸腺の絶対重量が雌雄ともに低値傾向を示したことから,免疫機能の低下による可能性を考慮し極軽微な変化ではあるが無影響量の推定根拠とした.しかし,追加試験において,80および250 mg/kg投与群では,対照群と比較して有意差は認められなかった.
一方,剖検時に,250 mg/kg投与群で消化管(回腸および盲腸)の内容物や器官および組織(回腸および腹腔内脂肪織)の赤色あるいは暗緑色の変色が認められ,この変化は先に実施した試験において被験物質そのものの色調を反映した毒性学的意義のない変化とされており,追加試験においても同様のものと判断した.
ディスパーズレッド206の80および250 mg/kg/dayを28日間連続経口投与し,250 mg/kg投与群において体重は対照群と同様に推移し,肝重量の増加ならびにγ-グロブリンの低値等はみられず,追加試験において先に実施した試験でみられた変化の再現性は認められないことから,これらの変化は再現できない極軽微な変化であると考えられた.
以上のことより,雄におけるディスパーズレッド206の無影響量(NOEL)は,先に実施したディスパーズレッド206のラットにおける28日間反復経口投与毒性試験において250 mg/kg/day未満と推定されていることから,80 mg/kg/dayとするのが妥当と考えられた.
| 連絡先 |
| 試験責任者: | 須永昌男 |
| 試験担当者: | 木口雅夫,咲間正志,笠原みゆき,平田真理子,古川正敏 |
| (株)化合物安全性研究所 |
| 〒004-0839 札幌市清田区真栄363-24 |
| Tel 011-885-5031 | Fax 011-885-5313 | |
| Correspondence |
| Authors: | Masao Sunaga(Study director)
Masao Kiguchi, Masashi Sakuma, Miyuki Kasahara, Mariko Hirata, Masatoshi Furukawa |
| Safety Research Institute for Chemical Compounds Co., Ltd. |
| 363-24 Shin-ei, Kiyota-ku, Sapporo-shi, Hokkaido, 004-0839, Japan |
| Tel +81-11-885-5031 | Fax +81-11-885-5313 | |

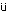 wald-Giemsa染色)を測定した.また,3.8 %クエン酸ナトリウムで処理し,3000回転/分10分間の遠心分離により得られた血漿を用いて,プロトロンビン時間(トロンボプラスチン法)および活性化部分トロンボプラスチン時間(エラジン酸法)(以上,血液凝固自動測定装置アメルングKC-10A,バクスター)を測定した.
wald-Giemsa染色)を測定した.また,3.8 %クエン酸ナトリウムで処理し,3000回転/分10分間の遠心分離により得られた血漿を用いて,プロトロンビン時間(トロンボプラスチン法)および活性化部分トロンボプラスチン時間(エラジン酸法)(以上,血液凝固自動測定装置アメルングKC-10A,バクスター)を測定した.
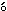 blewski & La Due法)およびグルコース(ヘキソキナーゼ法)を測定し,分離剤入り試験管に血液を採取し,3000 回転/分で10分間の遠心分離により得られた血清を用いて,GPT(IFCC法),アルカリホスファターゼ(GSCC法),γ-GTP(L-γ-グルタミル-3-カルボキシ-4-ニトロアニリド基質法),総コレステロール(酵素法),トリグリセリド(遊離グリセロール消去法),総ビリルビン(アゾビリルビン法),尿素窒素(ウレアーゼ・インド
フェノール法),クレアチニン(Jaff
blewski & La Due法)およびグルコース(ヘキソキナーゼ法)を測定し,分離剤入り試験管に血液を採取し,3000 回転/分で10分間の遠心分離により得られた血清を用いて,GPT(IFCC法),アルカリホスファターゼ(GSCC法),γ-GTP(L-γ-グルタミル-3-カルボキシ-4-ニトロアニリド基質法),総コレステロール(酵素法),トリグリセリド(遊離グリセロール消去法),総ビリルビン(アゾビリルビン法),尿素窒素(ウレアーゼ・インド
フェノール法),クレアチニン(Jaff 法),カルシウム(OCPC法),無機リン(Fiske-Subba Row法),総蛋白(ビウレット法)(以上,自動分析装置7150形,日立製作所),ナトリウムおよびカリウム(炎光光度法)(以上,自動炎光光度計480型,コーニング),クロール(電量滴定法,クロライドカウンターCL-6M,平沼産業),蛋白分画およびA/G比(セルロースアセテート膜電気泳動法,全自動電気泳動装置CTE-150,常光)を測定した.
法),カルシウム(OCPC法),無機リン(Fiske-Subba Row法),総蛋白(ビウレット法)(以上,自動分析装置7150形,日立製作所),ナトリウムおよびカリウム(炎光光度法)(以上,自動炎光光度計480型,コーニング),クロール(電量滴定法,クロライドカウンターCL-6M,平沼産業),蛋白分画およびA/G比(セルロースアセテート膜電気泳動法,全自動電気泳動装置CTE-150,常光)を測定した.













