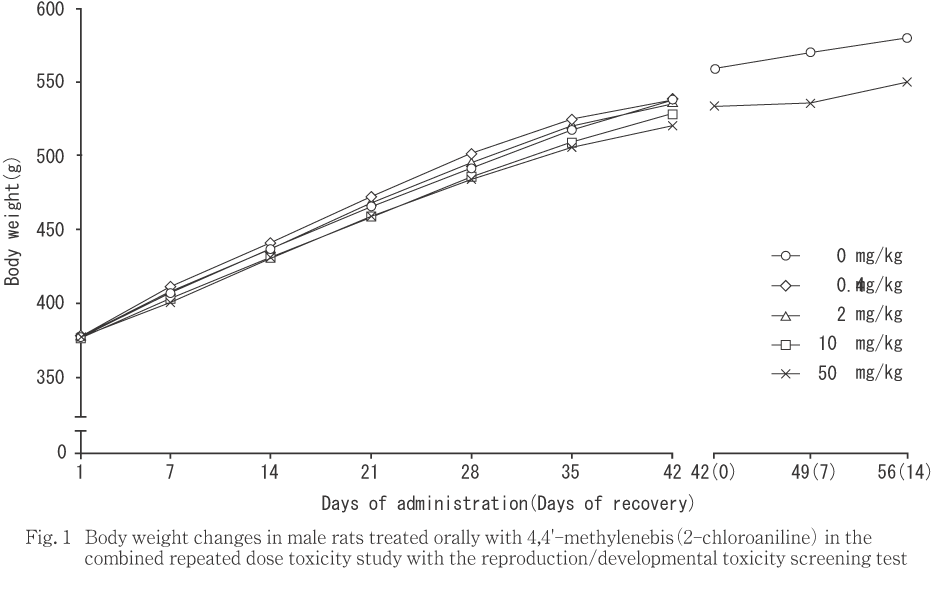
��4,4'-������ӥ�(2-���������˥��)�ϡ���˥��쥿�饹�ȥޡ����ݥꥦ�쥿�饹�ȥޡ������ݥ������顤���ݥ������쥿��������ιŲ��ޤ��Ѥ����Ƥ��벽��ʪ���Ǥ��롥��ʪ���������ˤĤ��ơ��и���Ϳ�ˤ�����LD50�ͤϡ��ޥ�����640��880 mg/kg����åȤ�1140��2100 mg/kg����ӥ���åȤ�400 mg/kg1, 2)���ޤ���in vitro�����Ѱۻ�������DNA����ޥ������ե��������ӥޥ������˻����������������ʬ�θ����������ΰ۾��DZ�������𤵤�Ƥ���3)��ȯ��������Ǥϡ��ޥ�������ӥ�åȤǼ�˴�¡���١������ʤɤˡ��ޤ�����ӡ����븤�������ȯ����������𤬤���3)��ȿ����Ϳ���������������ȯ�������˴ؤ������ϸ�������ʤ���
������4,4'-������ӥ�(2-���������˥��)�ˤĤ��ơ�SD��[Crj:CD(SD)IGS]��åȤ��Ѥ���0��0.4��2��10�����50 mg/kg/day���̤�ȿ���и���Ϳ����������ȯ������ʻ����»ܤ�����ưʪ��1����ͺ��12ɤ�Ȥ����︳ʪ���ϸ��۳���14��������ͺ�ϸ��۽�λ��13����(42����)�����ʬ�ڸ�Ӯ��4��(42��55����)�ޤ����������и���Ϳ������
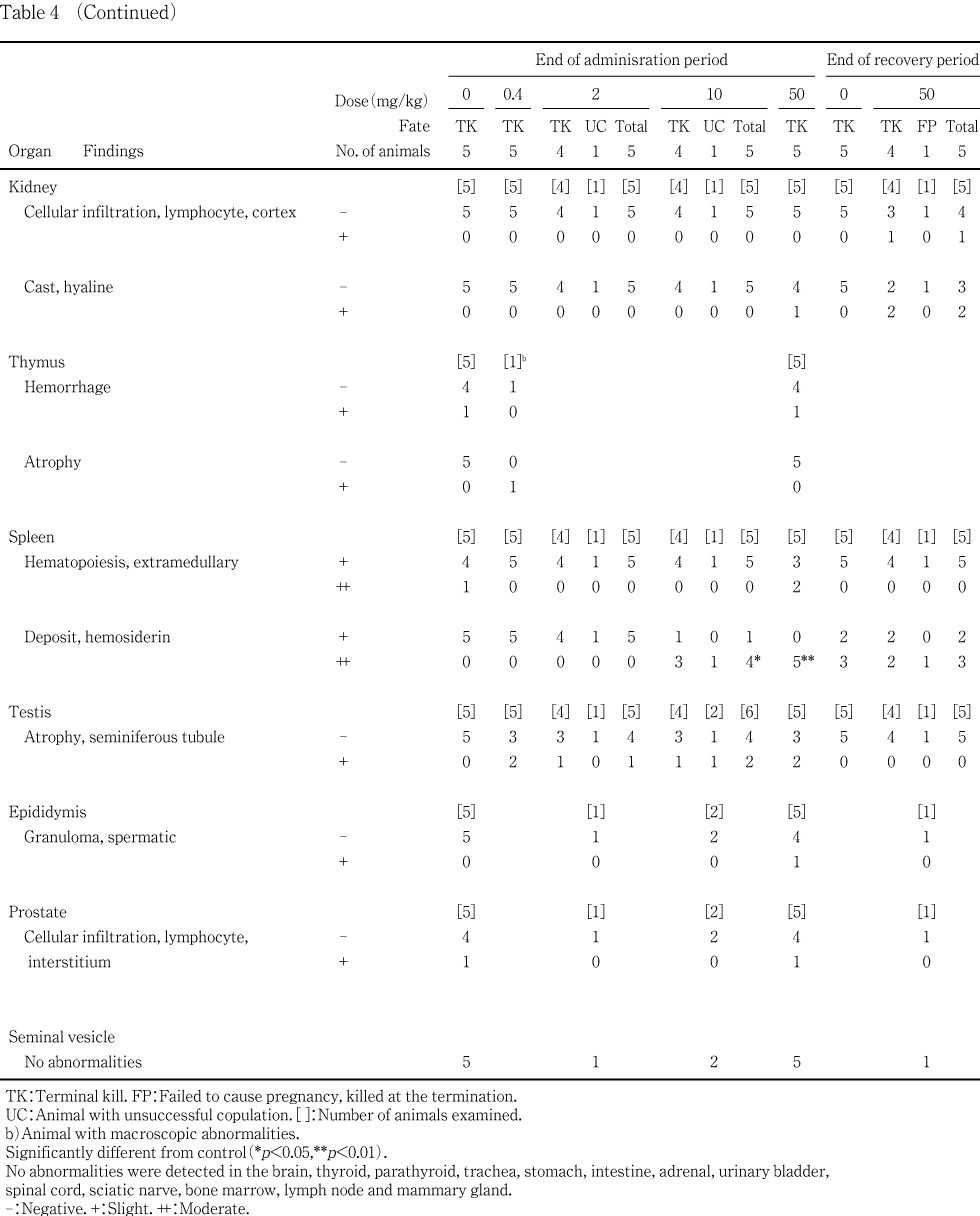
��50 mg/kg���ˤ�����۾���:��ͺ��ή����Ǥ�ǥ������νŤ����ͤ�ǧ���줿����ճظ����ˤ����ƻ�ͺ�ǥ�ȥإ⥰���ӥ�ǻ�٤����ä�����ַ����θ������ߤ�졤ͺ�ˤ����Ʒ쿧��ǻ�٤���ӥإޥȥ���å��ͤθ����¤Ӥ��־��ַ�������ӷ쾮�Ŀ������á���ˤ����Ƥϥϥ���ľ�����ͭ�ַ������ä�ǧ���줿����������ظ����ˤ����ƻ�ͺ��������ѥ�����ӥ���֥ߥ�θ������ߤ�졤ͺ�������쥹�ƥ����롤�ȥꥰ�ꥻ�饤�ɤ����̵���������äΤۤ�����ˤ�LDH�����g-GTP�������¤Ӥ�A/G��θ�����ǧ���줿���ﴱ���̤Ǥ�ͺ�˴�¡�����Ф�������н����¤Ӥ��¡�����н��̤����ä�������¡�����Ф�������н����¤Ӥ˴�¡����¡���þ��������н��̤Τ���������ä�ǧ���졤��¡�ˤ����Ƥ�����Ū�����������������ȿ��ظ����ˤ����ƻ�ͺ�˴κ�˦����(�����濴��)����Ӵκ�˦�λ�������(�����)��ǧ���줿�ۤ���ͺ�Ǥϴκ�˦��ñ��˦����(�濴��)����ӿ�¡�ˤ����빥������Ǣ�ٴɤ����÷������ߤ�졤��ͺ���¡�ˤ�����إ⥸�ǥ�����太��ӿ�¤������÷�����ǧ���줿���������Ѳ��ϡ��������ˤ����ƤϤ����������ʤ����������������ĵ�Ū���Ѳ��Ǥ��ä���
��10 mg/kg���ˤ����Ƥϡ�ͺ�ǿ�¡�ˤ����빥������Ǣ�ٴɤ�����¡�ˤ�����إ⥸�ǥ����������÷���������ǤϷ���������ѥ�����ӥ���֥ߥ�θ����¤Ӥ˿�¡�����н��̤����ä�ǧ���줿��
���ʾ�η�̤��顤4,4'-������ӥ�(2-���������˥��)�Υ�åȤؤ�ȿ����Ϳ�ˤ�ꡤ�����������ΤȤ����¡����¡������ӿ�¡���Ф��Ƥ���Ū�ʱƶ���ޤ��Ѳ���ǧ���줿��̵�ƶ���(NOEL)�ϻ�ͺ�Ȥ�2 mg/kg�ȿ��ꤵ�줿��
����ưʪ��������(��)��������Ω���֡�����Ψ������Ψ��ǥ�����֡����ο����徲Ψ���л�Ψ��ʬ��Ψ��ʬ�ڤ����Ӯ����֤��Ѳ���ǧ����ʤ��ä�����ưʪ���Ф��Ƥ⡤���л��������������������桤����Ψ���νš����֤����Ӯ��4����¸Ψ�ˤ����ơ��︳ʪ������Ϳ�˵��������Ѳ���ǧ����ʤ��ä���
���������äơ���ͺ��ưʪ������ǽ����ӻ�ưʪ��ȯ�����Ф���̵�ƶ��̤ϡ��������50 mg/kg/day�ȷ������줿��
��4,4'-������ӥ�(2-���������˥��)�ϡ�������ϡ������ȥ��DMSO�˰��Ϥ��˾�ʴ���뾽�Ǥ��롥��ˤϡ����ϥ饱�ߥ��빩��(���)��¤�Τ��(���å��ֹ�FG-3002������ 99.76 %)�����ꤷ����Ž�(3��5��)̩���ݴɤ������Ѥ������︳ʪ������Ϳ�դϡ������������[��߷����]�����ޤȤ��ơ��������Ϳ���̤Ȥʤ�ǻ�٤��ϱդ�Ĵ���������ѻ��ޤ���Ž�(3��5��)��̩���ݴɤ���Ĵ����7���ְ���˻��Ѥ������ݴɾ�ﲼ�������Ϳ���֤Ǥ��︳ʪ���ϰ���Ǥ��뤳�Ȥ��ǧ������
�����ܥ��㡼�륹����С�(������)�����������SD��[Crj:CD(SD)IGS]��åȤ�13�����벽�����ֻ��餷�����δ֤˻�ˤĤ��Ƥ�紹������ˤ���������γ�ǧ��Ԥ����۾��ǧ����ʤ�ưʪ�ˤĤ�1����ͺ��12ɤ�Ȥ�����ˤĤ��ƤϤ�����оȷ��Ⱥǹ����̷��β������Ȥ��Ƴ�5ɤ����ʤ�2���α��������ߤ���10����(ͺ335��435 g����198��267 g)�ǻ�˶��������ʤ�����β������ˤĤ��Ƥϸ��ۤ�Ԥ�ʤ��ä���ͺ�β������ˤĤ��Ƥϡ���Ϳ42�����оȷ��Ⱥǹ����̷����椫��̵������ˡ�ˤ�ꤽ�줾��5ɤ�����̤����������Ȥ�������åȤϼ�¬���� 21.2��24.9���¬����47��63 %���������10��ʾ�/��������12����(����7�����7��)�λ��鼼�ǡ����֥�������˸��̤˼��Ƥ����Ƿ�����[���MR���ȥå���������������]����ӿ��ͳ���ݼ褵��������������������ǧ��λ�ϡ��������[�ۥ磻�ȥե졼�������ܥ��㡼�륹����С�]�����줿�ݥꥫ���ܥ͡�������������˼��Ƥ�����
��1����ͺ��1ɤ�Υ�åȤ��︳ʪ����500�����1000 mg/kg��ñ�����и���Ϳ������̡�ξ���̤λ�ͺ�����桦Ǵ�������ȯ��ư�㲼�����۲��⤪����νŸ�����ǧ���줿��1����ͺ��3ɤ�Υ�åȤ�1��3��10��30�����100 mg/kg/day��14����ȿ���и���Ϳ������̡�100 mg/kg���ǡ���ͺ�����桦Ǵ��������ν����ä�������Ǣ�β��������������ַ������쿧���̡��إޥȥ���å��͡�������ѥ�������֥ߥ�A/G�椪��ӥʥȥꥦ������͡��ϥ���ľ�����ͭ�ַ��νи����쾮�Ŀ����ץ��ȥ���ӥ���֡�GOT��GPT��g-GTP���ȥꥰ�ꥻ�饤�ɡ����ӥ��ӥ��ꥦ�ࡤ��¡���̤�����¡���̤ι��ͤΤۤ�����¡������¡�ι������������ͺ���ݱ��̤θ������������LDH�ι��͡����ή��MCV��MCH��MCHC����������ʬ�ȥ���ܥץ饹������֤ι��͡�������ƥ顼�������ͤ�ǧ���줿��
���ʾ�η�̤��顤�ܻ�ˤ�������Ϳ�̤�50 mg/ kg/ day��ǹ����̤Ȥ����ʲ�10��2�����0.4 mg/kg�η�4���̤����ꤷ������Ϳ��ˡ�ϡ���Ϳ���̤��ν�100 g������0.5 mL�Ȥ����ƥե������ߥ���Ǥ����夷�����������Ѥ���1��1���۳���14��������ͺ��˶�������ޤǤ�42���֡���Ǥ�ʬ�ڸ��Ӯ��4��(42��55����)�ޤǡ����������и���Ϳ�������оȷ��ˤϡ��︳ʪ�������ޤȤ����Ѥ����������������Ʊ�ͤ���Ϳ������
����Ϳ���֤���Ӥ����³��14���֤β������֤��̤��ơ�ưʪ�����ࡤ���ѡ���ư���������ѻ�������
����Ϳ������������Ӥ��θ�Ͻ�1��ưʪ�ݥ�������Ф�������ӥ��������Υ�����������ץ�ե������(370 W��560D��40Hmm)�ǡ�����������νФ��פ�������������Ф����ΰ����פ����ζ���ĥ(�дˡ���ľ)������(��)�����¤ߡ�Ω�ӡ���ʬ��ʪ�������ĺ����֡�����ͽС�ή�ޡ���ɡʬ��ʪ(����)��ή����ʢ�����Ӥ�Ǣ�ˤ����졤������Ϥ��ؤˤ����졤ȯ�����Ƶۡ���������ڻ�����õ����ư(������)���ٲ�������ȯ��ư(��ư��)�����(����)���۾��ư(������������������)����Ʊ(���٤���������ȿ������ư��)���ռ�����(���¡�������ץ���������)���ͻ�ڶ�ĥ�١���Ǣ�������ʵ��29���ܤˤĤ��ƴѻ�������
��ͺ�Ϻǽ���Ϳ�������Ӯ��������1�ޤ��������λ�ͺ�Ϻǽ���Ϳ������Ӳ������ֽ�λ���ˡ�İ��ȿ�������ȿ��������ȿ��������ȿ�͡��˳�ȿ����Ʒ��ȿ�͡�Ʊ¦����ȿ�͡�����ȿ�ͤ��������ȿ�ͤ�Ĵ�٤���
��ͺ����Ϳ41�������Ӯ��������1�ޤ��������λ�ͺ�Ϻǽ���Ϳ������Ӳ���13���ˡ�ͺ��30ʬ�֤����60ʬ�֡����30ʬ�֤μ�ȯ��ư��(��ȯ��ư��¬�����֡�SUPERMEX����Į����)�����褪��Ӹ��ΰ���(��åȡ��ޥ����Ѱ���¬�����֡�MK-380R/FR����Į����)�¤Ӥ����ϳ�������¬�ꤷ�����������λ�μ�ȯ��ư�̤ϡ�60ʬ��¬�ꤷ����
���νŤ�¬���, ��Ϳ������(��Ϳ����ľ��)����Ӥ��θ��7���ֳ֤ǹԤ�������˺ǽ���Ϳ�����˻�����¬�ꤷ���������������ǥ����ϡ�ǥ�� 0��7��14 ����� 20����Ӯ��0�����4����¬�ꤷ�����ޤ����������ˤĤ��Ƥϲ���7�����14���ˤ�¬�ꤷ�����ݱ��̤ϡ��ν�¬�����˹�碌�������ޤǤ�24���֤λ��������̤�¬�ꤷ�����ݱ��̤κǽ�¬�����ϡ�ͺ�Ǥ���Ϳ41������Ǥ�Ӯ��3�����������Ǥϲ���13���Ȥ�����
����ˤĤ��ơ��벽�����ִ��֤˰���³������������ǧ�����ޤǡ�Giemsa�����ˤ��紹�����ɸ�ܤ�������������ˤ���������ʳ���Ƚ���Ԥä���ʿ���������ϡ��Ѳ���˦�Τߤ����ߤޤ��Ͻ������ˤߤ���ȯ������������������ʿ���ͤȤ�����
����Ϳ15���θ��ˡ�ͺ�Υ�������Ʊ�췲��λ������(1��1)����������ǧ�����ޤ�14���֤���٤Ȥ���Ϣ³Ʊ�蘆�����������γ�ǧ����ī�������˹Ԥ������������뤤��紹�������Ҥ���ǧ���줿����ǥ��0���Ȥ�����ʬ�ھ��֤δѻ���Ʊ������˹Ԥ���1ʢ���Ȥ�ʬ�ڤν�λ����ǧ���줿����Ӯ��0���Ȥ��������ۤ����ʬ�ڤδѻ���̤��顤�Ʒ��ˤĤ��Ƹ���Ψ[(������Ωưʪ��/Ʊ��ưʪ��)��100]������Ψ[(���ۻ��/������Ω���)��100]����ӽл�Ψ[(�����л����/��¸���ۻ��)��100]�ʤ�Ӥ�ʬ�ڤ���ǧ���줿��ˤĤ���ǥ������(ǥ��0������ʬ�ڤ���ǧ���줿���ޤǤ�����)���ꤷ����
��ͺ�ˤĤ��ơ���Ϳ40������Ӳ������ˤĤ��Ƥϲ���8���ˡ�ưʪ����3������ե������˼��Ƥ�������줿Ǣ�ˤĤ��ơ����Ѥδѻ������ˡ(�ޥ�ƥ����ƥ��å������Х����롦����)�ˤ��pH�����졤����ѥ����������ȥ��Ρ��ӥ��ӥ�ӥ����ӥ�Ρ����������Ū�����¤Ӥ����֤θ���(URI-CELL�ա�����֥�å����ߥ���ץ������ȼҡ����������ƶ���)��Ԥä�������ˡ�18���ּ��Ƥ�������줿Ǣ�ˤĤ��ơ�Ǣ��, ���(���ס��������)���ʥȥꥦ�प��ӥ��ꥦ��(�Ų����ưʬ�����֡�NAKL-132���찡���ȹ���)��¬�ꤷ����
���ǽ���Ϳ���������뤤�ϲ������ֽ�λ�������β�˶ľ���ˡ������ƥ���첼�dz�ʢ����ʢ��ư̮���η줷����ưʪ�������θ��5�������¤�����Τߤ�ͳ��Ϳ�������μ褷����դ�3ʬ�䤷�����ΰ�����EDTA-2 K�ǶŸ��˻߽�������¿���ܼ�ư��������(E-4000���찡�����Ż�)�ˤ�ꡤ�ַ���(�ŵ���������)���쿧����(�饦���β���ʥȥꥦ��-�إ⥰���ӥ�ˡ)���إޥȥ���å���(�ѥ륹��������)��ʿ���ַ������(MCV)��ʿ���ַ��쿧����(MCH)��ʿ���ַ��쿧��ǻ��(MCHC���ʾ塤����)�����������ӷ쾮�Ŀ�(�ʾ塤�ŵ���������)�ޤ�����ɸ�ܤ���������־��ַ���(Brilliant cresyl blue �������ƶ���)���ϥ���ľ�����ͭ�ַ���(Neutral red brilliant green �������ƶ���)���������ɴʬΨ(May-Giemsa�������ƶ���)����˥�ȥإ⥰���ӥ�ǻ��(Evelyn- Malloy��ˡ)��¬�ꤷ�����ޤ�����դΰ�����3.8 %��������ʥȥꥦ��դǶŸ��˻߽������Ʒ�����������նŸǼ�ư¬������(KC-10 A���ƹ���)�ˤ�ꡤ�ץ��ȥ���ӥ����(Quick����ˡ)����ӳ�������ʬ�ȥ���ܥץ饹�������(APTT������¥��������ˡ)��¬�ꤷ����
���μ褷����դΰ������������ʬΥ���������ؼ�ưʬ������(JCA-BM8������ʥ饤�����������Ż�)�ˤ�ꡤ������ѥ�(Biuretˡ)������֥ߥ�(BCGˡ)��A/G ��(����)�������������쥹�ƥ����롤�ȥꥰ�ꥻ�饤��(�ʾ塤����ˡ)�����ӥ��ӥ�(������ˡ)��Ǣ������(Urease-UVˡ)�����쥢���˥�(Jaffeˡ)��GOT��GPT��g-GTP��ALP(�ʾ塤JSCCˡ)��LDH(SFBCˡ)��������ƥ顼��(BTC-DNTBˡ)�����륷����(OCPCˡ)�����̵�����(����ˡ)�ޤ��Ų����ưʬ������(NAKL-132���찡���ȹ���)�ˤ�ꡤ�ʥȥꥦ�ࡤ���ꥦ�प��ӱ���(�ʾ塤�������Ŷ�ˡ)��¬�ꤷ����
��ͺ�ηײ��˻�ưʪ����Ϳ42������������Ǥ�ʬ�ڤ�Ӯ����Ĵ�Ǥ��ä����Ӯ��5���ˡ���������Ω���ʤ��ä���ϸ��۴��ֽ�λ��24��(��Ϳ52��������)�ˡ���������Ω������ʬ��ͽ���4����ޤ�ʬ�ڤ�ǧ����ʤ��ä���Ϥ��������ˡ��ޤ�, �������ˤĤ��Ƥϲ���14���������ˡ�������⥨�ݥƥ���첼�������˻�������ɽ��������Ǵ�줪����������ﴱ������Ū�˴ѻ��������ޤ����Ʒ���ͺ��5ɤ�δ�¡����¡�����ա��������¡��Ǿ����¡�������Ρ��þ����Τۤ������Ƥ�ͺ����ǹ�¤Ӥ����Ƥ�ͺ�����㤪���������Τ�����(���н���)�����˻������νŤ˴�Ť������ν���(���н���)�Ф�������ˤĤ��Ƥϡ�����β��ο�����ӻҵܤ��徲����Ĵ�١��徲Ψ(%)[(�徲��/���ο�)��100]�Ф�����
������ˤĤ���Ǿ�������Ρ��þ��������������ɡ���(����դ������忻��)���ߡ�IJ����¡����¡���¡����¡�����ա���������㡤������Ρ���Ω������ǹ�����㡤�ҵܡ��Կ�(����������������)���������С�����(���ܹ�)��������(���������ᡤIJ���������)������������¾����Ū�۾����̤�μ褷��10 %���������˾ץۥ�ޥ���(���㡤������Τϥ֥���դ�������)�ˤƸ��ꤷ��¸�����������ȿ��ظ����ϡ��оȷ������50 mg/kg���λ�ͺ��5ɤ�Τ������¸�ﴱ�ˤĤ��Ƽ»ܤ���������ˤĤ��Ƥϡ����ҷ����������븡��(���ơ����������������������=)��»ܤ�����50 mg/kg����ͺ���︳ʪ������Ϳ�ˤ��ƶ����ߤ�줿��¡������¡�ˤĤ�����������ޤऽ��¾�η��λ�ͺ�ˤ����Ƹ�������������ˡ�ͺ�ˤ����ƤϿ�¡���������������ˤĤ��Ƥϴﴱ���̤��Ѳ���ǧ���줿��ο�¡�ˤĤ��Ƥ⸡���������Ʒ�������Ū�۾����̤˴ؤ��Ƥ�����ˤĤ��Ƹ����������ޤ�����������Ω�λ�ͺ����Ӹ�������Ω������ʬ��ͽ���4����ޤ�ʬ�ڤ�ǧ����ʤ��ä���ˤĤ��Ƥϡ�ͺ�Ǥ����㡤������Ρ���Ω���������ǹ��Ǥ����㡤�ҵܤ���Ӳ����Τ������������ȿ���Ū�����ϡ���ˡ�˽��äƥѥ�ե������Ҥ��������H-E������ܤ��ƶ����������ޤ����¡�Ͽ�������ʪ��Ʊ�ꤹ�뤿�ᡤ����ˤĤ���Ŵ(�٥���֥롼)�������оȷ������50 mg/kg����ͺ�γ�2ɤ�ο�¡�ˤĤ��Ƥ�PAS������Ԥä���
��ʬ�ڴ�λ�γ�ǧ�塤��ʢ�λ�����(�������Ȼ�˴���ι��)��Ĵ�١�ʬ��Ψ[(���л�����/�徲��)��100]�ޤ�������������͵���Ĺû�ˤ�����̤�Ƚ�ꤷ, �����Ȥ�����Ф������������ˤĤ��Ƥϡ��������ޤɽ�ΰ۾��ѻ�������
���������̾��֤����������ǧ��������Ψ[(�л���ǧ��������/���л�����)��100]����ӿ�������¸Ψ[(Ӯ��4��������/�л���ǧ��������)��100]�����
���������ˤĤ���Ӯ��0�������4���˻�ͺ�̤˳�ʢ���Ȥ����νŤ�¬�ꤷ��1ɤ�������ʿ���νŤФ���.
����˴��Ϥ������١���¸���Ӯ��4���˥����ƥ���첼������व�������������ʢ���ˤ�������״ﴱ������Ū�˴ѻ�������
������줿ʿ���ͤ��뤤�����٤ˤĤ��ơ��оȷ��Ȥ�ͭ�պ�(����Ψ5 %�ʲ�)������Ū�ǡ�������ӥѥ��ȥ�å��ǡ����ˤĤ��ơ������3���ʾ�ξ�硤Bartlett��ʬ�������Ԥ�, ʬ�������ͤʾ��ϰ층���֤�ʬ��ʬ�Ϥ�Ԥä���ʬ�������ͤǤʤ���礪��ӥΥ�ѥ��ȥ�å��ǡ����ϡ�Kruskal-Wallis�ν�̸����Ԥä��������η��ͭ�պ���ǧ���硤Dunnett�ʤ���Dunnett���θ���ˡ�ˤ��¿����Ӥ�Ԥä��������2���֤ξ��ϡ��ѥ��ȥ�å��ǡ����ˤĤ���F�����Ԥ������η��ʬ�������ͤʾ���Student��t�����ʬ�������ͤǤʤ�����Aspin-Welch��t�����Ԥä����ޤ����Υ�ѥ��ȥ�å��ǡ����ϡ�Mann-Whitney��U�����Ԥä������ƥ��ꥫ��ǡ����ˤĤ��Ƥϡ�Fisher��ľ�ܳ�Ψˡ���Ѥ��Ƹ��ꤷ�����ʤ����������˴ؤ���ǡ����ϡ�1ʢ��1ɸ�ܤȤ�����
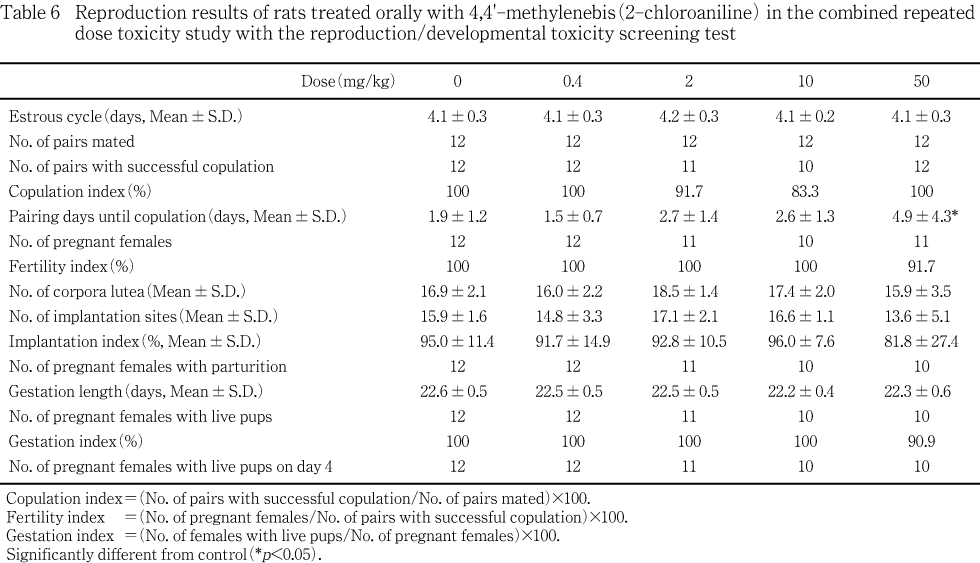
����Ϳ������ˤ����ơ�ή��50 mg/kg������Ϳ8���ʹߤ˳�12ɤ��ͺ��6��Ȼ��3���ǧ���줿����α�������50 mg/kg���ˤ�5ɤ��3���ή��ǧ���줿��ή�ϳ�����Ϳ��10ʬ����30ʬ�δ֤�ǧ���졤��Ϳľ�夫��ǧ�������⤢�ä����������֤ˤ����Ƥϡ����̾��֤��Ѳ���ǧ����ʤ��ä�����˴��ϡ���Ϳ�����椪��Ӳ�����������̤���ǧ����ʤ��ä���
����Ϳ������Ϳ�����椪��Ӳ���������γƻ����δѻ����̤��ơ��õ����٤��۾�긫��ǧ����ʤ��ä���
����Ϳ6������Ӳ���2���Ǥθ����ˤ����ơ��۾�긫��ǧ����ʤ��ä���
����Ϳ6������Ӳ���2���Ǥθ����ˤ����ơ��۾�긫��ǧ����ʤ��ä���
����Ϳ������ˤ����ơ�50 mg/kg���ǻ��ǥ��14�������20�����νŤ�ͭ�դ����ͤ�ǧ���졤ǥ����������ν������̤����ͷ����ˤ��ä���Ʊ���λ��Ӯ��0�������4�����νŤ��оȷ���뷹���ˤ��ä��������δ֤��ν������̤ˤ����Ƥ��оȷ�����ٺ���ǧ����ʤ��ä�����α������Ǥϡ��оȷ����䲼��äƿ�ܤ��뷹���ˤ��ä���ΤΡ�ͭ�դ���ư�ǤϤʤ��ä���ͺ�Ǥϡ��νŤ�����ν������̤��Ѳ���ǧ��ʤ��ä����������֤ˤ����Ƥϡ���ͺ���˳�¬��������νŤ�����ν������̤�ͭ�դ���ư��ǧ��ʤ��ä���
����Ϳ������ˤ����ơ��ݱ��̤�ͭ�դ����ͤ���50 mg/kg ��ͺ����Ϳ1����ǧ���줿���ʤ�����α������ǡ��ݱ��̤���Ϳ14�������42����ͭ�դʹ��ͤ��������ݱ��̤ηл�Ū��ܤ���ߤơ������������оȷ����ݱ��̤�¾��¬��������٤����ͤ�������ǡ��︳ʪ������Ϳ�ˤ��ƶ������������褦����ư�ǤϤʤ���Ƚ�Ǥ��줿������������ˤ����Ƥϡ�ͭ�դ���ư��ǧ����ʤ��ä���
����Ϳ�����椪��Ӳ���������θ����ˤ����ơ��Ƹ������ܤ�ͭ�դʰ۾�긫��ǧ����ʤ��ä���
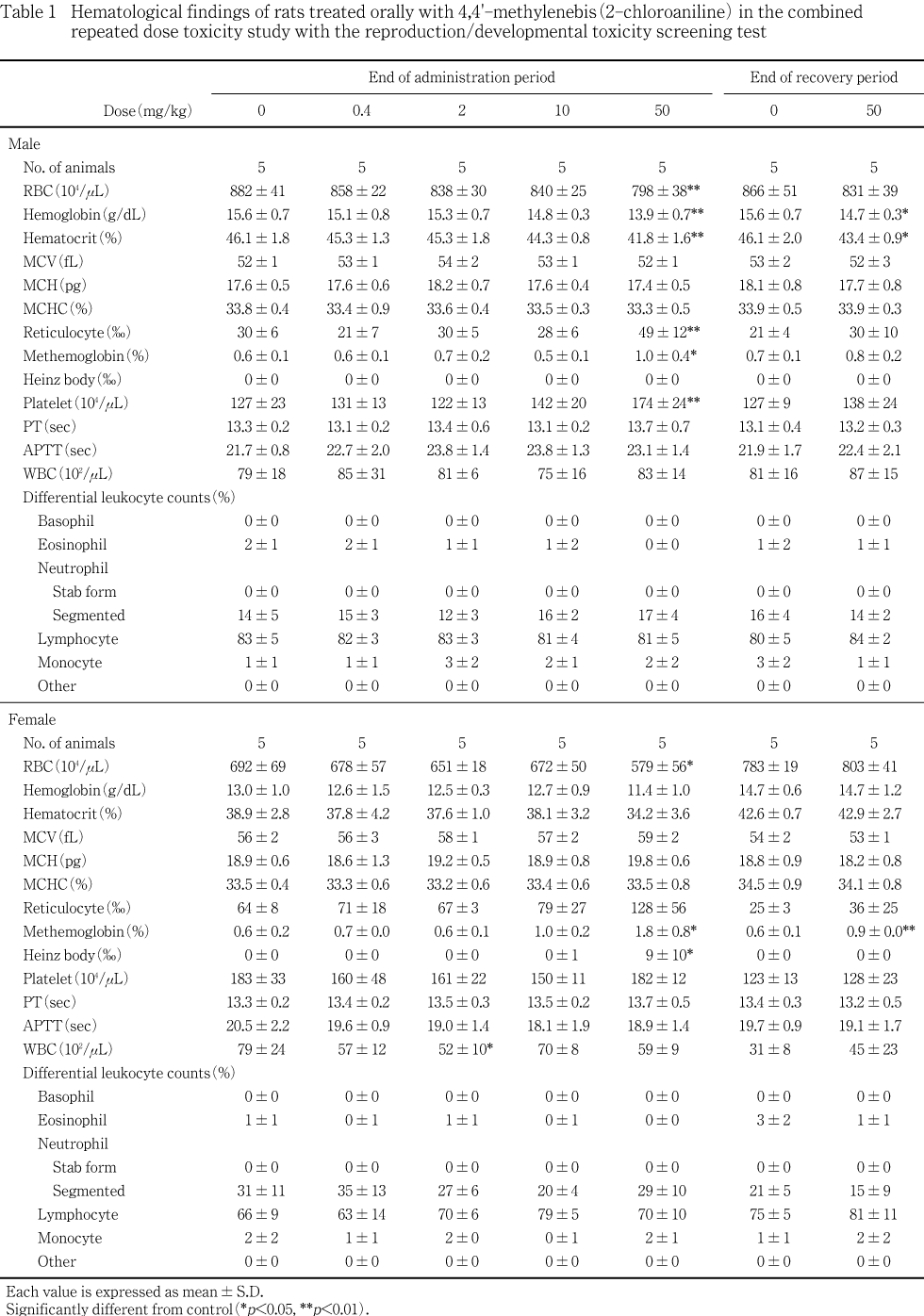
����Ϳ���ֽ�λ���θ����ˤ����ơ�50 mg/kg���ǻ�ͺ���ַ�����ͭ�դʸ�������ӥ�ȥإ⥰���ӥ�ǻ�٤�ͭ�դ����á������ͺ�ˤϷ쿧��ǻ�٤���ӥإޥȥ���å��ͤ�ͭ�դʸ����¤Ӥ��־��ַ�������ӷ쾮�Ŀ���ͭ�դ����á���ˤϥϥ���ľ�����ͭ�ַ���ͭ�դ����ä�ǧ���줿���ޤ����쿧��ǻ�٤���ӥإޥȥ���å��ͤ����ͷ����¤Ӥ��־��ַ����ι��ͷ����ϡ�50 mg/kg���λ�ˤ�ǧ���줿���ʤ���2 mg/kg���λ���������ͭ�դ����ͤ������Ѳ��������������ǧ���줺���ޤ��طʥǡ����ˤ����������ϰ�(38��113��10^2/��L)���ͤǤ��ä����Ȥ��顤�︳ʪ������Ϳ�Ȥ�̵�ط��ʽ긫��Ƚ�Ǥ��줿���������ֽ�λ���θ����ˤ����Ƥϡ�ͺ�η쿧��ǻ�٤���ӥإޥȥ���å��ͤ�ͭ�պ����Ĥ��Τ��Ѳ������٤Ϸڸ���������¾���Ѳ���ǧ����ʤ��ä����ʤ�����Υ�ȥإ⥰���ӥ�ǻ�٤��оȷ�����٤Ƥ����ͤ�ͭ�պ���ǧ���줿�������ϰ�(0.2��1.0 %)���ͤǤ��ä���
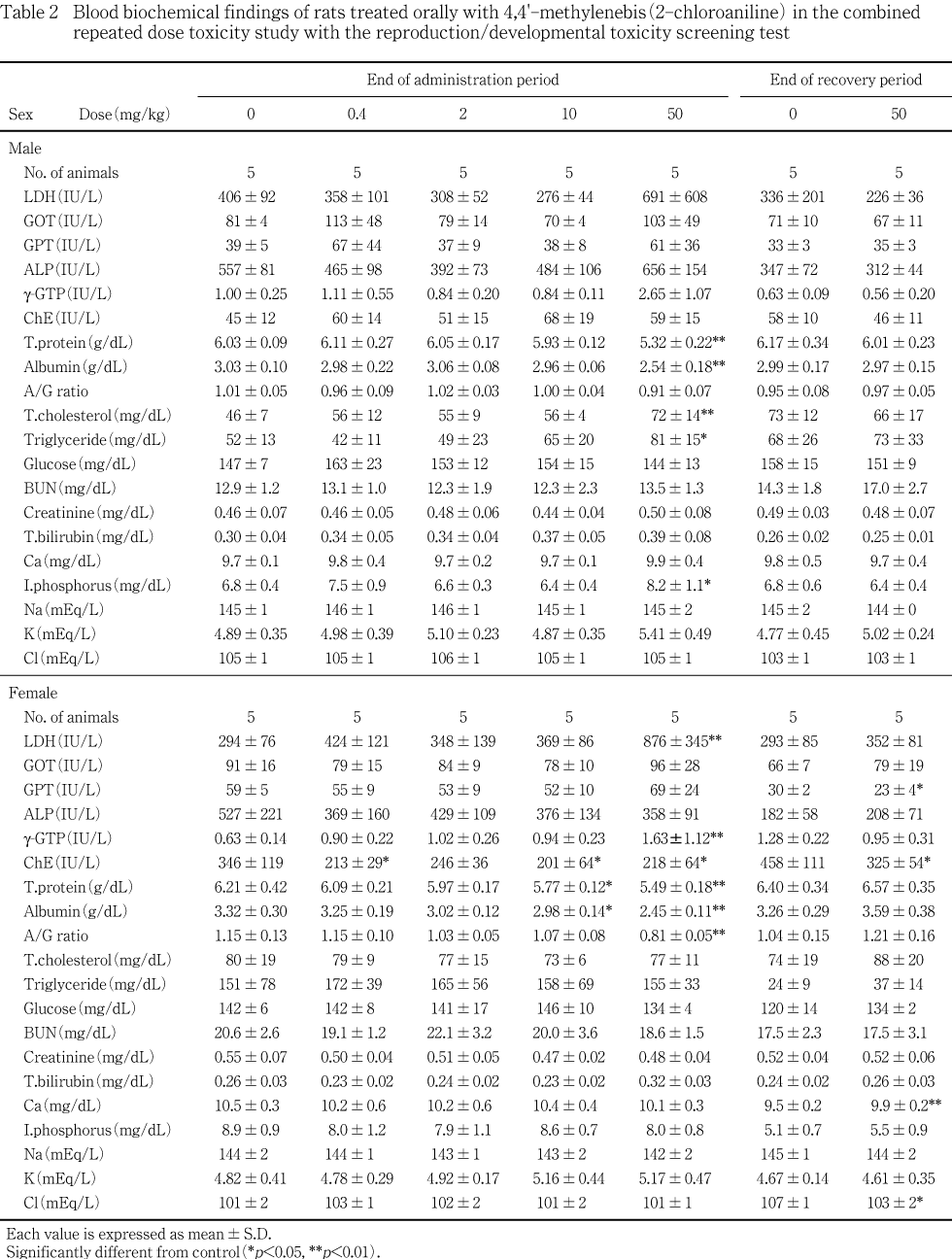
����Ϳ���ֽ�λ���θ����ˤ����ơ�50 mg/kg����ͺ�Ǥ�������ѥ�����ӥ���֥ߥ��ͭ�դʸ�������ͺ��ǧ���졤A/G��Ǥϻ��ͭ�դ�����, ͺ�����ͷ�������������ˡ�ͺ�Ǥ������쥹�ƥ����롤�ȥꥰ�ꥻ�饤�ɤ����̵�����Ǥ�LDH �����g-GTP�Τ������ͭ�դ����ä�ǧ���졤ͺ��LDH �����g-GTP����ͷ����ˤ��ä����ޤ�����ͺ�Ȥ⥫�ꥦ��Ϲ��ͷ����ˤ��ä����ʤ����︳ʪ����Ϳ�Ʒ��λ�Υ�����ƥ顼�����оȷ�����٤�����Ū�����ͷ����ˤ��ꡤ0.4��10 �����50 mg/kg����ͭ�պ����ߤ�줿���Ѳ���������������ʤ�����������طʥǡ����ˤ����������ϰ�(157��519 IU/L)����ͤǤ��ä����Ȥ��顤�︳ʪ������Ϳ�Ȥ�̵�ط��ʽ긫��Ƚ�Ǥ��줿���������ֽ�λ���θ����ˤ����Ƥϡ��Ƹ������ܤ������ϰϤ��æ����۾��ͤϤߤ��ʤ��ä���
��10 mg/kg���ǻ��������ѥ�����ӥ���֥ߥ��ͭ�դʸ�����ǧ���줿��
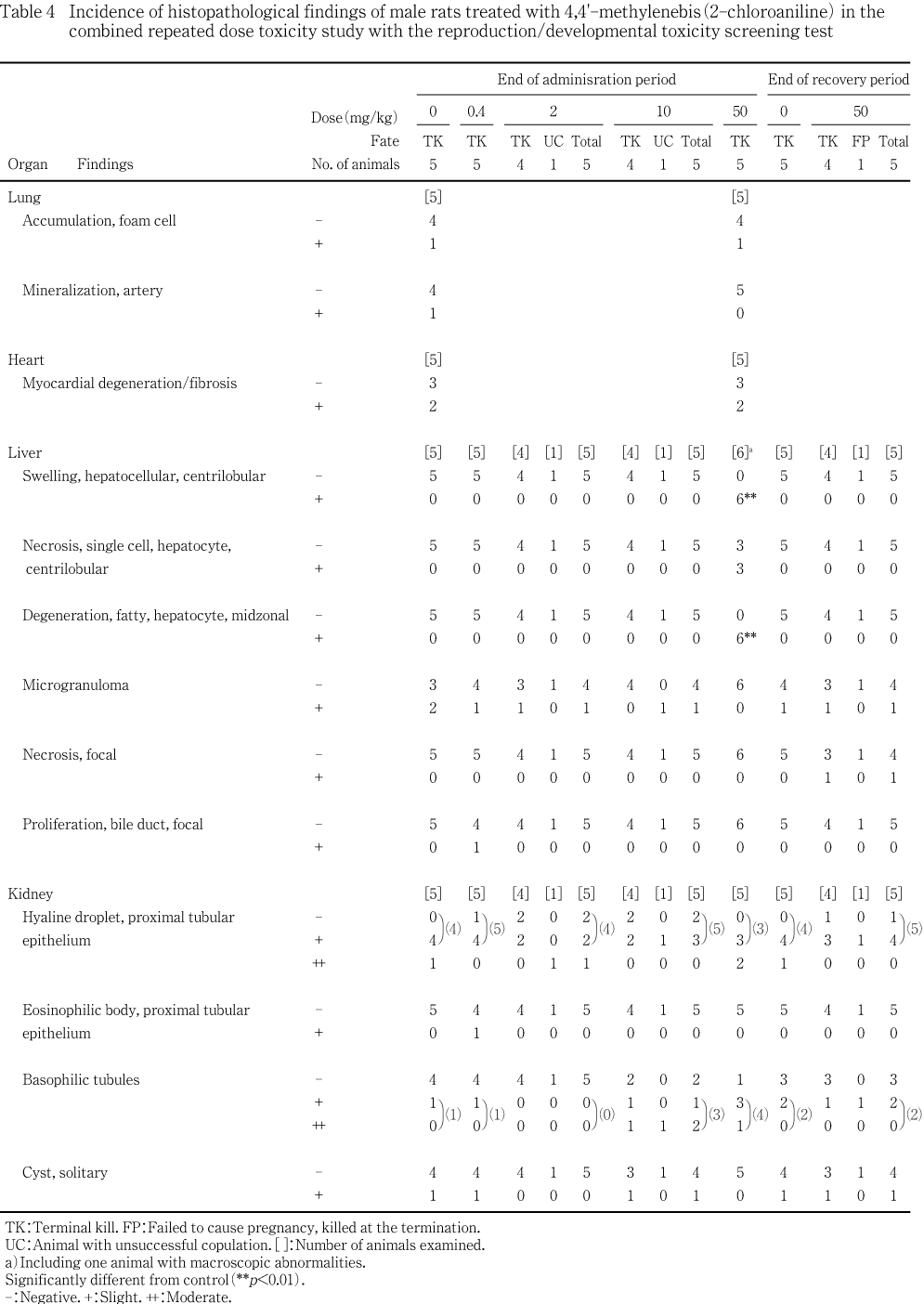
����Ϳ���ֽ�λ�����˻�����ưʪ�Τ�����ǥ������Ω������ͺ�ˤ����ơ���¡��������50 mg/kg���Ǥ�7ɤ��6���ǧ���졤��3��Ǥϴ�¡���緿����ǧ���줿��ʬ�ڤ���Ӯ����Ĵ�Ǥ��ä���ˤ����Ƥ⡤��¡��������50 mg/kg����10ɤ��6���ǧ���졤2��Ǥ��緿����ǧ���줿��50 mg/kg���λ�ͺ�δ�¡��������ȯ��Ψ�ˤϡ��оȷ�����٤�ͭ�պ���ǧ���줿�� 50 mg/kg����ǧ���줿ǥ������Ω��1�ФǤϻ�ͺ�˰۾��ǧ���줺��Ʊ���μ��۸��ۻ���˴(�ҵ���˿����ۻ�1ɤ�Τ�ǧ���줿)��ǧ���줿1��Ǥϴ�¡��������ǧ���줿��������¾�δﴱ�˰۾��ǧ����ʤ��ä�����������Ω���ФǤϡ�10 mg/kg����1�Фλ�λҵܤ˽��٤ʻҵܹп��ǧ���줿����2 mg/kg����1�Ф����10 mg/kg����¾��1�ФǤϻ�ͺ�Ȥ�۾��ǧ����ʤ��ä����������ֽ�λ�����˻�ưʪ�ˤ����Ƥϡ���¡���Ѳ���ǧ����ʤ��ä����ʤ����︳ʪ������Ϳ�Ȥ�̵�ط��ˡ������ξ�������0.4 mg/kg����ͺ��1�㡤�������ֿ��褬Ʊ���λ��1�㡤����ξ�������50 mg/kg����ǥ����Ω��ͺ��1�㡤�¤Ӥ˺�¦��¡���礭�����50 mg/kg���β������λ��1���ǧ���줿��

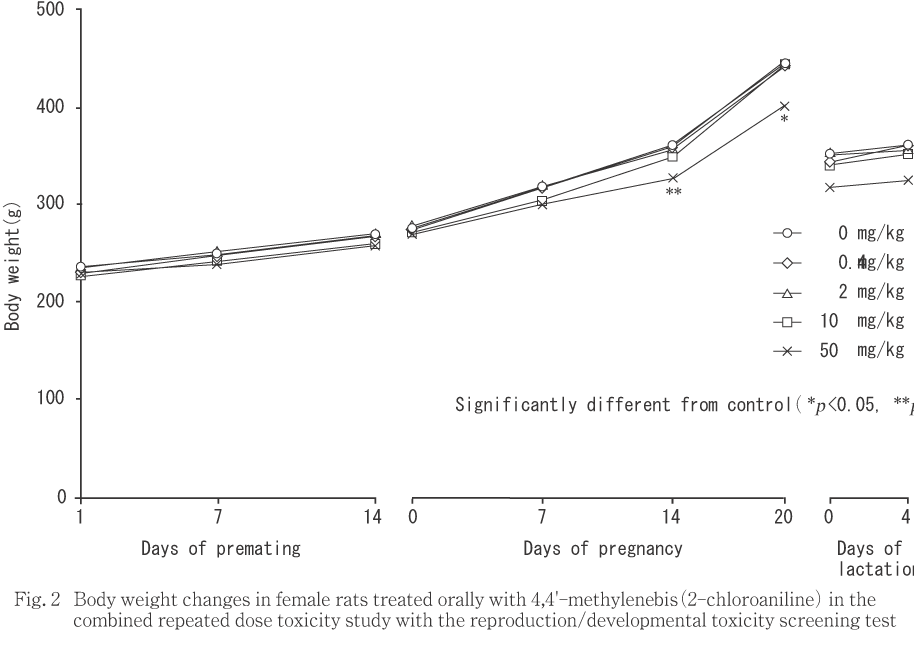
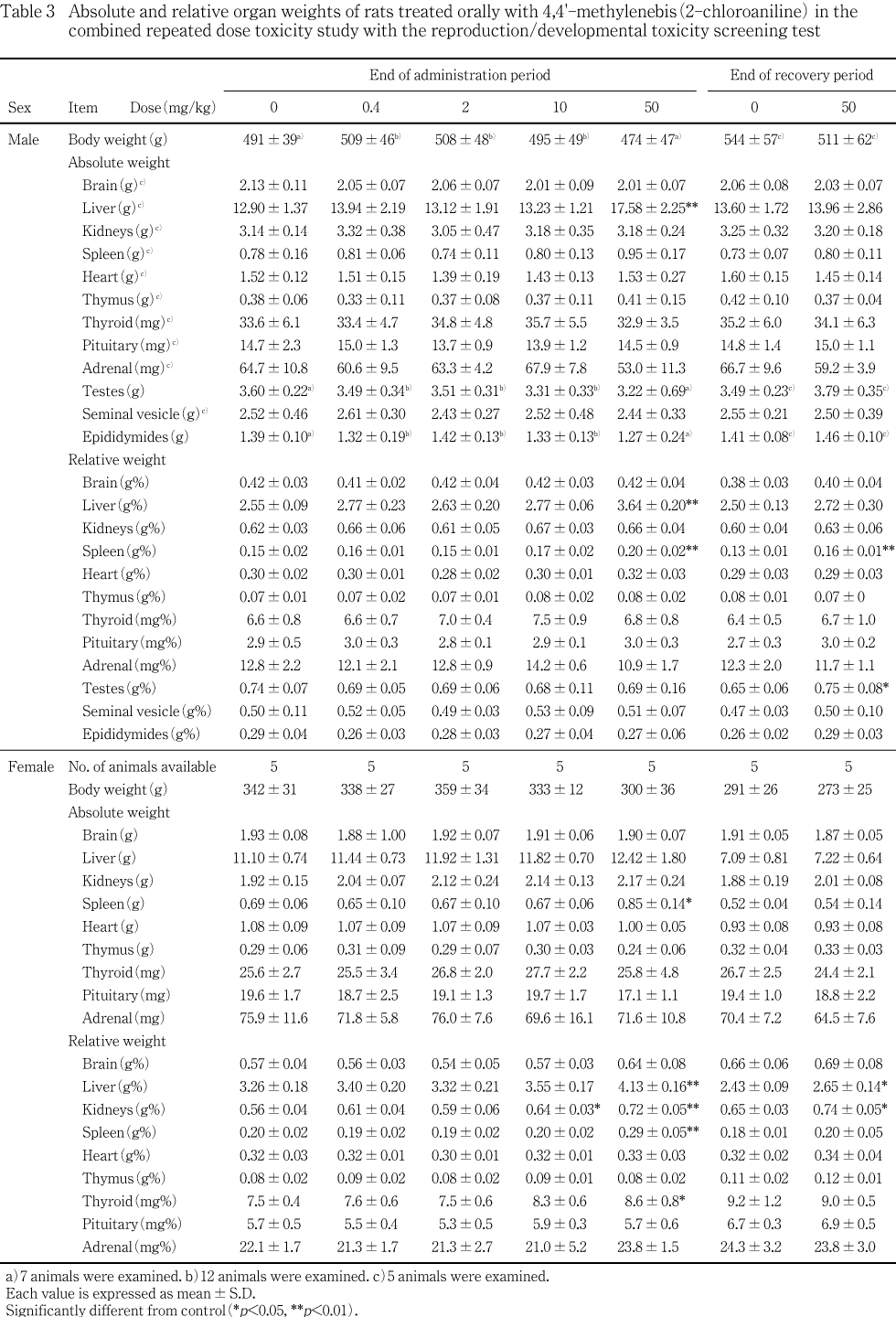
����Ϳ���ֽ�λ���˻�ưʪ�Τ�����50 mg/kg���Ǥϻ�˿�¡�����н��̤�ͭ�դ����ä�ǧ���줿¾��ͺ�Ǥϴ�¡�����Ф�������н����¤Ӥ��¡�����н��̤�����Ǥϴ�¡����ӹþ��������н��̤Τۤ����¡�����Ф�������н��̤�ͭ�դ����ä������������ֽ�λ�����˻�ưʪ�ˤ����Ƥϡ�ͺ���¡������Ǵ�¡����ӿ�¡�����н��̤�ͭ�պ����Ĥä������Ѳ������٤Ϸڸ����뷹���ˤ��ꡤͺ�δ�¡������¡����ӹþ����ˤ��Ѳ���ǧ����ʤ��ä����ʤ����������ֽ�λ�����˻�ưʪ�ˤ�����ͺ����������н��̤�ͭ�դʹ��ͤ�ǧ���줿���ޤ���10 mg/kg���ǻ�˿�¡�����н��̤�ͭ�դ����ä�ǧ���줿��
���︳ʪ������Ϳ�ȴ�Ϣ����Ȼפ����Ѳ�������¡���¡����ӿ�¡��ǧ���줿��
��50 mg/kg ���ǡ��κ�˦�μ���(�����濴��)����ӻ�������(�����)����ħ�Ȥ����Ѳ���ͺ��6ɤ��6�㤪��ӻ��8ɤ��6���ǧ���줿�������Τ���ͺ��3��Ǥϡ������濴���κ�˦��ñ��˦�����ǧ���줿����Ǥϡ������ʳ��ˡ����������Τߤ����餫��1�㤬ǧ���줿����ͺ�δκ�˦�μ��礪��ӻ���������ȯ��Ψ�ˤϡ��оȷ�����٤�ͭ�պ���ǧ���줿���������ǤϤ��Τ褦���Ѳ���ǧ����ʤ��ä����������Ѳ��ʳ��ˡ��︳ʪ������Ϳ�Ȥ�̵�ط��ˡ���������𤬳Ʒ��ˡ�������ब2 mg/kg���λ��1�㤪���50 mg/kg���β�������ͺ��1��ˡ��¶�������������0.4 mg/kg����ͺ��1���ǧ���줿��
��ͺ�ˤ����ơ����٤ʹ�������Ǣ�ٴɤ����Ʒ�5ɤ�桤50 mg/kg���Ǥ�4�㡤10 mg/kg���Ǥ�3��ǧ���졤ȯ��Ψ�����÷�����ǧ���줿�ۤ����Ѳ������٤��������뷹���ˤ��ä������������оȷ��ˤ����Ƥ�1���ǧ���줿����ˤϡ���������Ǣ�ٴɤ����÷�����ǧ����ʤ��ä����������Ǥϡ�ͺ�ι�������Ǣ�ٴɤ�ȯ��Ψ���оȷ��Ⱥ���ǧ����ʤ��ä����������Ѳ��ʳ��ˡ��︳ʪ������Ϳ�Ȥ�̵�ط��Ȼפ����Ѳ��Ȥ��ơ����Ǣ�ٴɾ���ξ˻�ũ���Ʒ���ͺ������ʬ�ˡ���Ω��ǹ˦�����������ѵ忻��Ʒ��λ�ͺ�˻�ȯŪ�ˡ��ޤ���50 mg/kg���Ǿ˻ұ��줬ͺ��1��ˡ��ղ�𤬲������λ��1��ߤ�줿�ۤ������Ǣ�ٴɾ���ι��������Τ�0.4 mg/kg����ͺ��1���ǧ���줿��
���¡����磿�ˤ�����إ⥸�ǥ������ϡ��оȷ��ˤ����Ƥ��ͺ����˷��٤�ǧ���줿����50 mg/kg����ͺ��5�㤪��ӻ��4��ˤ������٤����夬ǧ���줿�ۤ���10 mg/kg����ͺ�ˤ����Ƥ�4���ǧ���졤����������������ȯ��Ψ��ͭ�դǤ��ä����ޤ��������磿�ˤ������¤��ϡ�50 mg/kg���Ǥ�4��������٤ο�¤���ж�ʷ�����ǧ���줿�����оȷ��Ǥ�1�㤬�����٤Ǥ��ä��ۤ��Ϸ��٤Ǥ��ä����������Ǥϡ���Υإ⥸�ǥ����������÷������Ĥä�����ͭ�պ���ǧ���줺��ͺ�ˤ����Ƥϥإ⥸�ǥ�����太��ӿ�¤���ȯ�����оȷ��Ȥδ֤˺��Ϥߤ��ʤ��ä���
���оȷ������50 mg/kg���λ�ͺ�ʤ����Ϥ��Τ����줫�ˡ��٤�ˢ����˦���Ȥ����ư̮�ɹۼ����塤��¡�ο������������ݲ��������νз�ʤɤ�ǧ���줿�������������١����ġ���ȯŪ���Ѳ��Ǥ��ä����ޤ���˶�������︳ʪ������Ϳ�Ȥ�̵�ط��ν긫�Ȥ��ơ�0.4 mg/kg����ͺ��1��ξ��������������Ǥ϶����ΰ�̤���Ʊ���λ��1�㤪���50 mg/kg����ͺ��1��ˤߤ�줿�������ֿ���ˤϽз줬ǧ���줿��
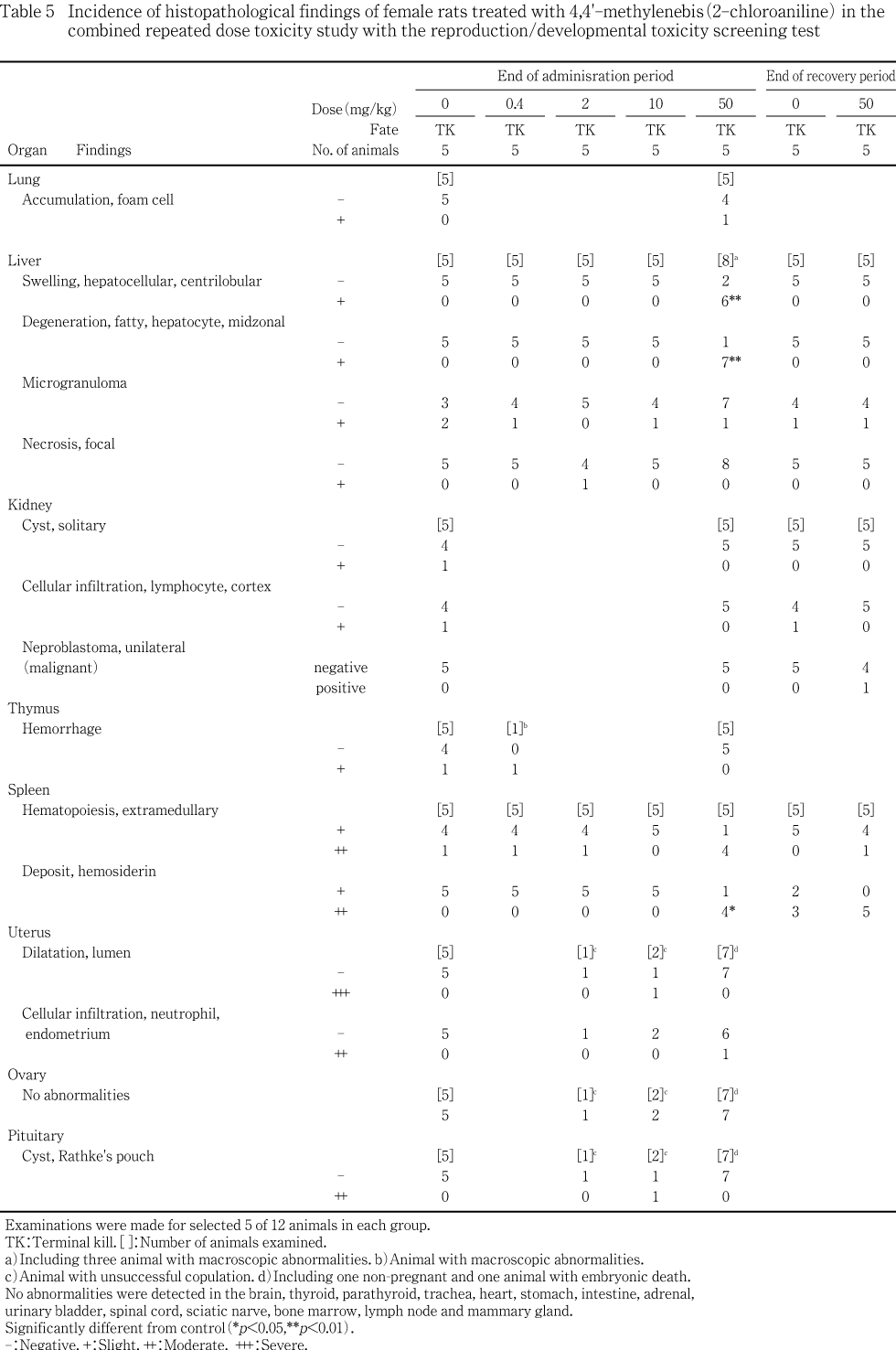
���︳ʪ������Ϳ�˵��������Ѳ��ϡ�ǧ����ʤ��ä���ǥ������Ω�������оȷ������50 mg/kg����ͺ�ˤ����ơ���Ω���ּ��Υ��ѵ忻��оȷ������50 mg/kg���dz�5ɤ���1�㡤������Τ����������(��¦��)�� 50 mg/kg����1���ǧ���줿���ޤ�������������Τʤ���������ٴɰ�̤�0.4 mg/kg����5ɤ��2�㡤2�����10 mg/kg���dz�4ɤ�椽�줾��1���¤Ӥ�50 mg/kg����5ɤ��2���ǧ���줿����ǹ�ˤ��Ѳ���ǧ����ʤ��ä����ޤ����оȷ���50 mg/kg���ˤĤ��Ƥ����ҷ����������븡���ˤ����Ƥ⡤�Ѳ���ǧ����ʤ��ä���ǥ������ʬ�ڤ�Ӯ����Ĵ�Ǥ��ä���Ǥϡ����㤪��ӻҵܤ��Ѳ���ǧ����ʤ��ä���
����������������Ω�Ǥ��ä�10 mg/kg����2�ФǤϡ�1�Ф�ͺ����������ٴɰ�̡��̤�1�Фǻ�˻ҵܤλҵܹг�ĥ��ǧ���졤�ҵܤ��Ѳ��Ͻ��٤Ǥ��ä����ޤ���1�Фλ�β����Τ˥�ȥ�ǹ��Ĥ�ǧ���줿������������Ω�Ȥ�̵�ط��ʽ긫�ȹͤ���줿��2 mg/kg ���Ǥߤ�줿��������Ω��1�С������50 mg/kg����ǧ���줿ǥ������Ω��1�Фϡ���ͺ��������ϴﴱ����ӻ�β����Τˤ��Ѳ���ǧ��ʤ��ä���50 mg/kg ����ǧ���줿�ۻ���˴�λ�Ǥϡ��ҵܤ�����ι���忻�ǧ���졤���㤪��Ӳ����Τˤϰ۾��ǧ��ʤ��ä���
����ʬ������������������ޤǤˤ����ơ����㤬4��5����ȯ��������������ͭ�դ��Ѳ���ǧ����ʤ��ä���
����������Ω��2 mg/kg����1�Ф����10 mg/kg����2�Ф�ǧ���졤����Ψ�Ϥ��줾��91.7 %�����83.3 %�Ǥ��ä���ͭ�պ���ǧ���줺���Ѳ��������������ǧ����ʤ��ä�������¾�η��Ǥ�����˸�������Ω������������Ω�ޤǤ������ϡ�50 mg/kg����ͭ�դ�Ĺ�����ä�3�Ф�7����13�������뤤��14����Ĺ���֤��פ�����������λ��紹������ˤ����ơ�50 mg/kg����2��Ǥϸ��۳��ϸ�2������ȯ��ٻߴ�����³�������۳��ϸ�12�����13����ȯ���������ǧ���졤���줾��������������Ω������¾��1��ϡ��������Ͻ�Ĵ�Ǥ��ä������ǽ�θ���Ŭ���˸���������Ω�Ȥʤꡤ���θ���Ŭ���˸�������Ω�������ᡤ�����ޤ�7�����פ�������������������3�����������θ�����Ω�ޤǤ������ˤϡ��оȷ��Ȥδ֤�ͭ�պ��Ϥʤ��ä���2 mg/kg����1�㤪���10 mg/kg����2��ˤĤ��Ƥ⡤���۳��ϸ�2������ȯ��ٻߴ����֤Ȥʤ���۴��ֽ�λ���ޤǻ�³������������Ω�Ȥʤä��������λ�ϡ��������������������ǤϽ�Ĵ�����������Ƥ��������ۤ�50 mg/kg����1��ǤΤ�ǧ���줺������Ψ��91.7 %�Ǥ��ä���ͭ�պ���ǧ����ʤ��ä���
��50 mg/kg���β��ο����徲��������徲Ψ�ϡ��оȷ�����٤Ƥ�����ͤ������������1�㤬���ο�:6���徲��:1������徲Ψ16.7 %�����ͤ������Ȥˤ���ΤǤ��ä����������ʤ��顤�оȷ�����٤Ƥ������ͭ�պ���ǧ����ʤ��ä���
��50 mg/kg����1��ˤΤ������νл���ǧ���줺�л�Ψ��90.9 %�Ǥ��ä�����ͭ�պ���ǧ����ʤ��ä���ǥ�����֤ˤ�ͭ�դ��Ѳ���ǧ����ʤ��ä���
��50 mg/kg����1���ʬ�ڤ�ǧ����ʤ��ä��ʳ��ϡ����������Ϳ���Ȥ�ʬ�ڤ����Ӯ����֤˰۾��ǧ����ʤ��ä���
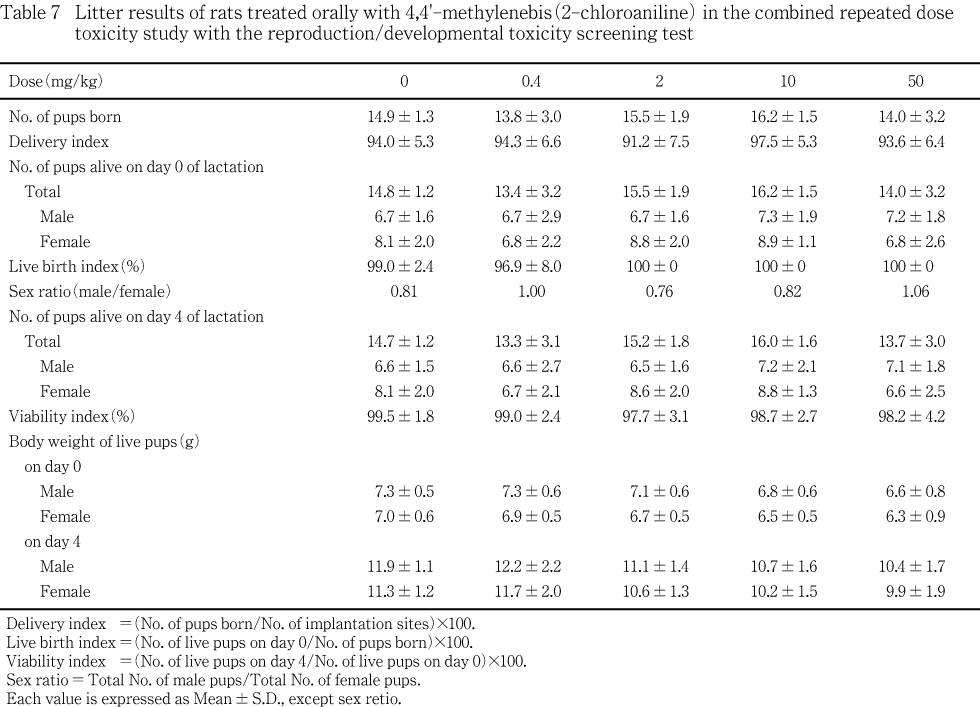
����ʢ����������л�������ʬ��Ψ��Ӯ��0�������4���ο�������������Ψ�������¤Ӥ�Ӯ��4������¸Ψ��ͭ�դ��Ѳ���ǧ���줺���������ΰ��̾��֤ˤ�۾��ǧ����ʤ��ä���Ӯ��0�������4�����νŤˤĤ��Ƥ⡤50 mg/kg���Ǥ���㤤�������ߤ�줿��ΤΡ���������طʥǡ���(Ӯ��0��:ͺ6.2��7.4 g����5.8��7.0 g; Ӯ��4��:ͺ9.8��12.0 g����9.3��11.4 g)���ϰ���Ǥ��ꡤ�оȷ��Ȥδ֤�ͭ�պ���ǧ����ʤ��ä���
��0.4 mg/kg���Ƕ������褹���������1��(ȯ��Ψ0.5 %)ǧ���줿�ʳ��ϡ�������η��ˤ����Ƥ⳰ɽ�������¡�۾��ͭ�����ưʪ��ǧ����ʤ��ä�����¡�ѰۤˤĤ��Ƥϡ�������������Ĥ��оȷ���3��(1.6 %)��0.4 mg/kg����8��(4.4 %)��2 mg/kg����4��(2.5 %)�����10 mg/kg����1��(0.6 %)������ư̮��Ĥ�2 mg/kg����2��(1.4 %)�����50 mg/kg����1��(0.7 %)���ع�Ǣ�ɤ��оȷ���1��(0.6 %)�����2 mg/kg����3��(1.8 %)���ޤ�����ⳳ�ĥ��10 mg/kg����1��(0.6 %)ǧ���졤��������¡�Ѱۤ�ͭ�����ưʪ�ϡ��оȷ���4��(2.1 %)��0.4 mg/kg����8��(4.4 %)��2 mg/kg����9��(5.7 %)��10 mg/kg����2��(1.2 %)�����50 mg/kg����1��(0.7 %)�Ǥ��ä�����������¡�Ѱۤ�ȯ��Ψ�ˤ��оȷ����︳ʪ����Ϳ���Ȥδ֤�ͭ�պ��Ϥʤ����ޤ������̤���ؤ������÷�����ǧ����ʤ��ä���
���︳ʪ������Ϳ�ˤ��ƶ�������˷����ʬ���Ф��Ƥߤ�졤������Ū�ƶ���ޤᡤ�¡����¡����ӿ�¡�ˤ�ǧ���줿.
����դ��Ф���ƶ��ˤĤ��ơ�50 mg/kg���ǻ�ͺ���ַ������쿧��ǻ�٤���ӥإޥȥ���å��ͤθ���������ǧ���줿���ޤ����������Ϸ�긫�˲ä��ơ�50 mg/kg���Ƿ쾮�Ŀ������ä�ǧ���줿�������ȿ��ظ����Ǥϡ��¡�˻�ͺ���˥إ⥸�ǥ����������ä�������˻�ǤϿ�¤���ж�ʤ�ǧ���졤�������ַ����˲�ж�ʤ���Ӥ���ˤ���Ϸ��¤Ӥ��Ϸ���Ф����������¤��ж�ʤη�̤ȹͤ����롥50 mg/kg ���λ�ͺ��ǧ���줿�¡�ν����Ѳ��ϡ������������ȿ���Ū�Ѳ���ȿ�Ǥ�����ΤȻפ��롥�ޤ���50 mg/kg���λ�ͺ��ǧ���줿���ꥦ����־��ַ������÷����⡤���줾���ַ����˲�ж�ʤ����¤��ж�ʤ������Ѳ��ǡ� ��ͺ�˥�ȥإ⥰���ӥ�ǻ�١���˥ϥ���ľ�����ͭ�ַ��Τ���������÷�����ǧ����Ƥ��뤳�Ȥ��θ����ȡ��ܻ��ǧ���줿�Ϸ�ϡ���ȥإ⥰���ӥ��ɤ�ȼ���Ϸ����Ϸ줬���°��ȹͤ����롥���Τ褦�ʥ�ȥإ⥰���ӥ��ɤ�ȼ���Ϸ����Ϸ�ϡ����ߥΥե��Ρ����ࡤN-�ҥɥ���������륢�ߥ��ࡤ���˻����ߥ롤�����¾�λ���²���˻����ޤ��ϻ���²�˻����ʤɤ�ȯ�����뤳�Ȥ��Τ��Ƥ���4)��
������ˡ�10 mg/kg���Ǥ⡤ͺ���¡�Υإ⥸�ǥ���������äΤߤ�ǧ���졤�Ϸ�긫�����餫�Ǥʤ��ä�����10 mg/kg���ˤ����Ƥ��︳ʪ���η�դ��Ф���ƶ������٤�ȯ�����Ƥ��뤳�Ȥ��������줿��
����¡���Ф���ƶ��ˤĤ��ơ�50 mg/kg����ͺ�˴�¡�����Ф�������н��̡�������н��̤����ä�ǧ���졤����Ū�ˤϴ�¡�����ǧ���줿�������ȿ��ظ����Ǥϡ�Ʊ���λ�ͺ�δ�¡�˴κ�˦����(�����濴��)����ӻ�������(�����)��ǧ���졤ͺ�ǤϾ����濴�Ӵκ�˦��ñ��˦�����ȼ�����ǧ���줿����������ظ�����50 mg/kg ���λ�ͺ��ǧ���줿������ѥ�������֥ߥ�� A/G������ͷ����¤Ӥ�LDH�����g-GTP�ι��ͷ�����ͺ��ǧ���줿�����쥹�ƥ����뤪��ӥȥꥰ�ꥻ�饤�ɤι��ͷ����⡤�ε�ǽ���Ф���ƶ��ȴ�Ϣ����긫�ȹͤ���졤�Ϸ줪��ӽ۴ľ㳲�ˤ��η�ή�̤��㲼��ȿ�Ǥ�����Τȹͤ����롥�ޤ���10 mg/kg���Ǥϻ��������ѥ�����ӥ���֥ߥ�����ͷ�����ǧ����Ƥ��ꡤ��¡���Ф���ƶ������٤�ȯ�����Ƥ����Τ�Ƚ�Ǥ��줿��
����¡���Ф���ƶ��˴ؤ��ơ�10 mg/kg�������50 mg/kg���ǻ�������ȿ���Ū�Ѳ��䡤���������Ū�Ѳ��ǿյ�ǽ�۾�������Ѳ���ȼ��ʤ���¡�����н������ä�ǧ���줿��������ͺ�Ǥ�10�����50 mg/kg���ǹ�������Ǣ�ٴɤ����÷�����ǧ���줿�����㳲���줿Ǣ�ٴɤκ������Ȼפ�줿������¾��50 mg/kg��ͺ��ǧ���줿̵�����ι��ͤϡ��յ�ǽ���Ф���ƶ��˴�Ϣ������ư�ȹͤ���줿��
���������Ѳ��˲ä��ơ�50 mg/kg���ǻ�ͺ��ή�����ǥ��������νŤ����ͤ���ӹþ������н��̤ι��ͤ�ǧ���줿��
��ή�ˤĤ��ơ��ܺ٤����ѻ�������ȿ�͵�ǽ���������ϳ����������ϡ���ȯ��ư�����ˤ����ơ����й�ư�����������Ѳ���ǧ����ʤ��ä����ȡ�ή��������Ϳ��10ʬ����30ʬ�δ֤�ǧ���졤��Ϳľ�夫��ǧ�������⤢�ä����Ȥ��顤��Ϳ�դ�̣���Ф���ȿ��Ūȿ���β�ǽ����ͤ����롥
���ޤ����þ������н��̤ι��ͤˤĤ��ơ������ȿ��ظ����ˤ������︳ʪ������Ϳ�ˤ���Ѳ���ǧ���줺���ޤ����н��̤ˤ���ư��ǧ����ʤ����Ȥ��顤������Ū�յ��Ϥʤ���ΤȻפ��롥
�����Τ褦���︳ʪ������Ϳ�ˤ��ƶ��ϡ��������ˤ����Ʋ����ʤ�������������ǧ���줿���Ȥ��顤�ĵ�Ū���Ѳ��Ǥ����Ƚ�Ǥ��줿��
���ʤ�����������ͺ���������н��̤ι��ͤ�ǧ���줿���������ȿ��ظ����Ǥ��︳ʪ������Ϳ�ȴ�Ϣ�����Ѳ���ǧ���줺�������ƶ���������ư�ǤϤʤ��ȹͤ���줿���ޤ����������λ��1��˿�¡�οղ��ǧ���줿���ܼ���ϸ�ո���ͳ�������ۻ�������ǡ���åȤ˼���ȯ��Ū��ǧ����5, 6)��1��Τߤ�ȯ���Ǥ��ä����Ȥ��顤�︳ʪ������Ϳ�Ȥ�̵�ط��ʽ긫��Ƚ�Ǥ��줿��
���ʾ�η�̤��顤��ưʪ�ˤ�����ȿ����Ϳ�ˤ��̵�ƶ���(NOEL)�ϻ�ͺ�Ȥ��2 mg/kg/day�ȿ��ꤵ�줿��
����ưʪ�ˤ����ơ��ѻ������ƻ�ɸ�Ǥϡ���������оȷ�����٤�ͭ�դ��Ѳ���ǧ���줺�������ϴﴱ�ˤ��︳ʪ����Ϳ�˵�������������Ū�Ѳ���ǧ����ʤ��ä���
���ʤ�����������Ω��2 mg/kg����1�Ф����10 mg/kg����2�Ф�ǧ���졤�ޤ���������Ω�ޤǤ�Ĺ���֤��פ���3�Ф�50 mg/kg����ǧ���줿�������λ�ͺ�ˤĤ��ơ������ȿ��ظ����Ǥϸ�������Ω�˴�Ϣ����ȹͤ�����۾��ǧ���줺�������������η�̤��顤��ǥ�����������Ȥˤ���Τ�Ƚ�Ǥ��줿��
��50 mg/kg���ǡ����1��ˤĤ��Ƥ�ʬ�ڤ�ǧ���줺�������ۻ����ҵ����1��Τ�ǧ���줿��Ǥϡ��ҵ�����˱����ȿ����ǧ���졤���줬�ۻ�ȯ�餪���ʬ�ڤ˱ƶ���ڤܤ�����Τȹͤ����롥������ϡ������(���ο�)�����ʤ����徲����1�ĤǤ��ä���������䲼���Τʤ�¾��¡��˰۾��ǧ����ʤ��ä���
����ưʪ���Ф��Ƥϡ�ȯ����ȯ��˴ؤ���ƻ�ɸ�ˤ������︳ʪ������Ϳ�ˤ��ƶ���ǧ����ʤ��ä����оȷ���ޤ����Ϳ���Ǿ�����γ�ɽ�۾浪�����¡�Ѱۤ��ߤ�줿����������⼫��ȯ��Ū��ǧ������Τ�7)��ȯ��Ψ��ͭ�պ�����������������ʤ����Ȥ���Ŵ�����������Ѳ��ǤϤʤ���Ƚ�Ǥ��줿��
���ʾ�η�̤��顤��ͺ��ưʪ������ǽ����ӻ�ưʪ��ȯ�����Ф���̵�ƶ��̤Ϥ������50 mg/kg/day�ȷ������줿��
| 1) | Registry of Toxic Effects of Chemical Substances (RTECS), US NIOSH(1998)�� |
| 2) | Richardson ML, Gangolliet S:In ��The Dictionary of Substances and their Effects��, Volume 3, The Royal Society of Chemistry, England(1994)pp.293-295�� |
| 3) | IARC Monographs on the Evaluation of the Carcinogenic Risk of Chemicals to Humans, 57 (1993). |
| 4) | Kiese, M.:Methemoglobinemia, A Comprehensive Treatise. CRC Press, Cleveland(1974). |
| 5) | �������������ز�(��):�����������ȿ��؎������ڥå������(2000)p.258�� |
| 6) | Charles A. Montgomery, Jr., John Curtis Seely: Kidney, Hyperplastic and Neoplastic Lesions, Other Neoplasms:Nephroblastoma, In ��Pathology of the Fischer Rat��, Academic Press, Inc., San Diego (1990)p.143�� |
| 7) | Morita H, et al.:Spontaneous malformations in laboratory animals, Frequency of external, internal and skeletal malformations in rats, rabbits and mice. Cong. Anom., 27:147-206(1987)�� |
| Ϣ���� | |||
| ���Ǥ��: | ���ġ��� | ||
| �ô����: | ��ƣ���顤����������ƣ�Ȼ��ݡ� �������������ڡ�����������ҡ� ��ƣ��ɧ | ||
| 7�ܻ���ʪ�ʳذ�������� | |||
| ��229-1132����������ϸ��Զ�����3-7-11 | |||
| Tel 042-762-2775 | Fax 042-762-7979 | ||
| E-mail:a_noda@riasbt.or.jp | |||
| Correspondence | |||
| Authors: | Atsushi Noda(Study director) Masaya Ito, Tadami Sugimoto, Shiho Fujinami, Naomi Kon, Hiroshi Akagi, Makiko Yamaguchi, Yoshihiko Ito | ||
| Research Institute for Animal Science in Biochemistry and Toxicology | |||
| 3-7-11 Hashimotodai, Sagamihara-shi, Kanagawa, 229-1132, Japan | |||
| Tel +81-42-762-2775 | Fax +81-42-762-7979 | ||
| E-mail:a_noda@riasbt.or.jp | |||